Resumen
El cerebro es el órgano más complejo que poseemos y es el que nos define como seres humanos. Es la base de la inteligencia, de nuestros pensamientos y recuerdos. Además, interpreta el mundo a través de los sentidos, inicia movimiento y controla nuestros comportamientos.
El funcionamiento de este órgano se basa en el correcto establecimiento de los patrones de conectividad entre los millones de neuronas que lo componen, permitiendo una comunicación precisa y eficiente entre ellas.
Estas redes neuronales emergen durante el desarrollo embrionario y postnatal. La formación adecuada de estas conexiones requiere de diversos eventos orquestados de forma muy precisa y que están controlados por mecanismos moleculares específicos. Por tanto, alteraciones en estos eventos tempranos darán lugar a patologías cerebrales y trastornos complejos.
En las últimas décadas, se ha logrado un gran progreso en la identificación y comprensión de los mecanismos de acción de las moléculas que dirigen el desarrollo de los axones y de los circuitos neurales. Sin embargo, el rol que juegan in vivo en muchos aspectos de la formación de circuitos neuronales sigue siendo, en gran parte, desconocido, particularmente cómo la alteración temprana de esa conectividad deriva en patologías complejas del neurodesarrollo.
En este artículo, destaco parte de mis contribuciones y avances recientes que arrojan luz sobre la complejidad de los mecanismos que regulan la guía de los axones y ensamblaje de los circuitos bilaterales del sistema nervioso central. Además, discuto cómo la comprensión del desarrollo de los circuitos bilaterales del cerebelo es fundamental para comprender la aparición de diversas patologías del neurodesarrollo.Abstract
The brain is the most complex organ we have, and it is the one that defines us as human beings. It is the basis of intelligence, of our thoughts and memories. In addition, it interprets the world through the senses, initiates movement and controls our behaviors.
The correct functioning of this organ is based on the correct establishment of connectivity patterns between the millions of neurons which enable a precise and efficient communication between them.
These neural networks emerge during embryonic and postnatal development. The formation of proper neuronal circuitry relies on diverse and very precisely orchestrated events controlled by specific molecular mechanisms. Therefore, failures in these early events will lead to brain pathologies and complex disorders.
In the last decades, remarkable progress has been made in identifying and in understanding the mechanisms of action of the molecular that direct axon and neural circuitry development. However, their role in vivo in many aspects of neural circuit formation remains largely unknown, particularly how the impairment of this initial connectivity derives in complex neurodevelopmental pathologies.
Here, I highlight part of my contributions and recent advances that shed light on the complexity of mechanisms that regulate axon guidance and the wiring of the bilateral circuits of the central nervous system. Furthermore, I discuss about how understanding the development of bilateral circuits of the cerebellum is essential to understand the emergence of diverse neurodevelopmental pathologies.Palabras clave: Axones comisurales; Circuitos bilaterales; Netrina-1; Cerebelo.
Keywords: Commissural axons; Bilateral circuits; Netrin-1; Cerebellum.
INTRODUCCIÓN
El Sistema nervioso central (SNC), de todas las especies con simetría bilateral, contiene un tipo particular de neuronas denominadas comisurales, las cuales extienden sus axones a través del eje de simetría, la línea media, y conectan con otras localizadas en el lado opuesto.
Estos circuitos juegan un papel crítico en la coordinación e integración de la información originada en ambos lados del cuerpo, siendo así esenciales para múltiples funciones, tales como respuestas motoras, visión binocular o audición.
Durante las últimas décadas, multitud de estudios se han centrado en entender cómo esos axones son capaces de alcanzar y de navegar dianas intermedias, como la línea media ventral o placa del suelo durante el desarrollo del SNC de vertebrados. Esta placa del suelo una estructura glial especializada transitoria que desempeña un papel crucial en la regionalización dorsoventral del tubo neural, así como en la migración celular y la guía del crecimiento axonal.
Todos esos trabajos han contribuido ampliamente a incrementar nuestro conocimiento sobre cómo se forman los circuitos neuronales y han permitido identificar las moléculas que guían la formación de los circuitos en vertebrados durante el desarrollo temprano.
La teoría neurotrófica de Cajal
Uno de los grandes descubrimientos de D. Santiago Ramón y Cajal fue el cono de crecimiento(1). Lo describió como una estructura con forma de cono que se encuentra en el extremo de los procesos celulares en crecimiento y que determinaría los movimientos de este para alcanzar sus dianas sinápticas.
Cajal mostró un profundo interés en entender cómo las neuronas se organizaban durante el desarrollo. “Una de las cuestiones más arduas que nos plantea la histogénesis nerviosa, es la de averiguar en virtud de qué mecanismos crecen las dendritas y los axones adoptando direcciones prefijadas, y estableciendo sin revueltas ni equivocaciones, como guiadas por una fuerza inteligente, conexiones con determinados elementos nerviosos o extra-nerviosos…”– según sus propias palabras(2).
Estas observaciones junto a sus estudios en la médula espinal del embrión de pollo llevaron a Cajal postular la “Teoría neurotrófica”(2). En ésta Cajal sugería que, entre otros, los axones comisurales de la médula espinal en desarrollo se orientarían y alcanzarían sus dianas al ser atraídos a distancia mediante la secreción de sustancias químicas que formarían gradientes atractivos (quimiotropismo). Y serían los conos de crecimiento quienes, además, proporcionarían esa sensibilidad quimiotáctica a las neuronas en desarrollo.
Netrina-1, la primera molécula quimiotrópica
La primera evidencia de quimiotropismo aplicado al SNC de vertebrados surgió de experimentos in vitro dónde se confrontaba un explante dorsal de médula espinal de embrión de rata con un fragmento de la placa de suelo.
Tras cultivarlo, se observó que axones del explante emergían y se dirigían de forma preferente hacia la placa del suelo. Por consiguiente, este crecimiento de los axones comisurales también se estimulaba al cultivar los explantes dorsal de la médula espinal con medio de cultivo condicionado, en el cual se había cultivado previamente células de la placa del suelo(3).
Todos estos resultados apoyaban la idea de que la placa del suelo secretaba moléculas de guía capaces de dirigir la extensión de los axones comisurales.
Las evidencias in vivo se observaron al utilizar ratones modelos en los que se alteraba el desarrollo de la placa del suelo, y dónde los axones comisurales mostraban defectos en su trayectoria(4–6).
Pocos años después, los esfuerzos se centraron en determinar la identidad de esa molécula quimioatrayente presente en la placa del suelo. De esta forma, se aislaron dos proteínas, netrina-1 y netrina-2, en base a su capacidad de mimetizar el efecto de la placa del suelo(7).
En los estudios de expresión de estos genes, se observó que, en la médula espinal del embrión de pollo, netrina-1 estaba específicamente expresada por la placa del suelo, mientras que netrina-2 está expresada en los dos tercios ventrales de la médula espinal, excluyendo la placa del suelo(7).
Todo ello llevó a proponer un modelo, por el cual netrina-1 secretada por la placa del suelo actuaría como una molécula quimiotrayente que guiaría a larga distancia a los axones comisurales en la médula espinal.
Las evidencias in vivo para esta actividad propuesta para netrina-1 vinieron del estudio fenotípico de los ratones mutantes para netrina-1 y en los cuales se observó que la mayoría de los axones comisurales proyectan de forma anómala y fallan en alcanzar y en cruzar la línea media ventral(8,9).
Desde ese momento, ha sido involucrada como molécula de guía en múltiples regiones del cerebro actuando sobre multitud de tipos celulares. Así, netrina-1 se convirtió en una de las proteínas mejor estudiadas no sólo en el campo de la guía de los axones, sino que también se ha descrito que juega diferentes papeles en la formación del sistema nervioso, tales como sinaptogénesis(10–12), migraciones neuronales(13,14), supervivencia(15) o regeneración(16)
Nuevo modelo para la guía de los axones comisurales
Diversos estudios recientes, entre los que se incluye mi trabajo, han cuestionado la prevalencia de la acción quimiotrópica de netrina-1 y han revisado este mecanismo de larga distancia en la guía de los axones comisurales in vivo. En el rombencéfalo y en la médula espinal del embrión de ratón, netrina-1 está expresada por las células de la placa del suelo, pero también por los progenitores neurales (glía radial) de la zona ventricular(9,17,18).
A su vez, el patrón de distribución de la proteína netrina-1 es particularmente diferente al de su transcrito, el ARN. La proteína se acumula principalmente en la región más lateral de la superficie pial y esta además presente en los axones(17–19).
La hipótesis inicial nos sugería que la presencia de netrina-1 en la región lateral sería debida a la geometría bipolar de la glía radial, de forma que esta transportaría o secretaría netrina-1 en esa región.
Para demonstrar el origen de esta netrina-1 y su posible contribución a la guía de los axones comisurales utilizamos una estrategia genética que permitía eliminar de forma específica cada una de las fuentes de netrina-1, la de la placa del suelo y la de la zona ventricular.
En ausencia de netrina-1 en la placa del suelo, netrina-1 se distribuye de forma normal fuera de la línea media, confirmando así que el origen de dicha proteína era la zona ventricular.
Además, en el rombencéfalo, los fenotipos presentes en el mutante de netrina-1, como la proyección anómala en dirección dorsal, la desfasciculación y la ausencia de cruce en la línea media, solo se observaron cuando netrina-1 era eliminada de la zona ventricular y no de la placa del suelo(17,20).
De esta forma, propusimos que la fuente crítica de netrina-1 que guía los axones comisurales era la glía radial de la zona ventricular y no la placa del suelo, como se había sugerido previamente (Figura 1).
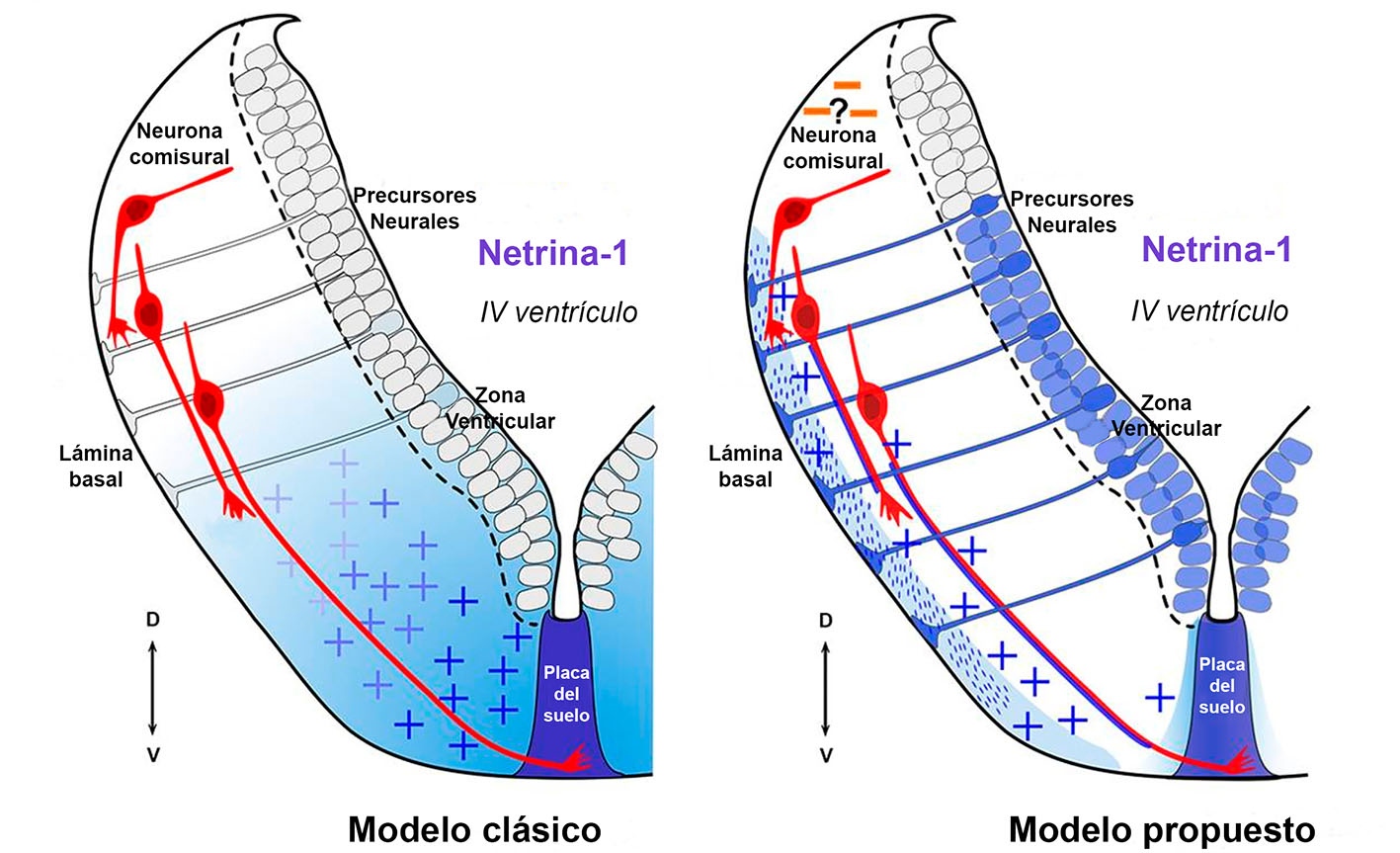
Figura y legendas adaptadas de Dominici, Moreno-Bravo et al., Floor-plate-derived netrin-1 is dispensable for commissural axon guidance(2017) Nature. doi: 10.1038/nature22331.
Esta netrina-1 de la superficie pial promovería la extensión de los axones comisurales de forma fasciculada y dirigida hacia la línea media ventral. Así, netrina-1 dirige la extensión de los axones comisurales del rombencéfalo por un mecanismo de acción que dirigiría el crecimiento de estos por contacto de una superficie permisiva o atractiva (haptotaxis) en vez de por un efecto quimiotrópico a larga distancia(17,18).
En particular, en la médula espinal, aunque la netrina-1 derivada de la zona ventricular actuaría como fuente principal, los defectos presentes en su ausencia son menores que en el caso del rombencéfalo(21). La ausencia de netrina-1 en ambas fuentes es requerida para evitar el cruce de la línea media. Además, la netrina-1 derivada de la placa del suelo podría estar afectando algunos aspectos relacionados con la fasciculación de los axones comisurales y del cruce de la línea media(22). De esta forma, nuestro trabajo demostraba que ambas fuentes de netrina-1 estarían actuando de forma sinérgica en la guía de los axones comisurales de la médula de espinal. Lo que a su vez sugiere que los mecanismos de guía entre el rombencéfalo y la médula espinal difieren. Estas diferencias podrían ser debidas tanto al tamaño de ambas estructuras en el momento de la extensión de los axones comisurales como a su trayectoria.
Por un lado, en el rombencéfalo dicha extensión se origina muy lejos de la línea de media ya que tiene un mayor tamaño que la médula espinal. De esta forma, la influencia de la placa del suelo sería menor. Además, los axones comisurales del rombencéfalo siguen, principalmente, una trayectoria circunferencial, lo que haría que la netrina-1 distribuida a lo largo de la superficie pial (la de origen ventricular) fuera requerida para toda su extensión. Sin embargo, los axones de la médula espinal tienen que separarse de la superficie pial para alcanzar la placa del suelo. Todo ello podría explicar el hecho de que la netrina-1 derivada de la zona ventricular sea una fuente preponderante para la guía de los axones comisurales en el rombencéfalo y en la médula espinal, y que la netrina-1 de la placa del suelo pueda contribuir en la guía de dichos axones incluso teniendo un efecto a distancia. Sin embargo, aún siguen sin existir evidencias in vivo de que los axones detecten netrina-1 en solución (quimiotaxis) en vez de que lo hagan cuando ésta se encuentra unida a un sustrato (haptotaxis)(21,22).
La navegación defectuosa de los axones comisurales se ha observado en diversos tipos de trastornos del neurodesarrollo que se sospecha que tienen un origen en la alteración temprana de la formación de los circuitos neuronales. Además, de caracterizaciones de mutaciones humanas en genes que codifican para receptores asociados a la función de netrina-1, como Dcc o Robo3, y cuya alteración deriva en déficits funcionales(23), han derivado en nuevas relaciones entre la patología y la guía de los axones durante el desarrollo temprano.
El entendimiento de los déficits funcionales asociados a las patologías del neurodesarrollo requiere de un estudio continuo y más profundo de cómo los circuitos comisurales se forman en estas situaciones fisiopatológicas.
Y una de las regiones que merece una mayor atención es el cerebelo. A pesar de haber sido objeto de interés en investigaciones durante siglos, el cerebelo sigue siendo una parte del SNC relativamente inexplorada y su posible implicación en algunas patologías requiere de un estudio más profundo desde una perspectiva del neurodesarrollo.
El cerebelo
El cerebelo ha sido clásicamente reconocido por su papel en el control sensitivomotor y la coordinación. Sin embargo, en las últimas décadas un gran número de evidencias tanto anatómicas, fisiológicas como clínicas están demostrando que puede jugar un papel importante en funciones no motoras, como la cognición y la emoción (24).
De hecho, el cerebelo ha sido relacionado con diversos trastornos mentales como esquizofrenia (25), trastorno bipolar (26) o depresión (27), con un particular foco en su relación con los trastornos del espectro autista (TAE)(28).
Apoyando la amplia evidencia de datos clínicos, diversos estudios en el ratón, también han implicado al cerebelo en el control de funciones de orden superior, como funciones cognitivas y comportamiento social (29), recompensa (30) o planificación motora (31). E incluso, se conoce que la disfunción cerebelosa es suficiente para generar comportamientos relacionados con los TAE en ratones (32–37).
Otra línea de evidencias indica que los factores de riesgo que afectan al crecimiento del cerebelo, como la lesión cerebral neonatal, se correlacionan con peores resultados del desarrollo neurológico general en etapas posteriores (28,38,39). Además, la concurrencia de déficits conductuales tempranos en la mayoría de los trastornos del neurodesarrollo, que abarcan dominios motores, sensoriales, cognitivos y emocionales, sugieren que el desarrollo anormal del cerebelo es un factor determinante e importante para esas situaciones fisiopatológicas.
Una de las principales razones de la mayor susceptibilidad del cerebelo se debe a su trayectoria de desarrollo prolongada. El cerebelo se encuentra entre las primeras estructuras cerebrales en comenzar la diferenciación celular y una de las últimas en madurar por completo (40,41).
Como tal, el cerebelo en desarrollo es vulnerable a la disfunción debido a factores genéticos y epigenéticos, al ambiente tóxico en el útero, o a la lesión cerebral neonatal focal o global. Esta complejidad de factores de riesgo que actúan a lo largo del desarrollo da como resultado una amplia gama de anomalías celulares, morfológicas y de circuitos que tiene un impacto global negativo en el correcto funcionamiento del SNC (38,42–44). De esta manera, todas estas evidencias apuntan hacia la idea de que el desarrollo y conectividad del cerebelo es un factor crítico en determinar el inicio y gravedad de una amplia gama de trastornos del neurodesarrollo.
Por esta razón, es esencial identificar los procesos clave que ocurren durante el desarrollo del cerebelo como paso esencial para descifrar el surgimiento de sus circuitos funcionales y poder entender cómo su disfunción afecta de forma global al funcionamiento del cerebro.
El cerebelo en desarrollo y su implicación en la maduración y función de la corteza cerebral
Se ha propuesto que la influencia del cerebelo en el procesamiento complejo es a través de efectos moduladores sobre la corteza cerebral.
El cerebelo es particularmente vulnerable a los insultos clínicos y ambientales alrededor del nacimiento (recién nacidos o niños con lesiones cerebelosas del desarrollo, hemorragia cerebelosa e infartos)(45). La lesión cerebelosa es una complicación frecuente tras el parto prematuro, que puede llevar a una reducción del tamaño del cerebelo y problemas a largo plazo, incluyendo el desarrollo motor, cognitivo, social y del lenguaje. Estas lesiones cerebelosas tempranas conducen a disfunciones cerebrales mayores que si ocurrieran en la edad adulta, lo que sugiere que la integridad del cerebelo en desarrollo es fundamental para el correcto funcionamiento del cerebro.
Es importante destacar que estudios clínicos indican que el daño cerebeloso temprano conduce a una amplia gama de cambios en la estructura y función de la corteza cerebral en desarrollo. En concreto, estas lesiones cerebelosas tempranas desencadenan modificaciones en el volumen de materia gris y de materia blanca de las áreas corticales que reciben, indirectamente, las proyecciones del cerebelo, que incluyen las áreas prefrontales, premotoras, sensitivomotoras y temporales mediales del hemisferio contralateral (46,47). Éstas alteraciones dan como resultado discapacidades en dominios específicos incluyendo disfunciones motoras y cognitivas(48).
Cabe recalcar, que estas lesiones tempranas del cerebelo están consideradas el principal factor de riesgo no genético para el desarrollo del TAE.
Una hipótesis que podría explicar el efecto remoto del cerebelo sobre la corteza es la “diasquisis del desarrollo”(28). Ésta sugiere que el daño focal en un área encefálica (cerebelo) puede afectar al desarrollo y la organización de regiones cerebrales distantes (corteza cerebral) debido a que existe un sustrato anatómico que las conecta. Este tipo de lesiones cerebelosas ocurren en un momento crítico para el desarrollo de ambas estructuras, lo que sugiere que el cerebelo podría estar modulando o influenciando el correcto desarrollo y la función de la corteza cerebral a través de los circuitos neuronales que conectan ambas estructuras.
A su vez, esas alteraciones corticales podrían derivar en alteraciones funcionales y/o comportamentales relacionadas con diversos trastornos complejos, como el TEA(28). Por lo tanto, es fundamental considerar que alteraciones discretas del desarrollo del cerebelo pueden producir anomalías en regiones distantes como la corteza cerebral. Y así, la diasquisis del desarrollo podría explicar el origen cerebeloso y su implicación en los principales trastornos del neurodesarrollo. Sorprendentemente, los mecanismos por los cuales el cerebelo influye en el desarrollo y la maduración de los circuitos corticales cerebrales de forma remota no han sido explorados.
Actualmente, nuestro trabajo se centra en entender cómo y cuándo se forma el sustrato anatómico que permitiría al cerebelo poder influenciar la corteza cerebral remotamente durante el desarrollo.
Son las neuronas de los núcleos profundos las que conectan primariamente el cerebelo con regiones extra cerebelosas. Estos núcleos están compuestos principalmente por neuronas comisurales(49) que decusan en la línea media ventral y alcanzan diversas poblaciones neuronales localizadas en el tálamo, en el mesencéfalo, en el rombencéfalo y en la médula espinal contralaterales.
Por tanto, estas neuronas permiten el establecimiento de los circuitos en bucles que relacionan al cerebelo con multitud y diversas funciones tanto motoras como no motoras. De esta forma, estas neuronas comisurales ocupan una posición estratégica en el circuito cerebeloso y su papel debería ser considerado como central tanto en la implicación del cerebelo en el desarrollo normotípico como patológico.
Actualmente, estamos determinando cómo, durante el desarrollo temprano, las neuronas de los núcleos profundos se conectan con estructuras intermedias que puedan mediar la influencia del cerebelo sobre la corteza cerebral. Y así, determinar los circuitos neuronales que actuarían como sustrato anatómico para el fenómeno de la diasquisis del desarrollo.
CONCLUSIONES
La formación anómala de los patrones de conectividad durante el desarrollo es una causa subyacente de una amplia variedad de defectos congénitos y trastornos del neurodesarrollo como, por ejemplo, los trastornos del espectro autista.
Para mejorar o restaurar la función de los circuitos neuronales dañados se necesita nuevos enfoques terapéuticos que, a su vez, requieren una mejor comprensión de los eventos bajo los cuales éstos se ensamblaron originalmente durante el desarrollo. Por estas razones, dilucidar los mecanismos celulares y moleculares que subyacen a la formación de circuitos neurales y su función normal, así como el impacto funcional que tiene su alteración sigue siendo un problema fundamental y objetivo prioritario de la neurobiología actual.
Nuestra comprensión integral sobre el desarrollo y función del cerebro requiere de un profundo estudio del cerebelo. Asimismo, como paso indispensable para seguir incrementado nuestro conocimiento sobre la complejidad de las patologías del neurodesarrollo es crítico entender e incluir la contribución del cerebelo en desarrollo.
AGRADECIMIENTOS
Este trabajo ha sido financiado por el Consejo de Investigación Europeo (ERC) bajo el programa de investigación e innovación Horizonte 2020 ERC-2020-StG “CERCODE” (GA No. 950013), el Plan Gen-T de la Generalitat Valenciana (SEJIGENT/2021/036) y por los proyectos de I+D+i RYC2018-023868-I y PID2021-122986NA-I00 financiados por MCIN/ AEI/10.13039/501100011033/ y “FEDER Una manera de hacer Europa”.
DECLARACIÓN DE TRANSPARENCIA
El autor/a de este artículo declara no tener ningún tipo de conflicto de intereses respecto a lo expuesto en el presente trabajo.
BIBLIOGRAFÍA
- Ramón y Cajal S. A quelle époque apparaissent les expansions des cellules nerveuses de la moelle épinière du poulet. Anat Anz. 1890; 5: 609-613.
- Ramón y Cajal S. La rétine des vertébrés. Cellule. 1892; 9: 121-255.
- Tessier-Lavigne M, Placzek M, Lumsden AGS, Dodd J, Jessell TM. Chemotropic guidance of developing axons in the mammalian central nervous system. Nature. 1988; 336(6201): 775-778.
- Bovolenta P, Dodd J. Perturbation of neuronal differentiation and axon guidance in the spinal cord of mouse embryos lacking a floor plate: Analysis of Danforth’s short-tail mutation. Development. 1991; 113(2): 625-639.
- Matise MP, Lustig M, Sakurai T, Grumet M, Joyner AL. Ventral midline cells are required for the local control of commissural axon guidance in the mouse spinal cord. Development. 1999; 126(16): 3649-3659.
- Charron F, Stein E, Jeong J, McMahon AP, Tessier-Lavigne M. The morphogen sonic hedgehog is an axonal chemoattractant that collaborates with netrin-1 in midline axon guidance. Cell. 2003; 113(1): 11-23.
- Kennedy TE, Serafini T, Torre JR de la, Tessier-Lavigne M. Netrins are diffusible chemotropic factors for commissural axons in the embryonic spinal cord. Cell. 1994; 78(3): 425-435.
- Yung AR, Nishitani AM, Goodrich LV. Phenotypic analysis of mice completely lacking Netrin-1. Development. 2015; 142 (21): 3686-3691.
- Serafini T, Colamarino SA, Leonardo ED, et al. Netrin-1 is required for commissural axon guidance in the developing vertebrate nervous system. Cell. 1996; 87(6):1001-1014.
- Glasgow SD, Labrecque S, Beamish IV et al. Activity-dependent Netrin-1 secretion drives synaptic insertion of GluA1-containing AMPA receptors in the hippocampus. Cell Rep. 2018; 25(1): 168-182.
- Goldman JS, Goldman JS, Ashour MA et al. Netrin-1 promotes excitatory synaptogenesis between cortical neurons by initiating synapse assembly. J Neurosci. 2013; 33(44): 17278-17289.
- Glasgow SD, Ruthazer ES, Kennedy TE. Guiding synaptic plasticity: Novel roles for netrin‐1 in synaptic plasticity and memory formation in the adult brain. J Physiol. 2021; 599(2): 493-505.
- Stanco A, Szekeres C, Patel N et al. Netrin-1–α3β1 integrin interactions regulate the migration of interneurons through the cortical marginal zone. Proc Natl Acad Sci. 2009; 106(18): 7595- 7600.
- Hamasaki T, Goto S, Nishikawa S, Ushio Y. A role of netrin-1 in the formation of the subcortical structure striatum: Repulsive action on the migration of late-born striatal neurons. J Neurosci. 2001; 21(12): 4272-4280.
- Mehlen P, Furne C. Netrin-1: When a neuronal guidance cue turns out to be a regulator of tumorigenesis. Cell Mol Life Sci. 2005; 62(22): 2599-2616.
- Dun XP, Parkinson D. Role of Netrin-1 signaling in nerve regeneration. Int J Mol Sci. 2017;18(3):491.
- Dominici C, Moreno-Bravo JA, Puiggros SR et al. Floor-plate-derived Netrin-1 is dispensable for commissural axon guidance. Nature. 2017 ;545(7654):350-354.
- Varadarajan SG, Kong JH, Phan KD et al. Netrin1 produced by neural progenitors, not floor plate cells, is required for axon guidance in the spinal cord. Neuron. 2017; 94(4): 790-799.
- Kennedy TE, Wang H, Marshall W, Tessier-Lavigne M. Axon guidance by diffusible chemoattractants: a gradient of netrin protein in the developing spinal cord. J Neurosci. 2006; 26(34): 8866-8874.
- Yamauchi K, Yamazaki M, Abe M et al. Netrin-1 derived from the ventricular zone, but not the floor plate, directs hindbrain commissural axons to the ventral midline. Sci Rep. 2017; 7(1): 11992.
- Moreno-Bravo JA, Puiggros SR, Mehlen P, Chédotal A. Synergistic activity of floor plateand ventricular-zone-derived netrin-1 in spinal cord commissural axon guidance. Neuron. 2019; 101(4): 625-634.
- Wu Z, Makihara S, Yam PT et al. Long-range guidance of spinal commissural axons by Netrin1 and sonic hedgehog from midline floor plate cells. Neuron. 2019; 101(4): 635-647.
- Izzi L, Charron F. Midline axon guidance and human genetic disorders. Clin Genet; 80(3): 226-234.
- Schmahmann JD. Emotional disorders and the cerebellum: Neurobiological substrates, neuropsychiatry, and therapeutic implications. Handb Clin Neurol. 2021; 183: 109-154.
- Moberget T, Doan NT, Alnæs D et al. Cerebellar volume and cerebellocerebral structural covariance in schizophrenia: a multisite mega-analysis of 983 patients and 1349 healthy controls. Mol Psychiatry. 2018; 23(6): 1512-1520.
- Shinn AK, Roh YS, Ravichandran CT, Baker JT, Öngür D, Cohen BM. Aberrant cerebellar connectivity in bipolar disorder with psychosis. Biol Psychiatry Cogn Neurosci Neuroimaging. 2017; 2(5): 438-448.
- Depping MS, Schmitgen MM, Kubera KM, Wolf RC. Cerebellar contributions to major depression. Front Psychiatry. 2018; 9: 634.
- Wang SS, Kloth AD, Badura A. The cerebellum, sensitive periods and autism. 2015; 83(3): 518-532.
- Badura A, Verpeut JL, Metzger JW et al. Normal cognitive and social development require posterior cerebellar activity. ELife. 2018; 7: e36401.
- Carta I, Chen CH, Schott AL, Dorizan S, Khodakhah K. Cerebellar modulation of the reward circuitry and social behavior. Science. 2019; 363(6424): eaav0581.
- Gao Z, Davis C, Thomas AM et al. A cortico-cerebellar loop for motor planning. Nature. 2018; 563(7729): 113-116.
- Tsai PT, Hull C, Chu Y et al. Autistic-like behaviour and cerebellar dysfunction in Purkinje cell Tsc1 mutant mice. Nature. 2012; 488(7413): 647-651.
- Mapelli L, Soda T, D’Angelo E, Prestori F. The cerebellar involvement in autism spectrum disorders: From the social brain to mouse models. Int J Mol Sci. 2022; 23(7): 3894.
- Kelly E, Meng F, Fujita H et al. Regulation of autism-relevant behaviors by cerebellarprefrontal cortical circuits. Nat Neurosci. 2020; 23: 1102-1110.
- Peter S, Brinke MMT, Stedehouder J et al. Dysfunctional cerebellar Purkinje cells contribute to autism-like behaviour in Shank2-deficient mice. Nat Commun. 2016; 7: 12627.
- Cupolillo D, Hoxha E, Faralli A et al. Autistic-like traits and cerebellar dysfunction in Purkinje cell PTEN knock-out mice. Neuropsychopharmacol. 2016; 41(6): 1457- 1466.
- Stoodley CJ, D’Mello AM, Ellegood J et al. Altered cerebellar connectivity in autism and cerebellar-mediated rescue of autism-related behaviors in mice. Nat Neurosci. 2017; 20(12): 1744-1751.
- Bolduc ME, Limperopoulos C. Neurodevelopmental outcomes in children with cerebellar malformations: a systematic review. Dev Med Child Neurol. 2009; 51(4): 256-267.
- Messerschmidt A, Fuiko R, Prayer D et al. Disrupted cerebellar development in preterm infants is associated with impaired neurodevelopmental outcome. Eur J Pediatr. 2008; 167(10): 1141-1147.
- Rakic P, Sidman RL. Histogenesis of cortical layers in human cerebellum, particularly the lamina dissecans. J Comp Neurol. 1970;139(4): 473-500.
- Altman J, Bayer SA. Prenatal development of the cerebellar system in the rat. I. Cytogenesis and histogenesis of the deep nuclei and the cortex of the cerebellum. J Comp Neurol. 1978; 179(1): 23-48.
- Spoto G, Amore G, Vetri L, et al. Cerebellum and prematurity: a complex interplay between disruptive and dysmaturational events. Front Syst Neurosci. 2021; 15: 655164.
- Stoodley CJ. The cerebellum and neurodevelopmental disorders. Cerebellum. 2016; 15(1): 34-37.
- Hortensius LM, Dijkshoorn ABC, Ecury-Goossen GM, et al. Neurodevelopmental consequences of preterm isolated cerebellar hemorrhage: a systematic review. Pediatrics. 2018; 142(5): e20180609.
- Volpe JJ. Cerebellum of the premature infant: Rapidly developing, vulnerable, clinically important. J Child Neurol. 2009; 24(9): 1085-1104.
- Limperopoulos C, Soul JS, Haidar H et al. Impaired trophic interactions between the cerebellum and the cerebrum among preterm infants. Pediatrics. 2005; 116(4): 844- 850.
- Limperopoulos C, Chilingaryan G, Guizard N et al. Cerebellar injury in the premature infant is associated with impaired growth of specific cerebral regions. Pediatr Res. 2010; 68: 145-150.
- Limperopoulos C, Chilingaryan G, Sullivan N, Guizard N, Robertson RL, Plessis AJD. Injury to the premature cerebellum: Outcome is related to remote cortical development. Cereb Cortex. 2014; 24(3): 728-736.
- Friocourt F, Kozulin P, Belle M et al. Shared and differential features of Robo3 expression pattern in amniotes. J Comp Neurol. 2019; 527(12): 2009-2029
ranm tv
Juan Antonio Moreno Bravo
Instituto de Neurociencias de Alicante. Av. Santiago Ramón y Cajal, s/n.
Campus de San Juan · 03550 San Juan de Alicante
Tlf.: +34 965 233 729 | E-Mail: Juan.moreno@umh.es
An RANM. 2022;139(03): 229-235
Enviado*: 29.09.22
Revisado: 06.10.22
Aceptado: 12.10.22
* Fecha de lectura en la RANM


