RECEPTOR SIGMA-1: MODULACIÓN DE LA SENSIBILIZACIÓN PERIFÉRICA
Enrique J. Cobos del Moral1
1. Departamento de Farmacología, Centro de Investigación Biomédica e Instituto de Neurociencias, Universidad Granada e Instituto de Investigación Biosanitaria ibs.GRANADA.
Las neuronas sensoriales periféricas detectan las sustancias químicas que se generan durante la inflamación, incluyendo mediadores lipídicos como la prostaglandina E2 (PGE2), entre otros. Estas sustancias incrementan la excitabilidad de las neuronas nociceptivas favoreciendo la aparición de dolor mediante el proceso conocido como sensibilización periférica. Durante la inflamación también se producen péptidos opioides endógenos, que aunque tienen cierta capacidad analgésica, no son capaces de contrarrestar el dolor inflamatorio.
El receptor sigma-1 es una proteína chaperona. En respuesta al incremento del Ca2+ intracelular, migra desde localizaciones intracelulares a la membrana plasmática, donde modula receptores, como los receptores opioides µ (MOR), así como ciertos canales iónicos, como los TRPV1. El papel del receptor sigma-1 en el dolor ha sido estudiado principalmente a nivel del sistema nervioso central. Sin embargo, este receptor está presente en todas las neuronas sensoriales periféricas, y no sólo en ratones, sino también en muestras humanas. La administración de antagonistas sigma-1 en ratones, incluyendo el S1RA (el cual está actualmente en ensayos clínicos de fase II), revierte la hiperalgesia inflamatoria inducida por carragenina. Este efecto antihiperalgésico es abolido por el antagonista opioide periférico metioduro de naloxona, así como por un anticuerpo dirigido frente a la secuencia consenso presente en la mayoría de los péptidos opioides endógenos (Tyr-Gly-Gly-Phe), y además, por la inhibición de la infiltración neutrofílica en la pata inflamada mediante la administración de un anticuerpo frente al Ly6G, una molécula importante para la adhesión de este tipo de células inmunitarias. Estos datos sugieren que el bloqueo de los receptores sigma-1 produce analgesia opioide en el sitio inflamado a través de opioides endógenos de origen inmunitario.
Además, hemos estudiado la modulación de la hiperalgesia inducida por la administración directa de sensibilizadores periféricos, como la PGE2. La inyección intraplantar de PGE2 produce hiperalgesia mediante un efecto neuronal directo (en ausencia de reclutamiento inmunitario). Esta hiperalgesia también es revertida completamente por el antagonismo del receptor sigma-1. El efecto del antagonismo sigma-1 es abolido por la administración de metioduro de naloxona y de un anticuerpo frente al agonista MOR endógeno endomorfina-2. Curiosamente, la endomorfina-2 se localiza casi exclusivamente en los nociceptores TRPV1+, los cuales juegan un papel fundamental en la hiperalgesia inflamatoria. Usando proteínas recombinantes, mostramos que el receptor sigma-1 se une a TRPV1, y que en respuesta al S1RA, este receptor se mueve desde el TRPV1 a MOR. Por último, mostramos que la PGE2 incrementa las corrientes de calcio inducidas por capsaicina, el agonista prototipo TRPV1, en cultivos de neuronas sensoriales. Este efecto es revertido por el S1RA, y de una manera sensible al antagonista opioide naloxona, lo que concuerda con los efectos opioides del antagonismo sigma-1 observados in vivo.
En resumen, el receptor sigma-1 participa en la comunicación TRPV1-MOR modulando el tono analgésico opioide. El antagonismo de este receptor disminuye la sensibilización periférica mediante el incremento de la acción de los péptidos opioides endógenos inmunitarios y neuronales presentes en la zona dolorida.
Agradecimientos:
Agencia Estatal de Investigación (10.13039/501100011033 – SAF2016-80540R y PID2019-108691RB-I00), Junta de Andalucía (grupo CTS-109) y fondos FEDER.
AGONISMO SIGMA-1 Y DOLOR: PAPEL DE LAS CÉLULAS INMUNITARIAS Y DE LAS NEURONAS TRPV1+
Miguel Ángel Huerta1, M Carmen Ruiz-Cantero1, Miguel Á. Tejada1, Eduardo Fernández-Segura2, Francisco J. Cañizares2, José M Baeyens1, Enrique J Cobos1
1. Departamento de Farmacología1 y Departamento de Histología2, Centro de Investigación Biomédica e Instituto de Neurociencias, Universidad Granada e Instituto de Investigación Biosanitaria ibs.GRANADA.
El receptor sigma-1 es una proteína neuromoduladora. Tanto los agonistas como los antagonistas sigma-1 tienen posibilidades terapéuticas. El dextrometorfano es un agonista no selectivo sigma-1 usado como antitusígeno. Hay otros agonistas sigma-1 más selectivos, como el PRE-084, el cual se usa en experimentación preclínica, y la pridopidina, la cual está en desarrollo clínico para el tratamiento de la enfermedad de Huntington.
Por otro lado, los antagonistas sigma-1 se están desarrollando como analgésicos. Nuestros estudios indican que el receptor sigma-1 es capaz de unirse al TRPV1, y que los antagonistas sigma-1 disminuyen la sensibilización de los nociceptores TRPV1+. Sin embargo, el efecto de los agonistas sigma-1 en el dolor no se ha estudiado en profundidad. La administración subcutánea de dextrometorfano, PRE-084 o pridopidina, en ratones de genotipo salvaje, incrementó el efecto de la administración intraplantar de una dosis baja de PGE2 (0,125 nmol), carente de actividad hiperalgésica per se. Puesto que la PGE2 es un mediador inflamatorio, usamos un modelo más próximo a una situación clínica real, y estudiamos el efecto de los agonistas sigma-1 tras una lesión quirúrgica de la superficie plantar.
La cirugía indujo una disminución del peso apoyado en la pata (medido mediante un Dynamic Weight Bearing) en el periodo postoperatorio inmediato, a las 3,5h, que se recuperó por completo a las 24h tras la cirugía. Pese a esta recuperación aparente, los animales mostraron un edema en la dermis y el tejido subcutáneo (determinado mediante tinciones de hematoxilina-eosina), y una infiltración neutrofílica (determinada mediante citometría de flujo). En esta circunstancia, la administración subcutánea de los agonistas sigma-1 hizo que el peso apoyado por la pata lesionada disminuyera como si el animal volviera a estar en el periodo postoperatorio inmediato. Se sabe que las células inmunitarias producen PGE2 durante la inflamación, y de hecho, el efecto pronociceptivo del agonismo sigma-1 desapareció completamente al bloquear la infiltración neutrofílica mediante la administración de un anticuerpo frente al Ly6G, una molécula importante para la adhesión de este tipo de células inmunitarias.
Además, encontramos que el efecto pronociceptivo de los agonistas sigma-1, tanto en la hiperalgesia inducida por la administración de PGE2 como tras la incisión plantar, fue abolido por la eliminación de las neuronas TRPV1+ mediante el bisturí molecular resiniferatoxina. Por último, los efectos de los agonistas sigma-1 en animales de genotipo salvaje revirtieron por la administración del antagonista sigma-1 BD-1063, y estuvieron ausentes en animales carentes del receptor sigma-1 (knockout). Estos resultados indican la selectividad de los efectos observados.
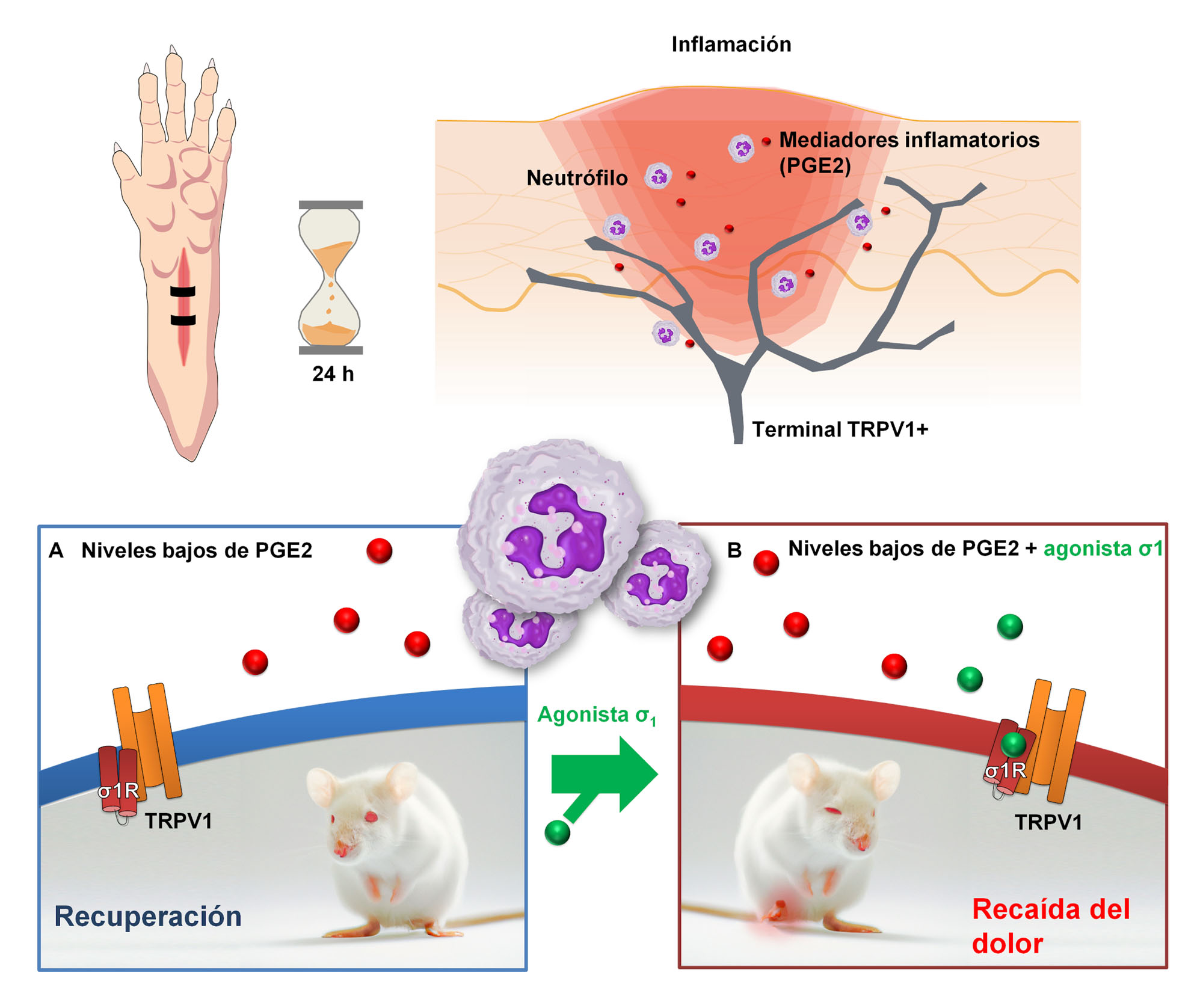
En resumen, el agonismo sigma-1 incrementa las respuestas dolorosas en ratones con una condición inflamatoria leve. El mecanismo de las acciones pronociceptivas del agonismo sigma-1 implica la potenciación de las acciones de los algógenos químicos liberados por las células inmunitarias, como la PGE2, capaces de sensibilizar a los nociceptores TRPV1+ (fig. 1A y B). Si esto se replicara en pacientes humanos, podría constituir un efecto adverso de los fármacos agonistas sigma-1.
Agradecimientos: MINECO (10.13039/501100011033 – PID2019-108691RB-I00, FPU16/03213 y PU21/02736), Junta de Andalucía (grupo CTS 109) y fondos FEDER.
DOLOR POSTOPERATORIO EN EL RATÓN: CARACTERIZACIÓN FARMACOLÓGICA Y PAPEL DE LAS CÉLULAS INMUNITARIAS
Miriam Santos-Caballero, Miguel Ángel Huerta, Makeya Abduljabbar Hasoun, Rafael González-Cano, Enrique J Cobos
1. Departamento de Farmacología, Centro de Investigación Biomédica e Instituto de Neurociencias, Universidad Granada e Instituto de Investigación Biosanitaria ibs.GRANADA.
El control farmacológico del dolor postoperatorio dista mucho de ser óptimo, puesto que la mayoría de los pacientes postquirúrgicos sufren dolor moderado o intenso a pesar del tratamiento analgésico. La laparotomía es el paso inicial para muchas cirugías abdominales, las cuales son las cirugías más frecuentes. Por lo tanto, es interesante caracterizar el dolor inducido por una laparotomía en animales de experimentación, y así profundizar en sus mecanismos de producción. Realizamos una laparotomía en ratones, mediante una incisión transversal de 1,5 cm hasta alcanzar la cavidad abdominal.
Usamos una sutura discontinua para cerrar la musculatura abdominal y el peritoneo, y un punto de colchonero horizontal para cerrar la piel. Valoramos la hipersensibilidad cutánea mediante el umbral de von Frey, el dolor en reposo mediante el análisis de las expresiones faciales de los ratones usando un algoritmo de inteligencia artificial basado en una red neuronal convolucional, y el dolor inducido por el movimiento mediante el análisis de la actividad exploratoria de los animales usando un actímetro de infrarrojos.
En el periodo postoperatorio inmediato (3,5 h), la laparotomía indujo una alodinia mecánica marcada, así como un incremento en el porcentaje de expresiones faciales de dolor y una disminución en la actividad locomotora. Para caracterizar farmacológicamente la laparotomía como modelo de dolor postoperatorio, usamos la administración del opioide morfina y del antiinflamatorio no esteroideo (AINE) ibuprofeno.
Cada conducta dolorosa explorada tuvo una sensibilidad diferente a estos fármacos. Mientras que morfina revirtió de manera más potente las expresiones faciales de dolor que la alodinia mecánica, no fue capaz de revertir el dolor inducido por el movimiento. Ibuprofeno mostró una potencia superior en la reversión de la alodinia mecánica comparada con el dolor en reposo, y pudo revertir significativa (aunque parcialmente) el dolor inducido por el movimiento tras la cirugía. Puesto que en pacientes postquirúrgicos es habitual asociar fármacos opioides con AINEs, también valoramos la asociación de morfina con ibuprofeno. La asociación de estos dos fármacos produjo un efecto sinérgico, alcanzando una reversión completa de los tres parámetros evaluados.
Las interacciones entre las células inmunitarias y las neuronas sensoriales juegan un papel clave en la generación del dolor de etiología diversa. Por lo tanto, estudiamos (mediante citometría de flujo) las células inmunitarias predominantes en la herida quirúrgica durante el periodo postoperatorio inmediato, y encontramos que el infiltrado inmunitario fue principalmente neutrofílico. La inhibición de la infiltración neutrofílica, mediante la administración de un anticuerpo frente al Ly6G, tuvo un efecto marginal en el desarrollo de la alodinia mecánica, mientras que tuvo un efecto muy marcado en el dolor en reposo y en el dolor inducido por el movimiento.
Nuestros resultados indican que las distintas facetas del dolor postquirúrgico difieren en su respuesta a fármacos analgésicos y en el papel de las células inmunitarias en sus mecanismos de producción.
Agradecimientos:
Agencia Estatal de Investigación (10.13039/501100011033 – PID2019-108691RB-I00, FPU21/02736 y PRE2020-096203), Junta de Andalucía (grupo CTS-109) y fondos FEDER.
