Resumen
La corteza y hojas de sauce han sido empleadas desde hace milenios por su efecto analgésico y antiinflamatorio. De ellas se sintetizó la Aspirina a finales del S XIX. A partir de los años 70 del siglo XX, conocemos bien su mecanismo de acción. A través del bloqueo que ejerce sobre la síntesis de las prostaglandinas derivadas del ácido araquidónico, tanto en el endotelio vascular como en las plaquetas. Entendemos el mecanismo de acción sobre la formación del trombo plaquetario y conocemos por múltiples ensayos clínicos cuales son sus indicaciones en la prevención primaria y secundaria de las complicaciones de la enfermedad cardiovascular. Con una indicación precisa en la prevención secundaria en los pacientes que han padecido un accidente coronario o cerebro vascular isquémico, pero con datos más controvertidos en el caso de la prevención primaria, que es el motivo de esta revisión actualizada de la acción de la Aspirina. En estos casos, la decisión de iniciar el tratamiento debe compartirse entre el médico y el paciente, y deben usarse tablas de riesgo y calculadoras para ayudar a determinar el nivel de riesgo cardiovascular y el de sangrado.
Abstract
Willow bark and leaves have been used for thousands of years for their analgesic and anti-inflammatory effect, and Aspirin was synthesized from them at the end of the 19th century. From the 70s of the 20th century, we know its mechanisms of action well. Through the blockade it exerts on the synthesis of prostaglandins derived from arachidonic acid, both in the vascular endothelium and in platelets. We understand the mechanism of action on the formation of platelet thrombus and we know from multiple clinical trials which are its indications in the prevention of complications of cardiovascular disease. With a precise indication in secondary prevention in patients who have suffered a coronary or ischemic stroke, but with more controversial data in the case of primary prevention, which is the reason for this updated review of the action of Aspirin. In these cases, the decision to start treatment should be shared between the clinician and the patient, and risk tables and calculators should be used to help determine the level of CVD and bleeding risk.
Palabras clave: Aspirina; Acido Acetilsalicílico; Prevención Primaria Cardiovascular; Cardiopatía isquémica; Accidente Cerebrovascular Agudo; Riesgo Hemorrágico.
Keywords: Aspirin; Acetylsalicylic acid; Cardiovascular Primary Prevention; Ischemic heart disease; Acute Cerebrovascular Accident; Hemorrhagic Risk.
ABREVIATURAS
AA: ácido araquidónico
AAS: ácido acetilsalicílico
ACVA: accidente cerebrovascular agudo
AIT : Accidente isquémico transitorio
CI: Cardiopatía Isquémica
COX : Ciclooxigenasa
CV: Cardiovascular
DM : diabetes mellitus
EA: Enfermedad arteriosclerosa
ECV: Enfermedad Cardiovascular
FRCV Factor de Riesgo Cardiovascular
HGI: Hemorragia Gastro intestinal
IM: infarto de miocardio
ITB: índice tobillo-brazo
LOX: Lipooxigenasa
NS: No significativo.
PHS: Physicians’ Health Study
PA: presión arterial
PGI2: prostaciclina
PrPr: prevención primaria
TXA2: tromboxano A2
1. INTRODUCCIÓN
Desde hace 4000 años distintas civilizaciones han empleado la corteza y hojas de sauce por su efecto analgésico y antiinflamatorio. En el siglo XVII se comenzó a emplear el extracto de corteza de sauce como antipirético y durante todo el XIX se desarrollan los análisis químicos que llevan al aislamiento de la sustancia activa cristalizada, salicina. Su acetilación permitió conseguir el ácido acetilsalicílico (AAS) con el que trabajó Félix Hoffmann a finales del S XIX y que en 1899 patentó el laboratorio Bayer con el exitoso nombre de aspirina (1).
2. DESARROLLO CIENTÍFICO DEL MECANISMO DE ACCIÓN DE LA ASPIRINA.
En 1970 se comienza a conocer el mecanismo de acción farmacológico de la aspirina y más de 50 años después, seguimos estudiando sus más interesantes indicaciones, la prevención de la enfermedad cardiovascular (ECV).
En la primera mitad del S XX se identifica en la membrana celular, el ácido araquidónico (AA), ácido graso poliinsaturado de 20 átomos de carbono y cuatro dobles enlaces, o ácido eicosatetraenoico. Deriva del aminoácico esencial ácido linoleico y por dos vías de oxidación enzimática se transforma en eicosanoides: La vía de la 5-Lipooxigenasa (LOX) da lugar a leucotrienos, con acción antiinflamatoria, y la vía de la Ciclooxigenasa (COX) sintetiza prostaglandinas, las más importantes para el propósito de esta revisión la prostaciclina o prostaglandina I2 (PGI2) y el tromboxano A2 (TXA2).
En 1970 se comprobó que la aspirina y fármacos similares inhibían las acciones biológicas de las prostaglandinas en la pared vascular (2). En 1971 Moncada y cols publicó que la aspirina y la indometacina inhiben la liberación de prostaglandinas y este mecanismo explica las acciones antiinflamatorias, analgésicas y antipiréticas de estos fármacos(3,4). Más tarde Moncada y cols encontraron el enzima plaquetario Tromboxano sintetasa o COX 1, que sintetiza el TXA2, un potente vasoconstrictor y proagregante plaquetario(6) y poco después(7) demostraron que la prostaglandina sintetizada en la pared arterial por acción de la COX2, la PGI2 o prostaciclina (8), además de vasodilatadora, era también un potente inhibidor de la agregación plaquetaria. Postularon la existencia de un equilibrio entre la síntesis de prostaciclina, vasodilatadora y antiagregante y el efecto proagregante y vasoconstrictor del TXA2, que contribuyen a mantener la integridad del endotelio vascular, el tono arterial y a explicar el mecanismo de formación de trombos intravasculares en ciertas condiciones patológicas. Ambas postaglandinas son sensibles al bloqueo de su síntesis por la aspirina.
La aspirina inhibe la COX plaquetaria con dosis más bajas que las precisas para la analgesia, siendo este efecto irreversible, porque las plaquetas al no tener núcleo, no son capaces de sintetizar proteínas, por lo que la inhibición solo puede realizarse en los megacariocitos antes de que se incorporen a la circulación en forma de plaquetas(9). La COX endotelial o COX2 es menos sensible que la COX1 a la acción de la aspirina(10), se necesitan dosis más altas para su inhibición. Las dosis bajas de aspirina inhiben la síntesis de TXA2 al pasar las plaquetas por la circulación portal, expuestas a mayor concentración de aspirina que en la circulación periférica(11), que no afecta a la producción de PGI2. Esto condiciona un comportamiento antiagregante diferente de la aspirina respecto a otras drogas antiinflamatorias. También Moncada y O’Grady(12) demostraron que una dosis única y baja de Aspirina (0,3 g) producía en humanos, un aumento del tiempo de sangría que no conseguían las dosis altas (3,9 g).
El Prof. Pedro Sánchez García en su discurso de laudatio en la recepción del Prof. Moncada como Académico de Honor de la Real Academia Nacional de Medicina de España señaló: Al margen de su interés estrictamente científico, no debemos dejar de reseñar el profundo impacto que los hallazgos de Salvador Moncada han tenido en la práctica médica. Sirvan como ejemplo, la aceptación universal del efecto antitrombótico de la Aspirina a pequeñas dosis y su valor en la prevención de accidentes cardio y cerebro vasculares(13).
3. APLICACIÓN DE LA ASPIRINA EN LA PREVENCIÓN DE LA ENFERMEDAD CARDIOVASCULAR
En la primera mitad del S XX, algunos médicos clínicos como el Dr. Lawrence Craven, basados en la observación, recomendaron el empleo de la aspirina(14) indicando que podía tener propiedades antitrombóticas beneficiosas para prevenir el infarto de miocardio.
4. ASPIRINA EN PREVENCIÓN SECUNDARIA
En los años 80 del S XX, se conocía que los pacientes que habían padecido complicaciones CV, como IAM o accidente cerebro vascular agudo (ACVA) isquémico, tienen un elevado riesgo de presentar una nueva complicación CV, y la terapia con aspirina podría servir para prevenir nuevas complicaciones CV.
El primer estudio en el que se demostró esta eficacia fue el ISIS-2 (Second International Study of Infarct Survival) (15). Incluyeron 17.187 pacientes en las primeras 24 horas de sospecha de IAM, y tras aleatorizar a: (i) estreptoquinasa intravenosa; (ii) aspirina 160 mg; (iii) ambas pautas simultáneas; o (iv) ninguno de estos tratamientos. Se encontró que estreptoquinasa sola y la aspirina sola redujeron la mortalidad CV a las 5 semanas. Un (9,4%) con aspirina frente a (11,8%) con placebo (2 P< 0,00001).
La combinación de estreptoquinasa más aspirina (8,0% de fallecimientos) fue significativamente mejor (2 P < 0,0001) que cualquiera de los fármacos por separado o sin tratamiento (13,2% de fallecidos).
La aspirina redujo significativamente el reinfarto (1,0% frente al 2,0%) y los ACVA no mortales (0,3% frente al 0,6%), y no aumentó la hemorragia cerebral o hemorragia gastro intestinal (HGI) que requiriera transfusión.
Como conclusión, el tratamiento con aspirina reduce el reinfarto no fatal, los ACVA, la mortalidad CV y la mortalidad por todas las causas, lo que indica que la Aspirina es eficaz en prevención secundaria de complicaciones CV (Figura 1).
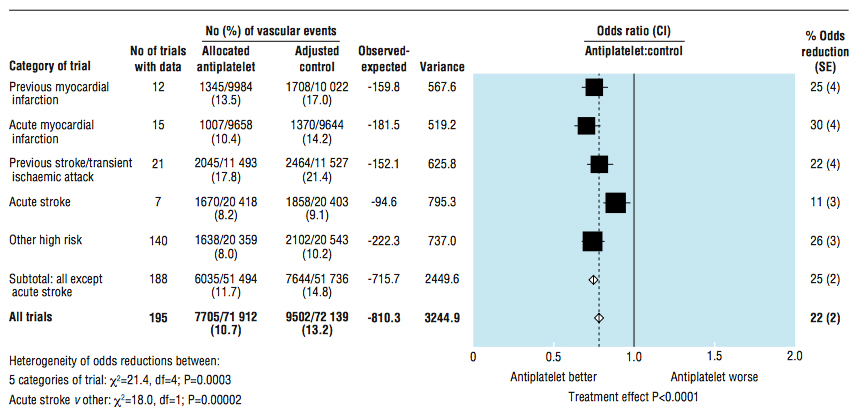
Tomado de cita 27.
5. ENSAYOS EN PREVENCIÓN PRIMARIA CON ASPIRINA
Ese año 1988 comenzaron los ensayos en prevención primaria (PrPr) con Aspirina que siempre ha demostrado un efecto favorable en prevención secundaria.
5.1. El British Male Doctors de 1988 estudió el efecto de 500 mg/día de aspirina en 5139 médicos varones aparentemente sanos, para ver si reducía la incidencia y mortalidad por ACVA, infarto de miocárdio (IM) u otras complicaciones CV(16).
La mortalidad total fue un 10% menor en el grupo aspirina que en el control, diferencia no estadísticamente significativa y ocurría por patologías que no fueron IM ni ACVAS.
Si redujo la incidencia de IM y ACVA no mortal.
Por tanto el estudio no demostró que la aspirina produjera beneficios absolutos en población sana. El beneficio podría producirse si el riesgo trombótico de los pacientes fuera elevado. Para lo que se siguieron realizando numerosos estudios posteriores
5.2. El segundo estudio en estos últimos treinta años en PrPr fue el Physicians’ Health Study (PHS) que ha producido más de 400 informes científicos(17,18).
En 1981, el equipo del PHS envió 261.248 cartas de invitación a todos los médicos varones entre 40 y 84 años de la Asociación Médica Estadounidense. Al final solo entraron en el estudio 22.071 y se asignaron aleatoriamente para recibir aspirina activa y betacaroteno activo (n=5517), aspirina activa y betacaroteno placebo (n=5520), aspirina placebo y betacaroteno activo (n=5519). La dosis de aspirina fue de 325 mg en días alternos.
Tras un seguimiento medio de 60,2 meses hubo una reducción del 44% en el riesgo de IM (P<0,00001) en el grupo de aspirina frente al placebo. Hubo un ligero aumento no significativo (P=0,06) de ACVA en los que tomaron aspirina. Análisis posteriores mostraron que la reducción en el riesgo de IM ocurrió solo en los mayores de 50 años. En definitiva la aspirina mostró una reducción muy significativa en el riesgo de IM, pero no de ACVA y muertes CV totales quizá por el bajo número de médicos que entraron en el ensayo.
5.3. El Thrombosis Prevention Trial (1988).
En el Reino Unido reclutaron 5499 hombres entre 45 y 69 años con alto riesgo de cardiopatía isquémica (CI)(19). Se asignó aleatoriamente warfarina o placebo y aspirina activa o placebo.
La aspirina produjo una reducción del 20 % (P=0,04) en todos las complicaciones de CI, casi en su totalidad por una reducción del 32% (P=0·004) en complicaciones no fatales.
La aspirina sin warfarina redujo todas las complicaciones de CI un 23 % frente a un 15 % con warfarina. La aspirina sin warfarina redujo las complicaciones no fatales en un 36 % en comparación con un 27 % en su presencia. Sin embargo, el empleo conjunto de warfarina/aspirina no produjo reducción significativa en ninguna de las complicaciones de CI(p=0,67), CI fatal (P =0,67) o CI no fatal (P=0,64).
Estos hallazgos indican que se evitarían cinco complicaciones de CI tratando a 1000 hombres con warfarina y aspirina combinadas durante un año; alrededor de tres episodios con warfarina o aspirina solas, y que la aspirina reduce la CI no fatal. El aumento de sangrado, desde Ictus hemorrágico a sangrados menores, siempre fueron más con la warfarina, pero no fueron significativos.
5.4. The Hypertension Optimal Treatment (HOT) randomised trial. La Aspirina en pacientes con Hipertensión.
El estudio HOT(20), investigó el efecto del tratamiento con aspirina en 18790 pacientes hipertensos de 50 a 80 (media 61,5) años y un seguimiento medio de 3,8 años. Se asignaron a un tratamiento con felodipino para reducir la TA diastólica por debajo de 90, 85, u 80 mm Hg. 9.399 pacientes se aleatorizaron a 75 mg/día de aspirina y 9391 a placebo.
La aspirina redujo significativamente las complicaciones CV mayores (con muertes) en un 15 % (P=0,03). El beneficio de la aspirina se redujo al 9 % cuando se incluyeron en el análisis los IM silentes. En el grupo de aspirina los IM fueron un 36% menos frecuentes (P=0,002). No hubo diferencia en la incidencia de ACVAS entre aspirina o placebo. Hubo 7 hemorragias fatales en el grupo aspirina y 8 en el placebo, y las hemorragias mayores no fatales fueron 129 en aspirina versus 70 en placebo (P<0·001).
Las muertes CV y todos los IM fueron prácticamente iguales en los subgrupos de pacientes con diabetes mellitus y cardiopatía isquémica que en la población global HOT.
Las hemorragias mortales (incluidas las cerebrales) fueron igual de frecuentes en los dos grupos. Las hemorragias mayores no mortales y las hemorragias menores fueron más frecuentes en los pacientes con aspirina que en los placebo (P<0,001).
En resumen, la reducción intensa de la presión arterial diastólica (≤85 mm Hg) redujo la tasa de complicaciones CV. La aspirina redujo significativamente las principales complicaciones CV, más el IM, sin afectar la incidencia de ACVAs o hemorragias fatales, pero doblaron la tasa de hemorragias mayores no fatales.
5.5. Dosis Bajas de Aspirina y vitamina E en personas con riesgo cardiovascular. El estudio Primary Prevention Project (PPP)
Este estudio fue realizado en 4495 personas, 2583 mujeres, con edad media 64,4 años. Seguimiento medio 3,6 años. Los pacientes fueron asignados a aspirina (100 mg); no aspirina y vitamina E ( cápsula de 300 mg -tocoferol al día), o sin vitamina E (21).
La aspirina redujo todos los criterios de valoración: muertes CV (P=0·049), IM no fatal, ACVA no fatal, AIT, angina de pecho, enfermedad arterial periférica y procedimientos de revascularización (P=0·l). No hubo diferencias entre los dos grupos en el tipo de ACVA.
Hubo un mayor sangrado gastrointestinal, pero solo uno fatal, lo que supone uno entre 8000 personas-año en tratamiento con aspirina. No hubo exceso de ACVAs hemorrágicos. En conclusión la aspirina fue beneficiosa para todos los objetivos propuestos.
5.6. Aspirina a dosis bajas en la prevención primaria de enfermedad cardiovascular en mujeres
Hasta este trabajo de 2005 la mayor parte de los datos de prevención primaria con aspirina eran en varones en los que se produce una reducción de los infartos y poca reducción del ictus isquémico. Este trabajo se diseñó para reproducir los efectos en mujeres sanas. Incluyeron 39.876, de 45 o más años y se aleatorizaron a 100 mg de aspirina o placebo. Se siguieron durante 10 años para comprobar sus efectos CV. En resumen en el grupo con aspirina se produjeron 477 complicaciones CV mayores frente a 522 en el grupo placebo(22)
Esa reducción con aspirina se debió a que las mujeres tuvieron un 17 % de reducción en el riesgo de ACVA, frente a las del grupo placebo (P = 0,04), principalmente por reducción del 24 % de ACVA isquémico (P=0,009) pero con un aumento no significativo del ACVA hemorrágico (P=0,31). No hubo ningún efecto en la incidencia de IM.
En el análisis de subgrupos la aspirina redujo significativamente las complicaciones CV mayores, (ACVA isquémico e IAM) en las mujeres de 65 o más años (Figura 2).
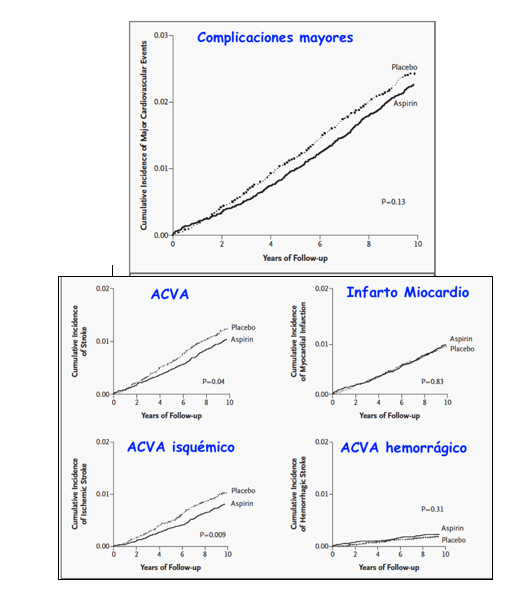
Modificado de Fowles et al (25)
En conclusión, en las mujeres, la aspirina redujo el riesgo de ACVA sin afectar el riesgo de IAM o muerte por causas CV.
5.7. Ensayo de prevención de la progresión de la enfermedad arterial y la diabetes (estudio POPADAD).
Este estudio tuvo como objetivo determinar si 100mg de aspirina diaria y un antioxidante compuesto de 9 sustancias diferentes, administrados solos o combinaos, son superiores al placebo para reducir el desarrollo de ECV en pacientes con diabetes mellitus (DM) y enfermedad arterial periférica asintomática.
Entraron en el ensayo 1276 adultos de 40 o más años con DM tipo 1 o tipo 2 y un índice de presión tobillo-brazo de 0,99 o inferior, pero sin ECV sintomática(23).
En los 6,7 años de seguimiento medio, de 638 complicaciones CV hubo 116 en los grupos con aspirina y 117 de 638 en los grupos sin aspirina (18,2 % frente a 18,3 %). Asimismo ocurrieron 43 muertes por enfermedad coronaria o ACVA en los grupos de aspirina frente a 35 en los grupos sin aspirina (6,7 % frente a 5,5 %). No hubo diferencias en los casos de ictus hemorrágicos entre los grupos. En conclusión este ensayo no proporciona evidencia para emplear aspirina o antioxidantes para PrPr de complicaciones CV y muertes en población diabética.
5.8. Aspirina a dosis bajas en el prevención primaria de arteriosclerosis en pacientes con diabetes tipo 2 (estudio JPAD. Japanese Primary Prevention of Atherosclerosis With Aspirin for Diabetes)
Este estudio japonés examinó la eficacia de baja dosis de aspirina en PrPr en pacientes con DM-2 sin enfermedad arteriosclerosa (EA).(24).
Estudiaron 2567 pacientes, con DM tipo 2, sin enfermedad EA. En los 4,37 años de seguimiento se produjeron 154 complicaciones ateroscleróticos, 68, (5,4%) en el grupo aspirina y 86 ( 6,7 %) en el grupo sin aspirina, (P=0,16, NS). Fueron iguales también el número de ACVAS hemorrágicos, 13 casos, 6 con aspirina y 7 sin aspirina. Los pacientes de más de 65 años del grupo aspirina presentaron 45 complicaciones arteriosclerosas, (6,3%) frente a 59 (9,2%) los controles (P=0,047). En menores de 65 años hubo 23 complicaciones (4,2 %) con aspirina frente a 27 (4,3 %) sin aspirina (P = 0,98). Tampoco hubo diferencias en las complicaciones hemorrágicas.
En conclusión en pacientes diabéticos tipo 2, la aspirina en baja dosis no redujo el riesgo de complicaciones CV en PrPr.
5.9. Aspirina en aterosclerosis asintomática.
La EA asintomática subclínica se diagnostica por un índice tobillo-brazo (ITB) reducido que asocia aumento del riesgo CV que puede precisar tratamiento preventivo. Hasta este estudio de metaanálisis de Fowkes y cols(25), los estudios disponibles de aspirina para prevención de ECV incluían tres ensayos en pacientes con diabetes y seis en los que los diabéticos eran subgrupos dentro de ensayos más amplios de prevención con aspirina. Ningún ensayo aislado había proporcionado resultados definitivos, por lo que se realizó este metanálisis.
Incluyó 28.980 personas entre 50 a 75 años. 3350 pacientes presentaron un índice tobillo-brazo (ITB) reducido. En sus estudios fueron aleatorizados a aspirina (n=1675) o placebo (n=1675).
El objetivo primario fue: muerte o complicación coronaria no fatal, ACVA o revascularización. No mostró diferencias significativas (Aspirina, 13,7; Placebo, 13,3; P= NS).
Los objetivos secundarios (cualquier complicación CV que apareciera por primera vez, o mortalidad por cualquier causa) ocurrieron en 578 participantes (22,8 eventos por 1000 años-persona en el grupo aspirina vs 22,9 en el grupo placebo). Tampoco hubo diferencia significativa en la mortalidad por cualquier causa entre grupos (176 vs 186 muertes). Ni hemorragia mayor que requiriera ingreso (34 pacientes con aspirina y 20 con placebo (P= NS).
Por tanto en población sin ECV clínica, pero con un ITB bajo, la aspirina no produjo una reducción significativa de las complicaciones vasculares frente a placebo.
5.5.1. Aspirina en prevención primaria de complicaciones cardiovasculares en diabéticos. Metaanálisis.
Aproximadamente el 5 % de la población de los estudios de PrPr CV son diabéticos, y son escasos los estudios con todos los pacientes diabéticos. Ningún estudio individual había proporcionado resultados concluyentes con diabéticos. Por esta razón se realizan meta análisis, como este de Pignone y cols (26) en el que se analizan los datos de todos los diabéticos de cada estudio, y los tres realizados exclusivamente en diabéticos (JPAD Japanese Primary Prevention of Atherosclerosis With Aspirin for Diabetes), POPADAD (The prevention of progression of arterial disease and diabetes), y ETDRS: Early Treatment of Diabetic Retinopathy Study).
En los seis estudios con población general entraron 95000 participantes de los que 4000 eran diabéticos. En los estudios exclusivamente en diabéticos, cada estudio incluyó: El JPAD 2539 pacientes diabéticos, El POPADAD 1276 diabéticos, y El ETDRS 3711 Diabéticos.
En total el metaanálisis incluyó 11526 pacientes diabéticos. En resumen se encontró que la aspirina reducía el riesgo de complicaciones (Enfermedad Coronaria) fatal y no fatal (IAM) el 9%, no estadísticamente significativo. Gran parte de los hallazgos dependían del ensayo ETDRS, sin él la reducción sobre los efectos coronarios fueron más pequeños.
Se encontró también una reducción en el riesgo de ictus del 10% tampoco estadísticamente significativa. Los resultados en la diabetes eran consistentes con los hallazgos del metanálisis Antithrombotic Trialists’ (ATT) Collaboration (27) y sugieren que la aspirina en diabéticos produce una modesta reducción en el riesgo de ECV no significativa.
5.5.2. Más recientemente se ha publicado el estudio ASCEND (Effects of Aspirin for Primary Prevention in Persons with Diabetes Mellitus)(28) también en 15.480 pacientes diabéticos seguidos durante 7,4 años. El grupo aspirina representaba 57,000 persona/año y el grupo placebo. 56,945 personas/año. Fueron varones el 62,6% del grupo aspirina y el 62,5% del placebo. Todos eran DM, y no tenían historia clínica de aterosclerosis.
El objetivo primario consistió en la aparición de complicaciones CV graves (combinación de: IM no fatal, ACVA isquémico no fatal, Accidente isquémico transitorio(AIT), o muerte por cualquier causa vascular, excluyendo hemorragia intracraneal confirmada). En el grupo aspirina se produjeron 658 complicaciones vasculares severas (8,5%) vs 743 (8,6%) en el grupo placebo, (P = 0.01, NS), una reducción del 12% frente al grupo placebo.
En contraste, se produjeron 314 (4,1%) Hemorragias mayores gastro intestinales y extracraneales, en el grupo aspirina, frente a 245 (3,2%) en el grupo Placebo (P = 0,003), es decir la aspirina aumentó un 20% el riesgo de hemorragia grave.
El empleo de dosis bajas de aspirina en diabéticos sin ECV previene pocas complicaciones CV graves, pero provoca complicaciones hemorrágicas importantes.
5.10. El Estudio ASPREE (Aspirin in Reducing Events in the Elderly)(29) investigó el efecto de la aspirina sobre las complicaciones CV y el sangrado en 19.114 ancianos sanos, de 74 años de edad media, seguidos 4,7 años. 9.525 en el grupo aspirina y 9.589 en el placebo. El 56 % fueron mujeres. El objetivo primario, tasa de ECV, la alcanzaron 10,7/1000 del Grupo aspirina y 11,3 /1000 del Grupo Placebo; P = 0.01)(P= NS.)
Las hemorragias mayores fueron 8,6/1000 p/año en el grupo aspirina y 6,2/1000 p/año en el placebo (P<0.001) Por tanto la aspirina a dosis bajas en pacientes mayores no redujo el riesgo de ECV y sin embargo aumentó significativamente el riesgo de hemorragia mayor (Figura 3).
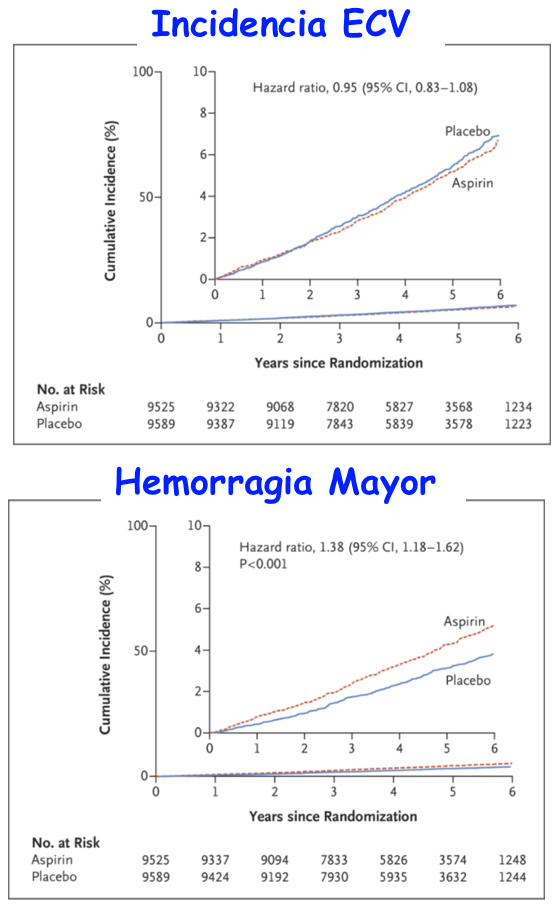
La aspirina a dosis bajas como prevención primaria en adultos mayores (74 años) produjo un riesgo significativamente mayor de hemorragia mayor y no redujo el riesgo de ECV más que el placebo. Hemorragias G Aspirina 8,6 /1000 pts /año vs G Placebo: 6,2 / 1000 p/año (P<0.001)
Modificado de McNeil et al (29).
5.11. Estudio ARRIVE (A Study to Assess the Efficacy and Safety of Enteric-Coated Acetylsalicylic Acid in Patients at Moderate Risk of Cardiovascular Disease).
Valoró la aspirina en pacientes con Riesgo CV Moderado(30). Fueron 12.546 pacientes de más de 55 años los varones y de 60 años las mujeres, que tuvieran al menos un riesgo CV moderado calculado en tablas de riesgo (10 al 20 % en 10 años), seguidos durante 5 años. Se excluían ECV patente, historia de HGI, ingesta de anticoagulantes o diabéticos. El Grupo aspirina incluyó 6270 pacientes y 6276 el Placebo
El objetivo primario lo alcanzaron 269 pacientes (4·29%) en el grupo aspirina y 281 (4·48%) en el grupo placebo. (P= NS). HGI 61 pacientes (0,97%) con aspirina frente a 29 (0,46 %) con placebo (p=0.0007).
La incidencia global de eventos relacionados con el tratamiento fue baja (n=1050 [16,75 %] frente a n=850 [13,54 %] en el grupo de placebo; p<0,0001). Hubo 321 muertes (n=160 [2,55 %] grupo aspirina frente a n=161 [2,57 %] en el grupo de placebo) (Figura 4).
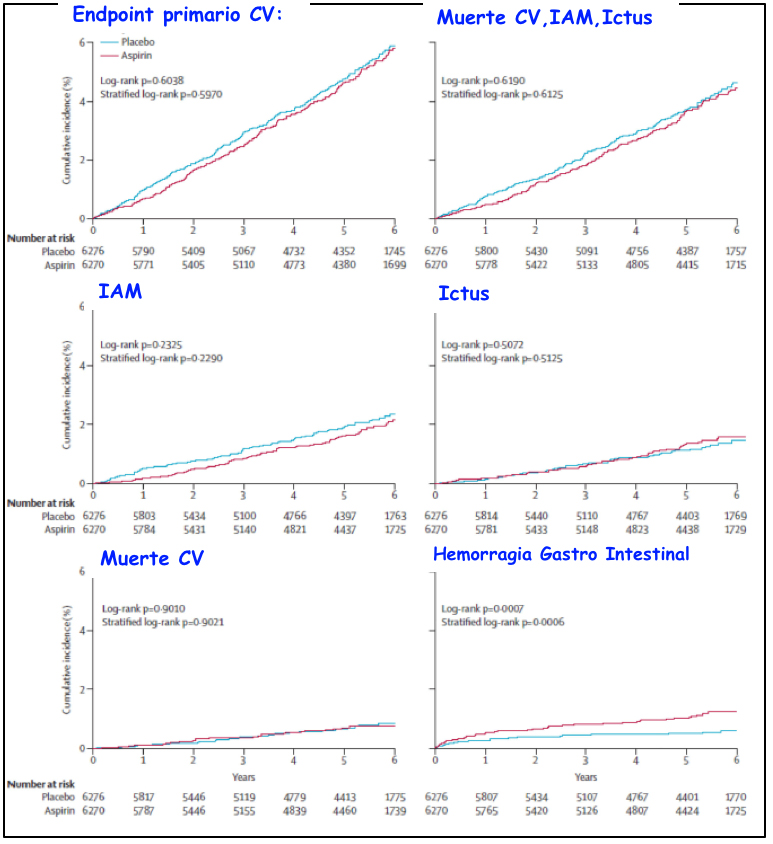
Modificado de Gaziano et al (30)
La tasa de complicaciones fue mucho más baja de lo esperado, probablemente por el mejor manejo actual del riesgo CV. Por lo que este estudio es más representativo de una población de bajo riesgo y no con riesgo moderado.
5.12. Diferencia de género
Numerosos estudios en los últimos 40 años han demostrado que la Aspirina en dosis bajas es eficaz en la prevención secundaria de la ECV tanto en hombres como en mujeres.
En PrPr, la aspirina en dosis bajas, que se valoró en 11 ensayos (N = 134.470 [63% mujeres]) no se asoció a reducción de la mortalidad por ECV o mortalidad por cualquier causa. Sin embargo redujo las complicaciones mayores de ECV (IAM e ictus no mortal y mortalidad por ECV)(31)
No hubo diferencias significativas por género, en los efectos del tratamiento para el objetivo principal de mortalidad por todas las causas, IAM o Ictus, por lo que no hubo evidencia para apoyar pautas diferentes de tratamiento por género.
Prácticamente la mitad de los datos utilizados para las mujeres (46%) procedían del primer gran estudio en mujeres, Women’s Health Study (39.876 mujeres) que comprobó que reduce el riesgo de ACVA total y de ACVA isquémico, de forma similar en todos los grupos de edad.
Las mujeres de 65 o más años experimentaron también reducciones en el objetivo principal de ECV (IAM mortal y no mortal, ACVA mortal y no mortal, y mortalidad por ECV) , mientras que las mujeres más jóvenes (< 64 años) no conseguían estas resultados.
En todos los estudios aparece un aumento relevante del riesgo de sangrado grave, en todas las edades siendo este riesgo mayor en los varones(32) el riesgo absoluto de sangrado aumenta con la edad y en los varones, especialmente después de los 60 años .
6. POR TODO LO EXPUESTO, SE HAN MODIFICADO LAS GUÍAS CLÍNICAS DE INDICACIÓN DE ASPIRINA EN PRPR CV, DE LAS DISTINTAS SOCIEDADES CIENTÍFICAS. EN TÉRMINOS GENERALES NO DEBEN DIFERIR LAS INDICACIONES POR GÉNERO PERO DEBE VALORARSE INDIVIDUALMENTE EL BENEFICIO Y EL RIESGO DE SANGRADO, Y TENER EN CUENTA LA PREFERENCIA INFORMADA DEL PACIENTE.
6.1. El American College of Cardiology y la American Heart Association(33) en la guía de PrPr de ECV de 2019 desaconsejan el empleo rutinario de aspirina en adultos de más de 70 años o en cualquier edad con un riesgo alto de sangrado.
La aspirina en dosis bajas puede considerarse para pacientes de 40 a 70 años y los que tengan un riesgo alto (más de 10%) de ECV a 10 años.
6.2. La Sociedad Europea de Cardiología en 2021 desaconseja la aspirina para los mayores de 70 años o con riesgo bajo/moderado de ECV(34)
6.3. La American Diabetes Association 2022 recomienda aspirina en dosis bajas en diabéticos de 50 o más años con riesgo CV elevado (1 factor de riesgo CV mayor). El riesgo parece superior al beneficio en mayores de 70 años(35).
6.4. Sólo la American Heart Association de 2011 hace recomendaciones para la PrPr CV en mujeres(36).
Recomiendan el aspirina en mujeres diabéticas sin enfermedad CV conocida (75–325 mg). Sugieren que la aspirina en dosis bajas puede ser útil en mujeres mayores de 65 años si la PA se controla cuidadosamente y el riesgo de ictus isquémico o IAM es mayor que el de HGI o de ACVA hemorrágico, mientras que en mujeres menores de 65 años sin ECV, la dosis baja puede ser razonable para prevenir el ictus isquémico.
Fuera de esta indicación ninguna otra de las guías hizo recomendaciones específicas por género.
6.5. Finalmente, el US Preventive Services Task Force. en 2021(37), indica dosis bajas de aspirina para la PrPr en adultos de 40 a 59 años con un 10% o más riesgo de ECV a 10 años.
Es probable el beneficio en personas sin riesgo mayor de sangrado y dispuestas a tomar aspirina en dosis bajas todos los días.
7. EPÍLOGO
Todos las recomendaciones resaltan la necesidad de que la decisión de iniciar el tratamiento debe ser compartida entre el clínico y el paciente y aconsejan el empleo de las tablas y calculadoras de riesgo para ayudar a conocer el nivel de riesgo de ECV y de sangrado.
DECLARACIÓN DE TRASPARENCIA
El autor/a de este artículo declara no tener ningún tipo de conflicto de intereses respecto a lo expuesto en el presente trabajo.
BIBLIOGRAFÍA
- ↑Tsoucalasi G, Karamanoui M, Androutsosi G. Traveling through time with aspirin, a healing companion. Eur J Inflammation. 2011; 9: 13-16.
- ↑Vane JR. Inhibition of prostaglandin synthesis as a mechanism of action for aspirin-like drugs. Nat New Biol. 1971; 231(25): 230-235.
- ↑Ferreira SH, Moncada S, Vane JR. Indomethacin and aspirin abolish prostaglandin release from the splen. Nat New Biol. 1971; 231(25): 237-239.
- ↑Ferreira SH, Moncada S, Vane JR. Prostaglndins and the mechanism of analgesia produced by aspirin-like drugs. Br J Pharmacol. 1973; 49: 86-97.
- Hamberg M, Svensson J, Samuelsson B. Thromboxanes: a new group of biologically active compounds derived from prostaglandin endoperoxides. Proc Natl Acad Sci USA. 1975; 72(8): 2994-2998.
- ↑Needleman P, Moncada S, Bunting S, Vane JR, Hamberg M, Samuelson B. Identification of an enzyme in platelet microsomes which generates thromboxane A2 from prostaglandin endoperoxides. Nature. 1976; 261: 558-560.
- ↑Moncada S, Gryglewski R, Bunting S, Vane JR. An enzyme isolated from arteries transforms prostaglandin endoperoxides to an unstable substance that inhibits platelet aggregation. Nature. 1976; 263(5579): 663-665. doi: 10.1038/263663a0.
- ↑Whittaker N, Bunting S, Salmon J et al. The chemical structure of prostaglandin X (prostacyclin). Prostaglandins. 1976; 126: 915-928. doi: 10.1016/0090-6980(76)90126-x.
- ↑Burch JW, Stanford N, Majerus PhW. Inhibition of platelet prostaglandin synthetase by oral aspirin. J Clin Invest. 1978; 61: 314-319.
- ↑Baenziger NL, Dillender MJ, Majerus PhW. Cultured human skin fibroblasts and arterial cells produce a labile platelet-inhibitory prostaglandin. Biochem Biophys Res Commun. 1977; 78(1): 294-301. doi: 10.1016/0006-291x(77)91253-0.
- ↑Pedersen AK, Garret A, FitzGerald GA. Dose-related kinetics of aspirin- presystemic acetylation of platelet cyclooxygenase. N Engl J Med. 1984; 311: 1206-1211. doi: 10.1056/NEJM198411083111902.
- ↑O’Grady J, Moncada S. Aspirin: a paradoxical effect on bleeding time. Lancet. 1978; 312(8093): 780. doi: 10.1016/s0140-6736(78)92661-2.
- ↑Moncada S. Aventuras en farmacología: Veinte años de casualidad y diseño: Discurso de ingreso como Académico de Honor de la Real Academia Nacional de Medicina. Laudatio por Pedro Sánchez García. An R Acad Nac Med. 1994; 111: 853-910.
- ↑Miner J, Hoffhines A. The discovery of aspirin’s antithrombotic effects. Tex Heart Inst J. 2007; 34(2): 179-186.
- ↑Second International Study of Infarct Survival Collaborative Group. Randomised trial of intravenous streptokinase, oral aspirin, both, or neither among 17,187 cases of suspected acute myocardial infarction: ISIS-2. Lancet. 1988; 2(8607): 349-360.
- ↑Peto R, Gray R, Collins R et al. Randomised trial of prophylactic daily aspirin in British male doctors. Br Med J (Clin Res Ed). 1988; 296: 313-316.
- ↑Steering Committee of the Physicians’ Health Study Research Group. Final report on the aspirin component of the ongoing Physicians’ Health Study. N Engl J Med. 1989; 321(3): 129-135.
- ↑Steering Committee of the Physicians’ Health Study Research Group. Final report on the aspirin component of the ongoing Physicians’ Health Study. N Engl J Med. 1989; 321(3): 129-135.
- ↑The Medical Research Council’s General Practice Research Framework. Thrombosis prevention trial: Randomised trial of low-intensity oral anticoagulation with warfarin and low-dose aspirin in the primary prevention of ischaemic heart disease in men at increased risk. Lancet. 1998; 351(9098): 233-241.
- ↑Hansson L, Zanchetti A, Carruthers SG et al. Effects of intensive blood-pressure lowering and low-dose aspirin in patients with hypertension: Principal results of the Hypertension Optimal Treatment (HOT) randomised trial. HOT Study Group. Lancet. 1998; 351(9118): 1755-1762.
- ↑De Gaetano G; Collaborative Group of the Primary Prevention Project. Low-dose aspirin and vitamin E in people at cardiovascular risk: a randomised trial in general practice. Lancet. 2001; 357(9250): 89-95.
- ↑Ridker PM, Cook NR, Lee IM. A randomized trial of low-dose aspirin in the primary prevention of cardiovascular disease in women. N Engl J Med. 2005; 352(13) :1293-1304.
- ↑Belch J, MacCuish A, Campbell I et al; Prevention of Progression of Arterial Disease and Diabetes Study Group; Diabetes Registry Group; Royal College of Physicians Edinburgh. The prevention of progression of arterial disease and diabetes (POPADAD) trial: factorial randomised placebo controlled trial of aspirin and antioxidants in patients with diabetes and asymptomatic peripheral arterial disease. BMJ. 2008; 337: a1840.
- ↑Ogawa H, Makayama M, Morimoto T et al; Japanese Primary Prevention of Atherosclerosis With Aspirin for Diabetes (JPAD) Trial Investigators. Low-dose aspirin for primary prevention of atherosclerotic events in patients with type 2 diabetes: a randomized controlled trial. JAMA. 2008; 300(18): 2134-2141.
- ↑Fowkes FG, Price JF, Stewart MC et al; Aspirin for Asymptomatic Atherosclerosis Trialists. Aspirin for prevention of cardiovascular events in a general population screened for a low ankle brachial index: a randomized controlled trial. JAMA. 2010; 303(9): 841-848.
- ↑Pignone M, Alberts MJ, Colwell JA et al. Aspirin for primary prevention of cardiovascular events in people with diabetes: a position statement of the American Diabetes Association, a scientific statement of the American Heart Association, and an expert consensus document of the American College of Cardiology Foundation. Circulation. 2010; 121(24): 2694-2701.
- ↑Antithrombotic Trialists’ (ATT) Collaboration; Baigent C, Blackwell L, Collins R et al. Aspirin in the primary and secondary prevention of vascular disease: Collaborative meta-analysis of individual participant data from randomised trials. Lancet. 2009; 373(9678): 1849-1860. doi: 10.1016/S0140-6736(09)60503-1.
- ↑ASCEND Study Collaborative Group; Bowman L, Mafham M, Wallendszus K et al. Effects of aspirin for primary prevention in persons with diabetes mellitus. N Engl J Med. 2018; 379(16): 1529-1539. doi: 10.1056/NEJMoa1804988
- ↑McNeil JJ, Wolfe R, Woods RL et al; ASPREE Investigator Group. Effect of aspirin on cardiovascular events and bleeding in the healthy elderly. N Engl J Med. 2018; 379(16): 1509-1518. doi: 10.1056/NEJMoa1805819
- ↑Gaziano JM, Brotons C, Coppolecchia R et al; ARRIVE Executive Committee. Use of aspirin to reduce risk of initial vascular events in patients at moderate risk of cardiovascular disease (ARRIVE): a randomised, double-blind, placebo-controlled trial. Lancet. 2018 ; 392(10152): 1036-1046. doi: 10.1016/S0140-6736(18)31924-X
- ↑Shufelt Ch L, Mora S, Manson JE. Aspirin for the primary prevention of atherosclerotic cardiovascular disease in women. JAMA. 2022; 328(7): 672-673. doi: 10.1001/jama.2022.11951.
- ↑Guirguis-Blake JM, Evans CV, Perdue LA et al. Aspirin use to prevent cardiovascular disease and colorectal cancer. JAMA. 2022; 327(16): 1585-1597.
- ↑Arnett DK, Blumenthal RS, Albert MA et al. 2019 ACC/AHA guideline on the primary prevention of cardiovascular disease: a report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines. Circulation. 2019; 140(11): e596- e646. doi:10.1161/CIR.0000000000000678
- ↑Visseren FLJ, Mach F, Smulders YM et al; ESC National Cardiac Societies; ESC Scientific Document Group. 2021 ESC Guidelines on cardiovascular disease prevention in clinical practice. Eur Heart J. 2021; 42(34): 3227-3337.
- ↑American Diabetes Association Professional Practice Committee. 10.Cardiovascular disease and risk management: Standards of Medical Care in Diabetes-2022. Diabetes Care. 2021; 45(suppl 1): S144-S174.
- ↑Mosca L, Benjamin EJ, Berra K et al. Effectiveness-based guidelines for the prevention of cardiovascular disease in women–2011 update: a guideline from the American Heart Association. J Am Coll Cardiol. 2011; 57(12): 1404-1423.
- ↑US Preventive Services Task Force. Aspirin Use to Prevent Cardiovascular Disease: US Preventive Services Task Force Recommendation Statement. JAMA. 2022; 327(16): 1577-1584. doi:10.1001/jama.2022.4983
ranm tv
José Ramón de Berrazueta Fernández
Real Academia Nacional de Medicina de España
C/ Arrieta, 12 · 28013 Madrid
Tlf.: +34 91 159 47 34 | E-Mail: joseramon@berrazueta.com
Año 2023 · número 140 (02) · páginas 114 a 124
Enviado*: 30.05.23
Revisado: 05.06.23
Aceptado: 20.06.23
* Fecha de lectura en la RANM


