Resumen
Hay 850 millones de personas en el mundo con enfermedad renal crónica (ERC), una de las causas globales de muerte de más rápido crecimiento que fue el factor de riesgo más importante para COVID-19 letal. La esperanza de vida restante de las personas con ERC en terapia de reemplazo renal es hasta 40 años menor que en la población general. Si bien los estilos de vida saludables y el control de factores de riesgo como la diabetes y la hipertensión pueden contribuir a proteger del desarrollo de ERC, la carga global de ERC sigue aumentando. A pesar de estos malos resultados, ensayos clínicos recientes indican que hay que desarrollar el concepto de prevención primaria de la ERC. En análisis post-hoc de al menos dos ensayos clínicos, los inhibidores de SGLT2 previnieron el desarrollo de ERC en personas sin ERC previa, pero con alto riesgo de ERC. Proponemos una definición de trabajo de prevención primaria de la ERC con el objetivo de conservar la salud renal, que debe incluir la población diana (quién), el momento (cuándo) y la intervención (qué).
Abstract
There are 850 million people in the world with chronic kidney disease (CKD), one of the fastest growing global causes of death that was the most important risk factor for fatal COVID-19. The remaining life expectancy of people with CKD on renal replacement therapy is up to 40 years less than in the general population. While healthy lifestyles and control of risk factors such as diabetes and hypertension can help protect against the development of CKD, the global burden of CKD continues to increase. Despite these poor results, recent clinical trials indicate that the concept of primary prevention of CKD must be developed. In post-hoc analyses of at least two clinical trials, SGLT2 inhibitors prevented the development of CKD in people without prior CKD but at high risk for CKD. We propose a working definition of primary prevention of CKD with the aim of preserving renal health, which should include the target population (who), the moment (when) and the intervention (what).
Palabras clave: Enfermedad renal crónica; Carga de enfermedad; Prevención; Tratamiento; Mortalidad; Inhibidores de SGLT2.
Keywords: Chronic kidney disease; Disease burden; Prevention; Treatment; Mortality; SGLT2 inhibitors.
LA ENFERMEDAD RENAL CRÓNICA (ERC)
La ERC se define como anomalías de la estructura o función renal, presentes durante más de 3 meses, con implicaciones negativas para la salud [1]. Las anomalías que definen la ERC incluyen una tasa de filtración glomerular (FGe) por debajo de 60 mL/min/1.73 m2 o evidencia de daño renal como albuminuria [tasa de excreción de albúmina ≥ 30 mg/24 h; cociente de albúmina y creatinina en orina (CACo) ≥ 30 mg/g] o anomalías en el sedimento urinario o en electrolitos u otras anomalías debidas a trastornos tubulares o anomalías detectadas por histología o anomalías estructurales detectadas por imágenes o antecedentes de trasplante renal. Si bien varios criterios pueden diagnosticar la ERC de forma independiente, los riesgos para la salud asociados con la ERC se evalúan combinando los valores de FGe y CACo (Figura 1) 1,2,3, ya que ambas variables predicen independientemente el riesgo de progresión de la ERC, lesión renal aguda y muerte cardiovascular. y, sobre todo, la muerte por cualquier causa 1. Por lo tanto, conceptualmente, un diagnóstico de ERC identifica a las personas con un riesgo aproximadamente de 2 a 7 veces mayor de muerte prematura en comparación con las personas sin ERC. Combinando FGe y CACo, la organización KDIGO, que es la principal fuente internacional de guías clínicas en Nefrología, identifica cuatro categorías de riesgo: bajo riesgo (sin ERC, si no hay otros criterios presentes que diagnostiquen la ERC); riesgo moderadamente aumentado; alto riesgo y muy alto riesgo 1. Más recientemente, la Sociedad Europea de Cardiología usó los términos más intuitivos de ERC leve, moderada y grave para referirse a las categorías de riesgo KDIGO definidas por la combinación de valores de FGe y de CACo y equiparó la ERC moderada y grave con un riesgo cardiovascular alto y muy alto, respectivamente 2,3.
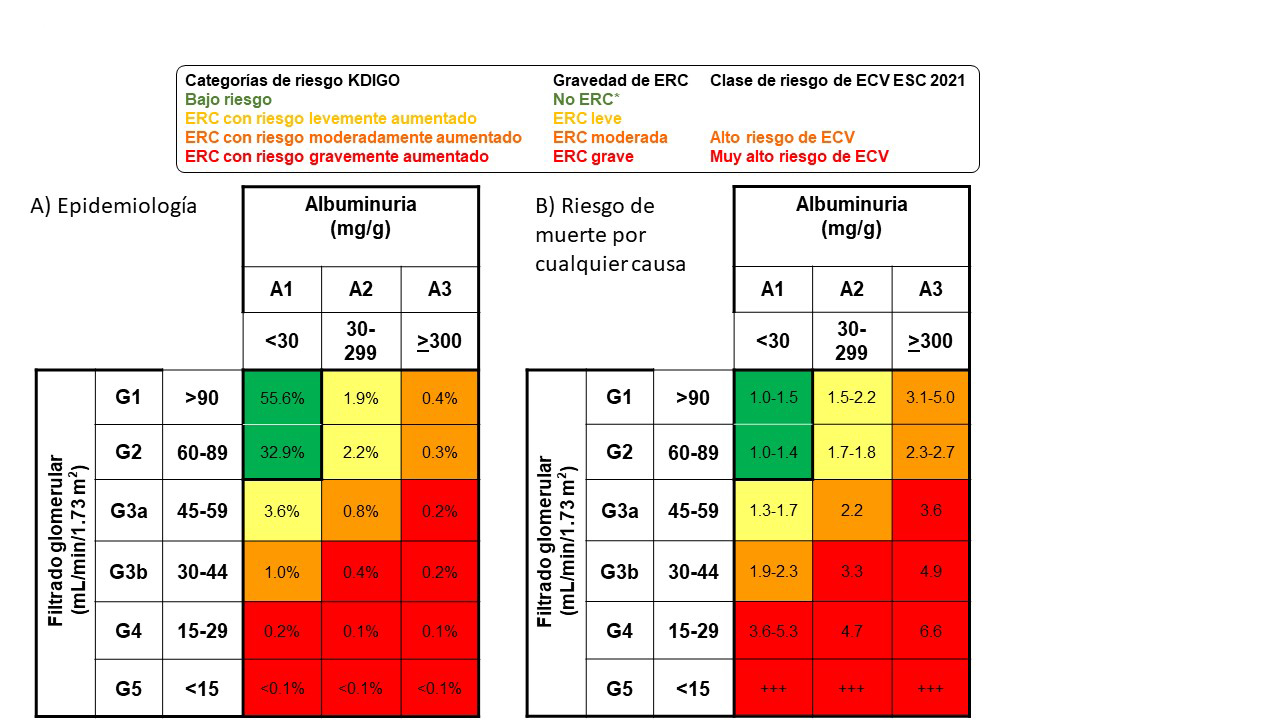
La carga global de enfermedad atribuible a la ERC es alta y además está aumentando dramáticamente. Hay 850 millones de personas con ERC en el mundo, se estima que se convertirá en la quinta causa de muerte en el mundo en 2040 y fue el factor de riesgo relativo más fuerte para la enfermedad grave por coronavirus 2019 (COVID-19) 4,5,6,7,8. De hecho, una de cada cinco personas con ERC avanzada falleció tras una infección por COVID-19 9. A pesar del tratamiento de la ERC, el riesgo residual de resultados adversos para la salud sigue siendo alto. La esperanza de vida de las personas en terapia de reemplazo renal es considerablemente más corta (hasta 40 años menos para un joven de 20 años en diálisis) que para la población general 10,11.
El coste anual de la ERC en Europa supera los 140 000 millones de euros, un 40 % más que el coste del cáncer y supera al de la diabetes 12. Además, el impacto ambiental de la terapia de reemplazo renal es insostenible a largo plazo desde el punto de vista del consumo de energía, el consumo de agua y los desechos plásticos 13. La mala situación actual y las peores proyecciones de carga de enfermedad exigen novedosos enfoques proactivos para enfrentar la ERC basados en la prevención primordial en la población general y en la prevención primaria en atención primaria, respectivamente, encaminados a preservar la salud renal, en lugar del enfoque reactivo actual que intenta cerrar la puerta después de que el caballo se haya escapado, esto es, trata la ERC solo después de que se haya desarrollado utilizando enfoques terapéuticos que generalmente no restauran la salud renal.
EN LA ERC, A PESAR DEL TRATAMIENTO, HAY UN ELEVADO RIESGO RESIDUAL DE RESULTADOS DE SALUD ADVERSOS
Los tratamientos disponibles para personas con ERC no disminuyen los riesgos para la salud hasta los niveles de referencia para su sexo y edad. Ensayos clínicos recientes de pacientes con ERC diabéticos y no diabéticos han proporcionado información sobre el riesgo residual de los pacientes con ERC tratados con regímenes de última generación, que incluyen inhibidores del cotransportador de sodio-glucosa-2 (SGLT2) además de bloqueo del sistema renina-angiotensina. Estos regímenes mejoran los resultados renales, cardiovasculares y de supervivencia en personas con diabetes y/o ERC y/o insuficiencia cardíaca en comparación con el tratamiento convencional de estas afecciones, que ya incluía el bloqueo del sistema renina-angiotensina 14,15,16,17,18,19,20. Hay información adicional sobre el riesgo residual en personas con ERC y diabetes mellitus tipo 2 de los ensayos que compararon finerenona con placebo 21. . Sin embargo, a pesar de tratamiento óptimo, el pronóstico de la ERC avanzada sigue siendo francamente mejorable. En un ejemplo reciente, en el ensayo EMPA-REG OUTCOME, el riesgo residual de muerte por todas las causas fue 4 veces mayor entre los participantes con ERC grave aleatorizados a empagliflozina que entre los participantes sin ERC aleatorizados a empagliflozina (Figura 2) 22,23.
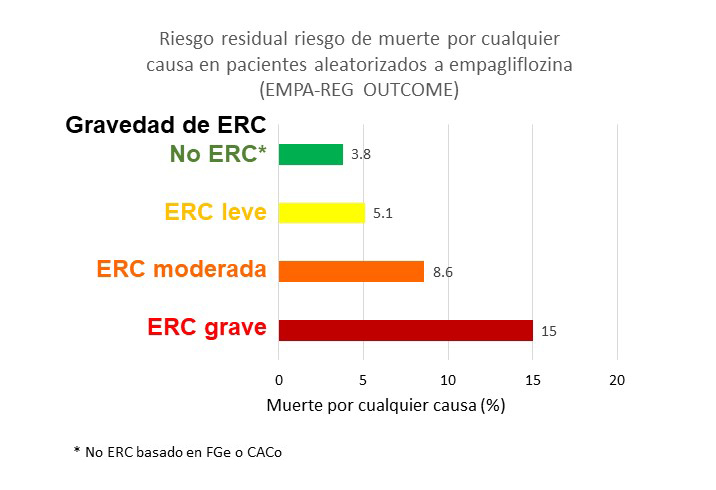
EMPA-REG OUTCOME reclutó a personas con diabetes tipo 2, enfermedad cardiovascular aterosclerótica establecida y FGe ≥30 ml/min/1,73 m2. Sin embargo, el subgrupo de ERC grave no incluyó pacientes G4-G5 que tienen el mayor riesgo de muerte por todas las causas y, por lo tanto, la mortalidad residual observada en el subgrupo de ERC grave aleatorizado al brazo de intervención podría haber subestimado la mortalidad residual en el mundo real para esta categoría.
PREVENCIÓN PRIMORDIAL Y PREVENCIÓN PRIMARIA DE LA ERC
El objetivo del Comité Directivo del Día Mundial del Riñón 2020 fue salud renal para todos en todas partes, desde la prevención hasta la detección y el acceso equitativo a la atención 24. La prevención primordial y primaria de la ERC son los únicos enfoques que promueven la salud renal, ya que el tratamiento de la ERC ya establecida no suele restaurar la salud renal (Figura 3). La prevención primordial de la ERC puede definirse como intervenciones en toda la población (independientemente del riesgo de desarrollar ERC) que promueven la salud renal, habitualmente mediante legislación que asegura la calidad del agua y limita la exposición a tóxicos o mediante medidas que promueven estilos de vida saludables. La prevención primaria de la ERC podría definirse como estilos de vida o intervenciones farmacológicas dirigidas a prevenir o retrasar la aparición de la ERC en personas con alto riesgo de ERC que aún no la tienen. Por el contrario, la prevención secundaria de la ERC se centra en la prevención de la progresión de la ERC en personas que ya la han desarrollado (sería un término equivalente al de tratamiento de la ERC) y puede asociarse con esfuerzos de prevención primaria o secundaria de complicaciones cardiovasculares y no cardiovasculares.
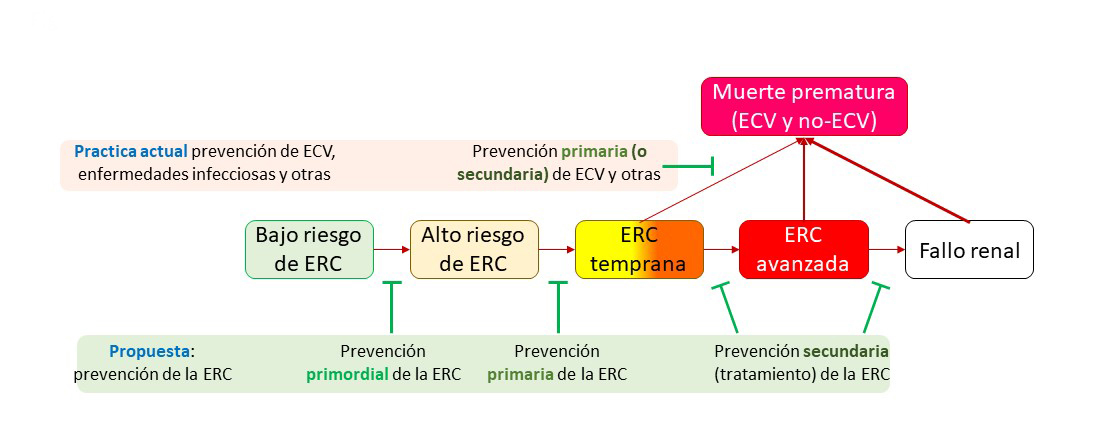
El concepto de prevención primaria de la ERC fue planteado en 2009 por un panel de expertos convocado por los Centros para el Control y la Prevención de Enfermedades de Estados Unidos 25. Sin embargo, el debate sobre la prevención primaria de la ERC se ha centrado en estilos de vida saludables y control de factores de riesgo como la diabetes y la hipertensión 26. Estas medidas, que en su mayor parte son compartidas por la prevención primaria de la enfermedad cardiovascular, hasta ahora no han detenido el aumento progresivo de la carga de la ERC, sin que sea posible distinguir si la causa es implementación o eficacia subóptimas. Una revisión sistemática y un metanálisis recientes de los factores modificables del estilo de vida para la prevención primaria de la ERC concluyeron que las asociaciones de los factores modificables del estilo de vida con la ERC eran consistentes, pero la evidencia era predominantemente de certeza baja a muy baja 26. De hecho, faltan pautas de prevención primaria de la ERC basadas en la dieta debido a la evidencia limitada 27. La combinación de abordar el estilo de vida junto con la prescripción de medicamentos dirigidos específicamente a la prevención ha sido una parte integral del éxito del enfoque de prevención primaria en la enfermedad cardiovascular 3. En este sentido, ensayos clínicos recientes han demostrado la viabilidad de prescribir medicamentos para prevenir o retrasar la aparición de la ERC en personas de alto riesgo sin ERC de base. De esta forma, el concepto de prevención primaria de la ERC se ha ampliado para incluir el uso de fármacos destinados a prevenir la ERC y no solo al control de otros factores de riesgo cardiometabólico 22,28.
FÁRMACOS PARA LA PREVENCIÓN PRIMARIA DE LA ERC
Los ensayos clínicos de seguridad cardiovascular identificaron por primera vez los posibles beneficios cardiovasculares y renales de los inhibidores de SGLT2 en personas con diabetes tipo 2 y alto riesgo cardiovascular o enfermedad cardiovascular establecida 29,30,31. Esta información condujo a la realización de ensayos que demostraron que los inhibidores de SGLT2 también mejoran los resultados de salud en pacientes con y sin diabetes que tenían ERC o insuficiencia cardíaca, cuando se agregan a la terapia de referencia de última generación para estas afecciones, o incluso en monoterapia para ERC 14–19. En los análisis iniciales post-hoc o preespecificados de ensayos clínicos de seguridad cardiovascular, los participantes con FGe ≥60 ml/min/1,73 m2 o CACo <30 mg/g se beneficiaron de los inhibidores de SGLT2 en términos de resultados renales 29,31,32. Sin embargo, ambos subgrupos pueden incluir pacientes con ERC diagnosticada por CACo ≥30 mg/g o FGe <60 mL/min/1.73 m2, respectivamente. Más recientemente, un análisis post-hoc evaluó los resultados en diversas categorías de riesgo de KDIGO (que combinan CACo y FGe) y objetivó el beneficio renal en pacientes sin ERC inicial (es decir, con una FGe ≥60 mL/min/1,73 m2 y además CACo < 30 mg/g) 22,33. Aunque estos pacientes aún pueden tener ERC si cumplen con otros criterios (p. ej., enfermedad renal poliquística autosómica dominante diagnosticada por ecografía), es muy probable que la mayoría estuviera libre de ERC.
Ensayos clínicos de seguridad cardiovascular tanto con empagliflozina como con dapagliflozina sugieren que pueden prevenir o retrasar la aparición de la ERC 22,33. En el ensayo EMPA-REG Outcome, los participantes sin ERC inicial se beneficiaron de la empagliflozina en comparación con el placebo. El Hazard ratio (HR) y el intervalo de confianza del 95 % (IC del 95 %) para el resultado de la nefropatía incidente fue de 0,67 (0,47 a 0,94) y para la duplicación de la creatinina sérica, el inicio de la terapia de reemplazo renal o la muerte por enfermedad renal fue de 0,31 (0,16 a 0,63) 22. Ambos resultados coincidieron con los del ensayo DECLARE-TIMI 58 que evaluó dapagliflozina frente a placebo en personas con diabetes tipo 2 con alto riesgo cardiovascular con un aclaramiento de creatinina estimado ≥60 ml/min 33. En DECLARE-TIMI 58, el HR (IC del 95 %) para un resultado renal compuesto de disminución de la FGe de ≥40 % desde el valor inicial a una FGe <60 ml/min/1,73 m2, fallo renal o muerte relacionada con el fallo renal en participantes sin ERC inicial aleatorizados a dapagliflozina fue 0,54 (0,38 a 0,77) 33. Resulta muy interesante que en ambos ensayos los participantes sin ERC tuvieron el riesgo residual más bajo de resultados renales adversos (0,6 % al 0,8 %), que fue de 11 a 12 veces menor que en los pacientes con ERC grave 22,33. Por lo tanto, los mejores resultados en términos de salud renal se obtuvieron cuando los inhibidores de SGLT2 se recetaron de una manera que previene la ERC, en lugar de tratarla. Además, la pendiente crónica de la FGe se ralentizó en los participantes sin ERC inicial para una pendiente crónica con el fármaco que osciló entre una FGe estable y -1,4 ml/min/1,73 m2 por año, cerca de la pendiente esperada de la FGe asociada con la edad. En resumen, dos ensayos clínicos grandes contemporáneos (con casi 14.000 participantes sin ERC entre los dos) indican que la prevención primaria de la ERC mediante la prescripción de ciertos medicamentos (p. ej., inhibidores de SGLT2 además del bloqueo del sistema renina angiotensina) es posible y da como resultado un riesgo residual más bajo de progresión de la ERC que tratar la ERC con los mismos medicamentos.
Otros fármacos podrían también prevenir la ERC. Así, los agonistas de receptores de GLP-1 o la twincretina tirzepatide mejoraron el pronóstico renal en pacientes con FGe ≥60 mL/min/1,73 m2 y además CACo <30 mg/g 34. Otros fármacos podrían eventualmente ser estudiados para la prevención de la ERC, en base a los buenos resultados obtenidos en el tratamiento de la ERC, aunque todavía no se han comunicado resultados que evalúen específicamente su impacto sobre participantes que combinan normoalbuminuria y FGe conservado (es decir, >60 ml/in/1.73 m2) 35.
¿CUÁL ES LA POBLACIÓN DE ALTO RIESGO QUE PODRÍA BENEFICIARSE DE LA PREVENCIÓN PRIMARIA DE LA ERC?
Los resultados de los ensayos clínicos de seguridad cardiovascular sugieren que las personas con DM tipo 2 que cumplen los criterios de inclusión, pero que no tienen una ERC inicial, pueden beneficiarse de la prevención primaria de la ERC mediante el uso de inhibidores de SGLT2 22,33. Un análisis en profundidad de estos ensayos puede caracterizar mejor las características de los participantes con mayor probabilidad de beneficiarse de una intervención preventiva. Se necesitan estudios que definan otras poblaciones de alto riesgo que pueden beneficiarse de la prevención primaria de la ERC, incluidas las poblaciones no diabéticas. Las puntuaciones clínicas o mixtas junto con biomarcadores derivadas de estudios observacionales o ensayos clínicos pueden ayudar a desarrollar criterios de alto riesgo 36,37 y pueden incluir variables como edad, antecedentes familiares, antecedentes de prematuridad o fracaso renal agudo, comorbilidades (obesidad, diabetes, hipertensión, enfermedad cardiovascular, preeclampsia, enfermedades inflamatorias sistémicas), medicamentos, o variables de laboratorio (FGe, CACo u otras). En el futuro, las puntuaciones de riesgo poligénico también pueden definir poblaciones con alto riesgo de ERC que pueden beneficiarse de la prevención primaria de la ERC 38. Los análisis coste-beneficio pueden aclarar si los sistemas de salud pública pueden adoptar dicha estrategia preventiva para la ERC. En este sentido, algunos análisis recientes de coste-beneficio de la terapia de primera línea para la diabetes tipo 2 con inhibidores de SGLT2 ya están desactualizados por la rápida evolución de la evidencia 39.
ÁMBITO DE LA PREVENCIÓN PRIMARIA DE LA ERC
Los candidatos para la prevención primaria de la ERC no estarán, en general, bajo seguimiento nefrológico. El contexto principal de la prevención primaria de la ERC será la atención primaria, siguiendo pautas de caracterización del riesgo e implementación similares a las usadas para determinar el riesgo de enfermedad cardiovascular o de diabetes 3,40. Por ello es necesaria una implicación de las Sociedades Científicas de Atención Primaria desde las etapas tempranas de la discusión del concepto. Por ejemplo, las directrices de la ESC de 2021 sobre prevención de enfermedades cardiovasculares en la práctica clínica fueron respaldadas por 13 Sociedades Científicas Europeas, incluida la Organización Mundial de Colegios Nacionales, Academias y Asociaciones Académicas de Médicos Generales/Médicos de Familia (WONCA) Europa, lo que podría facilitar su implementación en Atención Primaria 3. En España, la Sociedad Española de Nefrología (SENEFRO) ha liderado un documento sobre la necesidad de implementar la medida de la albuminuria como medida para optimizar la caracterización del riesgo cardiovascular que ha sido apoyado por 15 Sociedades Científicas 41. La implementación de la medida de la albuminuria en la rutina de la Medicina Preventiva facilitaría también el diagnóstico temprano de la ERC y del riesgo de ERC.
AGENDA DE INVESTIGACIÓN SOBRE LA PREVENCIÓN PRIMARIA DE LA ERC
Es necesario establecer una agenda de investigación con el objetivo de conservar la salud renal, que debe identificar la población diana (quién), el momento (cuándo) y la intervención (qué), con contribuciones de todas las partes interesadas. A final de año, una conferencia de controversias KDIGO intentará identificar las necesidades de investigación específicas y sentar las bases para el desarrollo, la implementación y la evaluación del desempeño de guías clínicas sobre la prevención primaria de la ERC (https://kdigo.org/conferences/controversies-conference-on-preventing-ckd/#). La ERC es un problema social y el éxito de los esfuerzos de prevención para promover la salud renal dependerá de la acción coordinada de los profesionales de la salud, las asociaciones de pacientes, los proveedores de atención médica y de los pagadores, además de los financiadores de la investigación y los legisladores para fomentar regulaciones alimentarias saludables, campañas sociales y de detección, entre otros.
AGRADECIMIENTOS
FIS/Fondos FEDER (PI22/00469, PI22/00050, PI21/00251, ERA-PerMed-JTC2022 (SPAREKID AC22/00027), Sociedad Española de Nefrología, Sociedad Madrileña de Nefrología (SOMANE), FRIAT, Comunidad de Madrid en Biomedicina P2022/BMD-7223, CIFRA_COR-CM. Instituto de Salud Carlos III (ISCIII) RICORS program to RICORS2040 (RD21/0005/0001) funded by European Union – NextGenerationEU, Mecanismo para la Recuperación y la Resiliencia (MRR) and SPACKDc PMP21/00109, FEDER funds. This publication is based upon work from COST Action PERMEDIK CA21165, supported by COST (European Cooperation in Science and Technology). PREVENTCKD Consortium. Project ID: 101101220 Programme: EU4H. DG/Agency: HADEA: 2023-2024
DECLARACIÓN DE TRANSPARENCIA
Colaboración con Adviccene, Alexion, Astellas, Astrazeneca, Amicus, Amgen, Boehringer Ingelheim, Fresenius Medical Care, GSK, Bayer, Sanofi-Genzyme, Menarini, Mundipharma, Kyowa Kirin, Lilly, Freeline, Idorsia, Chiesi, Otsuka, Novo-Nordisk, Sysmex y Vifor Fresenius Medical Care Renal Pharma. Director de Catedra UAM-Astrazeneca de enfermedad renal crónica y electrolitos. Acciones en Telara Farma.
BIBLIOGRAFÍA
- ↑KDIGO 2012. Clinical practice guideline for the evaluation and management of chronic kidney disease. Kidney Int Suppl. 2013; 3(1): 1-150.
- ↑Ortiz A, Wanner C, Gansevoort R et al. Chronic kidney disease as cardiovascular risk factor in routine clinical practice: a position statement by the Council of the European Renal Association. Nephrol Dial Transplant. 2023; 38(3): 527-531. doi:10.1093/NDT/GFAC257
- ↑Visseren FLJ, Mach F, Smulders YM et al. 2021 ESC Guidelines on cardiovascular disease prevention in clinical practice. Eur J Prev Cardiol. 2022; 29: 5-115.
- ↑Jager KJ, Kovesdy C, Langham R, Rosenberg M, Jha V, Zoccali C. A single number for advocacy and communication-worldwide more than 850 million individuals have kidney diseases. Nephrol Dial Transpl. 2019; 34: 1803-1805
- ↑Foreman KJ, Marquez N, Dolgert A et al. Forecasting life expectancy, years of life lost, and all-cause and cause-specific mortality for 250 causes of death: Reference and alternative scenarios for 2016-40 for 195 countries and territories. Lancet. 2018; 392(10159): 2052-2090.
- ↑Ortiz A, Cozzolino M, Duivenvoorden R et al. Chronic kidney disease is a key risk factor for severe COVID-19: a call to action by the ERA-EDTA. Nephrol Dial Transplant 2021; 36(1): 87-94.
- ↑Williamson EJ, Walker AJ, Bhaskaran K et al. Factors associated with COVID-19-related death using OpenSAFELY. Nature. 2020; 584: 430-436
- ↑Clark A, Jit M, Warren-Gash C et al. Global, regional, and national estimates of the population at increased risk of severe COVID-19 due to underlying health conditions in 2020: a modelling study. Lancet Glob Heal. 2020; 8: e1003–e1017
- ↑Jager KJ, Kramer A, Chesnaye NC et al. Results from the ERA-EDTA Registry indicate a high mortality due to COVID-19 in dialysis patients and kidney transplant recipients across Europe. Kidney Int. 2020; 98: 1540-1548.
- ↑Ortiz A, Roger M, Jiménez VM et al. RICORS2040: the need for collaborative research in chronic kidney disease. Clin Kidney J. 2021; 15(3): 372-387.
- ↑Boenink R, Astley ME, Huijben JA et al. The ERA Registry Annual Report 2019: summary and age comparisons. Clin Kidney J. 2021; 15(3): 452-472.
- ↑Vanholder R, Annemans L, Bello AK et al. Fighting the unbearable lightness of neglecting kidney health: the decade of the kidney. Clin Kidney J. 2021; 14(7): 1719-1730.
- ↑Vanholder R, Agar J, Braks M et al. The European Green Deal and nephrology: a call for action by the European Kidney Health Alliance. Nephrol Dial Transplant. 2023; 38(5): 1080-1088. doi: 10.1093/ndt/gfac160. PMID: 35481547.
- ↑Heerspink HJL, Stefánsson BV, Correa-Rotter R et al. Dapagliflozin in patients with chronic kidney disease. N Engl J Med. 2020; 383(15): 1436-1446.
- ↑The EMPA-KIDNEY Collaborative Group; Herrington WG, Staplin N, Wanner C et al. Empagliflozin in patients with chronic kidney disease. N Engl J Med. 2023; 388(2): 117-127.
- ↑Anker SD, Butler J, Filippatos G et al. Empagliflozin in heart failure with a preserved ejection fraction. N Engl J Med. 2021; 385(16): 1451-1461.
- ↑Packer M, Anker SD, Butler J et al. Cardiovascular and renal outcomes with empagliflozin in heart failure. N Engl J Med. 2020; 383: 1413-1424.
- ↑Solomon SD, McMurray JJV, Claggett B et al. Dapagliflozin in heart failure with mildly reduced or preserved ejection fraction. N Engl J Med. 2022; 387: 1089-1098.
- ↑McMurray JJV, Solomon SD, Inzucchi SE et al. Dapagliflozin in patients with heart failure and reduced ejection fraction. N Engl J Med. 2019; 381: 1995-2008.
- ↑Perkovic V, Jardine MJ, Neal B et al. Canagliflozin and renal outcomes in type 2 diabetes and nephropathy. N Engl J Med. 2019; 380: 2295-2306.
- ↑Agarwal R, Filippatos G, Pitt B et al; FIDELIO-DKD and FIGARO-DKD investigators. Cardiovascular and kidney outcomes with finerenone in patients with type 2 diabetes and chronic kidney disease: the FIDELITY pooled analysis. Eur Heart J. 2022; 43(6): 474-484.
- ↑Levin A, Perkovic V, Wheeler DC et al. Empagliflozin and cardiovascular and kidney outcomes across KDIGO risk categories: Post hoc analysis of a randomized, double-blind, placebo-controlled, multinational trial. Clin J Am Soc Nephrol. 2020; 15: 1433-1444.
- ↑https://academic.oup.com/ckj/advance-article/doi/10.1093/ckj/sfad082/7199787
- ↑Li PKT, Garcia-Garcia G, Lui SF et al. Kidney health for everyone everywhere-from prevention to detection and equitable access to care. Kidney Int. 2020; 97: 226-232.
- ↑Levey AS, Schoolwerth AC, Burrows NR, Williams DE, Stith KR, McClellan W. Comprehensive public health strategies for preventing the development, progression, and complications of CKD: Report of an expert panel convened by the Centers for Disease Control and Prevention. Am J Kidney Dis. 2009; 53: 522-535.
- ↑Kelly JT, Su G, Zhang L et al. Modifiable lifestyle factors for primary prevention of CKD: a systematic review and meta-analysis. J Am Soc Nephrol. 2021; 32: 239-253.
- ↑Paterson EN, Neville CE, Wallace SM et al. Dietary patterns associated with renal impairment in the Northern Ireland Cohort for the Longitudinal Study of Ageing (NICOLA). Eur J Nutr. 2021; 60: 4045-4054.
- ↑Staessen JA, Janssens S, Van de Werf F. Do clinical trial data suggest a role for SGLT2-inhibitors in primary prevention of heart failure and chronic kidney disease? Int J Cardiol Cardiovasc Risk Prev. 2021; 10: 200100. doi:10.1016/J.IJCRP.2021.200100.
- ↑Wiviott SD, Raz I, Bonaca MP et al. Dapagliflozin and cardiovascular outcomes in type 2 diabetes. N Engl J Med. 2019; 380: 347-357.
- ↑Neal B, Perkovic V, Mahaffey KW et al. Canagliflozin and cardiovascular and renal events in type 2 diabetes. N Engl J Med. 2017; 377: 644-657.
- ↑Wanner C, Inzucchi SE, Lachin JM et al. Empagliflozin and progression of kidney disease in type 2 diabetes. N Engl J Med. 2016; 375: 323-334.
- ↑Mosenzon O, Wiviott SD, Cahn A et al. Effects of dapagliflozin on development and progression of kidney disease in patients with type 2 diabetes: an analysis from the DECLARE-TIMI 58 randomised trial. Lancet Diabetes Endocrinol. 2019; 7: 606-617.
- ↑Mosenzon O, Raz I, Wiviott SD et al. Dapagliflozin and prevention of kidney disease among patients with type 2 diabetes: Post hoc analyses from the DECLARE-TIMI 58 Trial. Diabetes Care. 2022; 45: 2350-2359.
- ↑Bosch C, Carriazo S, Soler MJ, Ortiz A, Fernández-Fernández B. Tirzepatide and prevention of chronic kidney disease. Clin Kidney J. 2022; 16(5):797-808. doi:10.1093/CKJ/SFAC274
- ↑Ortiz A, Ferro CJ, Balafa O et al. Mineralocorticoid receptor antagonists for nephroprotection and cardioprotection in patients with diabetes mellitus and chronic kidney disease. Nephrol Dial Transplant. 2023; 38(1): 10-25.
- ↑Kress S, Bramlage P, Holl RW et al. Validation of a risk prediction model for early chronic kidney disease in patients with type 2 diabetes: Data from the German/Austrian diabetes prospective follow-up registry. Diabetes Obes Metab. 2023; 25(3):776-784. doi:10.1111/DOM.14925
- ↑Tofte N, Lindhardt M, Adamova K et al. Early detection of diabetic kidney disease by urinary proteomics and subsequent intervention with spironolactone to delay progression (PRIORITY): a prospective observational study and embedded randomised placebo-controlled trial. Lancet Diabetes Endocrinol. 2020; 8(4): 301-312.
- ↑Khan A, Turchin MC, Patki A et al. Genome-wide polygenic score to predict chronic kidney disease across ancestries. Nat Med. 2022; 28(7): 1412-1420.
- ↑Choi JG, Winn AN, Skandari MR et al. First-line therapy for type 2 diabetes with sodium-glucose cotransporter-2 inhibitors and glucagon-like peptide-1 receptor agonists : a cost-effectiveness study. Ann Intern Med. 2022; 175(10): 1392-1400.
- ↑Elsayed NA, Aleppo G, Aroda VR et al. 3. Prevention or delay of type 2 diabetes and associated comorbidities: Standards of care in diabetes-2023. Diabetes Care. 2023; 46(Suppl.1): S41-S48.
- ↑Ortiz A, Quiroga B, Díez J et al. Artículo especial por el Día Mundial del Riñón: Las sociedades científicas españolas ante la guía ESC 2021 de prevención de la enfermedad vascular: Generalizar la medida de la albuminuria para identificar el riesgo vascular y prevenir la enfermedad vascular. Nefrología. 2023; 43(2): 245-250.
Alberto Ortiz
IIS-Fundacion Jiménez Díaz
Av Reyes Católicos, 2 · 28040 Madrid
Tlf.: +34 91 159 47 34 | E-Mail: aortiz@fjd.es
Año 2023 · número 140 (02) · páginas 125 a 132
Enviado: 24.06.23
Revisado: 28.06.23
Aceptado: 05.07.23


