Resumen
En este trabajo se resumen una serie de proyectos y líneas de investigación que están desarrollando un grupo de investigadores españoles con alta repercusión internacional.
Los trabajos están relacionados con cambios de paradigmas tanto en desarrollo tumoral como a nivel terapéutico. Incluyendo los conceptos de plasticidad celular y transdiferenciación de células, por la Dra. María Abad, la importancia del metabolismo en fenómenos de transformación y progresión tumoral, por los Dres. Sancho y F. Efeyan, la relación ente inflamación y cáncer, por los Dres. Pardo y Abad, así como el todavía desconocido significado de los micropéptidos, sintetizados a partir de Non-Coding RNA, que pueden suponer un cambio de paradigma en la comprensión de las vías de señalización y otras vías bioquímicas.Es muy relevante el papel de la biopsia líquida, tras como demostró el Dr. Peinado, a nivel del estudio de mutaciones del B-RAF en exosomas en pacientes con melanomas y la realización de la biopsia virtual, con anticuerpos marcados con isótopos a nivel de patología cerebral, por el Dr. Schumacher. Todos estos conceptos necesitan de un apoyo bioinformático evidente y las aportaciones de los Dres. Varela y Quesada, con nuevas herramientas de secuenciación y de interpretación bioinformática suponen un avance extraordinario.
A nivel de tratamiento, destacar el desarrollo de inhibidores de dianas intocables, como la del MYC, por la Dra. Soucek, del fármaco de origen marino Trabectidina, con alta sensibilidad para liposarcomas mixoides y recientemente para carcinomas de pulmón de célula pequeña, el fascinante cambio de paradigma a nivel de la concepción del desarrollo de los tumores a partir de cooperación clonal y con células del microambiente. En este sentido, los trabajos de Manuel Valiente y la activación del factor STAT-3 de astrocitos en casos de metástasis cerebrales, y el aumento de la supervivencia tras su inhibición en ensayos clínicos. Destacar también los trabajos del grupo del Dr. Ramón y Cajal, con la propuesta de nuevos factores centrales de señalización que pueden ser dianas terapéuticas y que aumentan la sensibilidad a tratamientos convencionales y a inmunoterapia, como el factor EIF4E.
En resumen, las aportaciones diversas, tanto en investigación básica del desarrollo de la progresión tumoral como a nivel de nuevas dianas terapéuticas, muestran nuevas perspectivas que pueden suponer cambios de paradigmas de altísimo interés a corto plazo.
Abstract
This paper summarizes a series of projects and lines of research that are being developed by a group of Spanish researchers with high international impact.
The works are related to paradigm changes both in tumor development and at the therapeutic level. Including the concepts of cell plasticity and cell transdifferentiation, by Dr. María Abad, the importance of metabolism in phenomena of tumor transformation and progression, by Drs. Sancho and F. Efeyan, the relationship between inflammation and cancer, by Drs. Pardo and Abad, as well as the still unknown meaning of the micropeptides, synthesized from Non-Coding RNA, which can lead to a paradigm shift in the understanding of signaling pathways and other biochemical pathways.
The role of liquid biopsy is very relevant, after as Dr. Peinado demonstrated, at the level of the study of B-RAF mutations in exosomes in patients with melanomas and the performance of virtual biopsy, with antibodies marked with isotopes at the level of brain pathology, by Dr. Schumacher. All these concepts need an obvious bioinformatic support and the contributions of Drs. Varela and Quesada, with new tools for sequencing and bioinformatics interpretation, represent an extraordinary advance.
At the treatment level, it is worth highlighting the development of untouchable target inhibitors, such as that of MYC, by Dr. Soucek, of the drug of marine origin Trabectidine, with high sensitivity for myxoid liposarcomas and recently for small cell lung carcinomas, the fascinating paradigm shift at the level of the conception of the development of tumors from clonal cooperation and with microenvironment cells. In this sense, the works of Manuel Valiente and the activation of the STAT-3 astrocyte factor in cases of brain metastases, and the increase in survival after inhibition in clinical trials. Also highlight the work of Dr. Ramón y Cajal’s group, with the proposal of new central signaling factors that can be therapeutic targets and that increase the sensitivity to conventional treatments and immunotherapy, such as the EIF4E factor.
In summary, the diverse contributions, both in basic research on the development of tumor progression and at the level of new therapeutic targets, show new perspectives that may imply changes of paradigms of very high interest in the short term.
Palabras clave: Cooperación clonal; Biopsia liquida; Myc; eIF4E.
Keywords: Clonal cooperation; Liquid biopsy; Myc; eIF4E.
Apoyo financiero: SRYC admite el apoyo del Fondo de Investigaciones Sanitarias (P1170185, PI17/000564), Generalitat de Catalunya (AGAUR, 2017 SGR 9015), y CIBERONC 2017 (CB16/12/00363).
INTRODUCCIÓN
En los últimos años ha habido avances relevantes en la investigación del cáncer y en el tratamiento basado en alteraciones genéticas específicas que mejoran la supervivencia en algunos tumores. Sin embargo, el progreso sigue siendo discreto o malo en la mayoría de los carcinomas cuando se diseminan con metástasis; La supervivencia es inferior al 30% de los casos.
Por tanto, debemos avanzar en busca de nuevos paradigmas que puedan explicar los complejos mecanismos involucrados en la carcinogénesis y en los nuevos enfoques de tratamiento.
Con estos objetivos, nos reunimos en julio, del 2019 en el Pirineo aragonés, un grupo de 15 científicos que realizan investigaciones en España y que están cambiando muchos paradigmas en la investigación y desarrollando proyectos disruptivos. En una reunión de tres días, compartimos ideas y establecimos un marco ideal de colaboración, donde patólogos, oncólogos, biólogos, bioinformáticos y científicos de datos, en conjunto, buscaron nuevos enfoques y equipos sinérgicos. La mayoría de los investigadores tienen menos de 45 años y sus descubrimientos y talento sobresalientes nos hicieron ser optimistas para los grandes avances en los próximos años.
Algunos de los aspectos más destacados de la reunión se pueden resumir en los siguientes puntos:
1.-La propuesta de nuevos paradigmas en la investigación del cáncer:
a) La reprogramación celular y la plasticidad celular, en biología y cáncer, de la Dra. Maria Abad, que pueden explicar la heterogeneidad intratumoral y la dinámica de la progresión tumoral. La plasticidad celular es la capacidad de las células para transitar entre diferentes estados o identidades celulares, incluidas las transiciones entre estados epiteliales y mesenquimales, o entre estados diferenciados y desdiferenciados. El paradigma de la plasticidad celular está representado por las células madre embrionarias, que son capaces de generar todas las células especializadas que forman nuestro organismo adulto. El Dr. Yamanaka demostró en 2006 que podemos convertir células adultas especializadas en células madre embrionarias (llamadas iPS, de células madre pluripotentes inducidas) a través de un proceso llamado reprogramación celular. Más tarde, sus investigaciones mostraron que somos capaces de inducir la reprogramación celular dentro de los organismos vivos. (1)
La reprogramación celular tiene un potencial inmenso en la medicina regenerativa, ya que abre la posibilidad de generar células madre que a su vez regeneran cualquier tipo de célula dañada. Sin embargo, hoy sabemos que este proceso es un mecanismo que utilizan los tumores para generar, mantenerse y sobrevivir a terapias como la radio o la quimioterapia.
b) El papel del metabolismo celular en la transformación y la progresión tumoral, tal como lo presentó la Dra. Patricia Sancho (2), especialmente enfocado en vías metabólicas activas en células altamente agresivas como las células madre tumorales, como nuevas estrategias terapéuticas. La importancia de las enzimas mitocondriales en el desarrollo de muchos tumores está siendo clave para el diagnóstico de ellos, como IDH1 en los tumores cerebrales. Del mismo modo, el Dr. Alejo Efeyan enfatizó que el metabolismo reprogramado es un sello distintivo de las células tumorales, ya que la mayoría de las mutaciones seleccionadas en el cáncer aumentan la absorción de nutrientes, estimulan el anabolismo e incluso tienen un efecto negativo en el metabolismo del paciente. Afortunadamente, las demandas energéticas asociadas con las mutaciones oncogénicas constituyen una vulnerabilidad potencial que muchos laboratorios están tratando de enumerar y comprender, para luego explotarlas terapéuticamente. En particular, el Dr. Efeyan identificó vulnerabilidades de los linfomas foliculares causados por la activación de mutaciones en la cascada de señalización de nutrientes aguas arriba de la mTOR quinasa, un regulador maestro del anabolismo. El Dr. Efeyan describió la sensibilidad selectiva de este grupo de tumores a la inhibición farmacológica de mTOR usando ratones genéticamente modificados (3).
c) Los nuevos enfoques de inflamación y cáncer por el Dr. Julián Pardo y la Dra. María Abad, quienes contribuyeron en las presentaciones de datos que apoyan la relación entre la inflamación y el desarrollo de algunos tumores, así como la plasticidad y el cambio del fenotipo celular (4).
Los datos experimentales y clínicos más recientes sugieren que la relación entre la inflamación y el cáncer no se limita al inicio del proceso carcinogénico sino que, además, la composición del microambiente inflamatorio afecta el resultado de la terapia contra el cáncer, incluidos los tratamientos tradicionales como quimioterapia o radioterapia, así como los avances más recientes en productos biológicos e inmunoterapias. Sobre esta base, el Dr. Pardo revisó las nuevas posibilidades de modular selectivamente la respuesta inmune inflamatoria para prevenir el desarrollo del cáncer o tratarlo, minimizando los posibles efectos secundarios.
d) El significado aún desconocido de los micropéptidos, presentado por la Dra. Maria Abad, en biología celular y cáncer. Se derivan de secuencias que hasta hace poco se consideraban no codificantes para ADN, ARN no codificante largo, que tienen perspectivas impresionantes para la comprensión de la biología actual.
e) El diagnóstico en biopsias líquidas de marcadores oncogénicos, pronósticos y terapéuticos basados en exosomas liberados por las células tumorales a la sangre. El trabajo pionero de Hector Peinado en melanoma y en clínica (5).
c) La realización de la biopsia virtual para el diagnóstico por el Dr. Alberto J. Schuhmacher que combina la selectividad y la especificidad de los anticuerpos hacia un determinado marcador de células tumorales con imágenes de tomografía por emisión de positrones (PET) para generar inmuno-PET. Esta “biopsia virtual” es equivalente a realizar el diagnóstico no invasivo y la monitorizacion de pacientes a lo largo del tiempo, utilizando una aproximación de tipo inmunohistoquímica in vivo, integrada, cuantificable, 3D y de cuerpo completo. Este enfoque permitirá el diagnóstico de tumores donde el acceso por biopsia es imposible o puede conducir a una gran morbilidad en los pacientes. Estudios previos le están permitiendo proponer dianas especificas de los tumores y métodos para aislara poblaciones inmunes (6)
e) Los nuevos enfoques bioinformáticos y el análisis de secuenciación masiva. Los Dres. Ignacio Varela y Víctor Quesada (7,8) presentaron las herramientas que utilizan para los estudios de secuenciación masiva y para la secuenciación de células individuales. El Dr. Varela estudia desde una perspectiva bioinformática y molecular la heterogeneidad genética y funcional dentro de los tumores y su posible papel en la progresión tumoral y la metástasis. El Dr. Quesada resumió su contribución al nodo español del Consorcio Internacional del Genoma del Cáncer, estudiando la leucemia linfocítica crónica (CLL). Esta contribución incluyó el desarrollo del algoritmo Sidrón, que tiene en cuenta el proceso de secuenciación de alto rendimiento para mejorar la llamada al genotipo y filtrar los artefactos. Al aplicar esta herramienta a muestras emparejadas CLL / normales, este grupo descubrió nuevas vías bioquímicas involucradas en la tumorigénesis de CLL, tales como empalme, protección de telómeros y proteostasis. Estos resultados ilustran cómo la complejidad del desarrollo del cáncer puede conducir a futuras estrategias clínicas para enfatizar dos conceptos existentes: personalización y transversalidad. En cuanto a la personalización, los patrones mutacionales en CLL son extremadamente heterogéneos; Incluso diferentes mutaciones que afectan al mismo gen pueden tener diversos efectos bioquímicos. Por otro lado, algunos de los mecanismos novedosos de la tumorigénesis de la CLL juegan un papel importante en los tumores no relacionados, lo que sugiere que las estrategias transversales pueden ser útiles.
2.- La presentación de nuevos enfoques en el tratamiento del cáncer:
a) Basado en inhibir las llamadas “dianas intocables”, como los genes Myc, RAS,… El excelente trabajo de la Dra. Laura Soucek (9), quien ha desarrollado el primer inhibidor contra el factor de transcripción Myc basado en un péptido penetrante celular (Omomyc) con acción negativa dominante y que ya está en desarrollo clínico. La mini proteína purificada Omomyc se comporta como un péptido que penetra en las células y podría usarse como un fármaco. Esta característica novedosa e inesperada nos permitió tratar el cáncer de pulmón de células no pequeñas (NSCLC) in vitro e in vivo, mostrando una eficacia significativa y un excelente perfil de seguridad. Finalmente, gracias a un esfuerzo continuo durante más de 20 años, Omomyc alcanzará los ensayos clínicos en 2020 para el NSCLC y el cáncer de mama y, si se demuestra su eficacia, podría aplicarse a muchas más indicaciones oncológicas. (Figura 1)
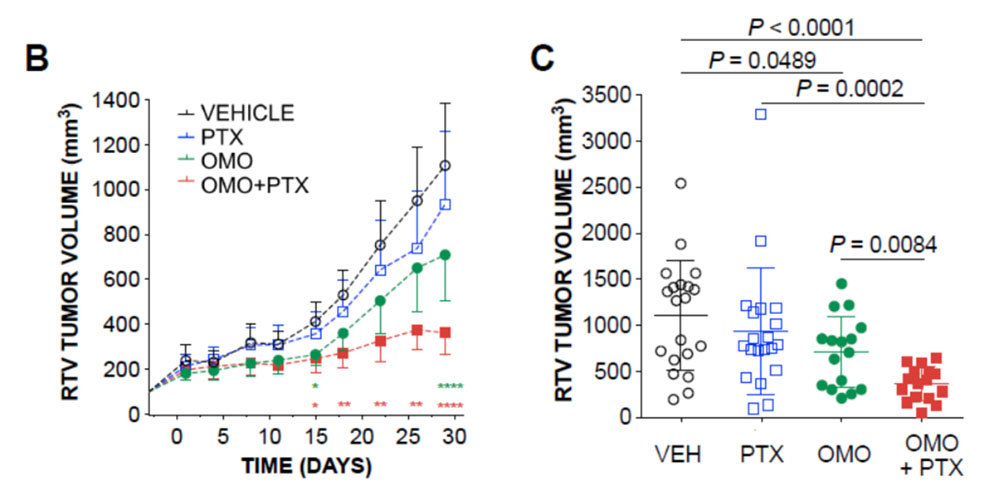
b) La presentación de un novedoso agente antitumoral, Trabectidina, de origen marino, Dr. José Jimeno (10). Presentó cómo se puede desarrollar la trabectidina, un fármaco anticancerígeno derivado del mar a través de la fusión de evidencia clínica y biología molecular: el modelo conduce a la identificación de pacientes con sarcoma de tejidos blandos, específicamente liposarcoma mixto de células redondas con t12; 16 que conducen al CHOP FUS gen de fusión: se puede lograr una tasa de 90% de respuestas duraderas y control tumoral, además, si se excluyen las translocaciones tipo III, el modelo de intervención terapéutica en estos pacientes con Trabectidina logra una tasa cien por ciento de control tumoral que incluye respuestas que duran más de 2 años. (Figura 2)

c) Basado en la heterogeneidad intratumoral, el nuevo paradigma de cooperación de clones tumorales y células del microambiente (fibroblastos, células vasculares, células gliales, células inflamatorias). El Dr. Manuel Valiente (11) presentó su trabajo para comprender el desarrollo de metástasis a nivel cerebral, con resultados terapéuticos muy novedosos basados en la prevención de la comunicación de las células tumorales con las células de la glía cerebral. Las células de metástasis a medida que crecen modifican el cerebro y lo transforman en un entorno que, a diferencia de lo que sucede en las etapas iniciales, protege las células metastásicas. Hemos identificado vías de señalización que marcan este microambiente alterado que promueve la metástasis, hemos diseccionado los mecanismos funcionales de la comunicación metástasis-microambiente y hemos generado una prueba de concepto pionera de la aplicación de esta biología a una nueva terapia que ha demostrado ser muy exitosa. solo en ratones pero también en pacientes. Estos hallazgos sugieren que una nueva vía potencial para mejorar las terapias antimetastásicas podría ser tener en cuenta los mecanismos de supervivencia específicos de los órganos que desarrollan las células cancerosas durante la colonización de cada órgano secundario. De hecho, esto podría generar en el futuro una novedosa terapia personalizada para la metástasis en la que se proporcionarían medicamentos específicos para desafiar la viabilidad de las células cancerosas que atienden a los órganos moleculares clave específicos de cada órgano. (Figura 3 y 4)
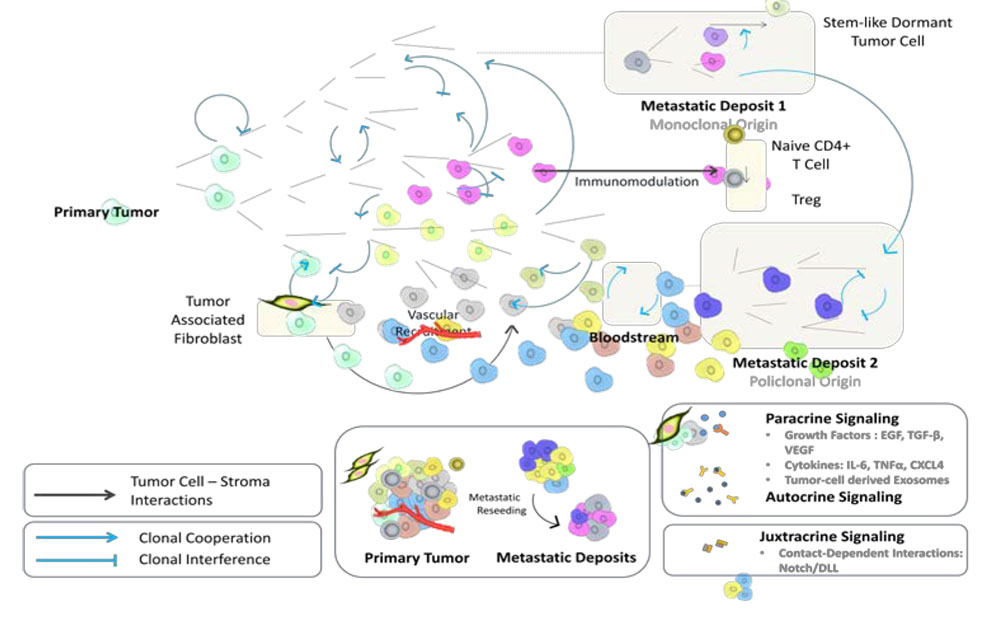
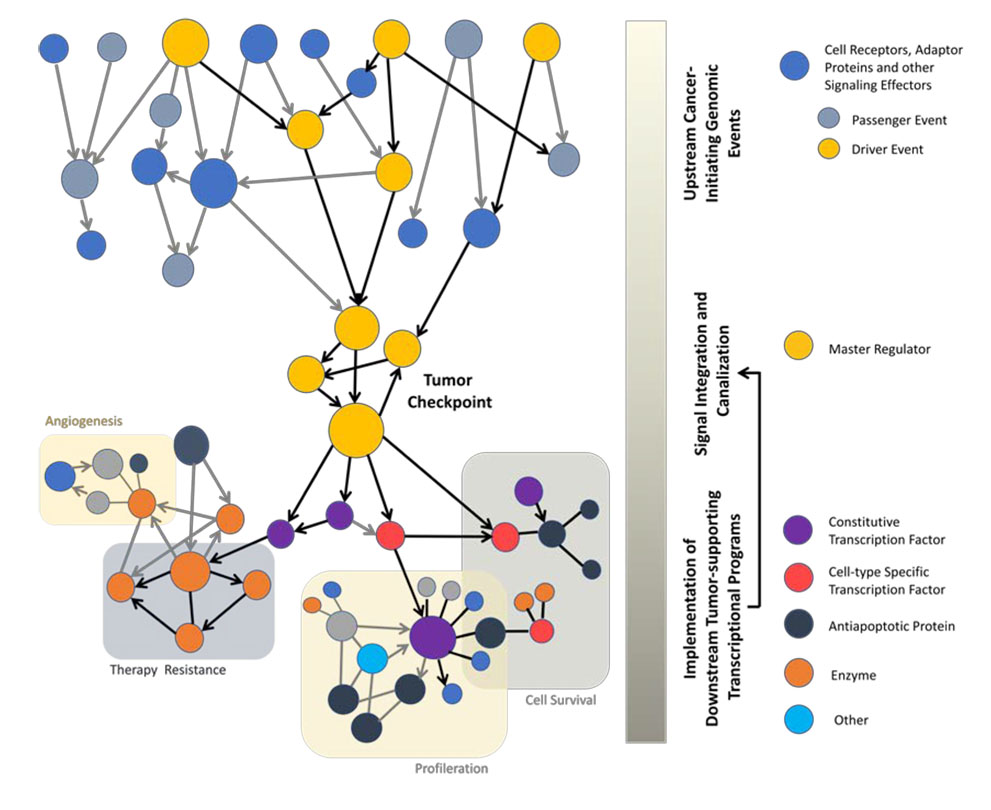
d) Buscando factores de embudo o centrales de señalización, el Dr. Ramón y Cajal (12,13) presentó los datos clínicos de la expresión de factores de señalización en tumores humanos. La expresión fue bastante heterogénea en la mayoría de ellos (pAKT, pmtor, pMAPK, pS6) pero 4EB-P1 y especialmente peIF4E que se sobreexpresaron en las células tumorales. La heterogeneidad de otros factores de señalización puede estar asociada con factores locales como hipoxia, estrés oxidativo, inanición … Debido a que peIF4E confiere resistencia a muchos estreses celulares y medicamentos contra el cáncer, presentó un nuevo inhibidor de la quinasa MNKS que fosforila eIF4E, desarrollado por el grupo del Instituto Químico Sarriá. Se presentó una propuesta de tratamiento basada en la combinación de quimioterapia anti-peIF4E más quimioterápicos tipo doxorubicina. (Figura 5)
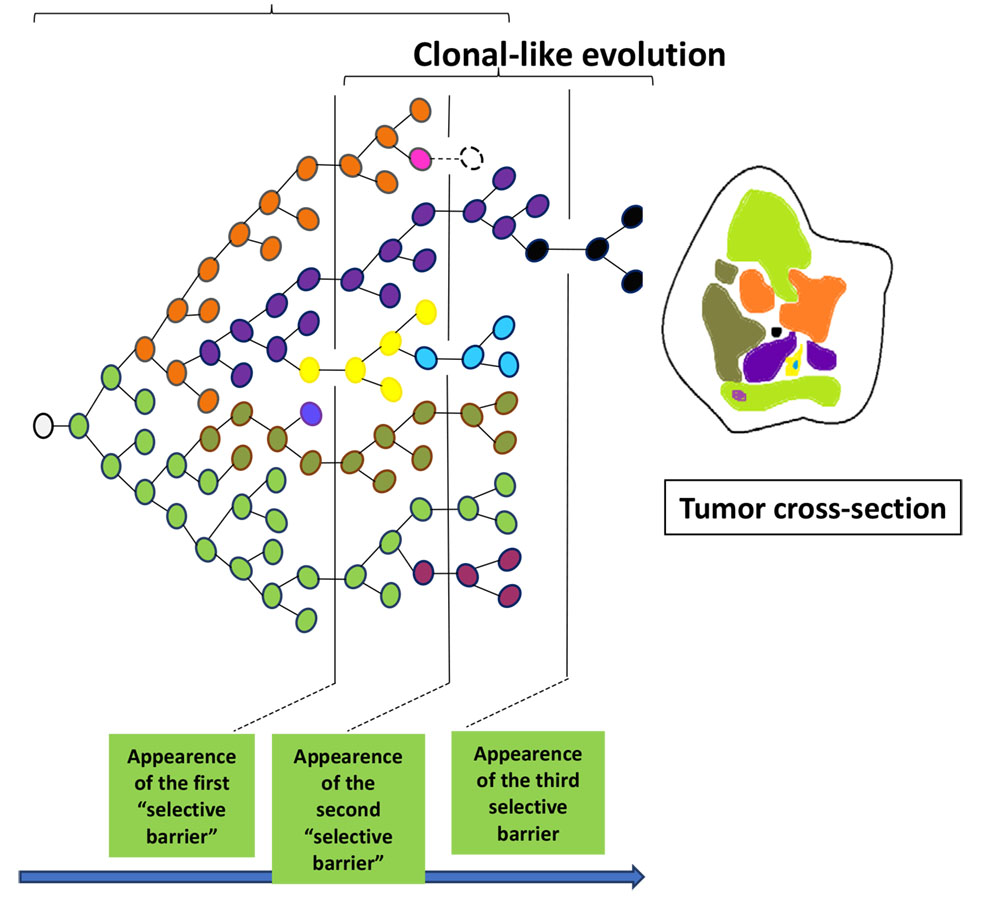
e) Proyectos basados en el bloqueo de la comunicación celular y con el microambiente (14,15). La Dra. Pilar Martín-Duque, el Dr. Santiago Ramón y Cajal y el Dr. Héctor Peinado presentaron nuevos enfoques terapéuticos basados en prevenir la comunicación celular y evitar el desarrollo de metástasis. El Dr. Martin-Duque está buscando “Caballos de Troya”, como vectores para transferir estas y otras terapias selectivamente a los tumores, evitando la toxicidad o los efectos secundarios en otros órganos. Hasta ahora, su grupo ha identificado varios de estos vectores utilizándolos con tratamientos propios o de sus colaboradores, como nanopartículas, drogas o virus. El Dr. Ramón y Cajal demostró que al inhibir la expresión la integrina B3, la entrada de exosomas disminuye muy significativamente y, por lo tanto, la comunicación celular, abriendo nuevas vías para prevenir la metástasis, evitando la comunicación entre clones tumorales y con céluls del microambiente.
CONCLUSIONES
En resumen, nuevos paradigmas y proyectos disruptivos vienen con perspectivas prometedoras e integradora (16). Solicitamos una mayor inversión en redes de fortalecimiento científico y equipos de investigación que promuevan investigaciones disruptivas que casi nunca son financiadas por las agencias estatales. La propuesta puede estar favoreciendo fiscalmente las donaciones privadas que pueden ayudar a las obras basadas en nuevos paradigmas y que las agencias estatales apoyan con aproximadamente el 20% de su presupuesto a las ideas disruptivas de los investigadores como lo hacen las empresas tecnológicas más exitosas.
BIBLIOGRAFÍA
- Abad M, Mosteiro L, Pantoja C, et al. Reprogramming in vivo produces teratomas and iPS cells with totipotency features. Nature. 2013; 502(7471):340-345
- Jagust P, de Luxán-Delgado B, Parejo-Alonso B, Sancho P. Metabolism-Based Therapeutic Strategies Targeting Cancer Stem Cells. Front Pharmacol. 2019; 10:203.
- Ortega-Molina A, Deleyto-Seldas N, Carreras J, et al. Oncogenic Rag GTPase signaling enhances B cell activation and drives follicular lymphoma sensitive to pharmacological inhibition of mTOR. Nat Metab. 2019; 1(8):775-789.
- Lanuza PM, Pesini C, Arias MA, Calvo C, Ramirez-Labrada A, Pardo J.Recalling the Biological Significance of Immune Checkpoints on NK Cells: A Chance to Overcome LAG3, PD1, and CTLA4 Inhibitory Pathways by Adoptive NK Cell Transfer? Front Immunol. 2020; 10:301
- García-Silva S, Benito-Martín A, Sánchez-Redondo S, et al. Use of extracellular vesicles from lymphatic drainage as surrogate markers of melanoma progression and BRAF V600E mutation. J Exp Med. 2019; 216(5):1061-1070
- Godino J, Schuhmacher AJ. Determination and Isolation of Immune Populations from Brain Tumor Microenvironments. Methods Mol Biol. 2019; 1884:177-188
- Quesada V, Araujo-Voces M, Pérez-Silva JG, Velasco G, López-Otín C. Genome Sequencing and Analysis Methods in Chronic Lymphocytic Leukemia. Methods Mol Biol. 2019; 1881:319-325.
- González-Silva L, Quevedo L, Varela I. Tumor Functional Heterogeneity Unraveled by scRNA-seq Technologies. Trends Cancer. 2020; 6(1):13-19.
- Massó-Vallés D, Beaulieu ME, Soucek L. MYC, MYCL and MYCN as therapeutic targets in lung cancer. Expert Opin Ther Targets. 2020 Jan 31.
- Jimeno J, Aracil M, Tercero JC. Adding pharmacogenomics to the development of new marine-derived anticancer agents. J Transl Med. 2006 Jan 9; 4:3.
- Priego N, Zhu L, Monteiro C, et al. STAT3 labels a subpopulation of reactive astrocytes required for brain metastasis. Nat Med. 2018; 24(7):1024-1035
- Ramón Y Cajal S, Sesé M, Capdevila C, et al. Clinical implications of intratumor heterogeneity: challenges and opportunities. J Mol Med (Berl). 2020; 98(2):161-177
- Ramon y Cajal S, Castellvi J, Hümmer S, Peg V, Pelletier J, Sonenberg N. Beyond molecular tumor heterogeneity: protein synthesis takes control. Oncogene. 2018; 37(19):2490-2501.
- Martín-Pardillos A, Valls Chiva Á, Bande Vargas G, et al. The role of clonal communication and heterogeneity in breast cancer. BMC Cancer. 2019; 19(1):666.
- Sancho-Albero M, Encabo-Berzosa MDM, Beltrán-Visiedo M, et al. Efficient encapsulation of theranostic nanoparticles in cell-derived exosomes: leveraging the exosomal biogenesis pathway to obtain hollow gold nanoparticle-hybrids. Nanoscale. 2019; 11(40):18825-18836.
- Ramón Y Cajal S, Hümmer S, Peg V, et al. Integrating clinical, molecular, proteomic and histopathological data within the tissue context: tissunomics. Histopathology. 2019; 75(1):4-19.
DECLARACIÓN DE TRANSPARENCIA
El autor/a de este artículo declara no tener ningún tipo de conflicto de intereses respecto a lo expuesto en la presente revisión.
ranm tv
Santiago Ramón y Cajal
Real Academia Nacional de Medicina de España
C/ Arrieta, 12 · 28013 Madrid
Tlf.: +34 91 159 47 34 | sramon@vhebron.net
Año 2019 · número 136 (03) · páginas 256 a 261
Enviado*: 15.10.19
Revisado: 24.10.19
Aceptado: 17.11.19
* Fecha de lectura en la RANM


