Resumen
En 1987 se demostró que el Óxido Nítrico (NO) era el Factor de Relajación Derivado del Endotelio, y se abrió una extensa historia donde se ha ido confirmado que el NO se sintetiza en todos los tejidos a través de las sintasas constitutivas endotelial y del sistema nervioso y la sintasa inducible en células del sistema inmunológico. Paralelamente se comprobó que los nitrovasodilatadores (NVD), como la Nitroglicerina (NTG) se transforman en NO y es a través de la acción de la Vía NO/GMPc como desarrollan su acción vasodilatadora. En 1990, comprobamos que la NTG transdérmica además de su acción relajadora de la célula lisa muscular, tenía una acción antiinflamatoria, en procesos inflamatorios accesibles por esta vía, como la Tromboflebitis Superficial o la Tendinitis del Supraespinoso. Diez años después otros autores comenzaron a confirmar este efecto de la NTG transdérmica, confirmando la primacía de nuestras publicaciones en la descripción de esta acción.
Abstract
In 1987, it was demonstrated that nitric oxide (NO) is the endothelium-derived relaxing factor (EDRF). This opened a long history of confirming that NO is synthesized in all tissues through constitutive synthases in the endothelium and nervous system, and inducible synthases in cells of the immune system. In parallel, it was proven that nitrovasodilators (NVDs), such as Glyceryl Trinitrate (GTN), are transformed into NO and develop their vasodilatory action through the action of the NO/cGMP pathway. In 1990, we verified that transdermic GTN, in addition to relaxing smooth muscle cells, also had anti-inflammatory effects in inflammatory processes accessible via this route, such as Superficial Thrombophlebitis or Supraspinatus Tendonitis. Ten years later, other authors began to confirm this effect of transdermal GTN, confirming the primacy of our publications in the description of this action.
Palabras clave: Óxido Nítrico (NO); Nitroglicerina (NTG); Gliceril Trinitrato (GTN); Tromboflebitis superficial; Tendinitis.
Keywords: Nitric Oxide (NO); Nitroglycerin (NTG); Glyceryl trinitrate (GTN); Superficial thrombophlebitis; Tendinitis.
DESCUBRIMIENTO DEL OXIDO NITRICO
En 1980, Robert Furchgott publicó un trabajo crucial en el que mostró que la acetilcolina (ACh) necesitaba la presencia del endotelio para ejercer su acción vasodilatadora (1). Sin el endotelio, la ACh causaba constricción. Esto demostró que la relajación vascular requiere la presencia de células endoteliales y que la ACh, al actuar sobre los receptores muscarínicos, estimula la liberación de una sustancia que denominó Factor de Relajación Derivado del Endotelio (Endothelium Derived Relaxing Factor) (EDRF) (2).
En los siguientes años, numerosas investigaciones demostraron que el EDRF, entre otras muchas propiedades, produce la relajación del músculo liso vascular (MLV), activando la guanilato ciclasa (GC) y elevando el Guanidín Monofosfato cíclico (GMPc).
En 1987, Moncada y colaboradores, fueron los primeros en demostrar que las células endoteliales en cultivo liberan EDRF, con efectos biológicos idénticos al Óxido Nïtrico (NO), en la cascada de baño de órganos, y que el EDRF y NO tienen el mismo espectro lumínico por quimioluminiscencia en su reacción con el Ozono (3).
Poco después, el grupo de Moncada descubrió que el NO se sintetiza a partir de la L-arginina (4). Esta vía enzimática L-arginina–NO–GMPc se confirmó también en el sistema nervioso, y en la regulación de la función plaquetaria. Se aislaron también las sintasas del NO, siendo unas constitutivas en tejidos como el endotelio y el cerebro, dependientes del Ca2+ y la calmodulina, y otras inducibles en células fagocíticas.
El entendimiento funcional de esta vía se logró gracias a análogos de la L-arginina que bloquean las sintasas, como la L-NG monometil arginina (L-NMMA) (5). Estos análogos permitieron demostrar que el NO regula el tono vascular arterial periférico, y su inhibición puede causar hipertensión arterial (6).
La expresión de la sintasa inducible y el aumento del NO en el tejido vascular explican la reducción del tono vascular en el shock endotóxico, efecto que puede ser inhibido por corticoides como la dexametasona (7) por el análogo L- N-iminoetil-ornithina (L-NIO).
ÓXIDO NÍTRICO Y FÁRMACOS NITROVASODILATADORES
El descubrimiento del NO permitió completar la historia de los fármacos nitrovasodilatadores (NVD), que comenzó con la síntesis del Nitrito de Amilo en 1844 (8) y más tarde de la nitroglicerina (NTG) como vasodilatador para la angina de pecho. En la primera mitad del siglo XX, se pensaba que la NTG ejercía su acción al transformarse en NO2 y NO3, pero más tarde se demostró que los nitratos orgánicos inducían una elevación de GMPc en el músculo liso, igual que el NO.
Feelisch y Noak demostraron que los NVD generaban NO en reacción con la cisteína, siendo el responsable principal de su mecanismo de acción (9). Los NVD tienen múltiples aplicaciones en las enfermedades cardiovasculares (CV), incluyendo en la angina de pecho y la insuficiencia cardíaca. También se usan en enfermedades vasculares periféricas, o como broncodilatadores y en tratamiento del glaucoma, entre otras aplicaciones.
La NTG transdérmica se ha empleado en el tratamiento de la enfermedad de Raynaud y en la prevención de la tromboflebitis. Aunque inicialmente se pensaba que el mecanismo de acción de la NTG podría deberse a la reducción en la síntesis de prostaciclina, se demostró que el NO actúa como analgésico periférico a través de la activación del GMPc (10).
En resumen, el NO donado por la NTG juega un papel dual en la regulación del dolor, mediando la nocicepción e induciendo un efecto analgésico, liberándose en localizaciones con inflamación y modulando la formación de edema. (11)
ACCIÓN ANTIINFLAMATORIA Y ANALGÉSICA DE LOS FÁRMACOS NVD O DONADORES DE NO COMO LA NITROGLICERINA
Basados en el hecho de que el NO además de ser un mediador de la relajación de la CLM, es un mediador biológico (12) que ejerce en el sistema nervioso una acción dual nociceptiva y antinociceptiva, y en el sistema inmunitario es mediador de acciones pro y antiinflamatorias, establecimos la hipótesis de que los fármacos NVD, donadores de NO como la NTG, podrían tener acción antiinflamatoria y analgésica.
Elegimos como modelo experimental, la tromboflebitis superficial (TFS), por su alta incidencia, fácil diagnóstico y por ser accesible a tratarse con NTG en pomada por vía transdérmica. Publicamos el tratamiento de prueba, antes del ensayo clínico, del caso de un paciente con tromboflebitis superficial post infusión en el antebrazo izquierdo, con dolor, rubefacción, edema perivenoso y cordón fibroso venoso. A las 24 horas de la administración de 2 cm de pomada equivalente a 12 mg de NTG, el dolor, el eritema y el edema se redujeron significativamente y el paciente fue dado de alta ese día (13).
El siguiente fue un estudio prospectivo, doble ciego y aleatorizado en 40 pacientes con tromboflebitis post infusión. A las 48 horas, el índice analgésico fue de 84,6 ± 18 unidades con NTG frente a 49 ± 45 unidades con pomada heparinoide (P<0,01). Todos los signos de la tromboflebitis desaparecieron en menos de 4 días en el grupo NTG en comparación con 9 días en el grupo control (P<0,005). Solo 2 pacientes en el grupo NTG presentaron cefalea. Además de concluir que la NTG transdérmica era una terapia útil para la tromboflebitis relacionada con la infusión, confirmamos que la NTG y los NVD tienen un efecto antiinflamatorio y analgésico, mediado por GMPc, el mismo mecanismo que induce la dilatación del MLV y explica la acción analgésica de la Ach en el sistema nervioso periférico. También se observó un alivio más rápido del edema en el grupo tratado con NTG , demostrando propiedades antiagregantes similares al NO endógeno. Estos mecanismos explican los efectos antiinflamatorios y analgésicos obtenidos con NTG o Gliceril trinitrato (GTN) (14) Figura 1.
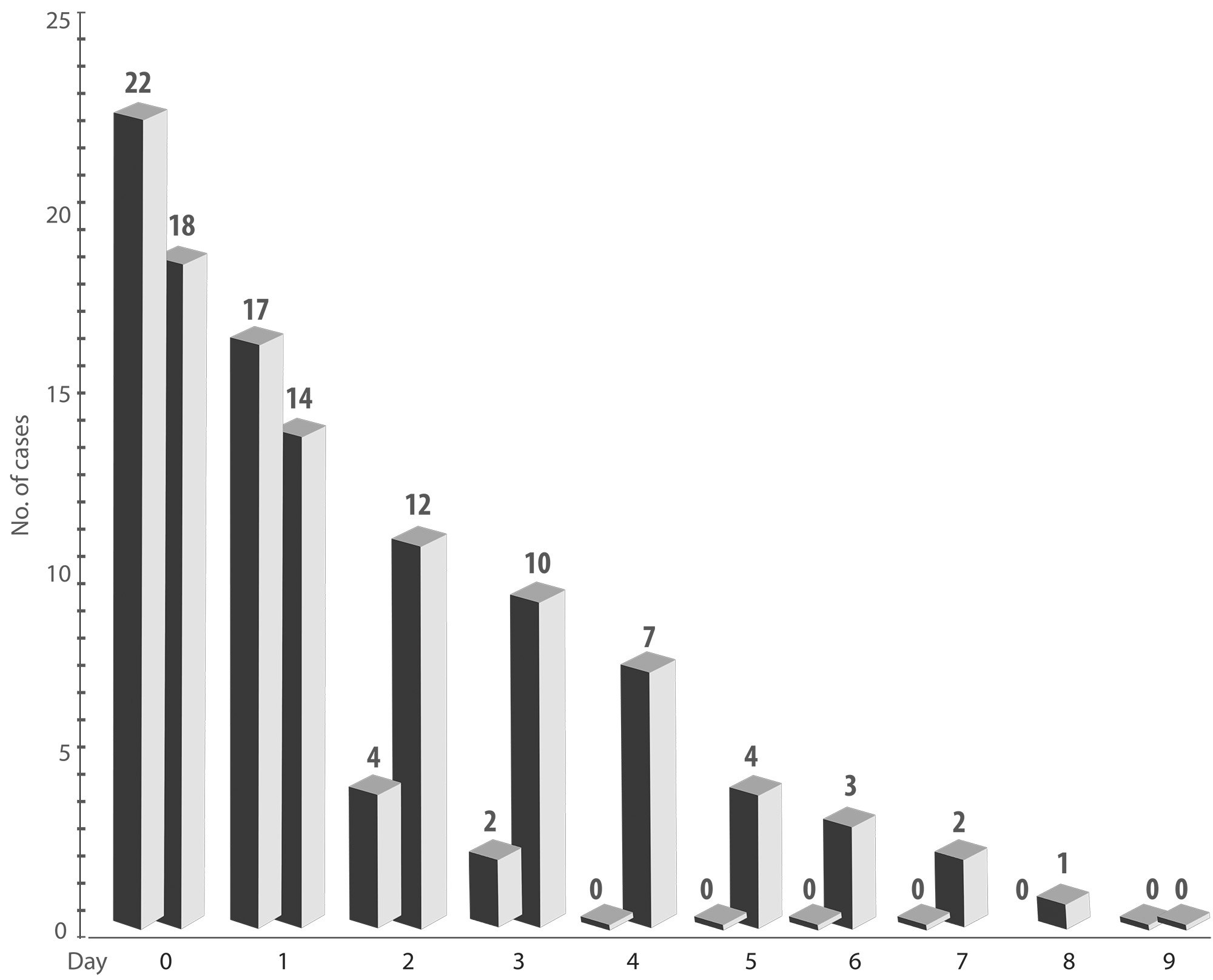
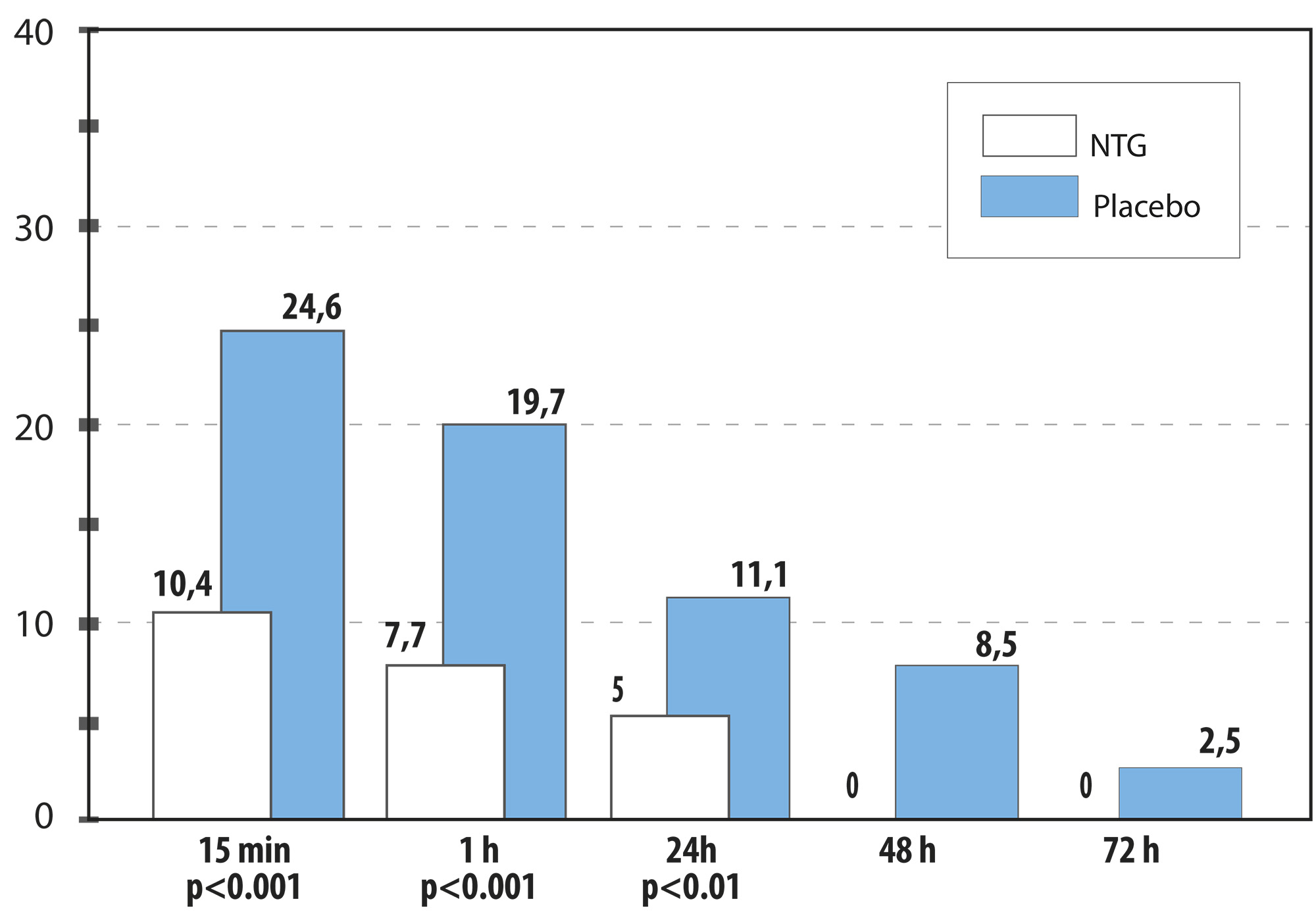
Para reproducir estos resultados recurrimos a un modelo de tromboflebitis inducido por escleroterapia de varices superficiales. Se aleatorizaron las venas de ambas extremidades inferiores y se aplicó gel de NTG al 2% en dosis de 6 mg (un cm.) o pomada placebo en la otra pierna. Los pacientes fueron evaluados registrando signos de TF inmediatamente después de la primera aplicación del gel, a los quince minutos, y a las horas 1, 24, 48 y 72 después de iniciado el tratamiento. Tras la aplicación del tratamiento, la intensidad de los signos de inflamación se valoró en un 26% (10,4 ±4,1) en las venas tratadas con NTG y en un 61,5% (24,6 ±6,3) (P < 0,001) en las venas tratadas con placebo. La reducción en la intensidad de los signos fue de 7,7 ±3,9 en el grupo NTG y 19,7 ±6,3 en el grupo placebo (P <0,001). Concluimos que la NTG tiene un efecto antiinflamatorio en la TF inducida por escleroterapia (15). (Figura 2 a y 2b)
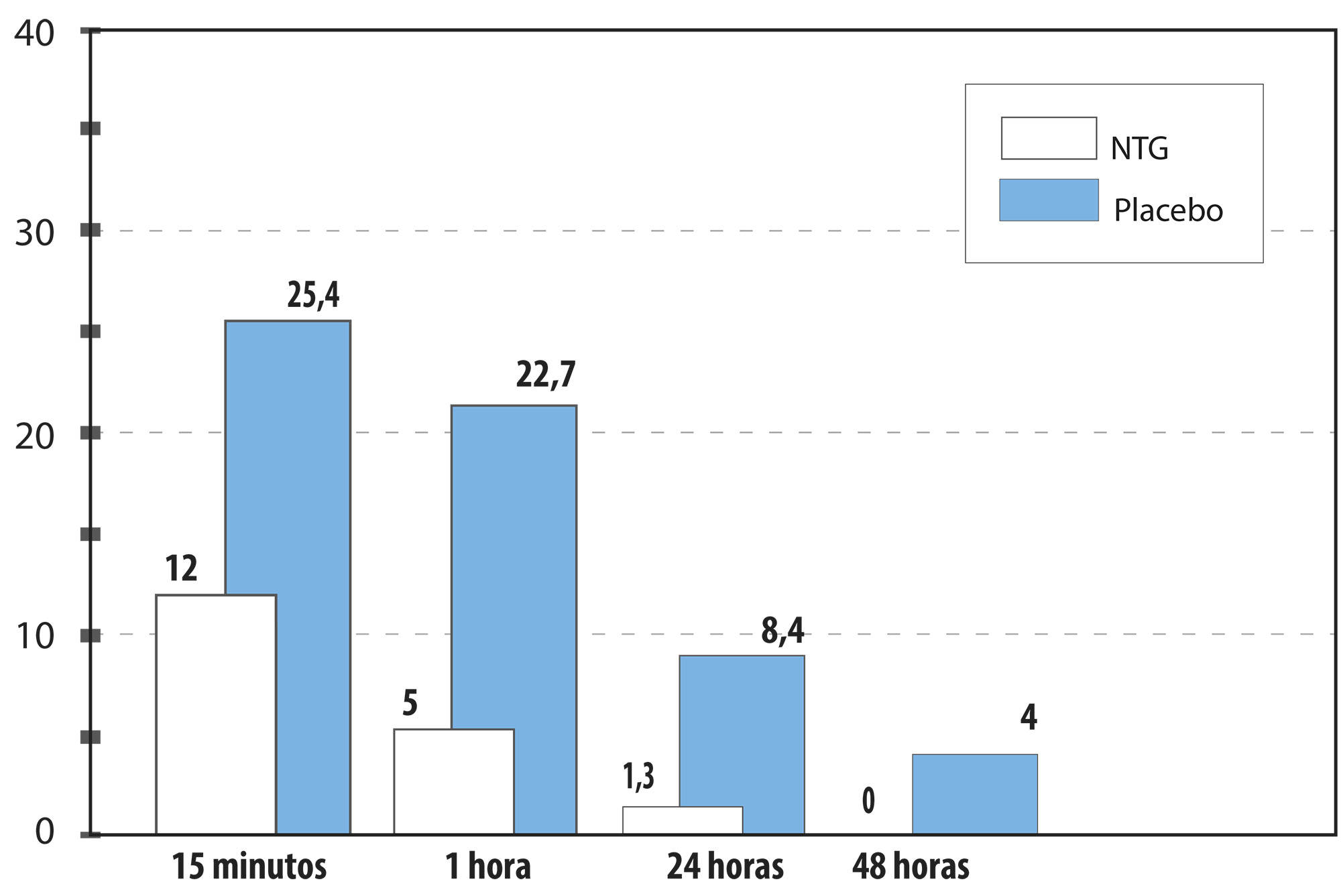
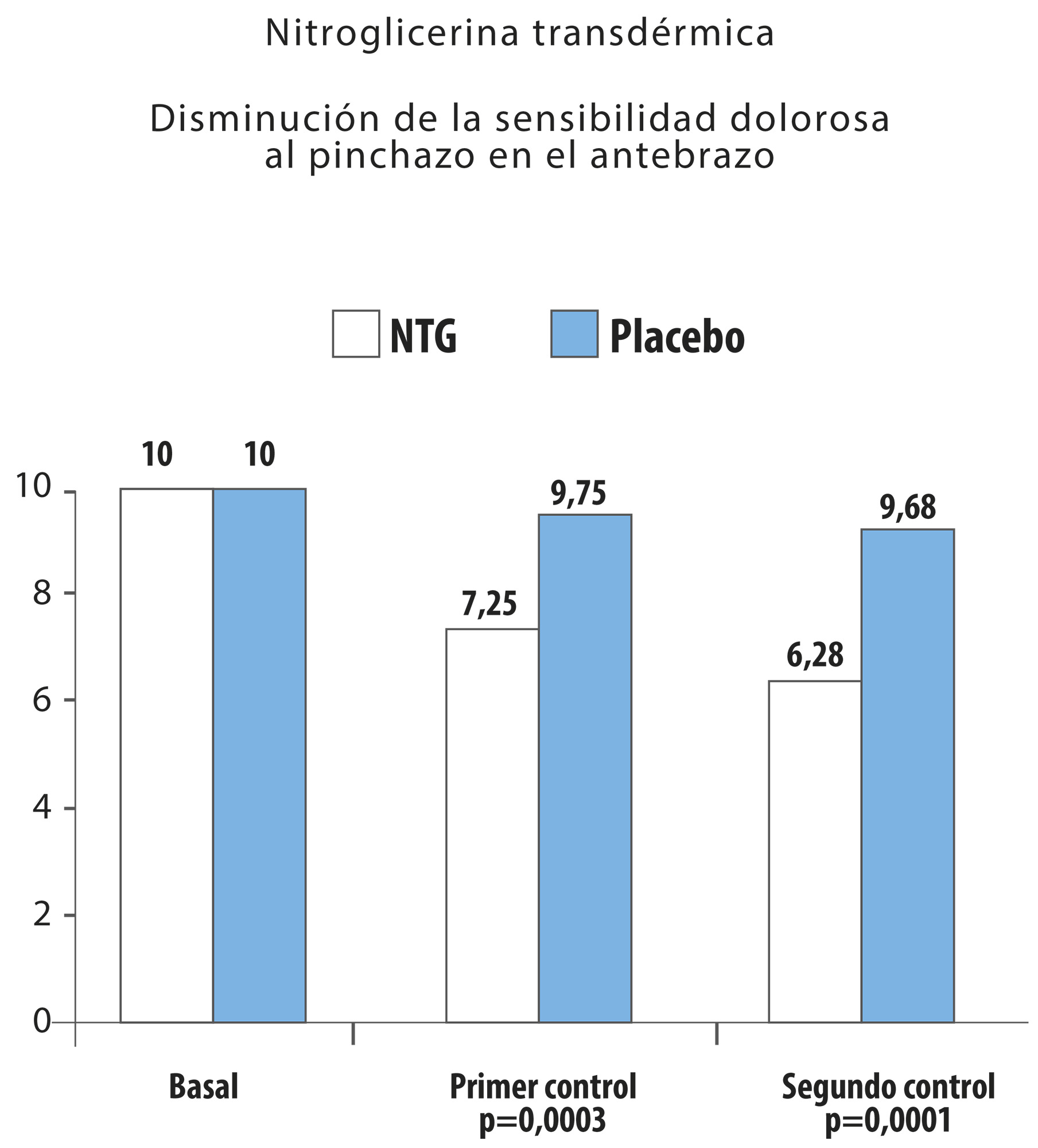
Continuando con la investigación clínica de la posible acción antiinflamatoria y analgésica de la NTG, realizamos un estudio de la sensibilidad dolorosa del antebrazo (16) en 16 voluntarios sanos con el pinprick test. En todos los casos, la sensibilidad basal fue simétrica entre ambos antebrazos, y expresada en la escala analógica visual, en el nivel máximo como 10. Dos sujetos presentaron una reducción de la sensibilidad al dolor más intensa con el placebo que con la NTG. Un sujeto no presentó reducción de la sensibilidad al dolor en la primera exploración con NTG. En el resto de los casos, los pacientes apreciaron una disminución significativa de la sensibilidad al dolor en la zona tratada con NTG transdérmica. El valor medio de la sensibilidad dolorosa en el primer control (al minuto de la aplicación) fue de 9.75 en el brazo con placebo y de 7.25 en el que se administró NTG, La diferencia entre ambos valores es de 2.5 (p=0.0003) y su intervalo de confianza al 95% de 1.3 a 3.6. En el Control 2, (entre el minuto 3 y 4 de la aplicación) el valor medio de la sensibilidad dolorosa fue de 9.68 en el brazo con placebo y de 6.28 en el que se administró NTG. La diferencia entre ambos valores es de 3.4 (p=0.0001) y su intervalo de confianza al 95% de 2.0 a 4.7. De este modo comprobamos que la NTG transdérmica tiene un efecto analgésico periférico en la prueba del pinprick test. Como ya hemos discutido, el efecto analgésico periférico de la NTG y los NVD se efectúa por su transformación en NO y la activación de la vía NO-GMPc es el común denominador del mecanismo de acción de los analgésicos periféricos que bloquean directamente la hiperalgesia (17). Lo que nos llevó a confirmar que la NTG y los NVD, ejercen una acción antiinflamatoria y que pueden formar un nuevo grupo de agentes antiinflamatorios. Figura 3.
PATENTE PARA LA UTILIZACIÓN DE NITROVASODILATADORES EN MEDICAMENTOS DE USO TÓPICO CON ACCIÓN ANTIINFLAMATORIA Y ANALGÉSICA
A la vista de los resultados de los ensayos, obtuvimos la patente para la utilización de nitrovasodilatadores en medicamentos de uso tópico con acción antiinflamatoria y analgésica inespecífica, excepto para la tromboflebitis superficial (18).
OTROS PROCESOS EN LOS QUE ENCONTRAMOS EFECTO ANALGÉSICO ANTIINFLAMATORIO
El Prurito Aquagénico (PA), es una enfermedad caracterizada por una picazón en la piel tras el contacto con agua potable, sin tratamiento establecido. Realizamos un estudio con NTG en un paciente con PA. La escala analógica fue de 8 ± 0 con placebo y 2,6 ± 0,57 con gel de nitroglicerina (P<0,001). Este mecanismo podría deberse a la desensibilización inducida por NO de los receptores del prurito (19).
APORTACIONES DE OTROS AUTORES AL TRATAMIENTO DE LA TROMBOFLEBITIS SUPERFICIAL POSTINFUSIÓN.
En 2015 se publicó una revisión Cochrane (20) sobre tratamientos de la tromboflebitis superficial postinfusión, incluyendo heparina, Essaven gel, Flebolan, diclofenaco tópico u oral, NTG transdérmica, crema de notoginsen y crema de heparinoide, ungüento de pentosano polisulfato de sodio, defibrotida, y dalteparina. En el apartado de NTG se referencia al nuestro (14) y otro artículo. (20). Consideran que la evidencia general para todos los tratamientos y también para la NTG, es baja debido a imprecisiones y ocultamiento de asignación poco claro (21).
ACCIÓN ANTIINFLAMATORIA EN PACIENTES CON ENFERMEDAD VASCULAR PERIFÉRICA
Además del efecto antiinflamatorio y analgésico en los procesos tromboflebíticos, comprobamos que la NTG tiene acción antiinflamatoria en pacientes con enfermedad vascular periférica. (22) En un estudio piloto con 40 pacientes, la NTG redujo significativamente los niveles de PCR y E-selectina, mejorando también la calidad de vida de los pacientes. No se modificaron otros parámetros. Esta patología aumenta su incidencia y severidad con la mayor incidencia de diabetes y pacientes en diálisis. En pacientes con grados avanzados de severidad, autores japoneses han mostrado que los parches de NTG y Dinitrato de isosorbide mejoran el dolor y la claudicación (23).
En casos severos, las dosis continuas de NTG transdérmica aceleran la curación de úlceras y mejoran el índice de presión brazo-dedo del pie (24).
La NTG tópica también ha demostrado ser eficaz en neonatos con complicaciones del catéter arterial y en pacientes con dolor isquémico en reposo, proporcionando una analgesia rápida y segura. (25).
NTG EN LA CURACIÓN DE LAS HERIDAS QUIRÚRGICAS
Diversos estudios han evaluado el uso de NTG después de la mastectomía, concluyendo que la NTG puede ser recomendada para la curación de heridas quirúrgicas, especialmente en casos donde se realiza desbridamiento del colgajo (26).
ACCIÓN ANTIINFLAMATORIA Y ANALGÉSICA DE LA NTG, EN EL SISTEMA MUSCULO ESQUELÉTICO
Buscamos una patología en la que pudiéramos demostrar la acción antiinflamatoria y analgésica de la NTG en el sistema musculo esquelético. Elegimos el síndrome de hombro doloroso por tendinitis del supraespinoso de menos de siete días de evolución.
Fue un estudio clínico piloto, doble ciego y controlado con placebo, usando parches de NTG de 5 mg aplicados diariamente durante tres días en la zona dolorosa. Hubo una reducción significativa de la intensidad del dolor a las 24 h y 48 h en el grupo NTG, mientras que no hubo cambios en el grupo placebo. La movilidad articular mejoró significativamente en el grupo NTG. Dos pacientes presentaron cefaleas como efecto secundario a las 24 h de iniciado el tratamiento en el grupo con NTG (27).
La eficacia del tratamiento con NTG en esta como en las anteriores condiciones las atribuimos a la generación de NO por la NTG, que produce sus acciones y estimula la guanilato ciclasa. Esto reduce la acción vasoconstrictora inducida por la inflamación y produce una acción analgésica en el sistema nervioso periférico, modulando los procesos inflamatorios.
REPERCUSION DE LOS TRABAJOS DE LA NITROGLICERINA COMO FÁRMACO ANTIINFLAMATORIO Y ANALGÉSICO EN LA LITERATURA MEDICA. TENDINOPATÍA DEL SUPRAESPINOSO
En los últimos años, varios estudios han analizado el uso de NTG en patologías tendinosas, especialmente en la tendinopatía del supraespinoso (Paoloni et al., 2005) (28). En un ensayo clínico, trataron 53 pacientes con NTG tópica o placebo, mostrando una mejoría significativa en el aumento de la fuerza y la amplitud de movimiento del hombro y reducción del dolor en reposo, con actividad, y por la noche.
Asimismo, Giner-Pascual y cols. (2011) investigaron el uso de NTG en pacientes con lesiones medulares y dolor de hombro. Encontraron que el NTG redujo el dolor y mejoró la funcionalidad en un periodo de seis meses (29)
Finalmente, Cumpston et al. (2009) (30) realizaron una revisión Cochrane que evidenció la eficacia del NTG tópico en comparación al placebo en el tratamiento a corto plazo de la enfermedad del manguito de rotadores, con síntomas agudos (menos de siete días de duración), pero se requieren más estudios para confirmar su efectividad y seguridad a largo plazo.
TENDINOPATÍA DEL EXTENSOR DEL CODO. CODO DEL TENISTA
Los autores australianos han estudiado el efecto de la NTG en la tendinosis extensora crónica del codo o codo del tenista. Seleccionaron 86 pacientes, asignados aleatoriamente a recibir NTG o placebo, junto con un programa de rehabilitación. El grupo NTG mostró una reducción significativa del dolor a las 2 semanas y una mejora en la fuerza a las 24 semanas. A los 6 meses, el 81% de los pacientes tratados con NTG estaban asintomáticos en comparación con el 60% del grupo placebo (31).
Un estudio de seguimiento a 5 años no mostró beneficios adicionales a largo plazo. Sin embargo, una revisión de la literatura en 2022 encontró mejoras a corto y medio plazo con NTG combinado con rehabilitación. Tres estudios usaron una dosis de 1.25mg/24h y uno usó 1.44mg/24h. En general, la literatura actual demuestra que el uso de parches de NTG para la tendinosis crónica del codo, mejora el dolor a corto y mediano plazo, así como la función del codo. Sin embargo, se requieren más estudios para comprender completamente el efecto de la NTG tópica sobre el codo de tenista, particularmente el rango de dosis efectiva y los beneficios a largo plazo (32).
TENDINOPATÍA CRÓNICA DEL TENDON DE AQUILES
El mismo grupo se enfrentó a la tendinopatía no insercional del tendón de Aquiles, (33) ensayando la NTG tópica. Realizaron un estudio prospectivo, aleatorizado, doble ciego y controlado con placebo con 65 pacientes, comparando la aplicación continua de NTG tópico contra placebo, más rehabilitación para el tratamiento de la tendinopatía de Aquiles no insercional.
El diagnóstico se basó en antecedentes de dolor insidioso, nódulo doloroso localizado en la región de 2 a 6 cm de la inserción del calcáneo y examen ecográfico. Los criterios de exclusión incluyeron tendinopatía de menos de tres meses, embarazo, cirugía previa, dislocación del tobillo o pierna afectada y corticoides recientes. Asignaron 32 pacientes al grupo de NTG y 33 al de placebo. En comparación con el grupo control, el grupo de NTG mostró reducción del dolor con actividad, nocturno y sensibilidad, y aumento del trabajo del flexor plantar. A los seis meses, 78 % de los tendones en el grupo NTG estaban asintomáticos en comparación con el 49 % en el grupo placebo (p = 0,001). Concluyen que la NTG tópica redujo significativamente el dolor y mejoró medidas funcionales, pero es necesario más investigación (33). Pero la NTG es un medicamento bien probado en humanos, sin efectos secundarios irreversibles en sujetos sanos, por lo que parece que el tratamiento tópico continuo con NTG, junto a la rehabilitación, tiene un papel en el tratamiento de la tendinopatía crónica de Aquiles. Aunque Kane et al. no encontraron beneficio clínico adicional de la NTG (34), lo mismo que Kirwan et al (35) que valoraron el tratamiento diario de la tendinopatía crónica del tendón de Aquiles con pomada de NTG en dosis de 1 a 2 cm, durante 24 semanas combinado con ejercicios excéntricos 12 semanas en un estudio controlado frente a placebo. Los resultados no mostraron beneficios adicionales de la NTG en comparación con el uso de ungüento placebo y el mismo programa de ejercicios.
Sin embargo el grupo de Paoloni había informado que tras un periodo de 3 años de tratamiento existe un menor nivel de conciencia del dolor lo que indica que el mecanismo de acción de la NTG no es simplemente analgésico(36) sino que puede deberse al aumento de formación de cGMP a nivel cerebral. Se siguen abriendo nuevas líneas de investigación con nuevas moléculas y nuevas dianas que describiremos en la segunda parte de esta revisión.
ACTIVIDAD DE LAS SINTASAS DEL OXIDO NITRICO EN LAS LESIONES TENDINOSAS
Este grupo australiano ha profundizado en el estudio de la aplicación clínica de la NTG en las tendinopatías con estudios de laboratorio sobre la expresión temporal de las sintasas de NO en el proceso de lesión y reparación de tendones. Se sabía que el NO contribuye a la curación de heridas (37) y que las sintasas de NO se regulan positivamente tras una lesión, promoviendo el proceso de curación (38). Por ejemplo, los inhibidores de NOS retrasan la cicatrización, mientras que los donadores de NO aceleran la cicatrización (39).
En tendones no lesionados hay poca actividad de las sintasas de NO, pero tras una ruptura, la actividad de la NOS se quintuplica durante la curación. La iNOS aumenta 23 veces entre el día 4 y 7, la eNOS 24 veces en el día 7 y la bNOS 7 veces en el día 21. En tendones humanos también se observó actividad de NOS con sobreexpresión de iNOS y eNOS. Se comprobó que el NO mejora la síntesis de colágeno en cultivos celulares de tendón humano. La transfección del gen iNOS aumentó la síntesis de colágeno, que se inhibió al administrar un inhibidor de NOS (40).
Murrell revisó estudios clínicos con NTG, encontrando que en la tendinopatía del codo, los tratados con NTG mostraron menos dolor y mayor potencia. En tendinitis de Aquiles, el grupo con NTG tuvo mejor respuesta en la prueba de salto y fuerza. En la tendinopatía del supraespinoso, el grupo con NTG redujo el dolor y mejoró el rango de movimiento y potencia. A los 6 meses, el 46% de los pacientes con parches de GTN estaban asintomáticos frente al 24% de los que solo realizaron rehabilitación tendinosa (p = 0,007). La conclusión es que el NO es crucial para la curación de tendones, mejorando la síntesis de la matriz extracelular y las propiedades mecánicas de los tendones en curación (39).
TENDINOPATÍA DEL TENDÓN ROTULIANO
Steunebrink y colaboradores estudiaron 40 atletas con tendinopatía rotuliana, asignados al azar a tratamiento con parche de NTG o placebo. Treinta y tres (82.5%) completaron el estudio, con valoraciones de VAS y VISA-P al inicio y a las 6, 12 y 24 semanas. En la escala funcional, el grupo GTN pasó de 63,0 ± 16,4 a 75±16,2 y el placebo de 67,8 ± 10,9 a 80,7±22,1. En la escala de dolor, el grupo GTN mejoró de 4.1±2.9 a 6.6±3 y el placebo de 5.8±3 a 7.8±3. La conclusión principal fue que no hubo beneficio en el manejo de la tendinopatía crónica de la rótula con GTN tópica y ejercicios excéntricos a las 24 semanas(41).
NUEVOS METANÁLISIS DE NTG EN TENDINOPATÍAS
Challoumas y cols (42) realizaron una revisión sistemática sobre la NTG en el tratamiento de la tendinopatía patelar. Encontraron que la NTG tópica y la inyección de ácido hialurónico, combinados con ejercicio excéntrico y de resistencia moderado y lento, eran las intervenciones más efectivas. La NTG tópica demostró ser más efectiva que el placebo, especialmente en el control del dolor y la satisfacción a medio plazo. Recomiendan la GTN tópica como complemento de tratamiento cuando la carga del tendón no ha sido efectiva durante 12 semanas, advirtiendo de posibles efectos secundarios como reacciones cutáneas y dolores de cabeza (43).
Gambito y cols. (44) encontraron pruebas sólidas de que GTN frente al placebo, redujo el dolor en las actividades diarias en pacientes con tendinopatías crónicas. Incluyeron siete estudios clínicamente relevantes con 446 pacientes en total. El metanálisis mostró que la NTG tiene un efecto positivo en la reducción del dolor durante las actividades diarias en tendinopatías crónicas, con un odds ratio de 4,44 (IC del 95 %, 2,34–8,40). También existe evidencia sólida de que la NTG mejora la fuerza del tendón en la fase crónica. Existe una diferencia significativa en la incidencia de dolor de cabeza entre NTG y el control, con un odds ratio de 1,73 (IC 95 %, 1,01–2,97). En resumen la NTG alivia el dolor durante las actividades diarias y aumenta la fuerza del tendón en tendinopatías crónicas y se necesitan más estudios para explorar su papel en todas las fases de las tendinopatías.
En conclusión hace cerca de cuarenta años que se demostró que el NO era el Factor de Relajación Derivado del Endotelio y que esta sencilla molécula era mucho más que una simple sustancia vasodilatadora del músculo liso vascular, se comprobaron las numerosas acciones que realiza en diversos sistemas celulares del organismo. Casi simultáneamente se confirmó que los fármacos NVD como la NTG, ejercen su acción por su transformación en NO, y que son capaces de remedar algunas de las acciones del NO endógeno, como las acciones antiinflamatoria y analgésica. Treinta y cinco años después otros autores han confirmado nuestros hallazgos, con algunas discrepancias, y se abre un nuevo tiempo de desarrollo de nuevas moléculas capaces de transformarse y transportar este ubicuo mediador para que ejerza sus efectos en distintos e importantes campos de la medicina, que revisaremos en la segunda parte de esta revisión.
FINANCIACIÓN
No existe ningún compromiso de financiación de este trabajo.
DECLARACIÓN DE TRANSPARENCIA
El autor/a de este artículo declara no tener ningún tipo de conflicto de intereses respecto a lo expuesto en el presente trabajo.
BIBLIOGRAFÍA
- ↑Furchgott RF Zawadzki JV. The obligatory role of endothelial cells in the relaxation of arterial smooth muscle by acetylcholine. Nature 1980; 288(5789):373-376. doi: 10.1038/288373a0),
- ↑Cherry PD, Furchgott RF, Zawadzki JV, Jothianandan D, Role of endothelial cells in relaxation of isolated arteries by bradykinin. Proc. Nat. Acad. Sci. USA 1982; 79: 2106 – 2110.
- ↑Palmer RMJ, Ferrige AG, Moncada S. Nitric oxide release accounts for the biological activity of endothelium – derived relaxing factor. Nature 1987; 327: 524 – 526.
- ↑Palmer RM, Ashton DS, Moncada S. Vascular endothelial cells synthesize nitric oxide from L-arginine. Nature 1988; 16;333(6174):664-666. doi: 10.1038/333664a0. PMID: 3131684.
- ↑Rees DD, Palmer RM, Hodson HF, Moncada S. A specific inhibitor of nitric oxide formation from L-arginine attenuates endothelium-dependent relaxation. Br J Pharmacol. 1989; 96 :418-424. doi: 10.1111/j.1476-5381.1989.tb11833.x. PMID: 2924084; PMCID: PMC1854347.
- ↑Vallance P, Collier J, Moncada S. Effects of endothelium-derived nitric oxide on peripheral arteriolar tone in man. Lancet. 1989; 2(8670):997-1000. doi: 10.1016/s0140-6736(89)91013-1. PMID: 2572793.
- ↑Rees, D.D., Cellek, S., Palmer, R.M.J. and Moncada, S. .Dexamethasone prevents the induction by endotoxin of a nitric oxide synthase and the associated effects on vascular tone: an insight into endotoxin shock. Biochem. Biophys. Res. Commun. 1990; 173: 541- 547.
- ↑Balard JM. Premier memoire sur l’alcool amylique. Ann Chim Phys 1844;12: 294-330.
- ↑Feehlisch M, Noack EA. Correlation between nitnc oxide formation during degradation of organic nitrates and activation of guanylate cyclase. Eur J Pharmacol 1987;139:19-30.
- ↑Duarte ID, Lorenzetti BB, Ferreira SH. Peripheral analgesia and activation of the nitric oxide-cyclic GMP pathway. Eur J Pharmacol. 1990 ;186(2-3):289-293. doi: 10.1016/0014-2999(90)90446-d. PMID: 1981187..
- ↑Ialenti A, Ianaro A, Moncada S. Di Rosa M. Modulation of acute inflammation by endogenous nitric oxide. Eur J Pharm 1992; 211:177-182.
- ↑Berrazueta JR, López Jaramillo P, Moncada S. El óxido nítrico: de vasodilatador endógeno a mediador biológico. Rev Esp Cardiol 1990; 43: 421-431.
- ↑Berrazueta JR, Ochoteco J, Poveda JJ, et al. Tratamiento transcutáneo de la tromboflebitis superficial con el donador exógeno de óxido nítrico: Nitroglicerina. Rev Esp Cardiol 1991;44:424-426,
- ↑Berrazueta JR, Poveda JJ, Ochoteco J, et al. The anti-inflammatory and analgesic action of transdermal glyceryltrinitrate in the treatment of infusion-related thrombophlebitis. Postgrad Med J. 1993;69(807):37-40. doi: 10.1136/pgmj.69.807.37. PMID: 8383319; PMCID: PMC2399598
- ↑Berrazueta JR, Fleitas M, Salas E, et al. Local transdermal glyceryl trinitrate has an antiinflammatory action on thrombophlebitis induced by sclerosis of leg varicose veins. Angiology. 1994;45:347-351. doi: 10.1177/000331979404500503. PMID: 8172381
- ↑Berrazueta JR, Salas E, Ochoteco A, Poveda JJ, Sánchez de Vega MJ. Acción analgésica periférica del donador de óxido nítrico: Nitroglicerina. Estudio control frente a placebo de la acción de la Nitroglicerina transdérmica sobre la sensibilidad dolorosa del antebrazo. Rev Esp Cardiol. 1993; 46:10-14.
- ↑Ferreira SH, Lorenzetti BB, Faccioli LH. Blockade of hyperalgesia and neurogenic oedema by topical application of nitroglycerin. Eur J Pharmacol. 1992 ;217(2-3):207-209. doi: 10.1016/0014-2999(92)90871-z. PMID: 1425939.
- ↑PATENTE. Utilización de los nitrovasodilatadores en la preparación de medicamentos antiinflamatorios y analgésicos de uso tópico.Solicitante José Ramón de Berrazueta Fernández. N._ de publicación: ES 2 059 264. Número de solicitud: 920223. Fecha de publicación de la solicitud: 01.11.94 Prioridad 1992-11-05. Anticipated expiration 2012-11-05Priority to ES9202231A. 1992-11-05 1995-06-16 Berrazueta Fernandez JoseRamon USE OF NITROVASODILATORS IN THE PREPARATION OF ANTI INFLAMMATORY AND ANALGESIC MEDICINES FOR TOPICAL USE.
- ↑Berrazueta JR, Riestra A, Salas E, et al. Aquagenic pruritus response to the exogenous nitric oxide donor, transdermal nitroglycerin. Int J Dermatol. 1994; 33:752-753. doi: 10.1111/j.1365-4362.1994.tb01528.x. PMID: 8002150.
- ↑Di Nisio M, Peinemann F, Porreca E, Rutjes AW. Treatment for superficial infusion thrombophlebitis of the upper extremity. Cochrane Database Syst Rev. 2015;2015(11):CD011015. doi: 10.1002/14651858.CD011015.pub2. PMID: 26588711; PMCID: PMC6885032.
- ↑Almenar L, Hernández M, Gimeno JV, Palencia M, Algarra F. Heparinoides frente a nitroglicerina en el tratamiento de las flebitis superficiales [Heparinoids versus nitroglycerin in the treatment of superficial phlebitis]. Rev Clin Esp. 1993;193(5):229-231. Spanish. PMID: 8256008.
- ↑Berrazueta JR, Sampedro I, Garcia-Unzueta MT, Llorca J, Bustamante M, Amado JA. Effect of transdermal nitroglycerin on inflammatory mediators in patients with peripheral atherosclerotic vascular disease. Am Heart J. 2003;146(4):E14. doi: 10.1016/S0002-8703(03)00391-0. PMID: 14564337
- ↑Matsui A, Murakami M, Hata S, et al. The Efficacy of the Transdermal Isosorbide Dinitrate Patch in Patients With Chronic Limb-Threatening Ischemia. Int J Low Extrem Wounds. 2022 ;21(4):477-482. doi: 10.1177/1534734620959515. Epub 2020 Sep 23. PMID: 32962459)
- ↑McAra S. Effectiveness of glyceryl trinitrate (GTN) vasodilator patches in peripheral arterial disease. J Foot Ankle Res 2015;8(Suppl2): P8 http://www.jfootankleres.com/content/8/S2/P8)
- ↑Sushko,K, Litalien C, Ferruccio L et al. Topical nitroglycerin ointment as salvage therapy for peripheral tissue ischemia in newborns: a systematic review. CMAJ Open 2021; 9 (1) E252-E260; doi: https://doi.org/10.9778/cmajo.20200129)
- ↑Wang P, Gu L, Qin Z, Wang Q, Ma J. Efficacy and safety of topical nitroglycerin in the prevention of mastectomy flap necrosis: a systematic review and meta-analysis. Sci Rep. 2020;10(1):6753. doi: 10.1038/s41598-020-63721-1. PMID: 32317705; PMCID: PMC7174291.
- ↑Berrazueta JR, Losada A, Poveda J, et al. Successful treatment of shoulder pain syndrome due to supraspinatus tendinitis with transdermal nitroglycerin. A double blind study. Pain. 1996;66(1):63-67. doi: 10.1016/0304-3959(96)03021-7. PMID: 8857632
- ↑Paoloni JA; Appleyard RC; Nelson, J; Murrell GAC. Topical glyceryl trinitrate application in the treatment of chronic supraspinatus tendinopathy: a randomized, double-blinded, placebo-controlled clinical trial. Am J Sports Med 2005; 33: 806-813
- ↑Giner-Pascual, M., Alcanyis-Alberola, M., Querol, F et al. Transdermal nitroglycerine treatment of shoulder tendinopathies in patients with spinal cord injuries. Spinal Cord .2011;49: 1014–1019. https://doi.org/10.1038/sc.2011.41
- ↑Cumpston M, Johnston RV, Wengier L, et al. . Topical glyceryl trinitrate for rotator cuff disease. Cochrane Database Syst Rev 2009;3:CD006355. doi: 10.1002/14651858.CD006355.pub2. PMID: 19588386.
- ↑Paoloni JA, Appleyard RC, Nelson J, Murrell GA. Topical nitric oxide application in the treatment of chronic extensor tendinosis at the elbow: a randomized, double-blinded, placebo-controlled clinical trial. Am J Sports Med. 2003;31(6):915-920. doi: 10.1177/03635465030310062901. PMID: 14623657.)
- ↑McCulloch C, Hunter MM, Lipp C, Lang E, Ganshorn H, Singh P. Management of Lateral Epicondylitis Using Transdermal Nitroglycerin: A Systematic Review. Cureus. 2022; 14(12):e32560. doi: 10.7759/cureus.32560. PMID: 36654592; PMCID: PMC9840472.)
- ↑Paoloni J, Appleyard RC, Nelson J, Murrell GA, MBBS G. Topical Glyceryl Trinitrate Treatment of Chronic Noninsertional Achilles Tendinopathy : A Randomized, Double-Blind, Placebo-Controlled Trial. J Bone Joint Surg Am 2004;86(5):916-922.
- ↑Kane TP, Ismail M, Calder JD. Topical glyceryl trinitrate and noninsertional Achilles tendinopathy: a clinical and cellular investigation. Am J Sports Med 2008; 36:1160–1163.
- ↑Kirwan PD, Duffy T, French HP. Topical glyceryl trinitrate (GTN) and eccentric exercises in the treatment of mid-portion achilles tendinopathy (the NEAT trial): a randomised double-blind placebo-controlled trial.Br J Sports Med 2024;58:1035-1043.
- ↑Paoloni JA, Murrell GA. Three-year follow up study of topical glyceryl trinitrate treatment of chronic noninsertional Achilles tendinopathy. Foot Ankle Int 2007; 28: 1064–1068.
- ↑Schaffer MR, Tantry U, Gross SS, Wasserburg HL, Barbul A. Nitric oxide regulates wound healing. J Surg Res 1996;63:23740.
- ↑Shabanic M, Pulfer SK, Bulgrin JP, Smith DJ. Enhancement of wound repair with a topically applied nitric oxide-releasing polymer. Wound Repair Regul 1996;4:353-362.
- ↑Murrell GAC. Using nitric oxide to treat tendinopathy. Br J Sports Med 2007;41:227–231. doi: 10.1136/bjsm.2006.034447
- ↑Murrell G A C, Szabo C, Hannafin J A, et al. Modulation of tendon healing by nitric oxide. Inflamm Res 1997:4619–4627
- ↑Steunebrink M, Zwerver J, Brandsema R, et al. Topical glyceryl trinitrate treatment of chronic patellar tendinopathy: a randomised, double-blind, placebo-controlled clinical trial. Br J Sports Med 2013; 47, 34–39
- ↑Challoumas D, Pedret C, Biddle M, et al. Management of patellar tendinopathy: a systematic review and network meta- analysis of randomised studies. BMJ Open Sport & Exercise Med 2021;7:e001110. doi:10.1136/bmjsem-2021-001110
- ↑Challoumas D, Kirwan PD, Borysov D,et al. Topical glyceryl trinitrate for the treatment of tendinopathies: a systematic review. Br J Sports Med 2019;53:251–262.
- ↑Gambito ED, Gonzalez-Suarez CB, Oquiñena TI, Agbayani RB. Evidence on the effectiveness of topical nitroglycerin in the treatment of tendinopathies: a systematic review and meta-analysis. Arch Phys Med Rehabil. 2010;91(8):1291-1305.
ranm tv
José Ramón de Berrazueta Fernández
Real Academia Nacional de Medicina de España
C/ Arrieta, 12 · 28013 Madrid
Tlf.: +34 91 159 47 34 | E-Mail: joseramon@berrazueta.com
Año 2025 · número 142 (02) · páginas 140 a 149
Enviado*: 08.07.25
Revisado: 12.07.25
Aceptado: 28.07.25
* Fecha de lectura en la RANM


