Resumen
Los contrastes ecográficos han evolucionado desde su descubrimiento en 1968, consolidándose como herramientas diagnósticas seguras y eficaces gracias a su carácter estrictamente intravascular y su capacidad para potenciar la señal ecográfica mediante microburbujas de gas estabilizadas. Esta revisión explora sus mecanismos de acción, fundamentos físicos, estructura química y principales aplicaciones. La oscilación no lineal de las microburbujas bajo ultrasonido y su fragilidad controlada permiten visualizar la microvascularización en tiempo real, favoreciendo su uso en el diagnóstico de diversas lesiones y en procedimientos intervencionistas guiados por imagen. También destaca su potencial en pediatría, donde su perfil de seguridad ha ampliado su uso a nuevas indicaciones como el reflujo vesicoureteral o el traumatismo abdominal cerrado. A pesar de ciertas limitaciones frente a otras técnicas en sensibilidad o resolución anatómica, la ecografía con contraste representa una alternativa no invasiva, libre de radiación, con un futuro prometedor tanto en el diagnóstico como en posibles usos terapéuticos.
Abstract
Ultrasound contrast agents have evolved since their discovery in 1968, becoming safe and effective diagnostic tools thanks to their strictly intravascular nature and their ability to enhance ultrasound signals through stabilized gas microbubbles. This review explores their mechanisms of action, physical principles, chemical structure, and main clinical applications. The nonlinear oscillation of microbubbles under ultrasound and their controlled fragility enables real-time visualization of microvascularization, supporting their use in the diagnosis of various lesions and in image-guided interventional procedures. Their potential in pediatrics is also noteworthy, as their safety profile has expanded their use to new indications such as vesicoureteral reflux and blunt abdominal trauma. Despite certain limitations in sensitivity or anatomical resolution compared to other imaging techniques, contrast-enhanced ultrasound represents a non-invasive, radiation-free alternative with a promising future in both diagnostic and potential therapeutic applications.
Palabras clave: Ecografía; Contrastes; Microburbujas; Diagnóstico.
Keywords: Ultrasound; Contrast; Microbubbles; Diagnosis.
INTRODUCCIÓN
Los contrastes ecográficos se describen por primera vez en 1968 (1) al observarse que las microburbujas de gas generadas tras inyectar solución salina en la aorta producían un efecto de contraste en ecografía. Desde entonces, se ha potenciado este efecto modificando la estructura química de las soluciones y optimizando las secuencias ecográficas para detectarlas. Aunque inicialmente su uso se limitaba al sistema cardiovascular, se ha aprobado su aplicación en muchas más indicaciones dada su alta seguridad y baja tasa de efectos adversos (1,2).
Su permanencia intravascular ha consolidado su uso en la evaluación de múltiples condiciones principalmente cardiovasculares y oncológicas (3). Al permanecer exclusivamente en el espacio intravascular se usan para valorar la perfusión tisular e identificar vasos de muy pequeño calibre (2). Aunque existen distintas presentaciones según su forma física (gas, líquido o sólido) (3), los únicos aprobados clínicamente son las microburbujas de gas (4,5). En España están disponibles SonoVue/Lumason (microburbujas de hexafluoruro de azufre en membrana fosfolipídica), Definity/Luminity (perflutreno en membrana fosfolipídica) y Optison (perflutreno estabilizado en albúmina).
El uso del contraste ecográfico es menos extenso que el de los contrastes yodados en tomografía computarizada (TC) y los quelatos de gadolinio en resonancia magnética (RM). Esta revisión narrativa recopila los mecanismos de acción y bases físicas del realce ecográfico, revisando sus usos prácticos, contraindicaciones, reacciones adversas y principales diferencias frente a otros medios de contraste.
MATERIAL Y MÉTODOS
El trabajo está diseñado como una revisión narrativa de las publicaciones científicas, revisiones bibliográficas e informes de organizaciones profesionales sobre los mecanismos de acción de los contrastes ecográficos actualmente disponibles en España, y de sus usos más relevantes.
Se realizó una búsqueda de artículos y revisiones bibliográficas publicadas entre noviembre de 2024 y enero de 2025 en las bases de datos Pubmed (https://pubmed.ncbi.nlm.nih.gov/) y Research Gate (https://www.researchgate.net/). La búsqueda se realizó con los parámetros “best match” y “most cited”, en inglés y usando palabras clave (contrastes ecográficos, mecanismo de actuación, aplicaciones actuales) cruzadas por operadores booleanos “AND” y “OR”, y revisando los primeros 30 resultados obtenidos que fueran artículos de revisión, metaanálisis, ensayos clínicos o revisiones sistemáticas.
Para la extracción y análisis de datos se aplicaron los criterios de inclusión y exclusión para seleccionar aquellos trabajos que fuesen de mayor utilidad, y se realizó una lectura del título, resumen y, en caso de duda, del artículo completo. Aquellos trabajos que cumplían los criterios de inclusión, pero no aportaban información relacionada con esta revisión fueron descartados.
ESTRUCTURA QUÍMICA DE LOS CONTRASTES ECOGRÁFICOS
La estructura básica de un contraste ecográfico consta de una nube de microburbujas en suspensión que interactúa con el haz de ultrasonidos para visualizarse. Estos contrastes cuentan con dos componentes (Figura 1):
- Un núcleo gaseoso formado por un gas inerte de elevado peso molecular que permite su detección ecográfica gracias a la impedancia de la interfase gas-sangre.
- Una membrana estabilizadora que disminuye la tensión superficial del núcleo gaseoso para aumentar su vida media desde pocos segundos hasta los 5 minutos (6). Se han conseguido crear membranas con ligandos específicos a marcadores endoteliales, aumentando así su especificidad en la valoración de lesiones tumorales.
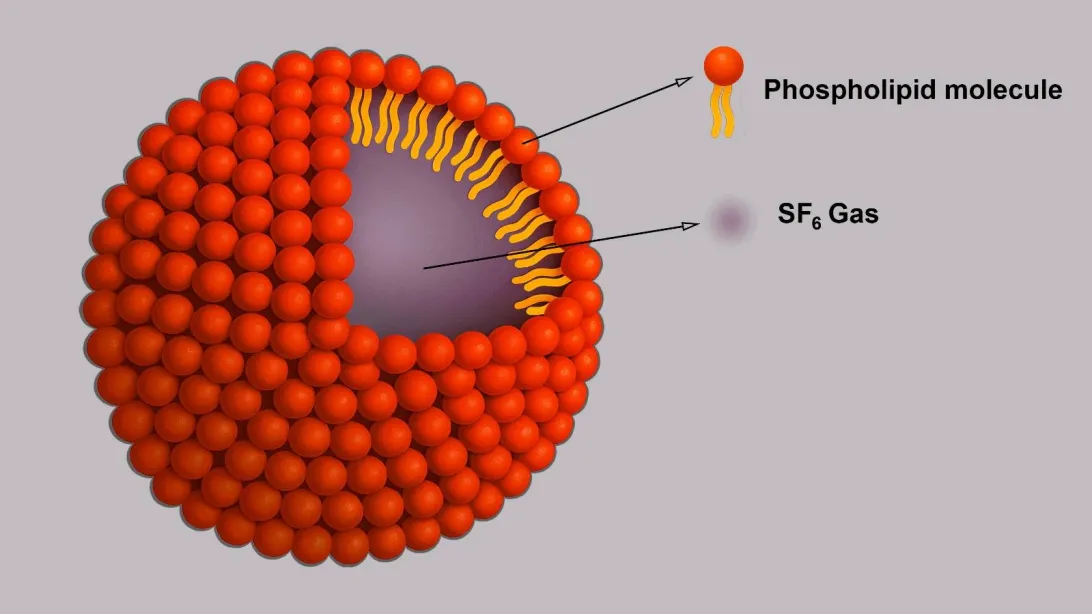
Estas microburbujas tienen un tamaño similar al de los eritrocitos (1-5 µm), lo que les permite circular por el sistema vascular sin extravasarse al espacio intersticial. Al destruirse, sus componentes se eliminan de forma inocua por los pulmones por lo que pueden emplearse en pacientes con insuficiencia renal (2). El componente membranoso es metabolizado a nivel hepático.
PRINCIPIOS FÍSICOS DE LOS CONTRASTES ECOGRÁFICOS
Oscilación
Los contrastes ecográficos amplifican la señal de la sangre unas 1000 veces, permitiendo visualizar la microvascularización de tejidos, órganos y lesiones. Este incremento de señal se debe a las microburbujas que oscilan por la elasticidad de su membrana bajo la influencia del ultrasonido (6). El fenómeno de oscilación se refiere a la capacidad de las microburbujas de contraerse y dilatarse al recibir la energía del ultrasonido, generando un movimiento oscilatorio no lineal, diferente a la respuesta lineal de los tejidos corporales.
Esta oscilación comporta la emisión de sonidos armónicos que son la base de la formación de la imagen. La oscilación varía según la amplitud de la onda incidente (Fig. 2) que a su vez depende de la potencia acústica (7):
- Potencias muy bajas: las burbujas no oscilan, no se crea señal.
- Potencias más elevadas: las burbujas oscilan de forma no lineal, generando sonidos armónicos y obteniéndose señal
- Potencias muy elevadas: las burbujas oscilan de forma no lineal bruscamente, destruyéndose en el proceso y dando una señal intensa pero fugaz.
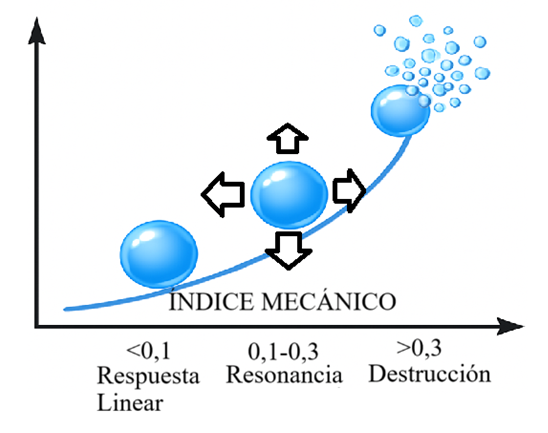
Como los ecógrafos convencionales no diferencian bien entre la señal procedente de los contrastes y la de los tejidos, se necesitan programas específicos para registrar esta diferencia. Estos programas permiten que la burbuja resuene sin romperse al emplear un bajo índice mecánico, mejorando su visualización (2). Gracias a la oscilación y a la emisión de frecuencias armónicas, pueden usarse técnicas específicas para el contraste con un pulso único o doble, como describimos a continuación.
Las técnicas ecográficas por pulso único diferencian los ecos de frecuencias armónicas producidos por los contrastes de los producidos por los tejidos que son de menor frecuencia. Entre estas técnicas se encuentran la imagen armónica que filtra los ecos de manera que sólo sean visibles aquellos de frecuencia más alta a la original; las de imagen superarmónicas que filtran los ecos de frecuencia mucho más alta a la original; y las técnicas de imágenes subarmónicas, que filtran los ecos para que sólo sean visibles aquellos de frecuencia más baja a la original (8).
Por otro lado, las técnicas de imagen por pulsos múltiples exacerban las diferencias entre los ecos de los contrastes con respecto a los tejidos mediante secuencias de fase y fuera de fase que usan dos pulsos consecutivos, siendo el segundo especular al primero, lo que produce una ausencia de eco por parte de los tejidos (al ser la suma de ambos ecos producidos igual a 0) (Fig. 3). Sin embargo, la respuesta no lineal de los contrastes ecográficos hace que la suma de sus ecos sea diferente a cero, siendo captados por el transductor (9).
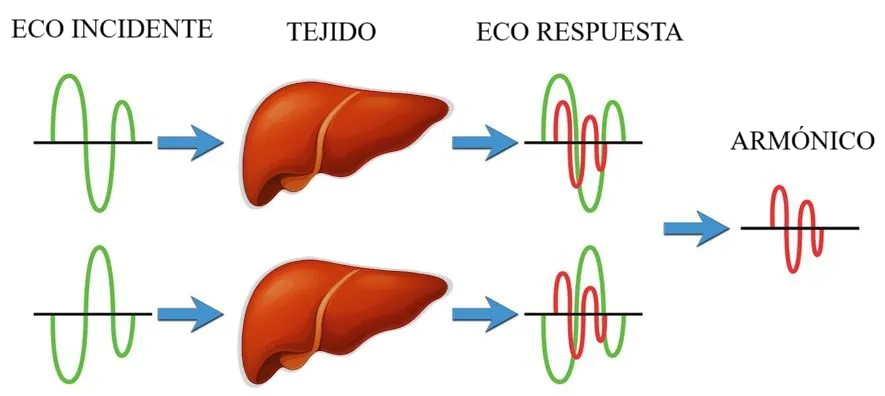
Fragilidad
Los primeros contrastes ecográficos se fragmentaban rápidamente con los pulsos de ultrasonidos, dando una imagen inestable que desaparecía a los pocos segundos. Actualmente, para preservar las microburbujas, se usan índices mecánicos (IM, parámetro que mide la intensidad acústica aplicada al cuerpo) bajos para mantener su integridad y prolongar su vida media.
Esta misma fragilidad puede aprovecharse con IM altos, como en la técnica de destrucción–reperfusión, que usa distintos IM en diversas fases para visualizar de manera dinámica el contraste: Primero se aplica un IM bajo que nos permite ver el contraste ecográfico en la circulación macro y microvascular. Luego, se aplica un IM alto que destruye las microburbujas, desapareciendo la imagen del contraste, y finalmente, se aplica de nuevo un IM bajo que permite al contraste acumularse en la circulación, facilitando la monitorización de la reperfusión en tiempo real.
Las oscilaciones a altos IM pueden producir efectos adversos como hemólisis y daño celular, por lo que se estudian como terapias combinadas en quimioterapia al aumentar la permeabilidad capilar o en la trombólisis (2).
SEGURIDAD Y EFECTOS ADVERSOS
Los contrastes ecográficos tienen una seguridad mayor que la de los usados en RM o TC gracias a su distribución exclusivamente intravascular y su eliminación completa. Aun así, pueden presentar efectos adversos comunes a otros tipos de contraste, como náuseas, vómitos, erupción cutánea o hipotensión. Muchos de estos efectos adversos se presentan en los pacientes de los grupos placebo (10), lo que implicaría una patogenia no relacionada con los componentes de los contrastes. Es importante resaltar la muy baja incidencia de reacciones anafilácticas (0,006%).
Estudios in vitro han relacionado el uso de contrastes ecográficos con efectos sobre hemólisis y agregación plaquetaria, dependiendo del número de microburbujas y el IM usado (10). Además, la presencia o sospecha de shunt cardíaco es una contraindicación al uso de todos los contrastes ecográficos. En estudios con roedores se observó que los que presentaban derivación intracardiaca desarrollaban estenosis arteriolar por las microburbujas mayores a 5 micras que pasaban a la circulación sistémica (11). Esta contraindicación está cuestionada al haberse observado sólo en roedores con efectos limitados, ya que solo el 1,2% de los roedores presentaron oclusión vascular, resuelta en un 85% de los casos en los primeros 10 minutos (11).
Su eliminación respiratoria y nula interacción con la vía urinaria permiten su uso aún en pacientes con insuficiencia renal grave, donde se contraindica el uso de contrastes en TC o RM. Múltiples estudios han demostrado su seguridad en poblaciones pediátricos y en pacientes con insuficiencia cardiaca congestive, hipertensión pulmonar y otras enfermedades cardiovasculares (11).
APLICACIONES CLÍNICAS DE LOS CONTRASTES ECOGRÁFICOS
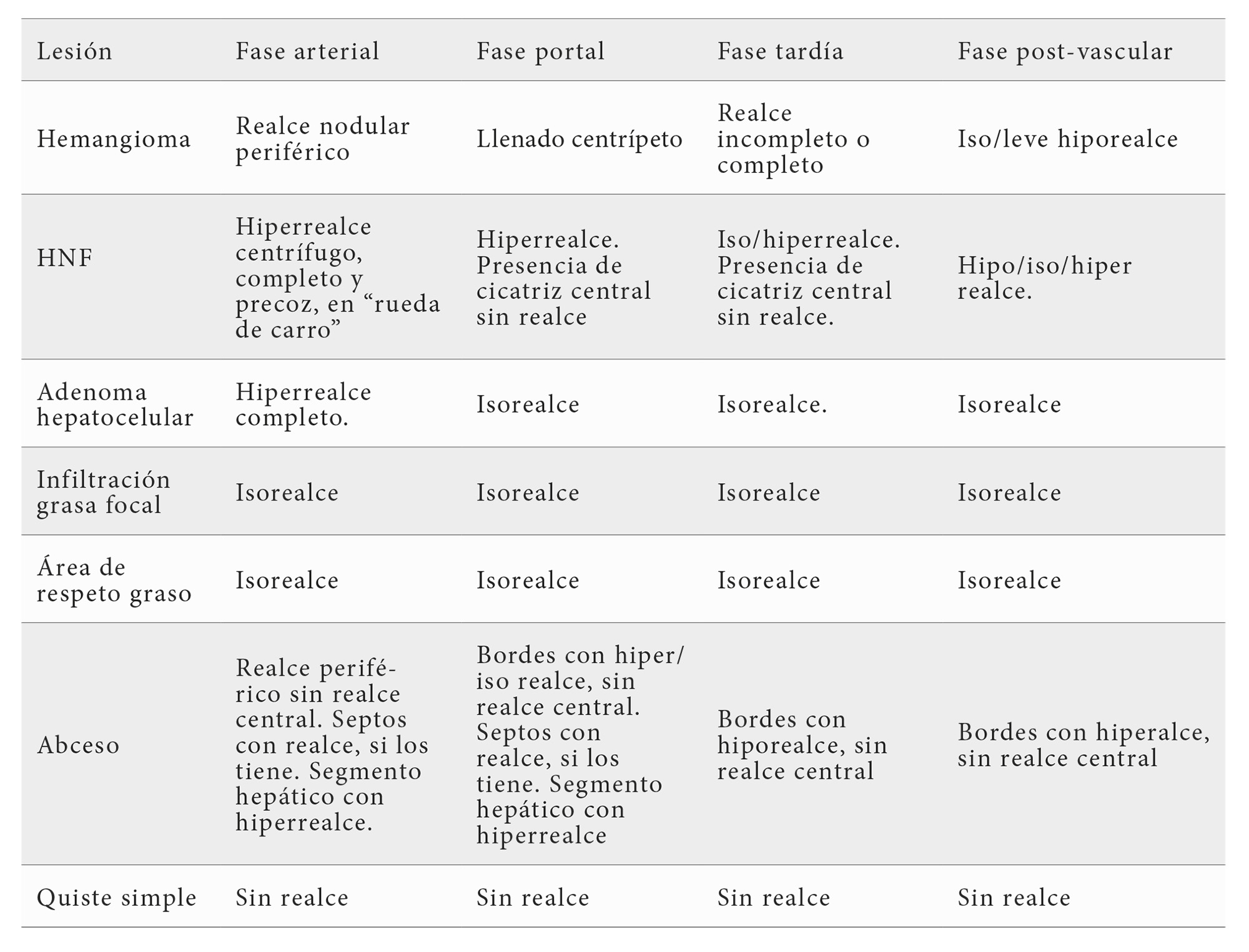
Valoración hepática
Se describen distintas fases de realce según el tipo de tejido y su aporte vascular. La fase arterial ocurre a los 10-20 segundos tras la inyección, la fase portal venosa entre los 30-120 segundos, y la fase tardía desde los 120 segundos hasta la desaparición del contraste (4-8 minutos). Existe una fase reticuloendotelial a partir de los 8 minutos sólo con el contraste Sonazoid (no comercializado en España), que se incorpora a las células de Kupffer. Los tumores suelen presentar un defecto de realce en esta fase (12,13,14).
Los patrones de realce ecográfico permiten diferenciar lesiones benignas y malignas, (Tablas 2 y 3), con sensibilidad y especificidad comparables a las de TC y RM. Las guías recomiendan su uso de primera línea ante lesiones incidentales, independientemente de la presencia de factores de riesgo de malignidad (14).
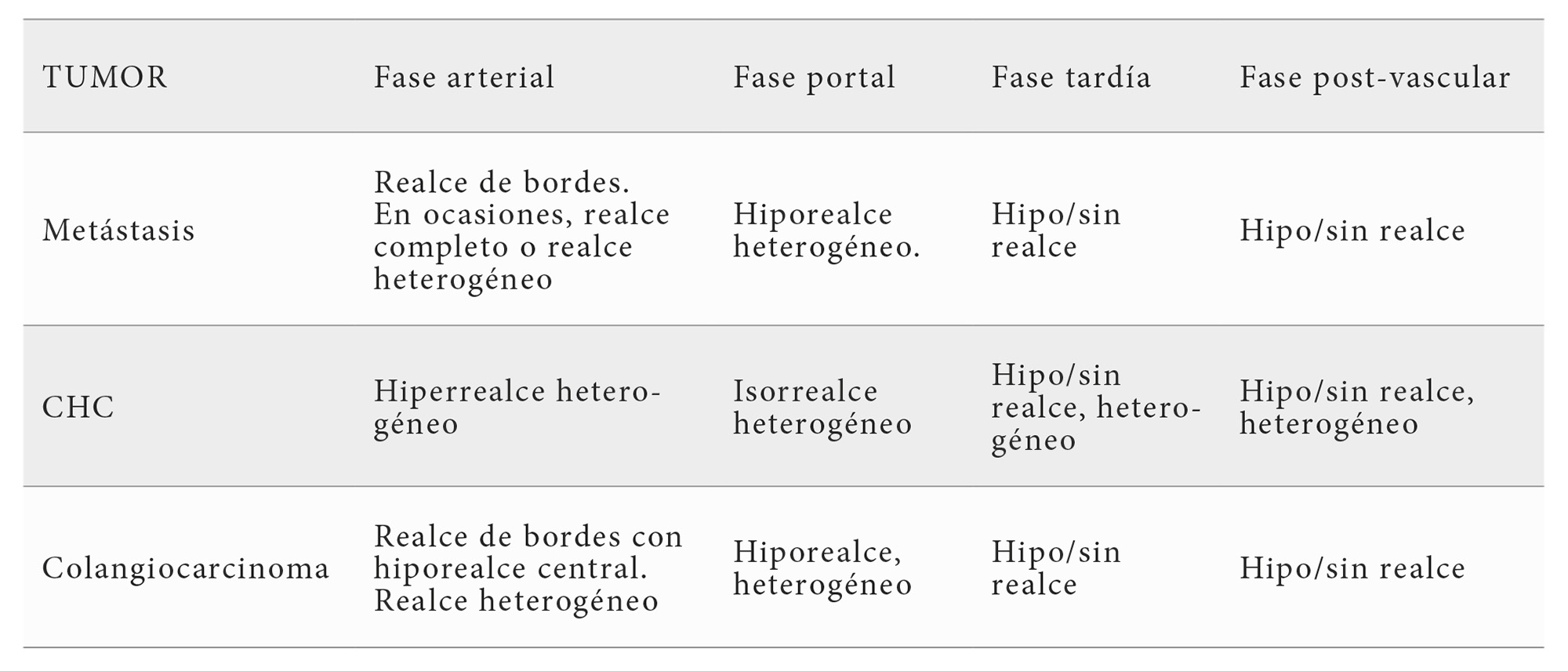
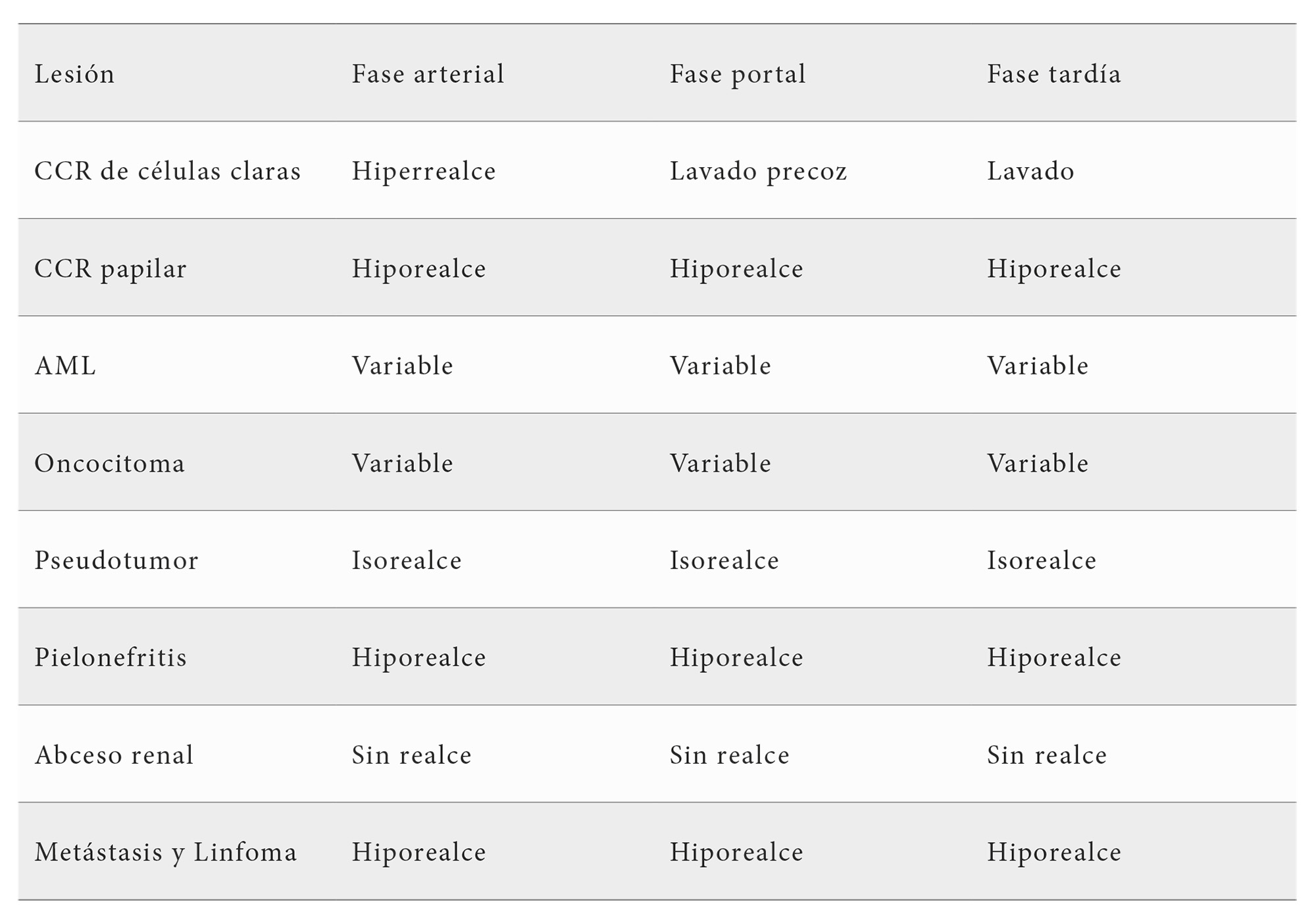
La interpretación de la lesión focal hepática mediante ecografía con contraste difiere según se trate de un hígado sano o un hígado cirrótico. En un hígado sano, el objetivo principal es diferenciar si se trata de una lesión benigna para evitar pruebas adicionales. En el hígado cirrótico, la ecografía con contraste puede utilizarse como primera línea para establecer un diagnóstico de malignidad (CEUS LR-M), específicamente del carcinoma hepatocelular (CEUS LR-5) (14), si bien la valoración por TC o RM sigue siendo necesaria para una caracterización precisa de la lesión.
También permite diferenciar trombosis portal benigna de maligna en pacientes con HCC: En la trombosis maligna se observa realce intravascular en la fase arterial debido a la neoangiogénesis tumoral, mientras que en la benigna no hay realce (14, 15).
Valoración renal
Las arterias renales principales y sus ramas realzan primero, seguidas del parénquima renal en dos fases. En la fase cortical (15-30 s tras inyección) la corteza renal presenta mayor realce que las pirámides medulares, mientras que en la fase medular (30 s a 5 min): se realza antes la porción externa de la pirámide medular, seguido de su llenado gradual hasta que el realce cortical y medular se igualan.
La Tabla 4 resume los principales patrones de realce de algunas lesiones como angiomiolipomas (AML), carcinomas de células renales (CCR), oncocitoma y pseudotumores. Dado que existe una superposición significativa en las características de imagen entre AML y CCR, la ecografía con contraste no debe ser empleada como única herramienta para diferenciarlos y no reemplaza otros estudios (16). En cuanto a los oncocitomas renales, la ecografía con contraste presenta importantes limitaciones para diferenciarlos de neoplasias renales sólidas malignas de bajo grado (al igual que con TC y RM) (16). En cuanto a las neoplasias no renales como metástasis o linfomas, algunos reportes los identifican como lesiones hipovasculares en todas las fases, si bien hay pocos estudios al respecto (16).
Los pseudotumores son falsas lesiones que imitan procesos neoplásicos, generalmente por variantes de desarrollo y otras etiologías benignas. La ecografía con contraste es útil para caracterizarlos y diferenciarlos de lesiones malignass, al demostrar en la fase arterial temprana una arquitectura normal del parénquima renal sin interrupción de los vasos o vasos aberrantes (16,17).
También ha mostrado ser eficaz en la caracterización de lesiones quísticas complejas mejorando la detección de septos, engrosamiento de paredes y realce de componentes sólidos, superando a la TC en algunos casos (si bien la presencia de calcificaciones puede impedir la correcta valoración de lesiones). Eñ hallazgo de realce en componentes nodulares o sólidos debe generar sospecha de malignidad. Los criterios de Bosniak, originalmente desarrollados para TC, pueden emplearse para caracterizar las lesiones quísticas complejas mediante la ecografía contrastada (16,18). Puede usarse también para caracterizar lesiones renales indeterminadas, siendo más sensible que la TC para detectar el flujo sanguíneo en lesiones hipovasculares (17).
En cuanto a infecciones, los hallazgos que sugieren pielonefritis incluyen defectos de perfusión y realce heterogéneo (15). En el riñón trasplantado, al igual que en los riñones nativos, el contraste ecográfico puede aportar información adicional acerca de la naturaleza de la lesión, siendo útil para identificar características sospechosas de malignidad. Además, permite la valoración vascular del trasplante (16).
En los casos en que el estudio de una masa renal requiere de biopsia, el contraste ecográfico puede ser útil para guiar la aguja hacia las partes más vascularizadas de la lesión, evitando componentes sin realce, potencialmente necróticos (16).
Valoración vía urinaria
En el diagnóstico de reflujo vesicoureteral en niños mediante ha mostrado utilidad la administración intracavitaria de contraste (17). De hecho, SonoVue™ (Bracco SpA, Milan) está aprobado por la A.E.M.P.S. para este propósito, presentando un perfil de seguridad favorable en pacientes pediátricos (16).
La principal utilidad del contraste ecográfico es orientar el diagnóstico diferencial entre cáncer vesical versus hematoma en pacientes con hematuria. En las lesiones neoplásicas encontraremos focos de captación, al contrario de los hematomas. No obstante, presenta importantes limitaciones ya que hay otras condiciones que pueden presentar realce focal de la pared vesical simulando lesiones malignas (16).
Valoración del sistema musculoesquelético
El principal uso de la ecografía con contraste en este ámbito es guiar la biopsia percutánea transtorácica con aguja. Si bien los estudios al respecto son heterogéneos, los resultados sugieren que mejora la precisión diagnóstica de las biopsias en comparación con el ultrasonido simple (precisión diagnóstica promedio de 95.4 % vs 80.8%) (19).
Su uso fuera de los procedimientos intervencionistas es seguro, pero menos investigado (19). Permite el diagnóstico precoz de cambios en la microcirculación de los pacientes con enfermedades inflamatorias u oclusivas, en las que encontramos una disminución del flujo capilar y un aumento del tiempo de llegada del contraste a los tejidos musculares al ejercicio. También sirve para caracterizar patologías que afecten a la circulación arterial como el síndrome compartimental crónico (20,21).
Sin embargo, su especificidad y sensibilidad siguen siendo menores que las de resonancia magnética en muchos casos como la miositis (en la que el aumento de vascularización por sí solo no resulta de suficiente ayuda diagnóstica), o la sacroileitis (en la que no es posible valorar adecuadamente los cambios en estructuras profundas) (21).
Se ha encontrado uso para el estudio de tendinopatías, encontrando aumento de la microvascularización de tendones afectados en situaciones en las que el estudio Doppler no había resultado diagnóstico (22).
También tienen utilidad diagnóstica en la valoración de patología articular inflamatoria activa al mejorar la visualización de los cambios en la vascularización (21), o el crecimiento anormal del pannus sinovial. Ayuda a diferenciar entre enfermedades activas e inactivas, permitiendo un seguimiento más preciso y un mejor control del tratamiento, especialmente en la artritis reumatoide.
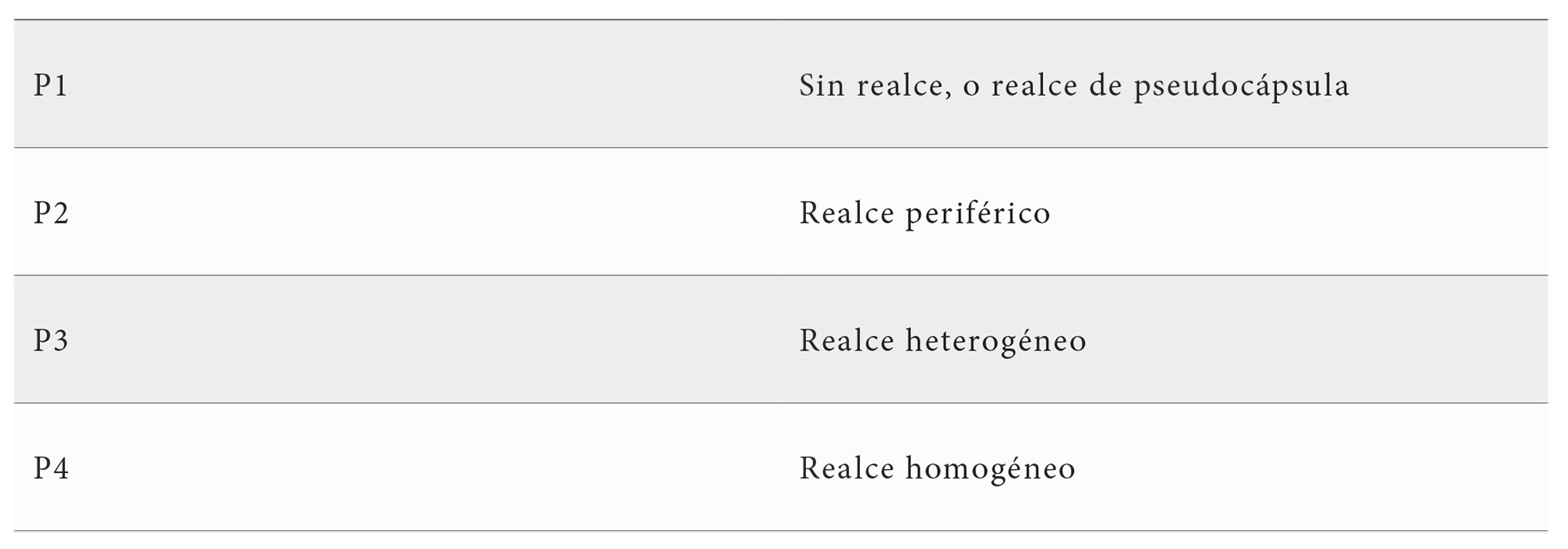
Finalmente, uno de sus usos más ampliados es la caracterización tumoral según el patrón de perfusión de las lesiones (Tabla 1). En los últimos años se ha extendido su aplicación en la escisión de masas y biopsias tumorales, en las que resulta de mayor utilidad en casos de heterogeneidad de la lesión o sospecha de necrosis (22) (Tabla 1).
Valoración testicular
En la torsión testicular, pueden confirmar la ausencia de vascularización, sin aportar grandes ventajas sobre el Doppler color. Ayudan a diferenciar infartos segmentarios de tumores poco vascularizados al mostrar áreas isquémicas separadas por vasos normales.
En casos de traumatismo testicular, la ecografía con contraste permite evaluar con mayor precisión qué zonas del tejido siguen siendo viables, diferenciar fracturas o hematomas y facilitar un tratamiento más conservador.
Valoración pancreática
En el páncreas, el contraste ecográfico ayuda a diferenciar tumores neuroendocrinos- hipervasculares en la fase arterial- de otras lesiones como el adenocarcinoma – hipervascular en todas las fases. También permite diferenciar los tumores quísticos pancreáticos del pseudoquiste (17).
Valoración gastrointestinal
Los contrastes ecográficos se han utilizado principalmente en la enfermedad inflamatoria intestinal, donde permiten evaluar la microvascularización producida por la neoangiogénesis inflamatoria, sin interferencias del peristaltismo (a diferencia del Doppler color que solo detecta vasos macroscópicos). También permiten valorar la extensión y presencia de actividad inflamatoria, facilitando la evaluación de la respuesta al tratamiento (14).
Valoración sistema vascular
El ultrasonido con contraste es útil en la evaluación del sistema vascular extracerebral mejorando la detección de flujo sanguíneo lento y la visualización de estructuras vasculares. Aumenta la sensibilidad del Doppler, permitiendo diferenciar entre oclusión total y estenosis suboclusiva, evaluar reestenosis post-stent e identificar disecciones carotídeas y patología vascular.
Uso en Intervencionismo
Ha mostrado utilidad para guiar procedimientos como biopsias, ablaciones o drenajes, o para monitorizar la respuesta terapéutica en quimioembolización transarterial (TACE) (14,15). Permite evitar la biopsia de tejido necrótico al dirigir la aguja hacia áreas vascularizadas dentro de la lesión, aumentando la precisión diagnóstica. También es útil en la biopsia de lesiones poco visibles en ultrasonido convencional, haciendo más evidentes las lesiones identificadas en otros estudios (17).
Indicaciones en pediatría
En pediatría, el contraste ecográfico ha ganado aprobación por su perfil de seguridad y eficacia. Aunque hay pocas publicaciones que describen sus aplicaciones en niños, la EFSUMB reconoce su potencial en indicaciones renales comparables a las de adultos. Sin embargo, la Agencia Europea de Medicamentos (EMA) solo ha aprobado su uso en niños para evaluar el reflujo vesicoureteral (SonoVue y Levovist). Por ello, su administración pediátrica sigue siendo poco indicada en Europa, y en Estados Unidos solo está aprobada para lesiones hepáticas focales (13,14,17,23).
El ultrasonido con contraste permite estudios sin radiación, lo que lo hace atractivo en pediatría para evaluar abscesos, pielonefritis o malformaciones vasculares, especialmente en el sistema renal y genitourinario, mejorando la detección y planificación quirúrgica (13,17). En tumores renales sólidos infantiles no se han descrito patrones de realce específicos, por lo que se recurre a TC o RM para su caracterización y estadificación (13,17).
En la artritis idiopática juvenil se observa realce articular por inflamación en formas precoces (21). También se ha estudiado su uso en la necrosis avascular idiopática de la epífisis femoral proximal (Legg-Calvé-Perthes), con mayor sensibilidad para detectar la revascularización arterial (21). Presenta resultados similares a la RM en displasia de cadera (21).
La ecografía con contraste muestra potencial en el traumatismo abdominal cerrado infantil, con alta sensibilidad (88.5%) y especificidad (98.5%) para lesiones de órganos sólidos, siendo una alternativa en niños hemodinámicamente estables tras traumatismos leves a moderados (30). No es útil para detectar lesiones en la vía excretora ni en el mesenterio, intestino, diafragma o retroperitoneo, donde su visualización es limitada. Se requieren más estudios para validar su uso diagnóstico y reducir la exposición a radiación (24,25,27).
Limitaciones del uso del contraste ecográfico
Aunque los contrastes han aportado numerosas ventajas a la ecografía, existen limitaciones que pueden agruparse en 3 categorías (17):
- Limitaciones propias de la ecografía: Requiere de una ventana ecográfica aceptable. La obesidad, interposición de gas o la presencia de lesiones profundas dificultan o imposibilitan la visualización del contraste (17,28,29). Es una técnica operador dependiente con una gran variabilidad inter-observador (28,29), existiendo hasta un 10% de solapamiento en las características de la imagen de quistes renales de categorías 2, 2F y 3 (28).
- Limitaciones técnicas y de formación: Al ser una técnica relativamente nueva y que requiere de equipos avanzados, es necesario profesional entrenado que no siempre está disponible en la práctica habitual (28). Existen diversos errores que el personal puede realizar y que podrían llevar a un error diagnóstico, como usar un IM elevado pensando que mejoraría la visualización de estructuras profundas (consiguiendo el efecto contrario al aumentar la destrucción de las microburbujas), usar dosis de contraste elevadas para aumentar la ecogenicidad de las lesiones (impidiendo la visualización de estructuras distales por bloqueo del haz ecográfico) o usar secuencias de pulsos a un frame rate que no sea lo suficientemente elevado como para permitir el estudio de lesiones de rápida captación de contraste (30).
- Limitaciones debidas al propio contraste: Al no eliminarse por vía urinaria, no son útiles para visualizar lesiones pielocaliciales o de la vía excretora renal (28). Tampoco permiten evaluar simultáneamente lesiones distantes entre sí, al tener que administrar un bolus de contraste para el estudio de cada lesión individual (28,30).
CONCLUSIONES
Los contrastes ecográficos utilizan microburbujas que interactúan con los ultrasonidos para hacerse visibles con técnicas específicas. Los comercializados en España presentan una mayor seguridad que los contrastes de TC y RM, lo que justifica su aplicación en muy diversas patologías, tanto en adultos como pacientes pediátricos, mejorando significativamente la sensibilidad y especificidad de la ecografía y el Doppler. Pese a sus limitaciones, representan una herramienta diagnóstica con constantes exoansiones en su uso clínico.
DECLARACIÓN DE TRANSPARENCIA
Los autores/as de este artículo declaran no tener ningún tipo de conflicto de intereses respecto a lo expuesto en el presente trabajo.
BIBLIOGRAFÍA
- ↑Gramiak R, Shah PM. Ecocardiografía de la raíz aórtica. Invertir Radiol. 1968; 3(5):356–366.
- ↑Chong WK, Papadopoulou V, Dayton PA. Imagen con contrastes ultrasónicos: estado actual y futuro. Abdom Radiol N Y. 2018; 43(4):762–72.
- ↑Tarighatnia A, Fouladi MR, Nader ND, Aghanejad A, Ghadiri H. Tendencias recientes de los agentes de contraste en la ecografía: una revisión de las clasificaciones y aplicaciones. Mater Adv. 2022; 3(9):3726–3741.
- ↑Yang Z, Lv M, Yu Z, et al. Un análisis bibliométrico de la ecografía con contraste en los últimos veinte años. Quant Imaging Med Surg. 2024 ; 14(8):5555570–5555570.
- ↑Frinking P, Segers T, Luan Y, Tranquart F. Tres décadas de agentes de contraste ultrasónicos: una revisión de las mejoras pasadas, presentes y futuras. Ultrasonido Med Biol. 2020; 46(4):892–908.
- ↑Stride E, Saffari N. Agentes de contraste de ultrasonido de microburbujas: una revisión. proc inst mech eng [h]. 2003; 217(6):429–447.
- ↑Greco A, Mancini M, Gargiulo S, et al. Biomicroscopía ultrasónica en la investigación con pequeños animales: aplicaciones en imagen molecular y preclínica. J Biomed Biotechnol. 2012;2012:519238.
- ↑Calliada F, Campani R, Bottinelli O, Bozzini A, Sommaruga MG. Agentes de contraste ultrasónicos: principios básicos. Eur J Radiol. 1998; 27 Supl. 2:S157-160.
- ↑Wilson SR, Greenbaum LD, Goldberg BB. Ecografía con contraste: ¿cuáles son las pruebas y cuáles son los obstáculos? AJR Am J Roentgenol. 2009 ; 193(1):55–60.
- ↑Jakobsen JA, Oyen R, Thomsen HS, Morcos SK, Miembros del Comité de Seguridad de Medios de Contraste de la Sociedad Europea de Radiología Urogenital (ESUR). Seguridad de los agentes de contraste ultrasónicos. Eur Radiol. 2005; 15(5):941–945.
- ↑Parker JM, Weller MW, Feinstein LM, et al. Seguridad de los agentes de contraste de ultrasonido en pacientes con derivaciones cardíacas conocidas o sospechadas. Am J Cardiol. 201310; 112(7):1039-1045.
- ↑Mandai M, Koda M, Matono T, Nagahara T, Sugihara T, Ueki M, et al. Assessment of hepatocellular carcinoma by contrast-enhanced ultrasound with perfluorobutane microbubbles: comparison with dynamic CT. Br J Radiol. 2011 Jun;84(1002):499–507
- ↑Back SJ, Acharya PT, Bellah RD, Cohen HL, Darge K, Deganello A, et al. Contrast-enhanced ultrasound of the kidneys and adrenals in children. Pediatr Radiol. 2021 Nov;51(12):2198–213.
- ↑Dietrich CF, Nolsøe CP, Barr RG, Berzigotti A, Burns PN, Cantisani V, et al. Guidelines and Good Clinical Practice Recommendations for Contrast-Enhanced Ultrasound (CEUS) in the Liver-Update 2020 WFUMB in Cooperation with EFSUMB, AFSUMB, AIUM, and FLAUS. Ultrasound Med Biol. 2020 Oct;46(10):2579–604.
- ↑Pang EHT, Chan A, Ho SG, Harris AC. Contrast-Enhanced Ultrasound of the Liver: Optimizing Technique and Clinical Applications. AJR Am J Roentgenol. 2018 Feb;210(2):320–32
- ↑Kazmierski B, Deurdulian C, Tchelepi H, Grant EG. Applications of contrast-enhanced ultrasound in the kidney. Abdom Radiol N Y. 2018 Apr;43(4):880–98.
- ↑Sidhu PS, Cantisani V, Dietrich CF, Gilja OH, Saftoiu A, Bartels E, et al. The EFSUMB Guidelines and Recommendations for the Clinical Practice of Contrast-Enhanced Ultrasound (CEUS) in Non-Hepatic Applications: Update 2017 (Short Version). Ultraschall Med Stuttg Ger. 2018 Apr 1;39(2):154–80.
- ↑Cantisani V, Bertolotto M, Clevert DA, Correas JM, Drudi FM, Fischer T, et al. EFSUMB 2020 Proposal for a Contrast-Enhanced Ultrasound-Adapted Bosniak Cyst Categorization – Position Statement. Ultraschall Med Stuttg Ger 1980. 2021 Apr;42(2):154–66.
- ↑Jacobsen N, Pietersen PI, Nolsoe C, Konge L, Graumann O, Laursen CB. Clinical Applications of Contrast-Enhanced Thoracic Ultrasound (CETUS) Compared to Standard Reference Tests: A Systematic Review. Ultraschall Med Stuttg Ger 1980. 2022 Feb;43(1):72–81.
- ↑Davidson BP, Hodovan J, Mason OR, Moccetti F, Gupta A, Muller M, et al. Limb Perfusion During Exercise Assessed by Contrast Ultrasound Varies According to Symptom Severity in Patients with Peripheral Artery Disease. J Am Soc Echocardiogr Off Publ Am Soc Echocardiogr. 2019 Sep;32(9):1086-1094.e3.
- ↑Ntoulia A, Barnewolt CE, Doria AS, Ho-Fung VM, Lorenz N, Mentzel HJ, et al. Contrast-enhanced ultrasound for musculoskeletal indications in children. Pediatr Radiol. 2021 Nov;51(12):2303–23.
- ↑Chen SY, Wang YW, Chen WS, Hsiao MY. Update of Contrast-enhanced Ultrasound in Musculoskeletal Medicine: Clinical Perspectives – A Reviewx. J Med Ultrasound. 2023 Jun;31(2):92
- ↑Dietrich CF, Augustiniene R, Batko T, Cantisani V, Cekuolis A, Deganello A, et al. European Federation of Societies for Ultrasound in Medicine and Biology (EFSUMB): An Update on the Pediatric CEUS Registry on Behalf of the “EFSUMB Pediatric CEUS Registry Working Group.” Ultraschall Med Stuttg Ger 1980. 2021 Jun;42(3):270–7.
- ↑Diagnostic performance of contrast-enhanced ultrasound in traumatic solid organ injuries in children: a systematic review and meta-analysis | Pediatric Radiology [Internet]. [cited 2025 Apr 4]. Available from: https://link.springer.com/article/10.1007/s00247-024-06127-9.
- ↑Pegoraro F, Giusti G, Giacalone M, Parri N. Contrast-enhanced ultrasound in pediatric blunt abdominal trauma: a systematic review. J Ultrasound. 2022 Sep;25(3):419–27.
- ↑Paltiel HJ, Barth RA, Bruno C, Chen AE, Deganello A, Harkanyi Z, et al. Contrast-enhanced ultrasound of blunt abdominal trauma in children. Pediatr Radiol. 2021 Nov;51(12):2253–69.
- ↑Jannatdoust P, Valizadeh P, Hassankhani A, Amoukhteh M, Ghadimi DJ, Heidari-Foroozan M, et al. Diagnostic performance of contrast-enhanced ultrasound in traumatic solid organ injuries in children: a systematic review and meta-analysis. Pediatr Radiol. 2025 Feb;55(2):226–41.
- ↑Cokkinos DD, Antypa EG, Skilakaki M, Kriketou D, Tavernaraki E, Piperopoulos PN. Contrast Enhanced Ultrasound of the Kidneys: What Is It Capable of? BioMed Res Int. 2013;2013:595873.
- ↑Chiorean L, Tana C, Braden B, Caraiani C, Sparchez Z, Cui XW, et al. Advantages and Limitations of Focal Liver Lesion Assessment with Ultrasound Contrast Agents: Comments on the European Federation of Societies for Ultrasound in Medicine and Biology (EFSUMB) Guidelines. Med Princ Pract. 2016 Aug;25(5):399–407.
- ↑Dietrich CF, Ignee A, Hocke M, Schreiber-Dietrich D, Greis C. Pitfalls and artefacts using contrast enhanced ultrasound. Z Gastroenterol. 2011 Mar;49(3):350–6
Rafael Picó Cantos
Hospital universitario y Politécnico La Fe
Avenida Fernando Abril Martorell, 106 · 46026 Valencia
Tlf.: +34 645 851 486 | E-Mail: pico_rafcan@gva.es
Año 2025 · número 142 (02) · páginas 180 a 190
Enviado: 12.04.25
Revisado: 29.04.25
Aceptado: 21.05.25


