Resumen
La Resonancia Magnética Cardiaca (RMC) es el estándar de oro para evaluar la morfología, función y la caracterización tisular miocárdica in vivo. Sin embargo, su complejidad y larga duración han limitado su uso. Los avances metodológicos han permitido desarrollo de protocolos de RMC ultrarrápidos y mejorar la cuantificación de parámetros fisiológicos como el estado de la vascularización del tejido cardiaco. Estos avances en la adquisición de RMC avanzada no solo mejora el diagnóstico, sino que se establece como una plataforma crítica para la investigación traslacional. En este aspecto en este trabajo nos centramos en una descripción de las técnicas y la impacto que estas han tenido en la comprensión del estado de la microcirculación en enfermedad cardiovascular subclínica y en la búsqueda de nuevas terapias para reducir el impacto que los tratamientos oncológicos tienen en el corazón.
Abstract
Cardiac magnetic resonance imaging (CMR) is the gold standard for evaluating ventricular morphology, function and myocardial tissue characterization in vivo. However, its complexity and long scan times have limited its use. Methodological advances have enabled the development of ultra-fast CMR protocols and improved the quantification of physiological parameters such as the vascularization status of cardiac tissue. These advances in advanced CMR acquisition not only improve diagnosis but also establish it as a critical platform for translational research. In this work, we focus on describing the techniques and their impact on understanding the microcirculatory status in subclinical cardiovascular disease and on the search for new therapies to reduce the impact of cancer treatments on the heart.
Palabras clave: Resonancia Magnética Cardiaca; Perfusión Miocárdica Cuantitativa; Disfunción Microvascular Coronaria (DMC); Cardiotoxicidad por Antraciclinas (CIA); Condicionamiento Isquémico Remoto (RIC); Protocolos Ultrarrápidos.
Keywords: Cardiac Magnetic Resonance; Quantitative Myocardial Perfusion; Coronary Microvascular Dysfunction (CMD); Anthracycline Cardiotoxicity (CIA); Remote Ischemic Conditioning (RIC); Ultra-Fast Protocols.
INTRODUCCIÓN
La Resonancia Magnética Cardiaca (RMC) es considerada el patrón oro para la evaluación de la función ventricular y la caracterización tisular miocárdica in vivo. A pesar de su superioridad diagnóstica, la RMC ha enfrentado retos importantes en términos de eficiencia de adquisición y la robustez de las técnicas cuantitativas. La integración de la RMC en la práctica clínica y la investigación traslacional ha impulsado el desarrollo de metodologías avanzadas que abordan estos desafíos (1,2). En este trabajo se describen algunos de los desarrollos realizados para acelerar significativamente la adquisición de estudios de función y caracterización tisular del músculo cardiaco. Asimismo, se presentan los avances dirigidos a mejorar la cuantificación de parámetros como la perfusión miocárdica, destacando el impacto que estos tienen en una mejor comprensión de los riesgos cardiovasculares subclínicos y la cardiotoxicidad por antraciclinas. (3,4,5).
INNOVACIONES METODOLÓGICAS DE LA RMC
Aunque la RMC es una de las técnicas de imagen médica que proporciona un mayor rendimiento diagnóstico para la evaluación e investigación de las enfermedades cardiovasculares su uso sigue principalmente restringido a centros altamente especializados. Uno de los mayores retos que limita su expansión es la complejidad tanto a la adquisición de imágenes como a su posterior interpretación.
1. Validación Clínica del Protocolo 3D Ultrarrápido (UFast CMR)
La adquisición de estudios de RM cardiaca normalmente requiere la búsqueda de las orientaciones adecuadas para permitir una correcta evaluación de la anatomía, la función y la caracterización miocárdica. Este proceso requiere un conocimiento profundo de la anatomía cardiaca y la colaboración por parte del paciente en la realización de distintas apneas hasta permitir localizar estas orientaciones. La necesidad de realizar múltiples apneas durante la adquisición hace que el paciente se fatigue, obligando a introducir tiempos de recuperación que prolongan significativamente la duración del estudio. Todo esto conduce a que la realización de estudios de RM cardiaca sea complicada y costosa en tiempos de ocupación de equipos de RM haciendo que su realización se limite principalmente en centros altamente especializados.
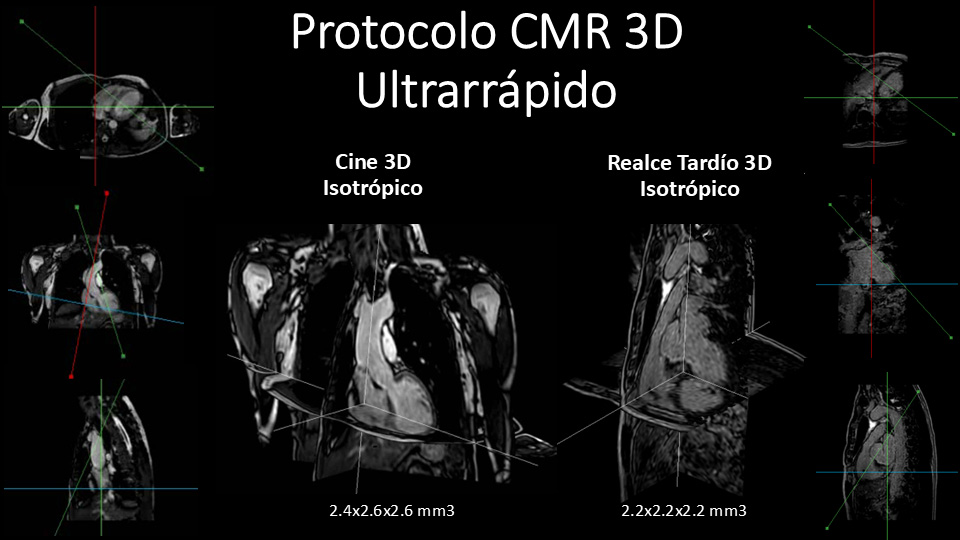
Esta dificultad abre el camino a explorar protocolos rápidos de adquisición. En los últimos años se han desarrollado técnicas que permiten la adquisición de volúmenes 3D isotrópicos en una sola apnea (figura 1), eliminando la necesidad de buscar las orientaciones del músculo cardiaco durante la adquisición. Esto simplifica drásticamente tanto los estudios de cine como los de realce tardío. Estas técnicas se han validado en una cohorte de más de 120 pacientes de distintas patologías cardiacas (3) y aórticas (5) demostrando una gran concordancia con la metodología convencional 2D en la cuantificación de la fracción de eyección tanto del ventrículo izquierdo (FEVI) como del derecho y del volumen de escara en estudios de realce tardío.
2. Optimización de la Cuantificación Absoluta de la Perfusión
Además del estudio de la anatomía y la función cardiaca, en los últimos años la resonancia magnética cardiaca ha evolucionado permitiendo una mejor comprensión del estado del músculo cardiaco mediante una mejor caracterización tisular. Esta caracterización ha evolucionado desde la medición del tamaño de la cicatriz cardiaca, mediante estudios de realce tardío, a métodos cuantitativos para estimar mapas paramétricos como los valores de T1 y T2 miocárdicos. Esta rápida evolución ha permitido que este tipo de adquisiciones estén incluidas en la mayoría de las exploraciones de RMC.
Junto a la caracterización y la evaluación de la función cardiaca y tejido miocárdico, el estudio de la microcirculación también juega un papel fundamental para una adecuada comprensión del estado del músculo cardiaco. Aunque existen distintas formas de medir la perfusión miocárdica por técnicas de medicina nuclear y tomografía computarizada (6,7) la RMC ha demostrado que tiene una buena correlación con estas técnicas sin necesidad de utilizar radiación ionizante. Por otro lado, también se ha demostrado lo no inferioridad diagnóstica compara con medidas invasivas (8). La evaluación del estado de la microcirculación en estudios de perfusión miocárdica mediante RMC se basa en el seguimiento dinámico de un primer paso de contraste intravenoso (bolo) a través de cavidades y tejido miocárdico. Para maximizar la sensibilidad al efecto T1 del contraste, estas imágenes se adquieren después de la aplicación de un pulso de saturación que anula toda la señal; a continuación, la señal se recupera de forma exponencial con la relajación T1 del tejido. Por tanto, la sensibilidad de la secuencia a concentraciones de contraste se puede modular por el tiempo que pasa entre la aplicación del pulso de saturación y en tiempo de adquisición de la imagen de RM.
En la actualidad, si bien existen métodos pseudo cuantitativos para analizar estos estudios dinámicos para ver diferencias entre regiones cardiacas, pierden sensibilidad cuando todos los territorios coronarios están afectados o para distinguir de forma adecuada entre estados de reposo o hiperemia (9). Por otro lado, para una adecuada interpretación de estos estudios es necesario una gran experiencia limitando la realización de estos estudios solamente a centros de referencia en imagen cardiaca (10). Para atajar estas limitaciones en los últimos años se han propuesto metodologías de adquisición y análisis que permiten estimar el flujo sanguíneo miocárdico (MBF de sus siglas en inglés, Myocardial Blood Flow).
Para estimar con precisión el MBF es necesario cuantificar la cantidad de contraste que le llega al miocardio desde la aorta, a través del seno coronario, y ponerlo en relación con la captación del contraste en el tejido. Esta medida en la aorta se utiliza para definir la función de entrada arterial (AIF de sus siglas en inglés Arterial Input Function). La diferencia de concentración de contraste entre la sangre que sale de la aorta y la sangre que llega al musculo cardiaco, combinada con la no linealidad de la señal de RMC con la concentración de contraste, hace complicado una evaluación precisa de las concentraciones en ambos territorios utilizando la misma metodología.
La primera aproximación que se propuso es la inyección del contraste en dos bolos de distinta concentración de forma consecutiva utilizando un bolo diluido al principio, para estimar la AIF, y otro bolo completo para estimar la llegada del contraste al miocardio (9). Si bien esta metodología permite una adecuada estimación de la microcirculación su preparación en un entorno clínico es complejo y su uso no se ha extendido más allá de centros de investigación.
Otra alternativa para poder medir de forma precisa en ambos territorios es realizando una secuencia distinta para evaluar la información de contraste en la aorta y el músculo cardiaco. Como se ha comentado anteriormente, el tiempo que transcurre entre la aplicación del pulso y la adquisición de la imagen es denominado tiempo de saturación (TS) y permite modular la sensibilidad de la señal de RMC a la concentración de contraste. Si este tiempo es muy corto, la imagen es poco sensible a pequeñas variaciones de la concentración de contraste, pero por otro lado hace que su señal no esté saturada para altas concentraciones de contraste. La adquisición de una imagen con un TS corto permite adquirir de forma precisa la señal de la aorta a pesar de su alta concentración de contraste. Por otro lado, con TS más largos la señal es muy sensible a pequeñas variaciones de la señal convirtiéndola en un método muy adecuado para estudiar la evolución del bolo de contraste en el miocardio (11). Esta forma de adquirir la información tanto en la aorta como en el músculo cardiaco se denomina adquisición de doble saturación con bolo único y no precisa de la inyección de distintos bolos de contraste para obtener la información de la AIF y del músculo cardiaco. En un trabajo experimental se ha demostrado su buen comportamiento para distintos valores de perfusión miocárdica tanto en estudios en reposo como en estudios en hiperemia (1).
IMPACTO DE LAS TÉCNICAS DE IMAGEN EN LA COMPRENSION DE LAS ENFERMEDADES CARDIACAS.
La enfermedad cardiovascular sigue siendo la primera causa de muerte por encima del cáncer siendo el infarto de miocardio la entidad clínica más común. Por otro lado, en los últimos años el éxito de los tratamientos oncológicos han permitido una mayor supervivencia de los pacientes. Este hecho ha puesto de manifiesto el impacto que estos tratamientos tienen en otros órganos como el corazón. Este efecto secundario se conoce como cardiotoxicidad y su comprensión y manejo se han convertido en una entidad clínica de relevancia (12) y en un campo muy activo de investigación. Gran parte de los tratamientos oncológicos incluyen el uso de las antraciclinas y se estima que más de un 5% de los pacientes oncológicos supervivientes al cáncer sufrirán fallo cardiaco derivado del tratamiento con este fármaco (13). Por lo tanto, el estudio del efecto que este fármaco tiene en el corazón es un objetivo fundamental para estudiar la cardioxicidad.
Según las guías europeas, los parámetros de imagen que definen criterios de cardiotoxicidad son una caída absoluta de la FEVI de un 10% o más respecto a la situación inicial antes del comienzo del tratamiento, o una caída entre un 5% y un 10% con una FEVI final por debajo del 50%. Por otro lado, también existen consideraciones de parámetros serológicos que están más allá del objetivo de este artículo. Esta definición de cardiotoxicidad hace fundamentales los estudios de función cardiaca para evaluar el impacto de estos tratamientos en el corazón. Siendo la RMC la técnica más precisa para medir la FEVI, la posibilidad de tener protocolos ultrarrápidos para la estimación de este parámetro funcional abre las puertas a que un mayor número de pacientes se beneficien.
En el campo de la cardiotoxicidad las técnicas avanzadas de RMC han permitido el estudio de los parámetros que predicen de forma precoz el impacto del tratamiento con antraciclinas. Un estudio seriado de RM en modelos animales durante la administración del tratamiento oncológico permitió establecer el aumento de T2 en el corazón como parámetro precoz y reversible, anterior a la disfunción cardiaca. Este aumento del T2 está asociado, entre otros factores, al aumento de líquido intersticial en el músculo cardiaco (2). En este caso, los aumentos de T2 se correlacionaron con la aparición de vacuolas intracelulares derivadas de la reparación mitocondrial, resultado del mecanismo de reparación miocárdica necesaria después del daño generado por el tratamiento con antraciclinas (14). Al mismo tiempo, se confirmó que si de forma precoz se retiraba la exposición a las antraciclinas esta vacuolización se revertía, recuperando los valores de T2 del miocardio sin tener un impacto de la función contráctil del corazón a corto plazo.
Por otro lado, la aparición de nuevas técnicas de imagen ha permitido tener una mejor comprensión de las enfermedades cardiacas, permitiendo entender mejor el impacto de las alteraciones de la perfusión miocárdica en estadios precoces de la enfermedad cardiovascular. Un claro ejemplo (figura 2) de esta sensibilidad es el trabajo donde se estudiaron a 453 individuos asintomáticos de mediana edad sin factores de riesgo cardiovascular (4). Este estudio demostró que la función microvascular coronaria (medida a través de la reserva de flujo coronario por RM) estaba comprometida en individuos que tenían un mayor riesgo cardiometabólico. Esta disfunción se correlacionó inversamente con el número y la severidad de los factores de riesgo vascular tradicionales y se asoció de manera independiente con la presencia y la extensión de placas de ateroma en arterias periféricas medidas, mediante imagen vascular 3D por ultrasonido.
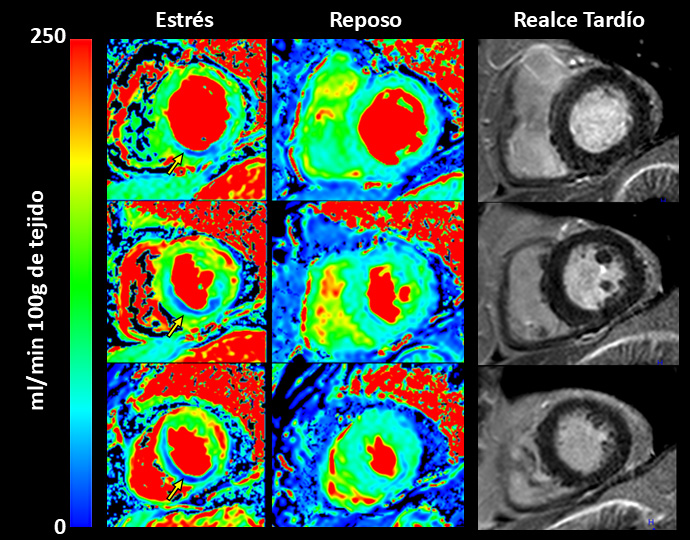
En el campo de la cardiotoxicidad la posibilidad de medir la perfusión miocárdica de forma cuantitativa reveló que la microcirculación se veía dañada de forma irreversible incluso en estos estadios precoces del tratamiento (15). Además, a medida que se aumentaba la exposición a las antraciclinas también aumentaba el daño en la microcirculación del corazón. La sensibilidad de esta técnica permitió obtener estas diferencias incluso en estado de reposo sin someter al corazón a situaciones de estrés, donde se requiere un aumento de la perfusión miocárdica para permitir un mayor consumo de energía por parte del corazón. Estos hallazgos se confirmaron también mediante técnicas histológicas estudiando la presencia de microcapilares en el tejido cardiaco y su endotelio. Este hallazgo es fundamental, ya que sugiere que el daño microvascular puede ser uno de los mecanismos que expliquen el daño a largo plazo que los tratamientos oncológicos pueden tener en el corazón con el posterior impacto en la función cardiaca.
ESTRATEGIAS PREVENTIVAS: EL ENSAYO RESILIENCE
Dado el papel central de las mitocondrias en la cardiotoxidad por antraciclinas, se han probado varias intervenciones dirigidas a los procesos mitocondriales, incluyendo antioxidantes, quelantes de hierro y terapia celular; sin embargo, a pesar de los prometedores resultados preclínicos, estos enfoques no han demostrado un beneficio clínico (16).
El condicionamiento isquémico remoto (RIC de sus siglas en inglés, remote ischemic conditioning) es una intervención no invasiva que consiste en ciclos breves y controlados de isquemia/reperfusión en una extremidad (generalmente el brazo). Aunque no se conoce el mecanismo de forma precisa, se ha demostrado que esta terapia tiene un efecto cardioprotector sistémico, principalmente a través de la liberación de mediadores humorales. Uno de los potenciales mecanismos de los beneficios de RIC es a través de la protección de la mitocondria (17) y también se ha demostrado la capacidad que esta terapia tiene en la protección del endotelio y la microcirculación (18, 19). Se ha demostrado la eficiencia de esta terapia en modelos animales preservando la contractibilidad de las regiones expuestas a antraciclinas comparado con un grupo control donde, estando expuestos a antraciclinas, no se aplicó la terapia de RIC (20).
Tras estos estudios iniciales en el modelo animal es necesaria una validación de esta terapia en un entorno más real en pacientes que va a ser tratados con antraciclinas. Con este objetivo se ha diseñado el estudio RESILIENCE (Rationale and dEsign of the RESILIENCE trial: a prospective randomIzed cLinical trial evaluating remote Ischemic conditioNing for the prEvention of anthracycline cardiotoxicity), que es un ensayo clínico de fase III, prospectivo, aleatorizado y multicéntrico, diseñado específicamente para validar una intervención no farmacológica dirigida a mitigar el daño inicial de la cardiotoxicidad por antraciclinas (20). El objetivo primario de este estudio es demostrar que el RIC puede reducir la incidencia de la cardiotoxicidad por antraciclinas, definida como la disminución de la FEVI o la elevación de biomarcadores (troponina).
Este ensayo se encuentra en fase de reclutamiento y asigna aleatoriamente a pacientes con cáncer que inician terapia con antraciclinas a un grupo de RIC activo o a un grupo simulado, donde los pacientes se aplican la terapia de RIC pero el manguito no aplica la presión suficiente para generar isquemia remota.
Para evaluar el efecto de la terapia se utiliza principalmente pruebas de imagen seriadas basadas en resonancia magnética cardiaca. El protocolo básico del estudio permite estudiar la FEVI, las variaciones de T1 y T2, la contractibilidad por técnicas de marcado miocárdico (tagging) y el realce tardío con técnicas 2D convencionales. Por otro lado, en un grupo limitado de centros, el protocolo también incluye la posibilidad de hacer técnicas más avanzadas donde se adquiere el protocolo ultrarrápido, el estudio de perfusión cuantitativa por RM, así como el estudio de la contractibilidad miocárdica por técnicas avanzadas (22). Este ensayo representa un paso clave en la medicina traslacional, aplicando el conocimiento mecanicista sobre el daño mitocondrial y microvascular (revelado por RMC) para guiar esta intervención preventiva.
CONCLUSIONES
Los avances recientes han transformado la RMC en una herramienta cuantitativa y eficiente, capaz de realizar un protocolo completo (función, viabilidad y perfusión) en un tiempo y con una precisión sin precedentes. Esta capacidad mejorada ha puesto de relieve la disfunción microvascular como un biomarcador de riesgo precoz siendo una señal temprana de la aterosclerosis subclínica en individuos con riesgo cardio-metabólico y es el primer signo de daño irreversible en la cardiotoxicidad por antraciclinas. El conocimiento derivado de la RMC está impulsando directamente el diseño de intervenciones clínicas como el ensayo RESILIENCE, cuyo objetivo es proteger el estado de la mitocondria y la microcirculación mediante el condicionamiento isquémico remoto (RIC). En última instancia, la RM cardiaca avanzada no solo mejora el diagnóstico, sino que también sirve como una plataforma crítica para la investigación traslacional dirigida a la prevención de la enfermedad cardiovascular.
DECLARACIÓN DE TRANSPARENCIA
Javier Sánchez-González y Alvaro Navarro Guzman son empleados de Philips Healthcare. El resto de los autores/as de este artículo declaran no tener ningún tipo de conflicto de intereses respecto a lo expuesto en el presente trabajo.
BIBLIOGRAFÍA
- ↑Sánchez-González J, Fernandez-Jiménez R, Nothnagel ND, López-Martín G, Fuster V, Ibañez B. Optimization of dual-saturation single bolus acquisition for quantitative cardiac perfusion and myocardial blood flow maps. J Cardiovasc Magn Reson. 2015;17(1):21.
- ↑Fernández-Jiménez R, Sánchez-González J, Aguero J, Del Trigo M, Galán-Arriola C, Fuster V, et al. Fast T2 gradient-spin-echo (T2-GraSE) mapping for myocardial edema quantification: first in vivo validation in a porcine model of ischemia/reperfusion. J Cardiovasc Magn Reson. 2015;17(1):92
- ↑Gómez-Talavera S, Fernandez-Jimenez R, Fuster V, Nothnagel ND, Kouwenhoven M, Clemence M, et al. Clinical validation of a 3-dimensional ultrafast cardiac magnetic resonance protocol including single breath-hold 3-dimensional sequences. JACC Cardiovasc Imaging. 2021;14(9):1742–54.
- ↑Devesa A, Fuster V, García-Lunar I, Oliva B, García-Alvarez A, Moreno-Arciniegas A, et al. Coronary microvascular function in asymptomatic middle-aged individuals with cardiometabolic risk factors. JACC Cardiovasc Imaging. 2025;18(1):48–58.
- ↑Gómez-Talavera S, Navarro-Guzmán Á, Fernández-Jiménez R, Fuster V, Sánchez-González J, Ibáñez B. ESSOS single breath-hold 3D magnetic resonance for the assessment of aortic dilation. Rev Esp Cardiol (Engl Ed). 2025.
- ↑Kikuchi Y, Oyama-Manabe N, Naya M, Manabe O, Tomiyama Y, Sasaki T, et al. Quantification of myocardial blood flow using dynamic 320-row multi-detector CT as compared with 15O-H2O PET. Eur Radiol. 2014;24(7):1547–56.
- ↑Morton G, Chiribiri A, Ishida M, Hussain ST, Schuster A, Indermuehle A, et al. Quantification of absolute myocardial perfusion in patients with coronary artery disease: comparison between cardiovascular magnetic resonance and positron emission tomography. J Am Coll Cardiol. 2012;60(16):1546–55.
- ↑Nagel E, Greenwood JP, McCann GP, Bettencourt N, Shah AM, Hussain ST, et al. Magnetic resonance perfusion or fractional flow reserve in coronary disease. N Engl J Med. 2019;380(25):2418–28.
- ↑Hsu L-Y, Rhoads KL, Holly JE, Kellman P, Aletras AH, Arai AE. Quantitative myocardial perfusion analysis with a dual-bolus contrast-enhanced first-pass MRI technique in humans. J Magn Reson Imaging. 2006;23(3):315–22.
- ↑Villa ADM, Corsinovi L, Ntalas I, Milidonis X, Scannell C, Di Giovine G, et al. Importance of operator training and rest perfusion on the diagnostic accuracy of stress perfusion cardiovascular magnetic resonance. J Cardiovasc Magn Reson. 2018;20(1):74.
- ↑Gatehouse PD, Elkington AG, Ablitt NA, Yang G-Z, Pennell DJ, Firmin DN. Accurate assessment of the arterial input function during high-dose myocardial perfusion cardiovascular magnetic resonance. J Magn Reson Imaging. 2004;20(1):39–45.
- ↑Lyon AR, López-Fernández T, Couch LS, Asteggiano R, Aznar MC, Bergler-Klein J, et al. 2022 ESC guidelines on cardio-oncology developed in collaboration with the European hematology association (EHA), the European society for therapeutic radiology and oncology (ESTRO) and the international cardio-oncology society (IC-OS). Eur Heart J. 2022;43(41):4229–361.
- ↑López-Sendón J, Álvarez-Ortega C, Zamora Auñon P, Buño Soto A, Lyon AR, Farmakis D, et al. Classification, prevalence, and outcomes of anticancer therapy-induced cardiotoxicity: the CARDIOTOX registry. Eur Heart J. 2020;41(18):1720–9.
- ↑Galán-Arriola, C., Lobo, M., Vílchez-Tschischke, J. P., López, G. J., de Molina-Iracheta, A., Pérez-Martínez, C., Agüero, J., Fernández-Jiménez, R., Martín-García, A., Oliver, E., Villena-Gutierrez, R., Pizarro, G., Sánchez, P. L., Fuster, V., Sánchez-González, J., & Ibanez, B. (2019). Serial magnetic resonance imaging to identify early stages of anthracycline-induced cardiotoxicity. Journal of the American College of Cardiology, 73(7), 779–791.
- ↑Galán-Arriola C, Vílchez-Tschischke JP, Lobo M, López GJ, de Molina-Iracheta A, Pérez-Martínez C, et al. Coronary microcirculation damage in anthracycline cardiotoxicity. Cardiovasc Res. 2022;118(2):531–41.
- ↑Yeh ETH, Chang H-M. Oncocardiology-past, present, and future: A review. JAMA Cardiol. 2016;1(9):1066–72.
- ↑Heusch G, Bøtker HE, Przyklenk K, Redington A, Yellon D. Remote ischemic conditioning. J Am Coll Cardiol. 2015;65(2):177–95.
- ↑Lau JK, Roy P, Javadzadegan A, Moshfegh A, Fearon WF, Ng M, et al. Remote ischemic preconditioning acutely improves coronary microcirculatory function. J Am Heart Assoc. 2018;7(19):e009058.
- ↑Zhao Z-Z, Li E, Li X-J, Guo Q, Shi Q-B, Li M-W. Effects of remote ischemic preconditioning on coronary blood flow and microcirculation. BMC Cardiovasc Disord. 2023;23(1):404.
- ↑Galán-Arriola C, Villena-Gutiérrez R, Higuero-Verdejo MI, Díaz-Rengifo IA, Pizarro G, López GJ, et al. Remote ischaemic preconditioning ameliorates anthracycline-induced cardiotoxicity and preserves mitochondrial integrity. Cardiovasc Res. 2021;117(4):1132–43.
- ↑Moreno-Arciniegas, A., García, A., Kelm, M., et al RESILIENCE Trial Investigators. (2024). Rationale and design of RESILIENCE: A prospective randomized clinical trial evaluating remote ischaemic conditioning for the prevention of anthracycline cardiotoxicity. European Journal of Heart Failure, 26(10), 2213–2222.
- ↑Neizel M, Lossnitzer D, Korosoglou G, Schäufele T, Peykarjou H, Steen H, et al. Strain-encoded MRI for evaluation of left ventricular function and transmurality in acute myocardial infarction. Circ Cardiovasc Imaging. 2009;2(2):116–22
Javier Sánchez-González; Borja Ibañez
E-Mail: javier.sanchez.gonzalez@philips.com; bibanez@cnic.es
Enviado: 12.11.25
Revisado: 20.11.25
Aceptado: 28.11.25


