Resumen
La Interfaz Regenerativa de Nervio Periférico (RPNI, por sus siglas en inglés) y la Reinervación Muscular Dirigida (TMR) son dos técnicas avanzadas de reinervación nerviosa para el tratamiento del dolor asociado a amputaciones de extremidad. En los últimos años, se han publicado estudios que sugieren una disminución con esta técnica de dolor de miembro fantasma (PLP), dolor residual del muñón (RLP) y neuromas dolorosos. Queda por ver que esta diferencia sea clínicamente significativa. Actualmente, no hay guías o protocolos de tratamiento que indiquen en qué casos se deben realizar. Por tanto, planteamos una revisión sistemática de la bibliografía publicada para los casos que realizan estas técnicas de forma profiláctica (en el momento de la amputación).
Se efectuó una búsqueda electrónica exhaustiva en diversas bases de datos para identificar estudios longitudinales en los que se realiza TMR o RPNI para la prevención de complicaciones dolorosas en una amputación. El protocolo de la revisión quedó detallado de antemano en PROSPERO (CRD42024617299).
Se incluyeron 27 estudios, de los cuales 24 evaluaban TMR (909 pacientes) y 5 evaluaban RPNI (117 pacientes). Encontramos una reducción de la aparición de PLP de la TMR (presente en el 32,6 % de los pacientes) comparada con controles (presente en el 71,47 %). Las cifras medias del PLP sobre 10 fueron inferiores en TMR (1,37) y RPNI (2,41) que en controles (4,15). También, una reducción en la presencia de RLP de la TMR (35 %) y RPNI (55 %) comparada con controles (74,5 %), y de sus medias sobre 10; siendo inferiores en TMR (2,22) y RPNI (1,64) que en controles (4,28).
Tanto la TMR como la RPNI pueden ser beneficiosas para prevenir el dolor tras una amputación de extremidad. Aun así, son necesarios más ensayos clínicos multicéntricos, especialmente centrados en la RPNI como técnica aislada.Abstract
Regenerative Peripheral Nerve Interface (RPNI) and Targeted Muscle Reinnervation (TMR) are two advanced nerve reinnervation techniques for the treatment of pain associated with limb amputations. Lately, studies have been published suggesting a decrease in phantom limb pain (PLP), residual limb pain (RLP), and painful neuromas with these techniques. It remains to be determined whether this difference is clinically significant. Currently, there are no treatment guidelines or protocols indicating in which cases they should be performed. Therefore, we conducted a systematic review of the published literature for cases where these techniques are performed prophylactically (at the time of amputation).
An exhaustive electronic search was conducted across various databases to identify longitudinal studies in which TMR or RPNI were performed for the prevention of painful complications in an amputation. The review protocol was detailed beforehand in PROSPERO (CRD42024617299).
Twenty-seven studies were included, of which 24 evaluated TMR (909 patients) and 5 evaluated RPNI (117 patients). We found a reduction in the occurrence of PLP with TMR (present in 32.6% of patients) compared to controls (present in 71.47%). Mean PLP scores out of 10 were lower in TMR (1.37) and RPNI (2.41) than in controls (4.15). Additionally, there was a reduction in the presence of RLP with TMR (35%) and RPNI (55%) compared to controls (74.5%), as well as in their mean scores out of 10; these were lower in TMR (2.22) and RPNI (1.64) than in controls (4.28).
Both TMR and RPNI may be beneficial for preventing pain following limb amputation. Even so, more multicenter clinical trials are needed, especially focusing on RPNI as an isolated technique.Palabras clave: Reinervación muscular dirigida (TMR); Interfaz regenerativa de nervio periférico (RPNI); Amputación; Dolor de miembro fantasma (PLP); Dolor de miembro residual (RLP); Control del dolor y prevención.
Keywords: Targeted muscle reinnervation (TMR); Regenerative peripheral nerve interface (RPNI); Amputation; Phantom limb pain (PLP); Residual limb pain (RLP); Pain control and prevention.
Introducción
En el Reino Unido, la prevalencia de amputaciones de extremidades inferiores es de aproximadamente 26 por cada 100.000 habitantes, la mayoría de las cuales se deben a enfermedad vascular periférica (1).
Durante el proceso de amputación, se produce la disrupción de los nervios, lo que provoca la regeneración desorganizada de sus axones y una proliferación de tejido cicatricial y conectivo, dando lugar habitualmente a un neuroma post-amputación (2). Aunque benigno, pueden volverse sintomáticos, causando dolor, entumecimiento o parestesias, y disminuyendo la calidad de vida. Puede aumentar la dependencia de opiáceos para el control del dolor y dificultar la rehabilitación protésica futura.
El dolor relacionado con el muñón de amputación con la amputación de una extremidad se conoce como dolor del miembro residual (RLP). El dolor de la extremidad que fue amputada, mediado por mecanismos centrales, se conoce como dolor del miembro fantasma (PLP) (2,3).
En la TMR (Targeted Muscle Reinnervation o Reinervación Muscular Dirigida, en español), los nervios motores seccionados se transfieren a las ramas motoras de segmentos musculares sanos cercanos que median una reinervación dirigida (4,5). Este proceso cambia la cicatrización del muñón nervioso por vías no conocidas, que podrían tener relación con una mejor reinervación axonal y puede disminuir el dolor (6). También parece que puede ayudar a mejorar el control de la prótesis en el futuro y podría servir como base para el desarrollo de mejores prótesis biónicas.
La RPNI (Regenerative Peripheral Nerve Interface o Interfaz de Regeneración Nerviosa Periférica en español) consiste en tomar un injerto de músculo de la extremidad amputada (habitualmente un segmento que se fuera a desechar) y envolver con dicho injerto muscular el extremo del nervio objetivo (7,8). Esto permite un trasplante de placas motoras a la zona con potencial de reinervación, aunque otros autores describen la necrosis de estos injertos que produce una estructura tridimensional y facilita la migración de los extremos nerviosos.
Ambas técnicas se pueden realizar de forma terapéutica, para el tratamiento de neuromas, dolor y miembro fantasma, meses u años tras realizar la amputación. También se pueden realizar de forma profiláctica, como técnica ancilar a la amputación. Es este segundo caso, el profiláctico, del que tratamos aquí.
Se han publicado varias revisiones sistemáticas y metaanálisis entre 2022 y 2024, incluyendo los de (Walsh et al.) (9), (Yuan et al.) (10), (Zimbulis et al.) (11), (Mauch et al.)(12) y (Hagiga et al.) (13). Muchas de estas revisiones recogen tanto casos profilácticos o terapéuticos, aunque parecen indicar superioridad de TMR o RPNI frente a la amputación convencional, así como que realizarlas de forma profiláctica mejora el pronóstico.
Materiales y métodos
Esta revisión sistemática fue registrada a priori en PROSPERO (CRD42024617299) y ha sido hecha siguiendo la guía metodológica del Cochrane Handbook for Systematic Reviews of Interventions (14) y de MECIR (Methodological Expectations for Cochrane Intervention Reviews) (15), y redactada conforme a PRISMA (16,17).
Se llevó a cabo una búsqueda en las siguientes bases de datos electrónicas: Web of Science, Scopus, PubMed, Cochrane Register of Controlled Trials (CENTRAL), CINAHL y Google Scholar. Además, para identificar estudios adicionales publicados, no publicados y en curso, se revisaron las listas de referencias de todos los estudios relevantes y se buscaron en MedRxiv.
Esta revisión incluye todos los estudios escritos en cualquier idioma, tanto aleatorizados como no aleatorizados, que involucren ensayos clínicos, estudios de cohortes, estudios de casos y controles, estudios cuasi-experimentales y series de casos (con n > 10).
Se excluyeron los informes de casos (descripciones detalladas de un individuo o de un pequeño grupo de individuos), las series de casos (con n < 10), los estudios cualitativos (aquellos que recopilan y analizan datos no numéricos) y las revisiones narrativas. Tampoco se incluyeron los estudios que empleaban TMR o RPNI con intención curativa o secundaria.
Se incluyeron pacientes adultos (mayores de 18 años), de cualquier género, con una amputación mayor de extremidad superior o inferior de cualquier etiología y seguimiento igual o superior al año. Se les estratificó en grupo TMR, grupo RPNI y grupo control y se extrajeron datos como edad, sexo, nivel de amputación, causa de esta, presencia de neuroma sintomático, presencia de PLP y RLP, y valor medio del PLP y RLP según la escala VAS. Todos los resultados de dolor y neuroma se valoran al año de la intervención, aunque muchos artículos presentan mediciones intermedias.
Se evaluaron todos los títulos y resúmenes identificados durante las búsquedas bibliográficas utilizando Covidence (18). Dos autores de la revisión (JM, MR) revisaron de manera independiente los resultados de la búsqueda e identificaron los informes mediante el cribado de todos los títulos y resúmenes restantes, excluyendo aquellos que no cumplían los criterios de inclusión. Posteriormente, se recuperó el texto completo de los artículos, y ambos autores de la revisión los examinaron de forma independiente para determinar su relevancia y extraer los datos. Contactamos con los investigadores para obtener información faltante en los estudios que así lo requerían. Cualquier desacuerdo se resolvió mediante discusión con el tercer autor (DG).
Resultados
Resultados de la búsqueda
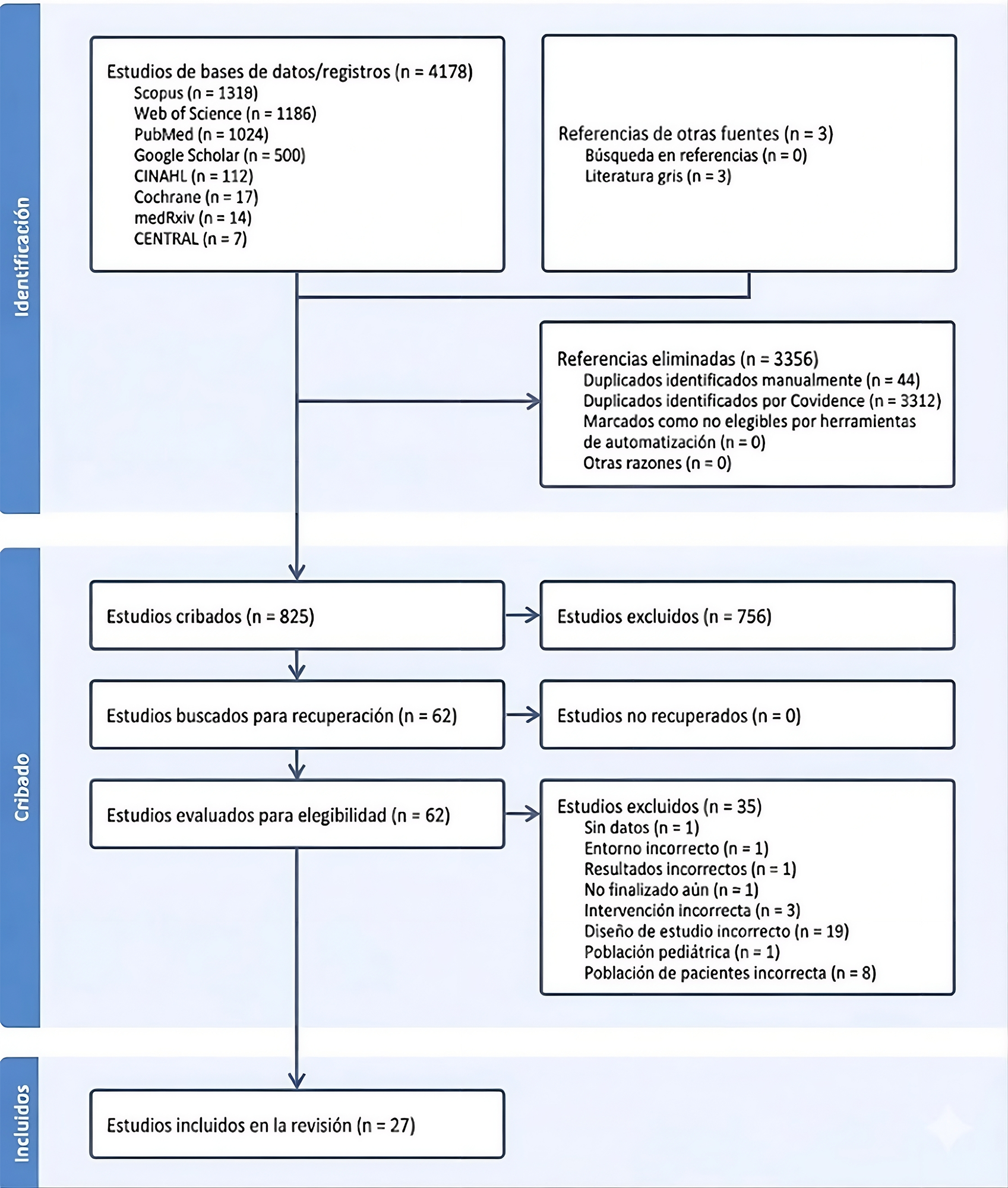
Tras la búsqueda electrónica inicial y dos repeticiones de la búsqueda para actualizar los resultados, se encontraron 4181 referencias, se procedió a la eliminación de duplicados y se hizo cribado por título y abstract de 825 estudios, en 62 se valoró el texto completo. Finalmente, 35 fueron excluidos y se incluyeron 27 para la extracción (Figura 1).
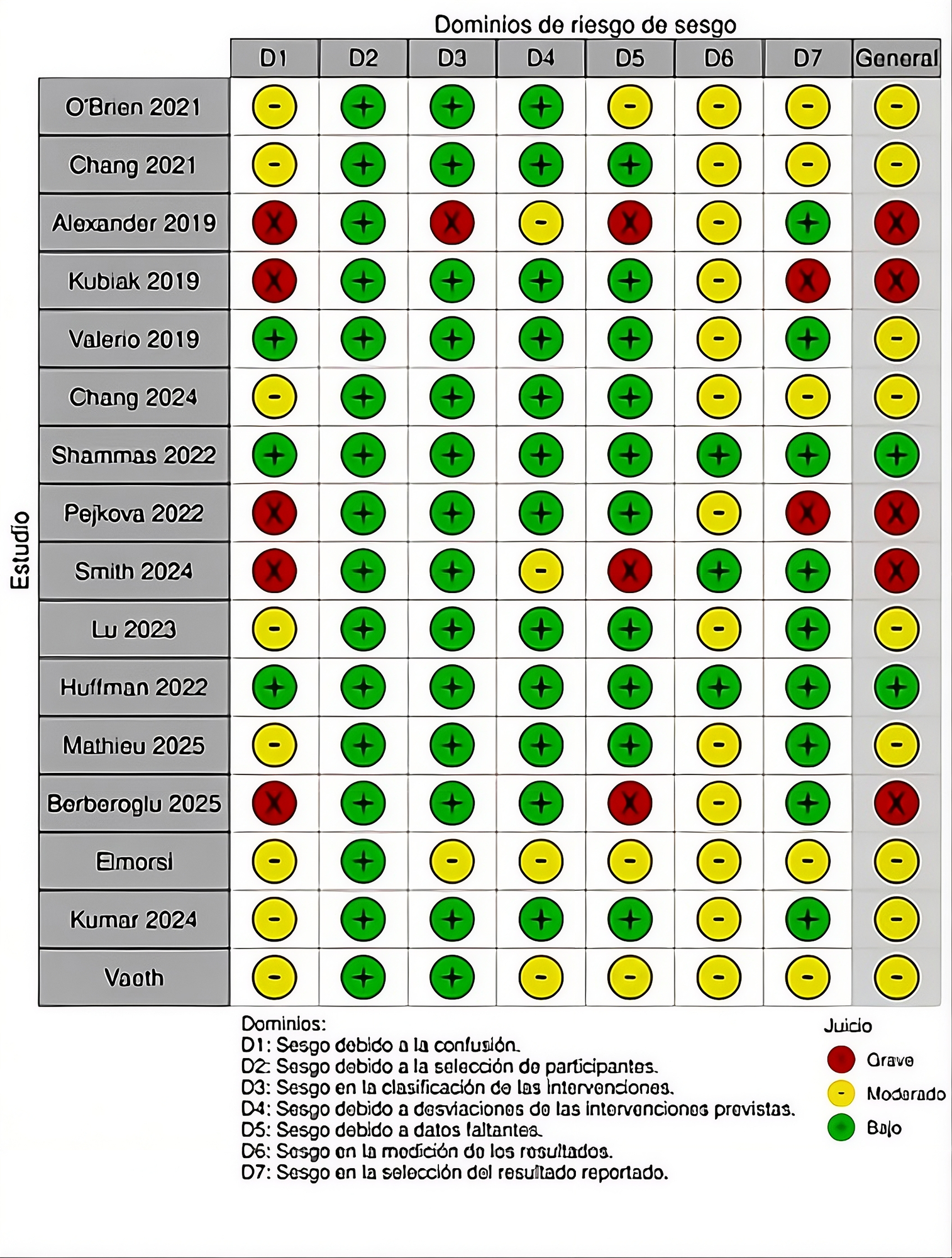
Riesgo de Sesgos
La evaluación del riesgo de sesgo en estudios no aleatorizados se estimó mediante la herramienta Risk Of Bias In Non-randomized Studies of Interventions versión 2 (ROBINS-I V2) (19). La evaluación del riesgo de sesgo en estudios de series de casos se estimó utilizando la Checklist for Case Series del Joanna Briggs Institute (20).
Características de los estudios incluidos
De los 27 estudios incluidos, 16 eran estudios de cohortes (prospectivos o retrospectivos) y 11 se tomaron como estudios de series de casos. 24 evaluaban TMR (21–44) (909 pacientes) y 5 evaluaban RPNI (41,42,45-47) (117 pacientes). La mayoría de estudios no evalúan todos los criterios de valoración que incluimos, por lo que los totales de cada evaluación serán menores.
Características de los pacientes incluidos
La edad media de los pacientes sometidos a TMR y/o RPNI fue de 49,9 años, el 64,7 % de los pacientes eran hombres y presentaban un IMC medio de 28,5.
La causa más frecuente de amputación fue la causa oncológica, representando el 37,6 % del total. Le siguió la causa traumática, con un 21,7 %, y en tercer lugar la causa infecciosa, que constituyó el 18,4 %. Las malformaciones congénitas u otras causas ocuparon el cuarto lugar con un 14,9 %, mientras que la causa cardiovascular fue la menos frecuente, con un 7,4 % del total acumulado.
El nivel de amputación más frecuente fue el transtibial 39,9 %, seguido de la transfemoral 19,2 %, desarticulación de rodilla 12,3 %, desarticulación de cadera 9,2 %, desarticulación de hombro 8 %, transradial 6,7 % y transhumeral 4,7 %.
Por su parte, los pacientes control presentaban una edad media de 51,9 años, el 64,9 % de los pacientes eran varones y un IMC medio de 21,7.
La causa más frecuente de amputación fue oncológica 30,1 %, seguida de la traumática 28,1 %, la infecciosa 19 %, malformaciones congénitas u otras 14,7 %, y cardiovascular 8,1 %.
El nivel de amputación más frecuente fue el transtibial, que representó el 43,7 % del total. Le siguió el nivel transfemoral con un 25,9 %, y en tercer lugar la desarticulación de rodilla, con un 9,8 %. La desarticulación de cadera constituyó el 9,3 %, mientras que la desarticulación de hombro y el nivel transhumeral representaron el 4,9 % y 4,7 %, respectivamente. Finalmente, el nivel menos frecuente fue el transradial, con un 1,5 % del total acumulado.
Presencia de neuroma sintomático
De los 260 individuos en los que se realizó la técnica de TMR y se midió el neuroma sintomático, un 14,7% acabaron desarrollándolo al año de seguimiento. En contraste, ningún caso de neuroma sintomático (0 %) fue reportado en el grupo que recibió RPNI, compuesto por 30 pacientes. Por otro lado, el grupo control, que no recibió técnicas de reinervación específicas, presentó una incidencia significativamente mayor de un 19,9 %, en una cohorte de 273 individuos.
Presencia de dolor de miembro fantasma
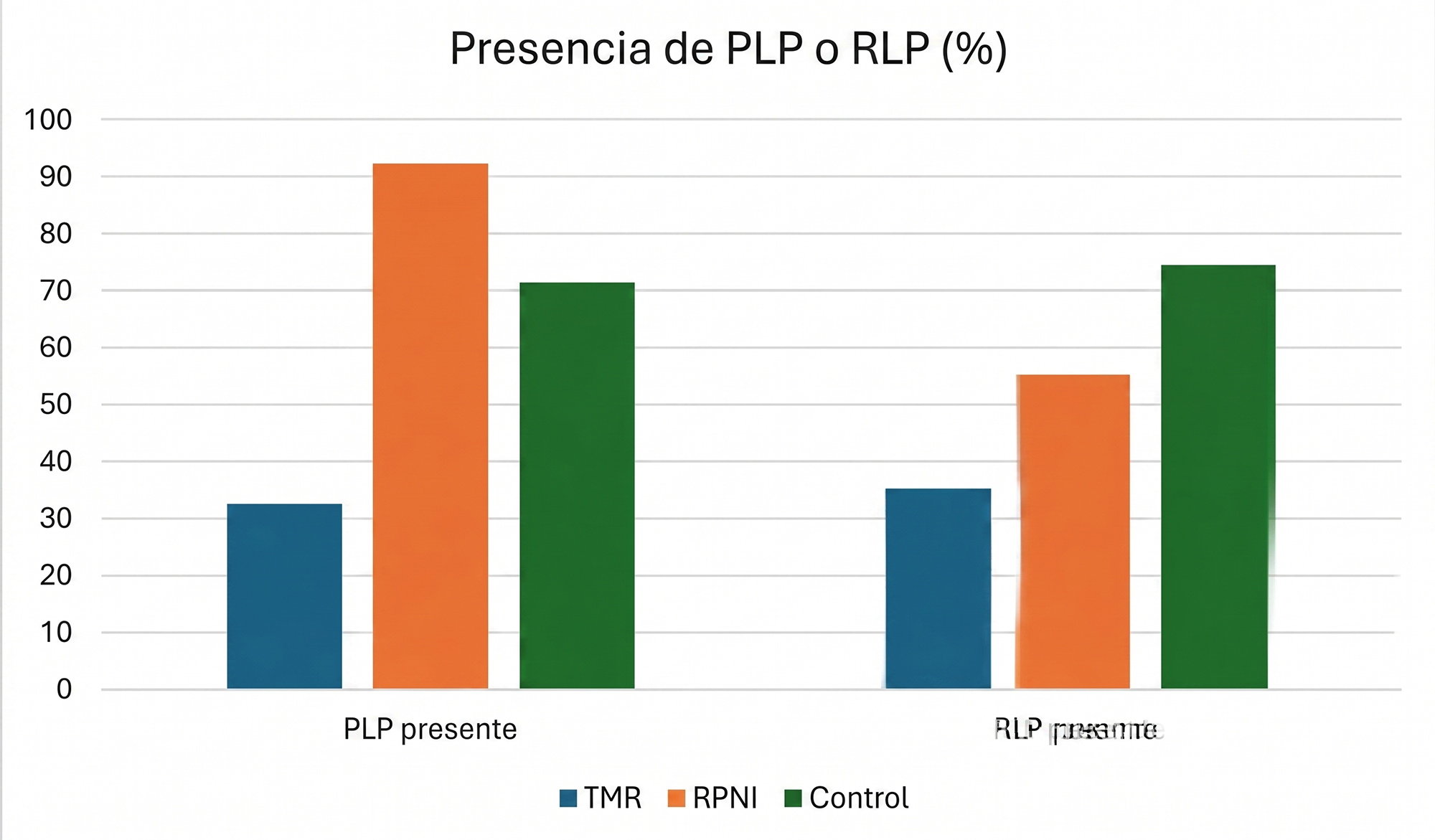
Sobre 367 individuos intervenidos con la técnica de TMR se evaluó la presencia de dolor de miembro fantasma. 32,6% de ellos presentaban dolor de miembro fantasma al año de seguimiento. En el grupo tratado con RPNI (n = 26), la incidencia fue considerablemente mayor, alcanzando el 92,3 %. Por su parte, el grupo control, compuesto por 726 individuos que no recibieron técnicas de reinervación específicas, presentó una incidencia del 71,5 % de PLP.
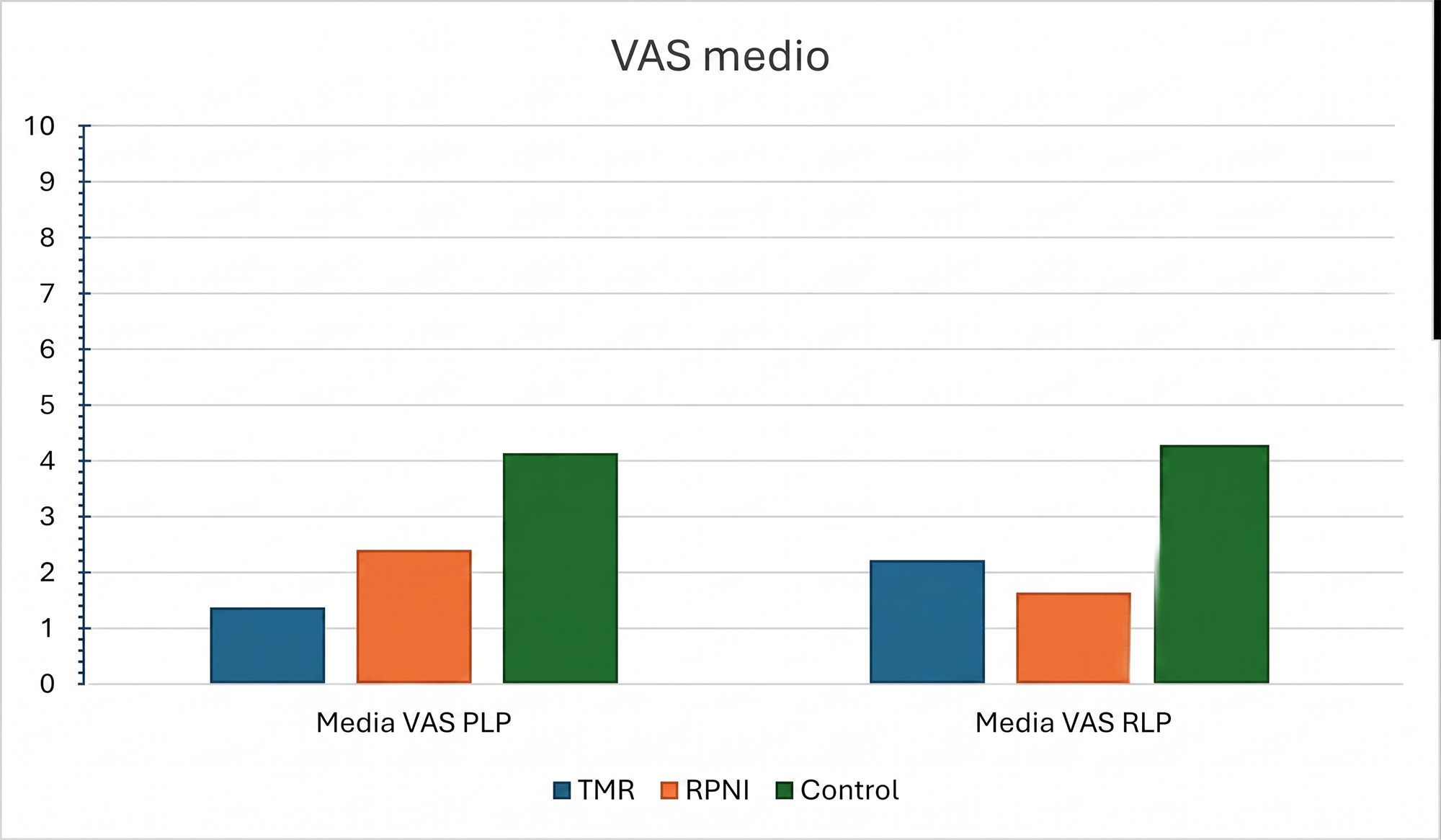
288 fueron tratados con TMR y medido el dolor con escala visual analógica del dolor o VAS. Este grupo presentó una media de dolor de 1,4 sobre 10, lo que representa el valor más bajo entre los grupos analizados. En el grupo que recibió RPNI (n = 23), la media de dolor fue de 2,4, mientras que el grupo control (n = 575), que no recibió técnicas específicas de reinervación, mostró una media significativamente más elevada de 4,2.
Presencia de dolor de miembro residual
En 431 individuos tratados con TMR se evaluó el dolor residual del muñón de forma dicotómica. De ellos se observó que el 35,3% lo presentaban. En el grupo que recibió RPNI (n = 46), la incidencia fue mayor, alcanzando el 55,2 %. Por su parte, el grupo control, compuesto por 766 individuos sin técnicas específicas de reinervación, mostró la incidencia más elevada, con un 74,5 % de dolor residual.
692 individuos tratados con TMR fueron evaluados de dolor residual del muñón con escala VAS. La media de dolor residual fue de 2,2 VAS sobre 10, indicando un nivel inferior de dolor en comparación con otros grupos. En el grupo que se realizó RPNI (n = 14), la media fue aún menor, con 1,7 puntos, lo que sugiere una reducción más marcada del dolor residual. Por el contrario, el grupo control (n = 845), sin técnicas específicas de reinervación, presentó una media significativamente más elevada de 4,3 sobre 10, reflejando una mayor carga de dolor residual.
Discusión
Esta revisión sistemática avala que la TMR se asocia con una menor incidencia de dolor de miembro fantasma y dolor residual, y junto a la RPNI destacan por reducir los dolores presentes en la escala VAS así como la incidencia de neuromas sintomáticos. Por su parte, el grupo de control, amputación sin técnicas de reinervación, presentó consistentemente los peores resultados en todas las variables analizadas.
Estos resultados son avalados por otras revisiones sistemáticas y metaanálisis como (Yuan et al.) (10) o (Zimbulis et al.) (11). Además, casi la totalidad de los estudios demostraron superioridad de las técnicas de reinervación frente a la amputación sin estas, exceptuando a (Chang et al.) (23) y (Smith et al.) (27) en términos de reducción de neuroma sintomático.
La principal indicación de amputación, especialmente en los grupos de intervención fue la oncológica, lo que resulta contrario a los estudios transversales sobre amputación que muestran como primera causa las amputaciones vasculares. Esto indica un sesgo de selección en la población de los estudios difícil de interpretar. Los pacientes oncológicos pueden tener un mayor riesgo de dolor postoperatorio debido al uso prolongado de analgésicos por la carga tumoral o intervenciones previas, y pueden carecer de nervios adecuados para la reinervación tras una resección completa (48). También pueden tener mayores tasas de radioterapia. En caso de amputaciones por causas vasculares se podría esperar encontrar una dificultad para la cicatrización, incluida la cicatrización de los extremos nerviosos.
Es también llamativo el IMC más bajo en los pacientes del grupo control, que parece indicar un sesgo de selección. Un IMC mayor suele ser predictor de peores resultados quirúrgicos aunque son necesarios estudios que lo evalúen para TMR o RPNI.
La principal limitación del estudio resulta de la falta de estudios que comparen RPNI vs control, lo que da resultados contradictorios como que la RPNI tenga porcentajes tan altos de aparición de miembro fantasma pero no de dolor residual ni de sus medias en la escala VAS. También hay que mencionar la alta heterogeneidad entre las poblaciones estudiadas, la diferencia en la metodología de las mediciones del dolor y la posibilidad de sesgos de publicación al tratarse de una revisión sistemática.
Conclusiones
Estos hallazgos refuerzan la necesidad de considerar las técnicas de reinervación como estrategias terapéuticas de primera línea en pacientes candidatos a amputación. Siguen siendo necesarios más estudios, especialmente ensayos clínicos multicéntricos que evalúen RPNI aislada frente a TMR aislada.
DECLARACIÓN DE TRANSPARENCIA
Los autores/as de este artículo declaran no tener ningún tipo de conflicto de intereses respecto a lo expuesto en el presente trabajo.
BIBLIOGRAFÍA
- ↑Valerio I, Schulz SA, West J, Westenberg RF, Eberlin KR. Targeted Muscle Reinnervation Combined with a Vascularized Pedicled Regenerative Peripheral Nerve Interface. Plast Reconstr Surg Glob Open. 2020;8:e2689.
- ↑Arnold DMJ, Wilkens SC, Coert JH, Chen NC, Ducic I, Eberlin KR. Diagnostic Criteria for Symptomatic Neuroma. Ann Plast Surg. 2019;82:420-427.
- ↑Vlot MA, Wilkens SC, Chen NC, Eberlin KR. Symptomatic Neuroma Following Initial Amputation for Traumatic Digital Amputation. J Hand Surg. 2018;43:86.e1-86.e8.
- ↑Cheesborough J, Smith L, Kuiken T, Dumanian G. Targeted Muscle Reinnervation and Advanced Prosthetic Arms. Semin Plast Surg. 2015;29:62-72.
- ↑Kuiken TA, Barlow AK, Hargrove LJ, Dumanian GA. Targeted Muscle Reinnervation for the Upper and Lower Extremity. Tech Orthop. 2017;32:109-116.
- ↑Henderson JT, Koenig ZA, Climov M, Gelman J. Demystifying Targeted Muscle Reinnervation: A Systematic Review of Nerve Transfers for the Lower Extremity. Plast Reconstr Surg Glob Open. 2023;11:e4894.
- ↑Hooper RC, Cederna PS, Brown DL, et al. Regenerative Peripheral Nerve Interfaces for the Management of Symptomatic Hand and Digital Neuromas. Plast Reconstr Surg Glob Open. 2020;8:e2792.
- ↑Kubiak CA, Kemp SWP, Cederna PS. Regenerative Peripheral Nerve Interface for Management of Postamputation Neuroma. JAMA Surg. 2018;153:681.
- ↑Walsh AR, Lu J, Rodriguez E, Diamond S, Sultan SM. The Current State of Targeted Muscle Reinnervation: A Systematic Review. J Reconstr Microsurg. 2023;39:238-244.
- ↑Yuan M, Gallo M, Gallo L, et al. Targeted Muscle Reinnervation and Regenerative Peripheral Nerve Interfaces Versus Standard Management in the Treatment of Limb Amputation: A Systematic Review and Meta-Analysis. Plast Surg (Oakv). 2024;32:253-264.
- ↑Zimbulis AJ, An VVG, Symes M, et al. Targeted Muscle Reinnervation Compared to Standard Peripheral Nerve Management Following Amputation: A Systematic Review and Meta-Analysis. Hand (N Y). 2025;20:1197-1206.
- ↑Mauch JT, Kao DS, Friedly JL, Liu Y. Targeted muscle reinnervation and regenerative peripheral nerve interfaces for pain prophylaxis and treatment: A systematic review. PM&R. 2023;15:1457-1465.
- ↑Hagiga A, Aly M, Gumaa M, Rehan Youssef A, Cubison T. Targeted muscle reinnervation in managing post-amputation related pain: A systematic review and meta-analysis. Pain Pract. 2023;23:922-932.
- ↑Higgins JPT, Thomas J, Chandler J, et al (editors). Cochrane Handbook for Systematic Reviews of Interventions version 6.5. Cochrane; 2024. Available from www.training.cochrane.org/handbook.
- ↑Higgins JPT, Lasserson T, Chandler J, et al. Methodological Expectations of Cochrane Intervention Reviews. Cochrane: London, Version February 2021. https://community.cochrane.org/mecir-manual.
- ↑Page MJ, Moher D, Bossuyt PM, et al. PRISMA 2020 explanation and elaboration: updated guidance and exemplars for reporting systematic reviews. BMJ. 2021;n160.
- ↑Page MJ, McKenzie JE, Bossuyt PM, et al. The PRISMA 2020 statement: an updated guideline for reporting systematic reviews. BMJ. 2021;n71.
- ↑Covidence systematic review software, Veritas Health Innovation, Melbourne, Australia. Available at www.covidence.org.
- ↑ROBINS-I V2 Development Group. ROBINS-I V2. https://www.riskofbias.info/welcome/robins-i-v2 (accessed 12 December 2024).
- ↑Moola S, Munn Z, Tufanaru C, et al. Chapter 7: Systematic reviews of etiology and risk. In: Aromataris E, Munn Z (Editors). Joanna Briggs Institute Reviewer’s Manual. The Joanna Briggs Institute, 2017. Available from https://reviewersmanual.joannabriggs.org/.
- ↑Trauma, Burn, and Critical Care. J Am Coll Surg. 2024;239:S508-S557.
- ↑O’Brien AL, Jordan SW, West JM, Mioton LM, Dumanian GA, Valerio IL. Targeted Muscle Reinnervation at the Time of Upper-Extremity Amputation for the Treatment of Pain Severity and Symptoms. J Hand Surg. 2021;46:72.e1-72.e10.
- ↑Chang BL, Hill AL, Mondshine J, et al. Primary Targeted Muscle Reinnervation in Above-Knee Amputations in Patients with Unsalvageable Limbs from Limb-Threatening Ischemia or Infection. J Reconstr Microsurg. 2024;40:109-117.
- ↑Chang BL, Mondshine J, Attinger CE, Kleiber GM. Targeted Muscle Reinnervation Improves Pain and Ambulation Outcomes in Highly Comorbid Amputees. Plast Reconstr Surg. 2021;148:376-386.
- ↑Huffman A, Schneeberger S, Goodyear E, et al. Evaluating hip disarticulation outcomes in a 51-patient series. J Orthop. 2022;31:117-120.
- ↑Alexander JH, Jordan SW, West JM, et al. Targeted muscle reinnervation in oncologic amputees: Early experience of a novel institutional protocol. J Surg Oncol. 2019;120:348-358.
- ↑Smith TP, Cognetti DJ, Cook A, et al. Similar rates of reoperation for neuroma after transtibial amputations with and without targeted muscle reinnervation. OTA Int. 2024;7. Disponible en: https://journals.lww.com/10.1097/OI9.0000000000000297.
- ↑Shammas RL, Azoury SC, Sergesketter AR, et al. Primary Targeted Muscle Reinnervation after Below-Knee Amputation Is Not Associated with an Increased Risk of Major or Minor Surgical Complications: A Multi-Institutional, Propensity Score–Matched Analysis. Plast Reconstr Surg. 2022;150:589-598.
- ↑Vaeth AM, Kochheiser M, Qin N, et al. D123.Advances in Neuroma Prevention: A Single Institutional Experience With TMR And TMRPNI in Lower Limb Amputees. Plast Reconstr Surg Glob Open. 2025;13:143-143.
- ↑Lu V, Zhou A, Krkovic M. Variation on a technique for the intra-muscular insertion of nerve endings to minimise neuropathic and residual pain in lower limb amputees: a retrospective cohort study. Eur J Orthop Surg Traumatol. 2022;33:1299-1306.
- ↑Valerio IL, Dumanian GA, Jordan SW, et al. Preemptive Treatment of Phantom and Residual Limb Pain with Targeted Muscle Reinnervation at the Time of Major Limb Amputation. J Am Coll Surg. 2019;228:217-226.
- ↑Mathieu L, Redais C, Diner C, et al. Curative and preemptive treatment of amputee pain by targeted muscle reinnervation: experience from a French military trauma center. Eur J Trauma Emerg Surg. 2025;51:37.
- ↑Li AT, Garcia N, Angliss M, Paul E, Gray S, Bruscino-Raiola F. Acute versus non-acute targeted muscle reinnervation for pain control following major limb amputation: A comparative study. J Plast Reconstr Aesthet Surg. 2024;94:229-237.
- ↑Pet MA, Ko JH, Friedly JL, Mourad PD, Smith DG. Does Targeted Nerve Implantation Reduce Neuroma Pain in Amputees? Clin Orthop Relat Res. 2014;472:2991-3001.
- ↑Raasveld FV, Hoftiezer YAJ, Gomez-Eslava B, et al. Early Postoperative Pain Course following Primary and Secondary Targeted Muscle Reinnervation: A Temporal Description of Pain Outcomes. J Reconstr Microsurg. 2025;41:459-468.
- ↑Raasveld FV, Mayrhofer-Schmid M, Johnston BR, et al. Targeted muscle reinnervation at the time of amputation to prevent the development of neuropathic pain. J Plast Reconstr Aesthet Surg. 2024;97:13-22.
- ↑Frantz TL, Everhart JS, West JM, Ly TV, Phieffer LS, Valerio IL. Targeted Muscle Reinnervation at the Time of Major Limb Amputation in Traumatic Amputees: Early Experience of an Effective Treatment Strategy to Improve Pain. JBJS Open Access. 2020;5:e0067-e0067.
- ↑Goodyear EG, O’Brien AL, West JM, et al. Targeted Muscle Reinnervation at the Time of Amputation Decreases Recurrent Symptomatic Neuroma Formation. Plast Reconstr Surg. 2024;153:154-163.
- ↑Bowen JB, Ruter D, Wee C, West J, Valerio IL. Targeted Muscle Reinnervation Technique in Below-Knee Amputation. Plast Reconstr Surg. 2019;143:309-312.
- ↑O’Brien AL, West JM, Gokun Y, et al. Longitudinal Durability of Patient-Reported Pain Outcomes after Targeted Muscle Reinnervation at the Time of Major Limb Amputation. J Am Coll Surg. 2022;234:883-889.
- ↑Mahmoud MA, Toyoda Y, McGraw JR, et al. 40. Development Of Neuropathic Pain After Primary TMR And RPNI In Lower Extremity Amputation: A 4-year Retrospective Analysis Of Prognostic Factors. Plast Reconstr Surg Glob Open. 2024;12:25-25.
- ↑Obinero CG, Green JC, Swiekatowski KR, et al. Surgical Complications after Targeted Muscle Reinnervation at a Safety-Net Hospital. J Reconstr Microsurg. 2025;41:531-539.
- ↑Elmorsi R, Shin A, Adelman DM, Mericli AF, Roubaud MJ. 52. Efficacy of Targeted Muscle Reinnervation and Regenerative Peripheral Nerve Interface in Reducing Pain in Cancer Amputees: A Patient-reported Outcomes Study. Plast Reconstr Surg Glob Open. 2025;13:26-26.
- ↑Reid RT, Johnson CC, Gaston RG, Loeffler BJ. Impact of Timing of Targeted Muscle Reinnervation on Pain and Opioid Intake Following Major Limb Amputation. Hand (N Y). 2024;19:200-205.
- ↑Pejkova S, Nikolovska B, Srbov B, et al. Prophylactic Regenerative Peripheral Nerve Interfaces in Elective Lower Limb Amputations. PRILOZI. 2022;43:41-48.
- ↑Kubiak CA, Kemp SWP, Cederna PS, Kung TA. Prophylactic Regenerative Peripheral Nerve Interfaces to Prevent Postamputation Pain. Plast Reconstr Surg. 2019;144:421e-430e.
- ↑Berberoglu I, Kemp SWP, Hooper RC. Regenerative Peripheral Nerve Interface (RPNI) for the Management of Postamputation Pain in Oncology Patients. Plast Reconstr Surg. 2025. Disponible en: https://journals.lww.com/10.1097/PRS.0000000000012312
- ↑Eberlin KR, Brown DA, Gaston RG, et al. A Consensus Approach for Targeted Muscle Reinnervation in Amputees. Plast Reconstr Surg Glob Open. 2023;11:e4928.
David Gurpegui
Servicio de Cirugía Plástica, Estética y Reparadora. Clínica Universidad de Navarra
Avenida Pío XII, 36 · 31008 Pamplona, Navarra
E-Mail: dgurpegui@unav.es
Enviado: 08.01.26
Revisado: 17.01.26
Aceptado: 15.02.26


