Resumen
Se presenta el caso de un paciente varón de 69 años con sospecha de carcinomatosis diseminada de origen desconocido e infiltración de médula ósea debido a bicitopenia y cuadro leucoeritroblástico. Durante el estudio se objetivó necrosis de la médula ósea e infiltración de la misma por células anaplásicas de origen extrahematológico. La infiltración de médula ósea por procesos extrahematológicos es infrecuente, pero puede ser predecible por medio de morfología de la sangre periférica, cuadro clínico con dolores óseos y/o presencia de metástasis óseas. El pronóstico en los pacientes con infiltración de la médula ósea por carcinomas y necrosis de la médula ósea es muy adverso.
Abstract
We present the case of a 69 year old male with suspected diagnosis of disseminated carcinomatosis of a tumor of unknown origin and bone marrow metastatization due to bicytopenia and leucoerythroblastic reaction. Bone marrow necrosis was shown, as well as bone marrow substitution by anaplastic cells of suspected extrahematologic origin. Bone marrow involvement by carcinomas is rare, but can be predicted by peripheral blood morphology, bone pain and/or presence of bone metastasis. Prognosis in patients with bone marrow metastasis and bone marrow necrosis is dismal.
Palabras clave: Cuadro leucoeritroblástico; Metástasis de médula ósea; Necrosis de médula ósea; Carcinoma neuroendocrino.
Keywords: Bone Marrow necrosis; Leucoerythroblastic reaction; Bone marrow metastasis; Bone marrow necrosis; Neuroendorine carcinoma.
Introducción
Presentamos el caso de un paciente varón de 69 años de edad, con antecedentes personales de hipotiroidismo, diabetes mellitus tipo 2, dislipemia, hipertensión arterial, cardiopatía isquémica revascularizada en 2024 y hepatopatía crónica con datos de hipertensión portal de origen metabólico, que consulta por dolor abdominal y pérdida de peso.
Inicialmente se propone estudio ambulatorio del cuadro, pero finalmente se realiza hospitalizado debido a empeoramiento clínico.
Caso clínico
Entre las pruebas realizadas destaca un PET-TC con 18FDG en el que se objetivan depósitos en adenopatías supraclaviculares, mediastínicas, axilares, y epifrénicas con SUVmax de hasta 17.6. Se identifica hígado sugerente de hepatopatía, en el que se observan múltiples lesiones, la mayor en el segmento 6-7, con centro necrótico, captación de hasta 12.6 SUVmax y un tamaño de 5,4×5,0 cm. En el abdomen se objetiva extensa afectación ganglionar patológica, incluyendo hilio hepático, ligamento gastrohepático, raíz del mesenterio y retroperitoneo, rodeando los grandes vasos. Se visualizan múltiples depósitos de FDG que afectan a la práctica totalidad del esqueleto visualizado, sin clara correlación con lesiones en TC.
En este momento se biopsia una adenopatía supraclavicular, sospechosa de malignidad, cuyo resultado se encuentra pendiente en el momento del contacto con Hematología.
Durante el proceso diagnóstico se contacta con Hematología debido a trombocitopenia progresiva hasta 42×103 plaquetas/mm3, sin presentar anemia ni leucopenia en un primer momento, planteándose entre los diagnósticos diferenciales la trombocitopenia secundaria a hepatopatía o secundaria a infiltración medular. Por tanto, se realiza inicialmente una revisión de la extensión de sangre periférica, en la que se objetiva cuadro leucoeritroblástico, con dianocitos y estomatocitos en la serie roja, sin objetivarse esquistocitos, y plaquetas de morfología normal. Se planifica realizar un estudio de médula ósea y, teniendo en cuenta que el tumor primario es desconocido, se prefiere la realización tanto de aspirado de médula ósea como de biopsia ósea en cresta iliaca.
Analíticamente, el paciente presenta como hallazgos más relevantes una hipertrigliceridemia de 254mg/dL (LSN 150mg/dL), con hipoalbuminemia de 2.7g/dL (LIN 3.5mg/dL), elevación de transaminasas con ALT 61 U/L (LSN 50 U/L), AST 296 U/L (LSN 50U/L), fosfatasa alcalina 712 U/L (LSN 120U/L), GGT 1006 (LSN 55U/L) e hipercalcemia con calcio corregido por albúmina de 11.95mg/dL (LSN 10.6). Presentaba una elevación de beta-2 microglobulina de 4.2mg/L (LSN 2.4mg/L), una ferritina de 10386ng/mL (LSN 307ng/mL) y una elevación del antígeno CA 125 hasta 75.8U/mL (LSN 35) y del antígeno CA 19-9 de 97U/mL (LSN 35 U/L).
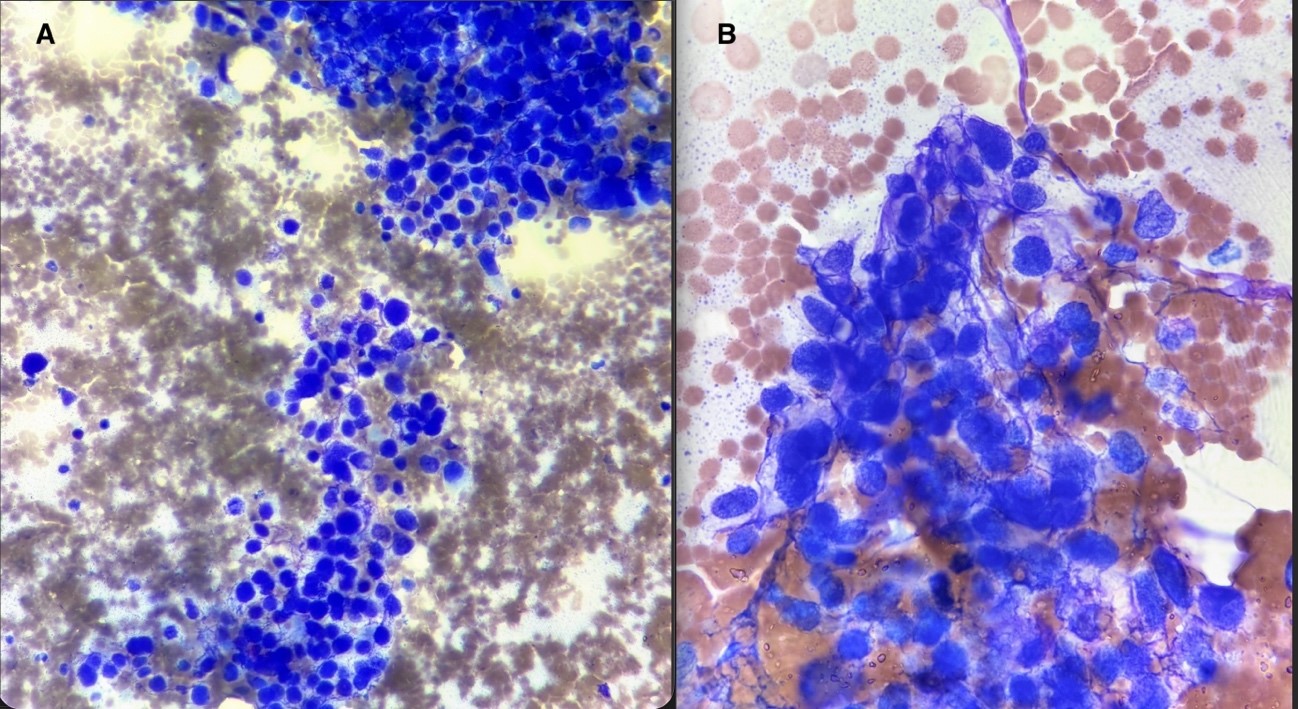
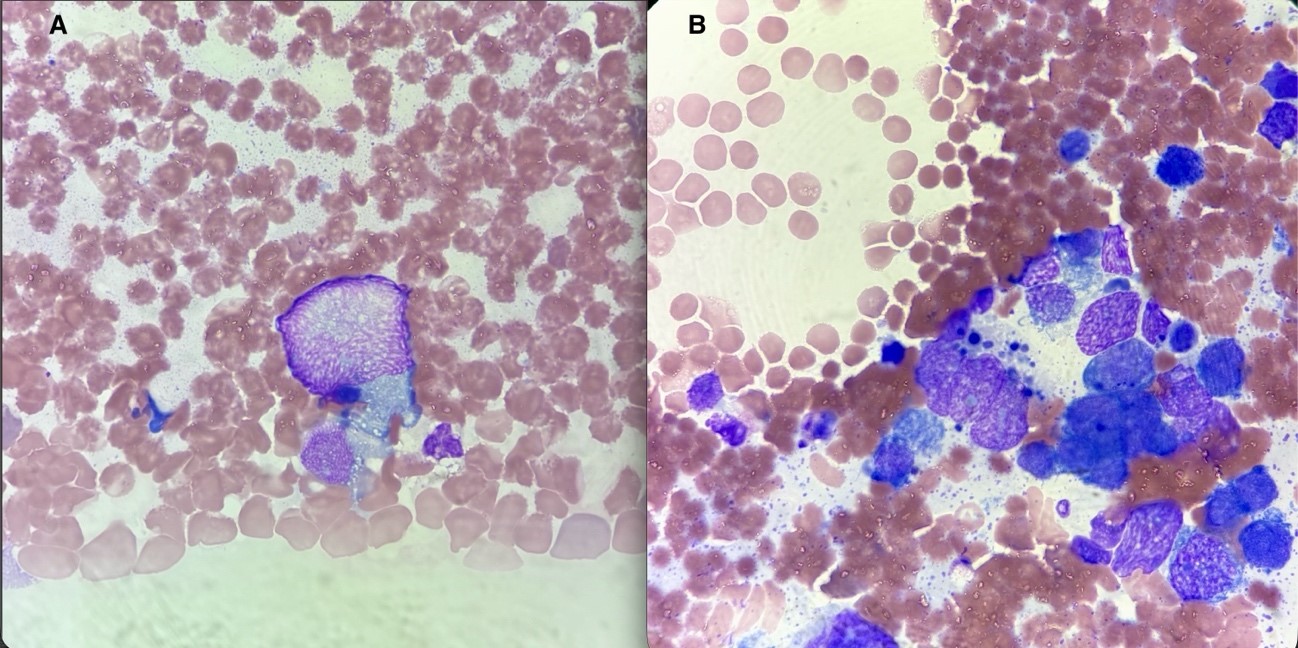
En el aspirado de médula ósea se extrae grumo medular, pero cuya morfología celular es sugerente de necrosis medular, con abundantes restos picnóticos celulares, así como muy escasa representación de las series hematopoyéticas (figura 1). Entre estos restos celulares sugerentes de necrosis se objetivan algunas células de gran tamaño, con núcleo grande, de contorno irregular, cromatina laxa y nucléolos, con citoplasma moderado, agranular y con vacuolas, que sugieren un origen extrahematológico, pero sin poder descartar neoplasia hematológica linfoide con morfología anaplásica (figura 2).
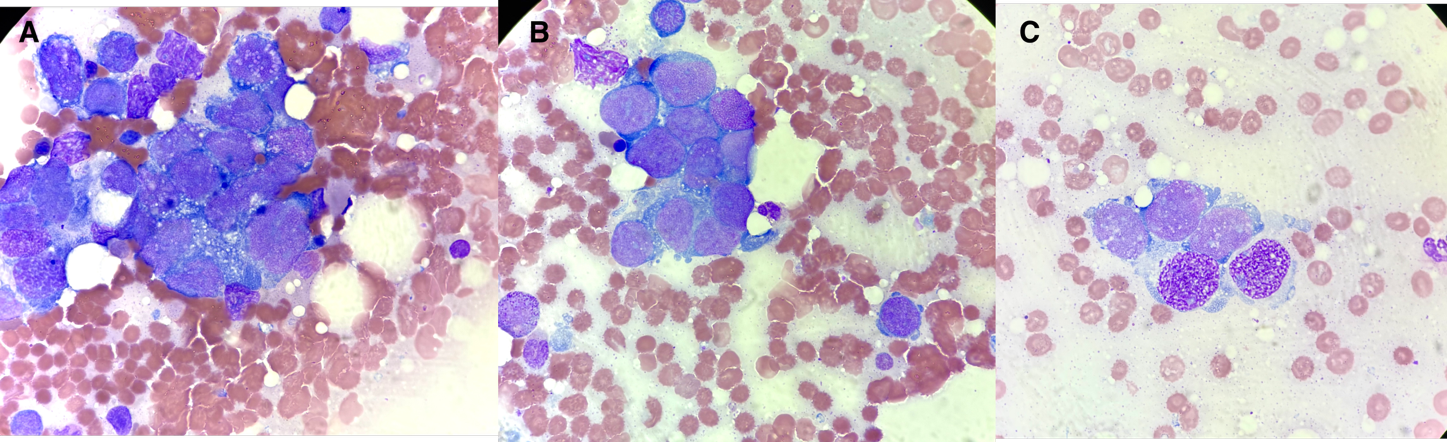
Durante la revisión de las extensiones de impronta ósea se identifican de nuevo signos sugerentes de necrosis medular, aunque con mayor representación de las series hematopoyéticas, y una mayor infiltración por las células descritas previamente en el aspirado, que en estas preparaciones se observan como coalescentes y con tendencia a formar acúmulos heterogéneos, sin clara tendencia a la formación de rosetas o empalizadas (figura3).
Se analizó de forma simultánea el inmunofenotipo del aspirado de médula ósea, no objetivándose un aumento significativo de células hematopoyéticas inmaduras ni clonalidad B, sin alteraciones significativas en el inmunofenotipo de linfocitos T.
El resultado de la anatomía patológica del ganglio linfático supraclavicular es de metástasis linfoganglionar de carcinoma de células pequeñas, con descripción microscópica de crecimiento neoplásico constituido por nidos y masas de células pequeñas, con expresión de sinaptofisina y CD56, ausencia de expresión de CK7, CK20, hpar-1, cromogranina, p40, TTF-1 y un índice proliferativo por ki-67 del 95%.
El resultado de la anatomía patológica de la biopsia ósea es de afectación medular por carcinoma neuroendocrino, descrito microscópicamente como crecimiento neoplásico de células pequeñas y grandes que muestran expresión de sinaptofisina y CD56.
Una vez confirmado el diagnóstico, el paciente inicia tratamiento antineoplásico con carboplatino y etopósido, presentando difícil manejo de citopenias, con neutropenia profunda prolongada complicada con candidemia por C. albicans y trombocitopenia de <20×103/mm3 mantenida, a pesar de recibir tratamiento con estimulantes de colonias granulocíticas y análogos de la trombopoyetina. Finalmente fallece 15 días tras el aspirado de médula ósea.
Discusión
La infiltración de la médula ósea por procesos metastásicos de neoplasias extrahematológicas es un evento raro, cuya frecuencia oscila en torno al 10% según series (1) y está más frecuentemente descrita en carcinomas de pulmón de células pequeñas, carcinomas de mama, adenocarcinomas de próstata y cáncer gástrico en la edad adulta, y neuroblastoma, retinoblastoma y sarcomas en la edad pediátrica. La presentación clínica suele ser variable, desde pacientes aparentemente asintomáticos a pacientes con dolor óseo y fracturas patológicas. Es frecuente la presentación con elevación de lactato deshidrogenasa, hipercalcemia, hipoproteinemia y elevación de fosfatasa alcalina (2). Se ha demostrado una alta correlación entre las metástasis óseas y la infiltración carcinomatosa de la médula ósea (3).
Desde el punto de vista hematológico, los hallazgos más frecuentes son anemia y trombocitopenia, con expresión en la morfología de sangre periférica como reacción leucoeritroblástica en relación con la mieloptisis y anemia hemolítica microangiopática en casos que asocian carcinomatosis diseminada, aunque en muchos casos pueden no observarse estos cambios. El hallazgo de células tumorales en sangre periférica es muy infrecuente, pero está descrita en algunos casos, principalmente en carcinomas de mama (2, 4, 5).
En la médula ósea infiltrada por metástasis, los hallazgos en casos de metástasis pueden ser células aisladas, células formando rosetas o acinos, células formando acúmulos, células en grandes acúmulos o en sábanas, o sustitución completa de la médula ósea. La morfología celular va desde células de pequeño tamaño y contorno redondeado, similar a linfoblastos, como los neuroblastomas; a células de gran tamaño, con citoplasmas basófilos y vacuolados y grandes núcleos vesiculares, como algunos adenocarcinomas. En general, son células pleomórficas que se diferencian del conjunto celular normal de la médula ósea, cuyo grado de diferenciación será variable según el grado histológico del tumor primario. También se pueden observar cambios indirectos asociados a las metástasis, como son la fibrosis medular, la necrosis medular o el aumento de células relacionadas con el proceso de resorción y metabolismo óseo, como son los osteoblastos y osteoclastos (1, 2, 6)
En casos en los que se sospecha infiltración de la médula ósea por un primario conocido, parece haber una diferencia de sensibilidad en cuanto a la infiltración entre el aspirado medular y la biopsia ósea, a favor de la segunda, aunque la aceptable rentabilidad del aspirado y la mayor facilidad y rapidez de su obtención, especialmente en pacientes críticos, hace que muchas veces sea la prueba elegida. Sin embargo, en el seno de enfermedad tumoral sin un claro primario, la biopsia aporta la posibilidad de un espécimen de análisis más adecuado para la inmunohistoquímica, que permita esclarecer el origen tumoral. Se han publicado experimentos satisfactorios de inmunohistoquímica en preparaciones de aspirado medular, aunque hay que tener en cuenta su limitación en cuanto a la ausencia de correlación célula a célula en comparación con cortes histológicos, así como la posibilidad de que las células sean muy escasas para el análisis, especialmente en casos de fibrosis secundaria (1,2,7).
Con todo, el pronóstico de los pacientes con metástasis medulares es muy adverso, con algunas series describiendo supervivencias desde 1 mes en pacientes con tratamiento de soporte hasta 3-8 meses en pacientes que reciben tratamiento (3, 8), teniendo en cuenta que las citopenias complican aún más el manejo de la toxicidad de los antineoplásicos en estos pacientes, sobre todo en casos que asocian necrosis.
Respecto a la necrosis de médula ósea, está descrita tanto en enfermedades no tumorales, como es el caso de la enfermedad de células falciformes o infecciones, como en tumorales. Dentro de las causas tumorales más frecuentes están las enfermedades hematológicas (leucemias y linfomas, especialmente de alto grado) y algunos tumores sólidos, (próstata, sarcoma de Ewing, rabdomiosarcoma, neuroblastoma y carcinoma de mama) (9). En su fisiopatogenia se establecen varios mecanismos que culminan en hipoxemia de la médula ósea, bien por embolismos o trombosis de la microcirculación (tras embolia grasa o por crecimiento expansivo de células tumorales), bien por toxicidad causante de apoptosis, como algunos fármacos (ATRA, fludarabina) o la radiación. (10)
Para el diagnóstico, sirven como apoyo la elevación de LDH, fosfatasa alcalina y la ferritina, reflejando esta última la activación inflamatoria y la liberación de hierro de los macrófagos desde la médula ósea. Morfológicamente, se caracteriza por la pérdida de la arquitectura normal de la médula ósea y la presencia de material eosinofílico amorfo o sombras celulares con bordes mal definidos (células fantasmas), observándose con frecuencia restos celulares y macrófagos cargados de hemosiderina. De forma similar a las metástasis, el pronóstico es infausto en los pacientes con necrosis de médula ósea, habitualmente de semanas a pocos meses tras el diagnóstico. (9, 10).
Como conclusiones de la revisión, cabe destacar la importancia pronóstica del diagnóstico de casos de necrosis medular y de la infiltración carcinomatosa de la médula ósea, dado que se relacionan con una evolución desfavorable y rápida, con alta mortalidad. Estos casos pueden ser sospechados a partir de la clínica (dolores óseos), resultados analíticos (anemia, trombocitopenia) y de los hallazgos morfológicos de la sangre periférica (cuadro leucoeritroblástico). Este diagnóstico diferencial es especialmente relevante en casos en los que existan dudas acerca de un origen tóxico-farmacológico de las citopenias frente a la posibilidad de infiltración medular o necrosis medular, cuyo manejo y pronóstico son muy dispares.
DECLARACIÓN DE TRANSPARENCIA
Los autores/as de este artículo declaran no tener ningún tipo de conflicto de intereses respecto a lo expuesto en el presente trabajo.
BIBLIOGRAFÍA
- ↑Kaspi E, Grosdidier C, Berda-Haddad Y, et al. Challenges and Clinical Relevance in Diagnosing Metastatic Cells From Non-Hematopoietic Malignancies in Bone Marrow Aspirates. Cancer Med. 2025; 14(3):e70645. doi: 10.1002/cam4.70645. PMID: 39907157; PMCID: PMC11795271.
- ↑Gajendra S, Sharma R. Cytomorphological evaluation of non-haematopoietic malignancies metastasizing to the bone marrow. Am J Blood Res. 2023;13(1):1-11. PMID: 36937461; PMCID: PMC10017595.
- ↑Zhou MH, Wang ZH, Zhou HW, Liu M, Gu YJ, Sun JZ. Clinical outcome of 30 patients with bone marrow metastases. J Cancer Res Ther. 2018; 14(Supplement):S512-S515. doi: 10.4103/0973-1482.172717. PMID: 29970716.
- ↑Kopp HG, Krauss K, Fehm T, et al. Symptomatic bone marrow involvement in breast cancer–clinical presentation, treatment, and prognosis: a single institution review of 22 cases. Anticancer Res. 2011 ;31(11):4025-4030. PMID: 22110237.
- ↑Farkh C, Debus J, Andrieu V, Gay J. Massive circulating metastatic cells: A case of carcinocythemia. Clin Case Rep. 2024;12(2):e8471. doi: 10.1002/ccr3.8471. PMID: 38333654; PMCID: PMC10849992.
- ↑Singh A, Rawat S, Kushwaha R, et al. Bone marrow metastasis in nonhematological malignancies: A study from tertiary care center. Ann Afr Med. 2024; 23(1):91-99. doi: 10.4103/aam.aam_55_23. PMID: 38358178; PMCID: PMC10922175.
- ↑Singh G, Krause JR, Breitfeld V. Bone marrow examination: for metastatic tumor: aspirate and biopsy. Cancer. 1977 ;40(5):2317-2321. doi:10.1002/10970142(197711)40:5<2317::aidcncr2820400546>3.0.co;2-z. PMID: 922673.
- ↑Kucukzeybek BB, Calli AO, Kucukzeybek Y, et al. The prognostic significance of bone marrow metastases: evaluation of 58 cases. Indian J Pathol Microbiol. 2014;57(3):396-399. doi: 10.4103/0377-4929.138728. PMID: 25118730.
- ↑Luan C, Zhao H, Ding Y. Bone marrow necrosis: Facts, controversies, and perspective. Int J Lab Hematol. 2024;46(5):770-776. doi: 10.1111/ijlh.14335. Epub 2024 Jun 25. PMID: 38923828.
- ↑Deucher A, Wool GD. How I investigate bone marrow necrosis. Int J Lab Hematol. 2019;41(5):585-592. doi: 10.1111/ijlh.13091. Epub 2019 Aug 19. PMID: 31424633.
Miguel Gómez Álvarez
Real Academia Nacional de Medicina de España
C/ Arrieta, 12 · 28013 Madrid
Tlf.: +34 685 955 657 | E-Mail: miguelgalvar@gmail.com
Enviado: 10.01.26
Revisado: 14.01.26
Aceptado: 26.01.26


