Resumen
La enfermedad renal crónica (ERC) se define como la disminución de la tasa de filtración glomerular estimado (TFGe) por debajo de 60 ml/min/1,73 m2 o evidencia de daño renal, como albuminuria mayor de 30 mg/g de creatinuria, que persisten más de 3 meses. Estos puntos de corte marcan un aumento del riesgo de progresión hasta la necesidad de tratamiento sustitutivo de la función renal y del riesgo de muerte prematura. La enfermedad por coronavirus 2019 (COVID-19) no es una excepción. El estudio Global Burden of Disease identificó la ERC como el factor de riesgo más prevalente a nivel mundial para COVID-19 grave. El proyecto OpenSAFELY analizó los factores asociados con la muerte por COVID-19 en 17 millones de personas. La diálisis (cociente de riesgo ajustado [aHR] 3,69), trasplante de órganos (aHR 3,53) y la ERC no en diálisis (aHR 2,52 para pacientes con TFGe <30 ml/min/1,73 m2) representan tres de las cuatro comorbilidades asociadas con el mayor riesgo de mortalidad por COVID-19. El riesgo asociado con la ERC es mayor que el riesgo asociado con la diabetes mellitus (rango aHR 1,31-1,95, dependiendo del control glucémico) o la enfermedad cardíaca crónica (aHR 1,17), mientras que la hipertensión no es un factor de riesgo independiente de muerte por COVID-19 (aHR 0,89). La alta prevalencia de ERC, en combinación con el elevado riesgo de mortalidad por COVID-19 en la ERC, requiere una acción urgente para proteger a los pacientes con ERC mediante su inclusión en ensayos clínicos de vacunas y tratamientos para COVID-19.
Abstract
Chronic kidney disease (CKD) is defined as an estimated glomerular filtration rate (eGFR) below 60 ml/min/1.73 m2 or evidence of kidney damage, such as albuminuria greater than 30 mg/g creatinuria, which persists more than 3 months. These cut-off points mark an increased risk of progression to the need for kidney replacement therapy and of the risk of premature death. Coronavirus disease-2019 (COVID-19) is no exception. The Global Burden of Disease collaboration identified CKD as the global most prevalent risk factor for severe COVID-19. The OpenSAFELY project analyzed the factors associated with death from COVID-19 in 17 million persons. Dialysis (adjusted hazard ratio [aHR] 3.69), organ transplantation (aHR 3.53) and CKD not on dialysis (aHR 2.52 for patients with eGFR <30 ml/min/1.73 m2) represent three of the four comorbidities associated with the highest risk of mortality from COVID-19. The risk associated with CKD is greater than the risk associated with diabetes mellitus (range aHR 1.31-1.95, depending on glycemic control) or chronic heart disease (aHR 1.17), whereas hypertension is not an independent risk factor for death from COVID-19 (aHR 0.89). The high prevalence of CKD, combined with the high risk of mortality from COVID-19 in CKD, requires urgent action to protect CKD patients from COVID-19 by offering the opportunity to participate in clinical trials of vaccines and treatments for COVID-19.
Palabras clave: Enfermedad renal crónica; Mortalidad; COVID-19; Factor de riesgo; Prevalencia.
Keywords: Chronic kidney disease; Mortality; COVID-19; Risk factor; Prevalence.
En esta revisión abordamos datos recientes que indican que la enfermedad renal crónica (ERC) es uno de los factores de riesgo más relevantes para mortalidad por enfermedad por coronavirus-2019 (COVID-19). Ante la inmensa literatura sobre COVID-19 (93,772 artículos según PubMed en enero de 2021), para realizar la revisión hemos seleccionado preferentemente grandes estudios epidemiológicos publicadas en revistas de primer nivel y la experiencia local con COVID-19.
¿Qué es la ERC?
La ERC se define actualmente como una disminución de la función renal medida por la tasa de filtración glomerular estimado (TFGe) o evidencia de daño renal (incluso con una TFGe normal), como aumento de albuminuria, sedimento urinario anormal, anomalías estructurales que persisten por más de 3 meses, con implicaciones para la salud (1). Los umbrales de TFGe y albuminuria que se cree que tienen implicaciones para la salud son <60 ml/min/1,73 m2 y >30 mg/g de creatinina urinaria, respectivamente. A pesar de que la definición de ERC consensuada se remonta a 2012, todavía existe un conocimiento insuficiente del concepto y el diagnóstico de ERC no se registra con frecuencia en las historias clínicas de los pacientes (2). Se ha estimado que la prevalencia de ERC en la población adulta es del 10 al 15%, y se estima que 850 millones de personas tienen ERC en todo el mundo. Se prevé que la ERC se convierta en la quinta causa de muerte para el año 2040 en todo el mundo y una de las dos principales causas de muerte antes de fin de siglo en algunos países europeos, particularmente donde la esperanza de vida es más larga (3-5). De hecho, los pacientes con ERC, especialmente aquellos con insuficiencia renal, tienen un mayor riesgo de muerte prematura por muchas causas, incluidas, entre otras, enfermedades e infecciones cardiovasculares (6). Varias publicaciones identificaron el nihilismo terapéutico (p. Ej., La retención de fármacos o las intervenciones que demostraron ser efectivas en la población general) como un contribuyente potencial a la alta mortalidad (6).
La ERC es el factor de riesgo más prevalente de COVID-19 grave en el mundo
El estudio Global Burden of Disease (GBD), que proporciona información anual sobre la salud de las poblaciones en todo el mundo, abordó recientemente la prevalencia de factores de riesgo de COVID-19 grave en todo el mundo (7,8). El GBD produce estimaciones de salud específicas por edad, sexo y país utilizando enfoques altamente estandarizados y validados aplicados a todas las fuentes de datos disponibles y ajustando las principales fuentes de sesgo. Utilizando los datos de prevalencia de 2017 y las estimaciones de población de la ONU para 2020, el GBD estimó el número de personas con mayor riesgo de COVID-19 grave por edad, sexo y país para 188 países. Este estudio estimó que la población mundial con alto riesgo de COVID-19 grave es de 1.700 millones de personas, lo que representa el 22% de la población mundial, de los cuales 349 millones requerirían hospitalización si se infectaran. La ERC fue el factor de riesgo más prevalente de COVID-19 grave en todo el mundo (7). Fue el factor de riesgo más común en los menores de 60 años y mayores de 80 años y tan frecuente como la enfermedad cardiovascular entre los 60 y 80 años. La eliminación de la ERC como factor de riesgo disminuiría el porcentaje de la población mundial con mayor riesgo de COVID-19 grave del 22% al 17%. Por lo tanto, la ERC representa el aumento del riesgo de COVID-19 grave para alrededor de 1 de cada 4 personas de alto riesgo en todo el mundo (Figura 1), equivalente al 5% de la población mundial o 86.530.000 personas.
La ERC es la enfermedad que conlleva el mayor riesgo de COVID-19 grave
Williamson et al publicaron recientemente el análisis más grande hasta la fecha de los factores de riesgo de COVID-19 grave con resultado de muerte (9). Analizaron datos de más de 17 millones de adultos y casi 11.000 muertes relacionadas con COVID-19 utilizando OpenSAFELY, una plataforma de análisis de salud que cubre el 40% de todos los pacientes en Inglaterra. En resumen, los autores afirman que la muerte relacionada con el COVID-19 se asoció con el sexo masculino (Hazard ratio (HR) 1,59 (intervalo de confianza del 95%: 1,53-1,65)), edad avanzada, privación, diabetes, asma grave, etnia africana o del sur de Asia y “varias otras condiciones médicas”. Aunque la ERC aún no se menciona en el resumen del artículo completo, está claro que la ERC avanzada (ERC G4 y G5) se encuentra entre las condiciones que conllevan el mayor riesgo de muerte y notablemente más alto que el conferido por todos los factores mencionados en el resumen. De hecho, en un modelo completamente ajustado (Adj), los pacientes con enfermedad renal, por ejemplo, los pacientes en diálisis (Adj HR 3,69), los receptores de trasplante (Adj HR 3,53) y los pacientes con ERC (Adj HR 2,52 para pacientes con TFGe <30 ml/min/1,73 m2, categorías de TFG G4-G5) representaron 3 de las 4 categorías de riesgo principales. El riesgo en estos subgrupos es mayor que el riesgo de muerte por COVID-19 en pacientes diabéticos (rango adjunto de HR 1.31-1.95, dependiendo del control glucémico) y en pacientes con cardiopatía crónica (Adj HR 1.17) (Figura 2). En análisis de sensibilidad con diferentes poblaciones (censura temprana, restringida a aquellos con datos completos de IMC / tabaquismo, ajustados por etnia registrada o imputada), el riesgo conferido por ERC G4-G5 fue consistentemente más alto que el riesgo transmitido por DM mal controlada o asma severa, lo que hace aún más desconcertante que la ERC no se encuentre entre los factores de riesgo detallados en el resumen. Los datos sobre hipertensión son interesantes. A pesar de haber sido ampliamente mencionado como un factor de riesgo de COVID-19 grave, en un análisis ajustado por edad y sexo, solo se asoció débilmente con el riesgo de muerte (HR 1,09; 1,05-1,14). De hecho, en un análisis completamente ajustado, el riesgo asociado con la hipertensión se revirtió (Adj HR 0,89; 0,85-0,93), lo que sugiere que la hipertensión puede ser un sustituto de otras afecciones, por ejemplo, la ERC, que conlleva el riesgo. Una explicación adicional podría ser que el riesgo asociado con la hipertensión está influenciado por el uso de ciertos medicamentos, por ejemplo bloqueadores del sistema renina-angiotensina (RAS). Aunque inicialmente se planteó la hipótesis de que el bloqueo de RAS puede aumentar el riesgo de COVID-19 grave al aumentar la expresión de ACE2 (y la entrada posterior del virus en las células), o disminuir el riesgo de COVID-19 grave al promover la síntesis de Ang1-7, ninguna de estas hipótesis ha sido probada hasta ahora en estudios epidemiológicos que más bien tienden a mostrar un efecto neutral (10, 11). El impacto potencial del bloqueo de RAS no se evaluó en OpenSAFELY. En última instancia, incluso cuando se demuestra claramente que la ERC se encuentra entre las comorbilidades que conllevan el mayor riesgo de muerte en COVID-19, se reemplaza en el ‘título’ del artículo, es decir, en el resumen, por afecciones más “populares” que, irónicamente, están realmente asociadas con menor riesgo de mortalidad por COVID-19 que la ERC.
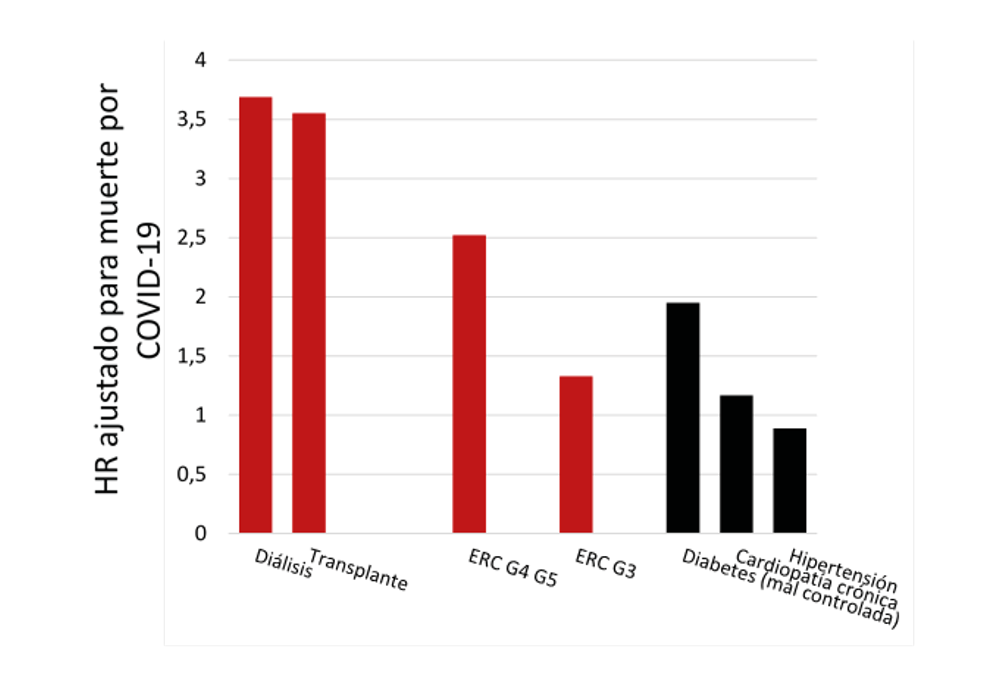
En un estudio de cohorte separado basado en la población del Reino Unido realizado en un contexto de práctica general, la edad y la TFGe fueron las variables que más afectaron las razones de riesgo ajustadas para la muerte relacionada con COVID-19 en personas con diabetes tipo 1 (DM1, n = 264390) y tipo 2 (DM2, n = 2874020) (12). El aumento del riesgo fue evidente a partir de la TFGe 45-59 ml / min / 1,73 m2, pero no con una TFGe superior a ese valor, tanto en DM1 como en DM2, es decir, fue evidente para los pacientes con ERC según lo definido por los umbrales de TFGe. Desafortunadamente, al igual que en el estudio OpenSAFELY, no se analizó el efecto del aumento de la albuminuria. Así, se confirmó el mayor riesgo de las personas con ERC G3-G5, pero faltaba información sobre ERC G1-G2, como en otros estudios epidemiológicos. Una TFGe <15 ml / min / 1,73 m2 confiere el mayor riesgo de muerte, con excepción de la edad, entre las diferentes variables analizadas, ambas en DM1 (FC adj frente a TFGe ≥ 90 ml / min / 1,73 m2 8,35; 5,50– 12,70) y en DM2 (4,91; 4,34-5,56). Otras variables analizadas incluyeron sexo, situación socioeconómica o privación, etnia, HbA1c, IMC, presión arterial, fármacos antihipertensivos, tabaquismo y comorbilidades cardiovasculares. Los HR para la función renal alterada fueron consistentes para hombres y mujeres y fueron mayores para personas menores de 70 años.
Los resultados del Registro ERA-EDTA respaldan aún más la alta mortalidad debida a COVID-19 en pacientes en diálisis y receptores de trasplantes de riñón en toda Europa (13). La mortalidad a los 28 días fue del 20,0% (intervalo de confianza del 95%: 18,7% -21,4%) en 3285 pacientes que recibieron diálisis y del 19,9% (17,5% -22,5%) en 1013 receptores de un trasplante renal. El riesgo de mortalidad fue 1,28 (1,02-1,60) veces mayor en los receptores de trasplantes en comparación con los pacientes de diálisis compatibles. En ambos grupos, la mortalidad está relacionada en gran medida con la edad y el estado de fragilidad (14). Además, la frecuentación de los centros de salud puede aumentar el riesgo de infección para los pacientes con ERT, siendo el transporte sanitario colectivo un factor de riesgo clave (15, 16,).
Un dato que falta es la cuantificación del riesgo que conlleva la albuminuria patológica. Este puede ser el único criterio que puede definir la ERC cuando la TFGe es ≥60 ml / min / 1,73 m2 o puede aumentar aún más el riesgo en pacientes con ERC con una TFGe más baja. En este sentido, también es interesante señalar que el COVID-19 en sí mismo puede causar daño glomerular como evidencia de proteinuria patológica que puede estar asociada con fracaso renal agudo (FRA) (17). En este sentido, el SARS-CoV-2 tiene un tropismo multiorgánico que incluye células glomerulares, pero también células tubulares (18-20).
Estudios recientes están caracterizando la naturaleza de COVID-19 en los pacientes con ERC, diálisis o trasplante, identificando factores de riesgo para enfermedad grave y mortalidad, así como el patrón de temporal de la alteraciones clínicas y analíticas (21-26). No obstante, no hay información sobre la respuesta ante la vacunación, que puede ser deficiente (27).
CONCLUSIONES
Aunque no figura en los informes iniciales como factor de riesgo de COVID-19 grave, la ERC es tanto la comorbilidad más prevalente asociada a riesgo de COVID-19 grave, sino también la que más aumenta el riesgo de COVID-19 grave. El aumento del riesgo es evidente por debajo del umbral de TFGe que define la ERC y el riesgo aumenta a medida que disminuye la TFGe; el riesgo más alto se observa en pacientes en terapia de reemplazo renal. Aunque se sabe que los pacientes con ERC tienen un mayor riesgo de muerte debido a enfermedades infecciosas, deben explorarse los factores que contribuyen a su mayor sensibilidad al COVID-19 grave, ya que pueden proporcionar información valiosa sobre los enfoques terapéuticos de la enfermedad en este grupo de pacientes.
Actualmente se desconoce si las categorías anteriores de ERC (G1 / G2, es decir, pacientes con función renal conservada pero con aumento de albuminuria) también tienen un mayor riesgo de COVID-19 grave y esto debe explorarse. Además, el reconocimiento de que la ERC contribuye significativamente a la gravedad de COVID-19 ahora debería resultar en esfuerzos enfocados para mejorar los resultados de los 850 millones de pacientes con ERC en todo el mundo (3, 13). Para ello, es fundamental la inscripción de pacientes que representen todas las etapas de la ERC, incluida la diálisis y el trasplante, en ensayos clínicos de vacunas para prevenir y medicamentos para tratar COVID-19.
Fundamentalmente, el diagnóstico de ERC no debe utilizarse como único criterio para denegar la admisión en cuidados intensivos con COVID-19 grave. Tanto las sociedades científicas como las asociaciones de pacientes deben estar atentas a este respecto. Además, hasta que se disponga de mejores datos epidemiológicos y se determine la base biológica del mayor riesgo de COVID-19 grave en pacientes con ERC, el nihilismo terapéutico puede seguir desempeñando un papel, y a las personas con ERC se les puede llegar a negar el apoyo vital debido a su mayor riesgo de muerte por COVID-19. Esto se convierte en una profecía autocumplida inaceptable. La amenazante escasez de capacidad de la UCI en algunas partes del mundo puede haber contribuido a la alta mortalidad de los pacientes con ERC en estas áreas. En aquellos con enfermedad renal, el nihilismo terapéutico se ha asociado repetidamente con resultados adversos (6). Frente a una pandemia en curso de duración no cuantificable, esta no es una estrategia aceptable, en particular si se considera la alta prevalencia de ERC.
Proponemos que las personas con ERC deben participar activamente en la investigación para garantizar un acceso equitativo a vacunas y tratamientos eficaces en el futuro (28). Además, es preciso que las autoridades sanitarias tomen conciencia de la necesidad de cuidar la salud mental de los trabajadores sanitarios en tiempo de catástrofe, como es la pandemia COVID-19 (29).
Agradecimientos y financiación
La investigación de los autores está financiada por Sources of support: FIS/Fondos FEDER (PI18/01366, PI19/00815, DTS18/00032, ERA-PerMed-JTC2018 (KIDNEY ATTACK AC18/00064 and PERSTIGAN AC18/00071, ISCIII-RETIC REDinREN RD016/0009), Sociedad Española de Nefrología, FRIAT, Comunidad de Madrid en Biomedicina B2017/BMD-3686 CIFRA2-CM, V Premio Jóvenes Investigadores AstraZeneca 2020.
BIBLIOGRAFÍA
- Kidney Disease: Improving Global Outcomes (KDIGO) CKD Work Group. KDIGO 2012 Clinical Practice Guideline for the Evaluation and Management of Chronic Kidney Disease. Kidney Int Suppl 2013; 3: 1–150
- Perez-Gomez MV, Bartsch LA, Castillo-Rodriguez E, et al. Clarifying the concept of chronic kidney disease for non-nephrologists. Clin Kidney J. 2019;12(2):258-261
- Jager KJ, Kovesdy C, Langham R, Rosenberg M, Jha V, Zoccali C. A single number for advocacy and communication-worldwide more than 850 million individuals have kidney diseases. Nephrol Dial Transplant. 2019;34(11):1803-1805
- Foreman KJ, Marquez N, Dolgert A, et al. Forecasting life expectancy, years of life lost, and all-cause and cause-specific mortality for 250 causes of death: reference and alternative scenarios for 2016-40 for 195 countries and territories. Lancet. 2018;392(10159):2052-2090
- Ortiz A, Sanchez-Niño MD, Crespo-Barrio M, et al. The Spanish Society of Nephrology (SENEFRO) commentary to the Spain GBD 2016 report: Keeping chronic kidney disease out of sight of health authorities will only magnify the problem. Nefrologia. 2019;39(1):29-34
- Ortiz A, Covic A, Fliser D, et al. Epidemiology, contributors to, and clinical trials of mortality risk in chronic kidney failure. Lancet. 2014;383(9931):1831-1843
- Clark A, Jit M, Warren-Gash C, et al. Global, regional, and national estimates of the population at increased risk of severe COVID-19 due to underlying health conditions in 2020: a modelling study. Lancet Glob Health. 2020;8(8):e1003-e1017 32553130
- Murray CJ, Ezzati M, Flaxman AD, et al. GBD 2010: a multi-investigator collaboration for global comparative descriptive epidemiology. Lancet. 2012;380(9859):2055-2058
- Williamson EJ, Walker AJ, Bhaskaran K, et al. Factors associated with COVID-19-related death using OpenSAFELY. Nature. 2020;584(7821):430-436 . 32640463
- Reynolds HR, Adhikari S, Pulgarin C, et al. Renin-Angiotensin-Aldosterone System Inhibitors and Risk of Covid-19. N Engl J Med. 2020;382(25):2441-2448
- Mancia G, Rea F, Ludergnani M, Apolone G, Corrao G. Renin-Angiotensin-Aldosterone System Blockers and the Risk of Covid-19. N Engl J Med. 2020;382(25):2431-2440
- Holman N, Knighton P, Kar P, et al. Risk factors for COVID-19-related mortality in people with type 1 and type 2 diabetes in England: a population-based cohort study. Lancet Diabetes Endocrinol. 2020;8(10):823-833
- Jager KJ, Kramer A, Chesnaye NC, et al. Results from the ERA-EDTA Registry indicate a high mortality due to COVID-19 in dialysis patients and kidney transplant recipients across Europe. Kidney Int. 2020;98(6):1540-1548.
- Hilbrands LB, Duivenvoorden R, Vart P, Franssen CFM for the ERACODA Collaborators. COVID-19-related mortality in kidney transplant and dialysis patients: results of the ERACODA collaboration. Nephrol Dial Transplant 2020;35(11):1973-1983.
- Rincón A, Moreso F, López-Herradón A, et al. The keys to control a COVID-19 outbreak in a haemodialysis unit. Clin Kidney J. 2020;13(4):542-549.
- Fernandez-Prado R, Gonzalez-Parra E, Ortiz A. Often forgotten, transport modality to dialysis may be life-saving. Clin Kidney J. 2020;13(4):510-512.
- Carriazo S, Kanbay M, Ortiz A. Kidney disease and electrolytes in COVID-19: more than meets the eye. Clin Kidney J. 2020;13(3):274-280
- Braun F, Lütgehetmann M, Pfefferle S, et al. SARS-CoV-2 renal tropism associates with acute kidney injury. Lancet. 2020;396(10251):597-598.
- Puelles VG, Lütgehetmann M, Lindenmeyer MT, et al. Multiorgan and Renal Tropism of SARS-CoV-2. N Engl J Med. 2020;383(6):590-592
- Couturier A, Ferlicot S, Chevalier K, et al. Indirect effects of severe acute respiratory syndrome coronavirus 2 on the kidney in coronavirus disease patients. Clin Kidney J. 2020;13(3):347-353.
- Stock da Cunha T, Gomá-Garcés E, Avello A, et al. The Spectrum of Clinical and Serological Features of COVID-19 in Urban Hemodialysis Patients. J Clin Med. 2020;9(7):2264
- Lano G, Braconnier A, Bataille S, et al. Risk factors for severity of COVID-19 in chronic dialysis patients from a multicentre French cohort. Clin Kidney J. 2020;13(5):878-888
- Prendecki M, Clarke C, Medjeral-Thomas N, et al. Temporal changes in complement activation in haemodialysis patients with COVID-19 as a predictor of disease progression. Clin Kidney J. 2020;13(5):889-896
- D’Marco L, Puchades MJ, Romero-Parra M, et al. Coronavirus disease 2019 in chronic kidney disease. Clin Kidney J. 2020;13(3):297-306.
- Fontana F, Giaroni F, Frisina M, et al. SARS-CoV-2 infection in dialysis patients in northern Italy: a single-centre experience. Clin Kidney J. 2020;13(3):334-339.
- Wang R, He H, Liao C, et al. Clinical outcomes of hemodialysis patients infected with severe acute respiratory syndrome coronavirus 2 and impact of proactive chest computed tomography scans. Clin Kidney J. 2020;13(3):328-333.
- Reddy S, Chitturi C, Yee J. Vaccination in Chronic Kidney Disease. Adv Chronic Kidney Dis. 2019;26(1):72-78.
- ERA-EDTA Council; ERACODA Working Group. Chronic kidney disease is a key risk factor for severe COVID-19: a call to action by the ERA-EDTA. Nephrol Dial Transplant. 2021;36(1):87-94
- Sever MS, Ortiz A, Maggiore U, Bac-García E, Vanholder R. Mass Disasters and Burnout in Nephrology Personnel: From Earthquakes and Hurricanes to COVID-19 Pandemic. Clin J Am Soc Nephrol. 2021 Jan 7:CJN.08400520. doi: 10.2215/CJN.08400520. Epub ahead of print. PMID: 33414153
DECLARACIÓN DE TRANSPARENCIA
Los autores/as de este artículo declaran no tener ningún tipo de conflicto de intereses respecto a lo expuesto en el presente trabajo.
ranm tv
Alberto Ortiz
IIS-Fundacion Jiménez Díaz
Av Reyes Católicos, 2 · 28040 Madrid
Tlf.: +34 91 159 47 34 | E-Mail: aortiz@fjd.es
Año 2020 · número 137 (03) · páginas 270 a 275
Enviado*: 12.11.20
Revisado: 15.11.20
Aceptado: 10.12.20
* Fecha de lectura en la RANM


