Resumen
En Colombia la intoxicación por paraquat (PQ) es una de las principales causas de intoxicación autoprovocada por plaguicidas. Aun no existe un tratamiento antídoto que contrarreste su toxicidad, lo cual ejerce un pronóstico incierto, con supervivencia variable.
Objetivo: Describir el pronóstico de los pacientes con intoxicación por PQ atendidos en un hospital de alta complejidad y evaluar la asociación de la mortalidad con las variables clínicas y de laboratorio teniendo en cuenta su variación en el tiempo.
Métodos: Estudio retrospectivo realizado entre 2011 y 2018 en el Hosptal San Vicente Fundación (Medellín, Colombia). Se incluyeron casos con diagnóstico de intoxicación por PQ que ingresaron vivos, de cualquier edad y sexo. Fueron excluidos diagnósticos de ingesta concomitante de otros tóxicos, enfermedad pulmonar de base, y traumatismo. Se describieron las características sociodemográficas y clínicas, se analizó el efecto sobre la mortalidad y la variación en el tiempo, para la búsqueda de criterios de investigación pronostica.
Resultados: Se reclutó una cohorte de 67 pacientes, predominaron hombres solteros, menores de 30 años, de área rural. Se encontró una mortalidad de 37,3% (IC95% 36,9 a 37,7%), mediana de tiempo de sobrevivencia de 117 h (IQR 62h-238h). El riesgo instantáneo de morir para el sexo masculino fue 1,93; IC95%1,44 a 10,26; p=0,007. Los cambios de laboratorios en el tiempo: AST (HR=1,009; IC95%; 1,007-1,012; p≤0,001), ALT (HR=1,008; IC 95% 1,006-1,01; p≤0,001), bilirrubina total (HR=1,23; IC95% 1,173-1,29; p≤0,001), creatinina (HR=1,53; IC95% 1,398-1,667; p≤0,001).
Conclusión: Factores asociados con mortalidad en intoxicación por PQ: Dosis ingerida, el carácter intencional de la ingesta, el sexo masculino y la edad. El cambio en el tiempo de AST, ALT, creatinina y bilirrubina total se relacionaron con la muerte. Crear modelos pronósticos dinámicos con variables clínicas y de laboratorio que incluyan su evolución durante la estancia hospitalaria puede optimizar la predicción del pronóstico.
Abstract
In Colombia, paraquat poisoning (PQ) is one of the main causes of self-inflicted pesticide poisoning. There is not antidotal treatment against its toxicity, influencing an uncertain prognosis and changeful survival.
Objective: To describe the prognosis of patients with PQ poisoning treated in a high-level hospital and to evaluate the association of mortality with clinical and laboratory test variables, considering its variation over time.
Methods: Retrospective study between 2011 and 2018 at the Hospital San Vicente Fundación (Medellín, Colombia). Included cases diagnosed with PQ poisoning, of any age and sex. Diagnoses of concomitant intake of other toxins, underlying lung disease, and trauma were excluded. Sociodemographic and clinical characteristics were described, the effect on mortality and variation over time were analyzed, to search for prognostic research candidates.
Results: Cohort of 67 patients, mostly single men, under 30 years of age, located in rural area was recruited. A mortality of 37.3% (95% CI 36.9 to 37.7%) was found, median time to death of 117 h (IQR 62h-238h). The instantaneous risk of dying for the male sex was 1.93; 95% CI 1.44 to 10.26; p = 0.007. Laboratory changes over time: AST (HR = 1.009; 95% CI; 1.007-1.012; p≤0.001), ALT (HR = 1.008; 95% CI 1.006-1.01; p≤0.001), total bilirubin (HR = 1.23; 95% CI 1,173-1.29; p≤0.001), creatinine (HR = 1.53; 95% CI 1,398-1,667; p≤0.001).
Conclusion: Factors associated with mortality in PQ poisoning: ingested dose, intentional intake, male sex, and age. The change over time of AST, ALT, creatinine, and total bilirubin is related to death. Design dynamic models with clinical and laboratory test variables that include their evolution during the hospital stay can optimize the prognosis prediction.
Palabras clave: Mortalidad; Paraquat; Intoxicación; Pronostico; Análisis bioquímicos.
Keywords: Mortality; Paraquat; Poisoning; Prognosis; Biochemical analysis.
introducción
El paraquat (PQ) (1,1-dimetil-4,4-bipiridilo dicloruro) es un herbicida de contacto no selectivo (1), considerado como moderadamente peligroso (categoría toxicológica II) según la clasificación de toxicidad aguda de la Organización Mundial de la Salud (OMS)(2). La intoxicación por PQ es una de las principales causas de muerte intencional por exposición a plaguicidas; según datos de la OMS entre 2010 y 2014 ocurrieron cerca de 110,000 muertes cada año por intoxicación autoinflingida por plaguicidas. En Asia el 80% de estas muertes se debieron a PQ, razón por la que se ha prohibido en alrededor de 60 países (3,4).
En Colombia es un herbicida de venta libre y de bajo costo, lo que favorece que su intoxicación se presente con relativa frecuencia. Según datos del Sistema Nacional de Vigilancia en Salud Pública (SIVIGILA) en 2019 se reportaron 3942 casos de intoxicación por plaguicidas y durante 2015 la Línea Nacional de Toxicología del Ministerio de Salud de Colombia asesoró 9,143 casos de eventos tóxicos por sustancias químicas, 2,497 (27,3%) correspondieron a plaguicidas, 90 (3,6%) fueron específicamente por PQ, de los cuales 16 fallecieron, casi todos por ingesta intencional (5,6). En Colombia la carga de enfermedad entre 2010 – 2016 para la intoxicación por PQ fue de 53,4 años de vida ajustados por discapacidad (DALY) por 100,000 habitantes (7). De tal manera que la intoxicación intencional por PQ es un preocupante problema de salud pública (3).
En los casos moderados a graves la intoxicación por PQ cursa con fallo renal, insuficiencia hepática, fallo multisistémico, fibrosis pulmonar y muerte (8). Los mecanismos de toxicidad implican el estrés oxidativo con activación del ciclo redox lo que lleva a la generación de especies reactivas de oxígeno (ROS), alteración mitocondrial y activación de la cascada inflamatoria (9). Con este fundamento se han propuesto tratamientos dirigidos a contrarrestar dichas alteraciones, acompañados de medidas para evitar la absorción y aumentar la excreción (5). Se han utilizado inmunosupresores (ciclofosfamida, glucocorticoides) y antioxidantes (N-acetil cisteína, vitamina A y E), pero los resultados sobre su efectividad para disminuir la mortalidad son inconsistentes, en consecuencia al no existir un tratamiento antídoto que contrarreste la toxicidad del PQ, su pronóstico es incierto con una supervivencia variable (10).
Para orientar la atención de la intoxicación varios estudios han evaluado factores pronósticos, de forma consistente se relaciona el tiempo transcurrido desde la ingesta con la concentración plasmática. Sin embargo es difícil conocer el tiempo desde su ingestión (11) y la cuantificación de los niveles está limitada a centros especializados (12). Por esto se han estudiado otros factores pronósticos que incluyen signos clínicos y exámenes de laboratorio, como el contaje de leucocitos, creatinina y lactato (13), aunque su asociación con la mortalidad ha sido heterogénea (14). Esto podría deberse a que estos factores pronósticos se miden solo al ingreso del paciente al hospital sin considerar las modificaciones que se presentan a lo largo de la hospitalización, por lo que se les da una interpretación que lleva a subestimación del riesgo de muerte (15). Se ha propuesto ampliar el conocimiento del pronóstico de estas variables y de su variación en el tiempo con el fin de mejorar la predicción de desenlaces (16).
Como se ha dicho, el objetivo de esta investigación es analizar el pronóstico de los pacientes con intoxicación por PQ atendidos en un hospital de alto nivel en Colombia y evaluar la asociación de variables clínicas y de laboratorio que cambian en el tiempo con la mortalidad.
MATERIAL Y MÉTODOS
Estudio de cohorte retrospectivo en el que se realizó una revisión de historias clínicas entre enero de 2019 y febrero de 2020 de pacientes con diagnósticos relacionados con intoxicación por PQ, de acuerdo con la décima revisión de la Clasificación Internacional de Enfermedades (CIE-10). Se llevó a cabo en el Hospital Universitario San Vicente Fundación (HUSVF) de Medellín, Colombia, que es un centro de alta complejidad y recibe pacientes de todos los niveles socioeconómicos y de todas las regiones del Departamento de Antioquia y otros departamentos. Este estudio fue aprobado por el Comité de Bioética del HUSVF.
Participantes
Se revisaron historias clínicas de todos los pacientes atendidos entre el año 2011 y 2018 en el HUSVF que tenían los siguientes diagnósticos CIE-10: Intoxicación por otros insecticidas (T60.2), Intoxicación por herbicidas y fungicidas (T60.3), Intoxicación por otros plaguicidas (T60.8), Intoxicación por plaguicida no especificado (T60.9), Efecto tóxico de sustancia corrosiva no especificada (T54.9), Efecto tóxico de sustancia no especificada (T659). Se incluyeron personas de cualquier edad y sexo que ingresaron vivos con diagnóstico de intoxicación por PQ confirmada en la historia clínica. Se excluyeron casos con ingesta concomitante de otra sustancia tóxica, enfermedad pulmonar de base o traumatismo.
Recolección de datos
Se construyó un formulario de Google encriptado y se introdujeron los datos obtenidos de las historias clínicas. Se realizó una prueba piloto para determinar la necesidad de ajustes y permitir la recolección de los tiempos en los que fueron captadas cada una de las variables. Se evaluaron las variables sociodemográficas (edad, sexo, estado civil, ocupación, escolaridad, procedencia, seguridad social) y clínicas (hora de ingesta, hora de ingreso a los servicios de salud, tipo de ingesta, cantidad ingerida, clasificación de la intoxicación por manifestaciones clínicas, estancia hospitalaria, tratamiento recibido y complicaciones) y los exámenes de laboratorios con su respectivo tiempo de realización (electrolitos, función renal, función hepática, gases arteriales).
Para la clasificación de la gravedad de las intoxicación por PQ se tomaron en cuenta los criterios propuestos por Dinis-Oliveira et al (8). Se definió como intoxicación leve aquella en la cual el paciente estuvo asintomático o presentó síntomas gastrointestinales leves, lesión renal o hepática mínima; moderada, la que presentó compromiso de órgano blanco con alteración en los exámenes de química sanguínea o estudios radiológicos y el paciente se recuperó; grave, presencia de afectación multisistémica con riesgo alto de muerte; y fulminante, aquella que por su afectación multisistémica, progresó hacia la muerte en las primeras 24 horas.
Análisis estadístico
Las variables sociodemográficas, clínicas y de laboratorio categóricas fueron resumidas por medio de frecuencias relativas y absolutas; las continuas con mediana y rango intercuartílico (RIQ) dado que no cumplieron el supuesto de distribución normal en la prueba de Shapiro-Wilk. Se realizó un análisis de supervivencia tomando como tiempo al evento, el comprendido entre la ingesta (o en su defecto al ingreso a una institución de salud) y el alta hospitalaria, y como desenlace la variable muerte; se excluyeron los que fueron dados de alta vivos. Se utilizó el método de Kaplan-Meier para la estimación de la función de supervivencia y para explorar diferencias entre las variables. Para comparar las curvas de supervivencia entre distintas categorías de una misma variable se aplicó la prueba de log-rank. Para el caso de variables continuas se realizó el cálculo de la mortalidad móvil para evaluar tendencias.
También se analizó el efecto de las variables sociodemográficas y clínicas sobre la mortalidad por medio de un modelo de riesgos proporcionales de Cox. La hipótesis de riesgos proporcionales se comprobó para cada una las variables por medio del análisis estadístico de los residuales de Schoenfeld. Para proponer los factores relacionados con la muerte se realizó únicamente un análisis univariado. Se compararon y se tomaron los exámenes de laboratorio como covariables que se modifican en el tiempo bajo el enfoque de búsqueda de candidatos de la investigación pronostica (17). Se consideró para todos los análisis el parámetro que era estadísticamente significativo con un valor de p menor de 0,05. Los análisis se realizaron con el paquete estadístico STATA versión 15. Se realizaron gráficos de espaguetis por pequeños grupos para explorar el comportamiento de las variables que cambiaron en el tiempo. Se utilizó el paquete plotly para la creación de gráficos de dispersión con línea en el software R 3.6.3.
RESULTADOS
Se revisaron 1309 historias clínicas y se conformó una cohorte con 67 pacientes de intoxicación por PQ (Figura 1). La mayoría de los sujetos fueron hombres, solteros, menores de 30 años y habitantes de áreas rurales. Salvo un paciente, todos fueron atendidos por primera vez en un hospital de baja complejidad y el tiempo de consulta tuvo una mediana de 2,5h (RIQ 1 – 5,5h). La ingesta fue intencional en el 86,6% y accidental en el 13,4%, con una mediana en la cantidad de PQ ingerida de 33,5ml (RIQ 15ml – 100ml), en datos obtenidos de 33 pacientes. El test de ditionito se realizó al 28,4% y su resultado fue reactivo en el 63,2%. En su mayoría se presentaron como intoxicaciones leves y graves (Tabla 1).
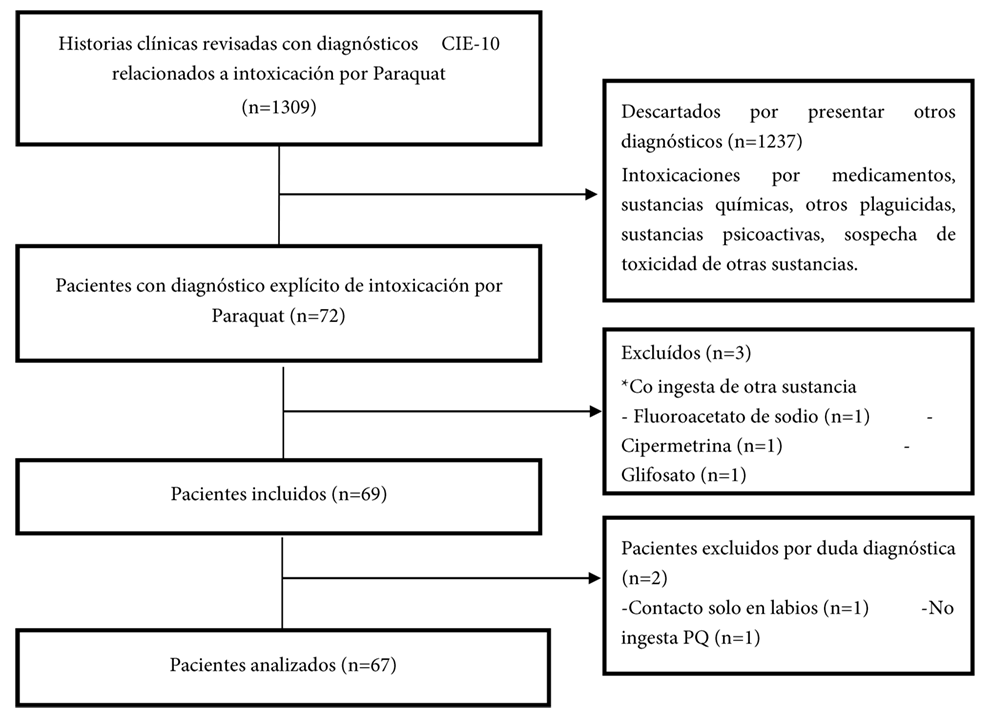
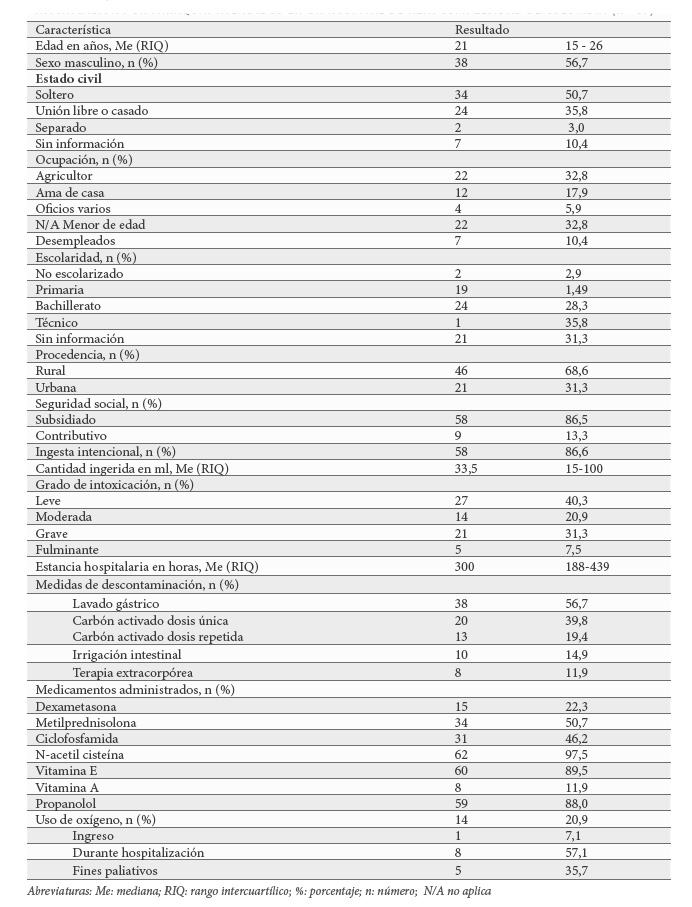
intoxicación por Paraquat atendidos en un hospital de alta complejidad de Colombia (n=67)
El 56,7% recibió lavado gástrico, 59% carbón activado y la terapia extracorpórea que se utilizó fue hemodiálisis.
El esquema de tratamiento fue variable e incluyó terapia inmunosupresora (dexametasona, metilprednisolona, ciclofosfamida), n-acetil cisteína, propanolol, vitamina A y E. En la mayoría de los casos la terapia inmunosupresora con metilprednisolona y ciclofosfamida se administró conjuntamente, y casi todos los pacientes recibieron tratamiento con n-acetil cisteína. Se encontró que 14 pacientes (20,9%) recibieron oxígeno, 8 (57,1%) durante la hospitalización, uno al ingreso y los demás en manejo paliativo; 12 de los 14 fallecieron.
El fallo renal agudo fue la complicación más frecuente y se presentó en 56,7% (63,3% en fallecidos y 36,8% en sobrevivientes). En segundo lugar, la lesión gastrointestinal 52,2% (45,7% en fallecidos vs 28,3% en sobrevivientes). La insuficiencia respiratoria se presentó en 24 pacientes (35,8%), todos fallecieron y 17,8% desarrollaron fibrosis pulmonar (81,8% fallecidos vs 18,2% en sobrevivientes). Se presentó insuficiencia hepática en el 29%, con 95% de mortalidad.
Análisis de supervivencia
Durante la estancia hospitalaria murieron 25 pacientes (Intoxicación fulminante 16% y grave 84%) lo que indica que la mortalidad intrahospitalaria fue de 37,3% (IC95% 36,9 a 37,7%), con una mediana de tiempo a la muerte de 117h (RIQ 62h-238h). La función de supervivencia se muestra en la Figura 2.
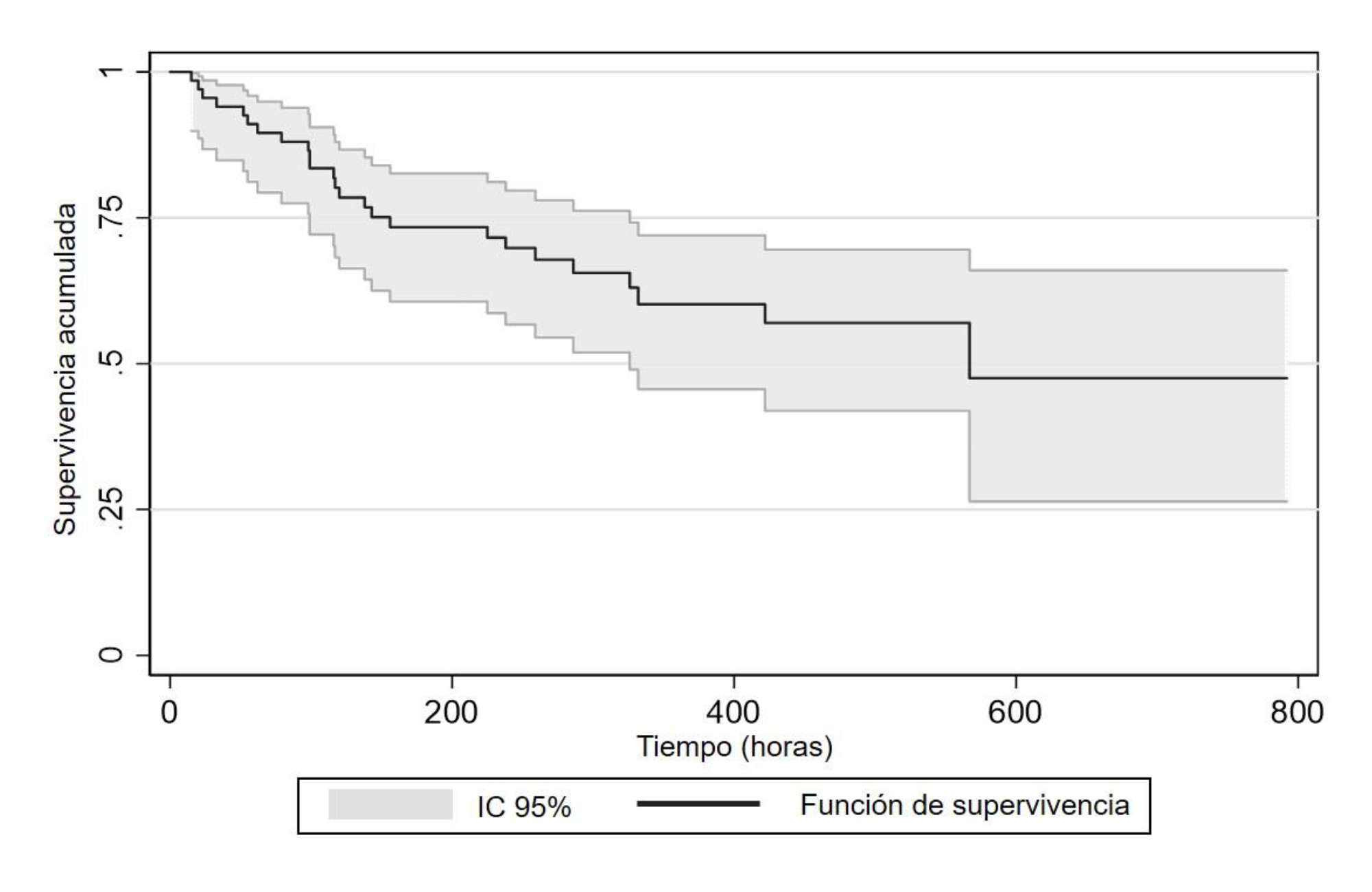
El sexo masculino presentó un mayor riesgo instantáneo de morir (HR=1,93; IC95% 1,44 a 10,26; p=0,007). El 55,3% de los hombres tuvo intoxicación grave o fulminante, mientras que el 53,84% de las mujeres tuvo una intoxicación leve. El riesgo de morir y la edad tuvieron una tendencia directamente proporcional (HR=1.04; IC95% 1,01 a 1,07; p=0,021). Así mismo, la dosis ingerida (HR=1,005; IC95% 1,003 a 1,009; p≤0,001) y el grado de intoxicación (HR=3,32; IC95% 2,17 a 5,08; p≤0,001) se relacionaron con el riesgo de morir.
En los pacientes con intoxicación grave los valores de electrolitos fueron variables al ingreso sin mostrar diferencia respecto a las intoxicaciones de menor gravedad; para el potasio el valor mínimo individual fue de 2,8 en las primeras 72 horas. Se observó que los valores de transaminasas fueron mayores en las intoxicaciones graves, al igual que los de bilirrubinas, creatinina y BUN; el nivel de pH fue menor, el de lactato y el tiempo de protrombina fueron casi iguales. (tabla 2)
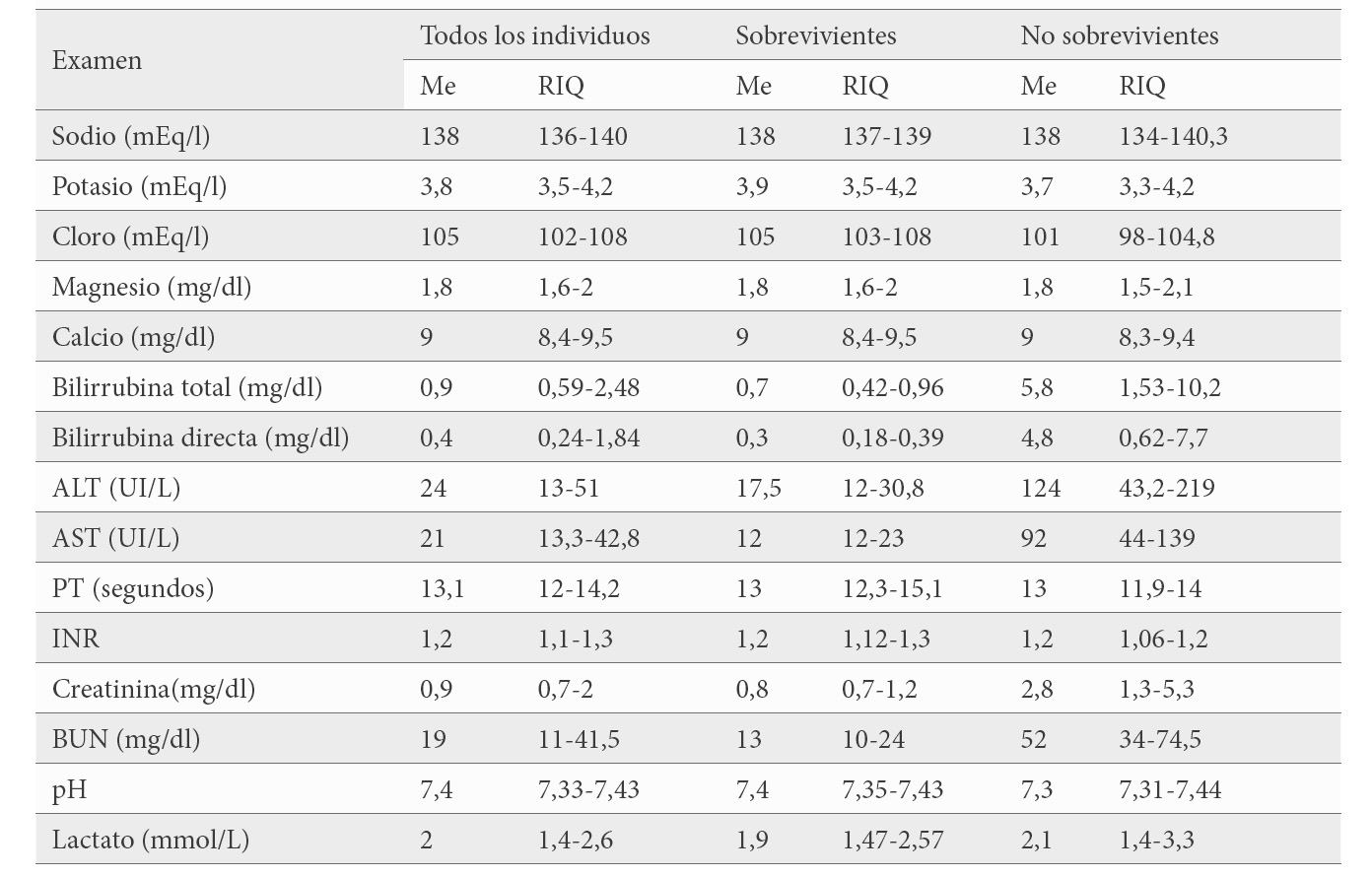
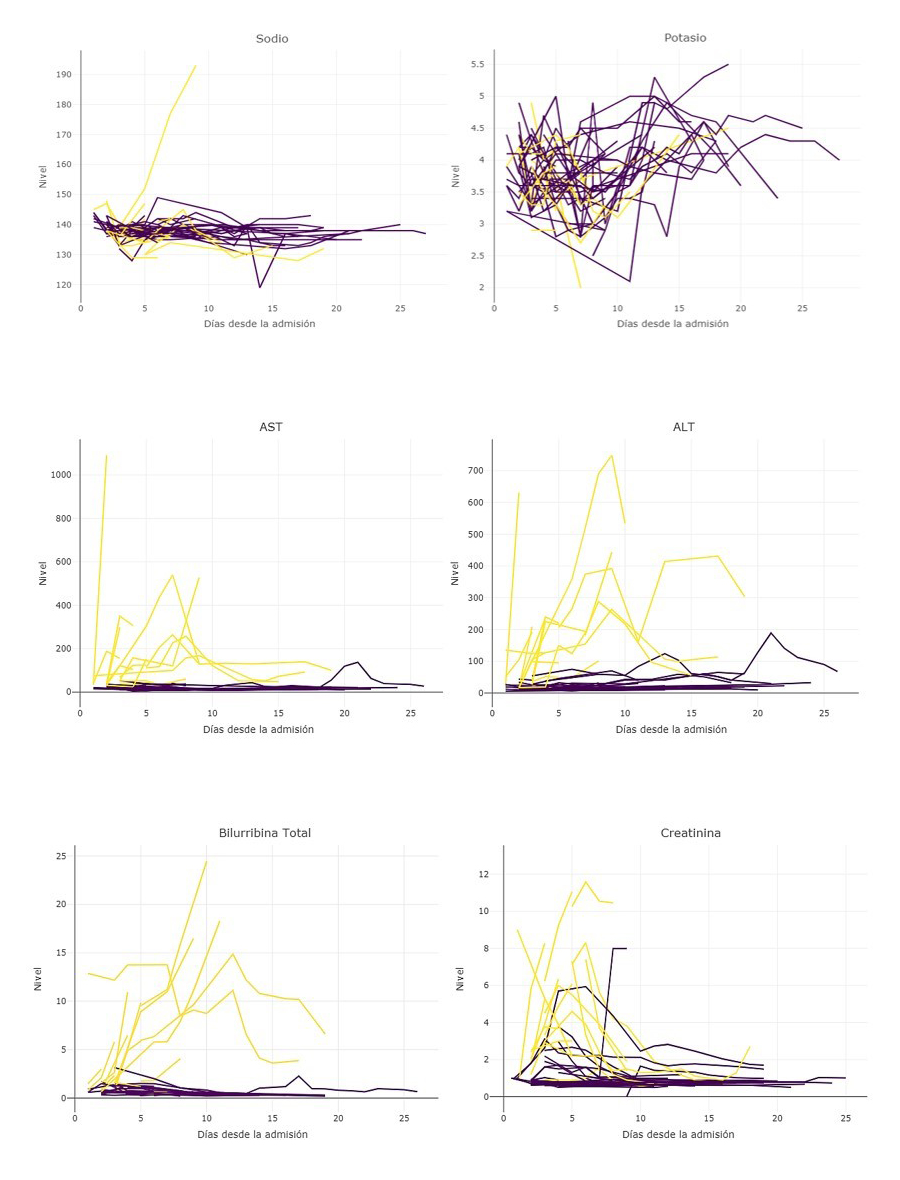
Al analizar el cambio de los valores en el tiempo se observó que en los casos graves después del tercer día se presentó insuficiencia renal y hepática, con un efecto estadísticamente significativo en el tiempo de la elevación de la creatinina (HR=1,53; IC95% 1,398-1,667), AST (HR=1,009; IC95%; 1,007-1,012), ALT (HR=1,008; IC 95% 1,006-1,01) y bilirrubina total (HR=1,23; IC95% 1,173-1,29) (Figura 3) Los valores de sodio, potasio, cloro, calcio y magnesio no mostraron una tendencia específica en el tiempo.
DISCUSIÓN
Este estudio evaluó las variables asociadas con la mortalidad en una cohorte de 67 pacientes con intoxicación por PQ atendidos en un hospital de referencia de Colombia durante 7 años. La mayoría de pacientes fueron hombres, en la tercera década de la vida, agricultores, con aseguramiento subsidiado de salud y procedentes del área rural, lo cual ya ha sido descrito en la literatura como un perfil de condiciones sociales que configuran un grupo vulnerable para intoxicaciones por PQ, principalmente provocadas (18,19).
Se encontró una mortalidad de 37,3%, lo cual está dentro del rango descrito en el mundo que oscila entre 36,7% y 73,6% (20,21), aunque disminuye a 6,5% en países con prohibición del uso de PQ (22). La cantidad ingerida de PQ es determinante en este riesgo pues encontramos un incremento del 0,5% por cada ml ingerido. En los pacientes en los que se obtuvo el dato, la mediana de la cantidad de PQ ingerida fue de 33,5cc (RIQ 15cc – 100cc), que corresponde a 97,5mg/kg para un paciente adulto de 70kg, considerando la presentación comercial de PQ al 20% disponible en Colombia. Esta cantidad sobrepasa la dosis tóxica (>20 mg/kg de PQ o concentraciones de PQ en suero > 0.2 μg / ml en 24 horas o niveles séricos mayores de 0.1 mg/ml en las primeras 48 horas) y que se asocia con resultados fatales (11,23).
El análisis de las concentraciones séricas conforma una de las aproximaciones más usuales en la práctica clínica para la estimación de la supervivencia. Algunas herramientas correlacionan las concentraciones de PQ y el tiempo desde la ingesta, entre ellas el nomograma de Proudfoot (24), el índice de Jones (25), y el Severity Index of Paraquat Poisoning -SIPP (26). En un análisis post hoc encontramos una correlación moderada entre la dosis ingerida y el grado de intoxicación (coeficiente de Spearman=0,46), de tal manera que la caracterización clínica del paciente podría tener valor pronóstico en caso de ser posible la medición de los niveles. A este respecto, es importante determinar la causa de la intoxicación pues en los casos autoprovocados la cantidad ingerida es mayor con aumento en la mortalidad (21,27).
De manera consistente en la literatura la mortalidad por PQ se atribuye a las complicaciones presentadas (21). Los pacientes no sobrevivientes de este estudio tuvieron mayores niveles de creatinina y BUN al ingreso, indicando insuficiencia renal, que fue la complicación más frecuente. La literatura describe como indicativo de toxicidad el desarrollo de insuficiencia renal durante las primeras etapas, debido a la peroxidación lipídica de la membrana celular en el túbulo proximal que evoluciona a necrosis tubular aguda, hipoperfusión y lesión glomerular directa (28). En una cohorte en Taiwán la mortalidad de los pacientes con falla respiratoria también fue el 100% (29), en estos pacientes el aumento de la FiO2 podría aumentar el estrés oxidativo y empeorar la lesión pulmonar aguda y la toxicidad sistémica por lo que la suplementación de oxígeno se reserva para tratamiento paliativo. Un hallazgo llamativo en nuestro estudio fue que se utilizó en un 11% de los casos durante la hospitalización sin esta indicación, lo que puede ser objeto de otro análisis para ahondar en el razonamiento clínico a la hora de prescribir la oxigenoterapia en estos pacientes.
En nuestro estudio todos los casos con insuficiencia respiratoria fallecieron y se asoció en 81,8% con fibrosis pulmonar. Esto se explica porque el pulmón concentra gran parte del tóxico, con lesión del epitelio alveolar favorecido por el trasporte de PQ en el sistema de poliaminas en la membrana de las células clara, células alveolares tipo I y II. Esto lleva a pérdida de tensoactivos pulmonares, disfunción de citocinas y generación de estrés oxidativo intracelular que altera el ciclo redox, produce alveolitis aguda que conduce a tejido fibrótico(8,30). La fibrosis pulmonar es irreversible (31). La muerte en una cohorte de Taiwán de los pacientes con fallo respiratorio, como en nuestro estudio fue el 100%, se evidencio que el aumento de FiO2 podría aumentar el estrés oxidativo y empeorar tanto la lesión pulmonar aguda como la toxicidad sistémica (29), dejando así su uso solo exclusivos para casos paliativos; aunque en nuestra cohorte utilizo para este fin, en un 11% fue usado durante la hospitalización, pero la indicación especifica no fue objeto de análisis.
No obstante, también fue frecuente el desarrollo de insuficiencia hepática en los fallecidos, lo cual no se ha descrito en muchos estudios. El hígado tiene potencial de generar ROS, haciéndolo susceptible de desarrollar lesión celular, se manifiesta con elevación de transaminasas y bilirrubinas (32), este hallazgo se asocio a menor supervivencia en 565 pacientes en Corea durante 1998 a 2001, por aumentos iniciales en la aspartato aminotransferasa 77,7±121,4 IU/L, alanina aminotransferasa 63,3±120 IU/L), BUN 22,6±26,6mg/dl y amilasa 512,2±794,9 IU/L dl (33). En el estudio de Hong et al (34) utilizando un análisis de regresión logística múltiple de 147 pacientes se encontró un aumento significativo de la mortalidad con la alteración de transaminasas y bilirrubinas (OR=8,07; IC95% 2,04-27,18; p=0.001), y función renal (OR=9,96; IC95% 3,23-30,74; p=<0.001).
En la cohorte estudiada, la variación en el tiempo de las transaminasas, la bilirrubina total y la creatinina tuvieron significancia estadística como factores pronósticos para mortalidad. Los estudios previos han considerado los valores iniciales como factores pronósticos (35), pero es necesario tener en cuenta que durante al abordaje clínico se instauran conductas médicas que determinan un cambio, al igual que la evolución en la fisiopatología de la toxicidad, por lo cual la estimación del pronóstico solo con valores iniciales de laboratorio pudiera resultar insuficiente. Esto abriría la posibilidad de crear modelos pronósticos dinámicos que incluyan variables y su evolución durante la estancia hospitalaria para una predicción más exacta.
Alteraciones en otros paraclínicos como lactato, pH, leucocitos y amilasas, también podrían tener un valor pronóstico (18), aunque los hallazgos de los estudios pueden ser controvertidos debido a problemas como la selección de los pacientes, tamaño de muestra pequeños y diferencias en la gravedad de la intoxicación(36). En nuestro estudio no detectamos significancia desde el punto de vista estadístico de otros parámetros de laboratorio, sin embargo dada la descripción de la hipokalemia (<3.5mmol/L) al ingreso como un factor de riesgo para morir (OR=2,07; IC95% 1,21-3,51; p=<0.001) (37), se debe estar atento a su medición.
Dentro de las limitaciones de este estudio se encuentran que, al ser un estudio observacional retrospectivo, se pudo presentar un sesgo de medición pues no se siguió un protocolo específico para la realización de exámenes. También, se presentaron datos perdidos por tratarse de la revisión de historias clínicas, aunque, por fortuna, los resultados de laboratorio fueron sistematizados y fue posible garantizar la calidad del dato y la hora de toma de la muestra. Así mismo, no se midieron otros factores descritos por la literatura como los niveles de PQ en plasma por la falta de disponibilidad de la técnica.
CONCLUSIONES
La dosis ingerida, el carácter intencional de la ingesta, el sexo masculino y la edad son factores asociados con la mortalidad en los pacientes con intoxicación por PQ. Además, las concentraciones de creatinina, AST, ALT y bilirrubina total mostraron un cambio durante el tiempo de estancia hospitalaria que se relacionó con la muerte, por lo cual su evaluación, dado el carácter variable de la toxicidad del PQ y en consecuencia su tratamiento, sería útil para estudios futuros sobre modelos pronósticos dinámicos y optimizar la predicción de la mortalidad en estos pacientes.
BIBLIOGRAFÍA
- Tsai W-T. A review on environmental exposure and health risks of herbicide paraquat. Toxicol Environ Chem [Internet]. 2013; 95(2): 197-206. Available from: http://www.tandfonline.com/doi/abs/10.1080/02772248.2012.761999
- Suárez Medina O, Narváez Rincón P. Perfil Nacional de Sustancias Químicas en Colombia. Vol II: actualización de los capítulos 2 y 3, con énfasis en sustancias de uso industrial. 2017.
- Mew EJ, Padmanathan P, Konradsen F, et al. The global burden of fatal self-poisoning with pesticides 2006-15: systematic review. J Affect Disord [Internet]. 2017;219: 93-104. Available from: http://dx.doi.org/10.1016/j.jad.2017.05.002
- Nagami H, Maejima F, Nishigaki Y, Natsukawa S. Trends in paraquat poisoning in Japan – viewed from surveys on clinical cases. J Rural Med JRM [Internet]. 2013; 8(2): 228-232. Available from: http://www.ncbi.nlm.nih.gov/pubmed/25648748
- Intoxicaciones. Periodo epidemiológico XIII. Colombia, 2019 [Internet]. 2019. Available from: https://www.ins.gov.co/buscador-eventos/Informesdeevento/INTOXICACIONES PE XIII 2019.pdf
- Línea Nacional de Toxicología. Ministerio de Salud y Protección Social. Consejo Colombiano de Seguridad. CISPROQUIM. Estadísticas de pacientes atendidos por la línea nacional de toxicología. 2015.
- Buendía JA, Chavarriaga GJR, Zuluaga AF. Burden of paraquat poisoning in the department of Antioquia, Colombia. BMC Pharmacol Toxicol. 2019; 20(1): 1-7.
- Dinis-Oliveira RJ, Duarte JA, Sánchez-Navarro A, Remião F, Bastos ML, Carvalho F. Paraquat poisonings: mechanisms of lung toxicity, clinical features, and treatment. Crit Rev Toxicol. 2008; 38(1): 13-71.
- Mainwaring G, Lim FL, Antrobus K, et al. Identification of early molecular pathways affected by paraquat in rat lung. Toxicology. 2006; 225(2-3): 157–172.
- Gawarammana I, Buckley NA, Mohamed F, et al. High-dose immunosuppression to prevent death after paraquat self-poisoning–a randomised controlled trial. Clin Toxicol. 2018; 56(7): 633-639.
- Cao ZX, Zhao Y, Gao J, Feng SY, Wu CP, Zhai YZ, et al. Comparison of severity index and plasma paraquat concentration for predicting survival after paraquat poisoning: a meta-analysis. Med (Baltimore). 2020; 99(6): e19063.
- Iyyadurai R, Mohan J, Jose A, Das S, Johnson J, Gunasekaran K. Paraquat poisoning management. Curr Med Issues. 2019; 17(2): 34-37.
- Mohamed F, Endre Z, Jayamanne S, et al. Mechanisms underlying early rapid increases in creatinine in paraquat poisoning. PLoS One. 2015; 10(3): 1-16.
- Eddleston M, Wilks MF, Buckley NA. Prospects for treatment of paraquat-induced lung fibrosis with immunosuppressive drugs and the need for better prediction of outcome: a systematic review. QJM – Mon J Assoc Physicians. 2003; 96(11): 809-824.
- Wolkewitz M, Allignol A, Harbarth S, De Angelis G, Schumacher M, Beyersmann J. Time-dependent study entries and exposures in cohort studies can easily be sources of different and avoidable types of bias. J Clin Epidemiol [Internet]. 2012; 65(11): 1171-1180. Available from: http://dx.doi.org/10.1016/j.jclinepi.2012.04.008
- Feng MX, Li YN, Ruan WS, Lu YQ. Predictive value of the maximum serum creatinine value and growth rate in acute paraquat poisoning patients. Sci Rep [Internet]. 2018; 8(1):1-7. Available from: http://dx.doi.org/10.1038/s41598-018-29800-0
- Hemingway H, Croft P, Perel P, et al. Prognosis research strategy (PROGRESS) 1: a framework for researching clinical outcomes. BMJ. 2013; 346: e5595.
- Wang WJ, Zhang LW, Feng SY, Gao J, Li Y. Sequential organ failure assessment in predicting mortality after paraquat poisoning: a meta-analysis. Sun Q, editor. PLoS One. 2018; 13(11): e0207725.
- Buendía JA, Restrepo Chavarriaga GJ, Zuluaga AF. Social and economic variables related with Paraquat self-poisoning: an ecological study. BMC Public Health [Internet]. 2020; 20(1): 404. Available from: http://www.ncbi.nlm.nih.gov/pubmed/32220225
- Oghabian Z, Williams J, Mohajeri M, et al. Clinical features, treatment, prognosis, and mortality in paraquat poisonings: a hospital-based study in Iran. J Res Pharm Pract [Internet]. 2019; 8(3): 129-136. Available from: http://www.jrpp.net/text.asp?2019/8/3/129/269278
- Goudarzi F, Armandeh J, Jamali K, Rahmati H, Meisami A AH. Mortality analysis of patients with Paraquat poisoning treated at two university hospitals in Shiraz, Iran. Asia Pacific J Med Toxicol [Internet]. 2014; 3: 141-145. Available from: http://apjmt.mums.ac.ir
- Kim J, Shin S Do, Jeong S, Suh GJ, Kwak YH. Effect of prohibiting the use of Paraquat on pesticide-associated mortality. BMC Public Health. 2017; 17(1): 1-11.
- Senarathna L, Eddleston M, Wilks MF, et al. Prediction of outcome after Paraquat poisoning by measurement of the plasma Paraquat concentration. Qjm. 2009; 102(4): 251-259.
- Proudfoot AT, Stewart MS, Levitt T, Widdop B. Paraquat poisoning: significance of plasma-Paraquat concentrations. Lancet [Internet]. 1979; 314(8138): 330-332. Available from: https://linkinghub.elsevier.com/retrieve/pii/S0140673679903453
- Jones AL, Elton R, Flanagan R. Multiple logistic regression analysis of plasma Paraquat concentrations as a predictor of outcome in 375 cases of Paraquat poisoning. QJM [Internet]. 1999; 92(10): 573-578. Available from: http://www.ncbi.nlm.nih.gov/pubmed/10627878
- Sawada Y, Yamamoto I, Hirokane T, Nagai Y, Satoh Y, Ueyama M. Severity index of Paraquat poisoning. Lancet [Internet]. 1988; 1(8598):1333. Available from: http://www.ncbi.nlm.nih.gov/pubmed/2897577
- Zhang Y, Yu B, Wang N, Li T. Acute poisoning in Shenyang, China: a retrospective and descriptive study from 2012 to 2016. BMJ Open. 2018; 8(8): 1-11.
- Weng CH, Chen HH, Hu CC, et al. Predictors of acute kidney injury after Paraquat intoxication. Oncotarget. 2017; 8(31): 51345-51354.
- Wang WJ, Zhang LW, Feng SY, Gao J, Li Y. Sequential organ failure assessment in predicting mortality after Paraquat poisoning: a meta-analysis. Sun Q, editor. PLoS One [Internet]. 2018; 13(11): e0207725. Available from: http://dx.plos.org/10.1371/journal.pone.0207725
- Sun B, Chen YG. Advances in the mechanism of Paraquat-induced pulmonary injury. Eur Rev Med Pharmacol Sci. 2016; 20(8): 1597-1602.
- Villanueva Cañadas E y Hernández Jerez A. Intoxicación por plaguicidas. En: Villanueva Cañadas Enrique, ed. Gisbert Calabuig Medicina legal y toxicológica. 7ª ed. Barcelona : Elsevier; 2018. p. 1011-1020.
- Yang CJ, Lin JL, Lin-Tan DT, et al. Spectrum of toxic hepatitis following intentional Paraquat ingestion: Analysis of 187 cases. Liver Int. 2012; 32(9): 1400-1406.
- Lee EY, Hwang KY, Yang JO, Hong SY. Predictors of survival after acute Paraquat poisoning. Toxicol Ind Health. 2002; 18(4): 201-206.
- Hong SY, Yang DH, Hwang KY. Associations between laboratory parameters and outcome of Paraquat poisoning. Toxicol Lett. 2000; 118(1-2): 53-59.
- Lee JH, Hwang SY, Kim HR, et al. Effectiveness of the sequential organ failure assessment, acute physiology and chronic health evaluation II, and simplified acute physiology score II prognostic scoring systems in Paraquat-poisoned patients in the intensive care unit. Hum Exp Toxicol. 2017; 36(5): 431-437.
- Chen H, Hu L, Li H, et al. An effective machine learning approach for prognosis of Paraquat poisoning patients using blood routine indexes. Basic Clin Pharmacol Toxicol. 2017; 120(1): 86-96.
- Chang MW, Chang SS, Chien-Chang LEE, Sheu BF, Young YR. Hypokalemia and hypothermia are associated with 30-day mortality in patients with acute Paraquat poisoning. Am J Med Sci. 2008; 335(6): 451-456.
DECLARACIÓN DE TRANSPARENCIA
Los autores/as de este artículo declaran no tener ningún tipo de conflicto de intereses respecto a lo expuesto en el presente trabajo.
Chinchilla-Escobar E. C.
Departamento de Farmacología y Toxicología Clínica.
Facultad de Medicina. Universidad de Antioquia. Medellín, Colombia
Email: ecarolina.chinchilla@udea.edu.co
Año 2021 · número 138 (01) · páginas 72 a 81
Enviado: 16.03.21
Revisado: 21.03.21
Aceptado: 14.04.21


