Resumen
La leucemia linfoblástica aguda continúa siendo la neoplasia más frecuente en la infancia, con una tasa de supervivencia alcanzada a 5 años que varía en un 78 y 91%. El aumento de la tasa de supervivencia en los últimos 40 años ha sido de un 30 a un 80%, no alcanzando mejoras comparables en casos de LLA refractarias o en recaída. Es por esto último, por lo que actualmente existen investigaciones en tratamientos innovadores, como es la terapia con células CAR-T. Este tratamiento implica la modificación genética ex vivo de las células T del propio paciente potenciando su especificidad y citotoxicidad frente a antígenos presentes en los blastos de forma mayoritaria, como es el CD19. En los ensayos clínicos realizados a nivel mundial se han obtenido resultados positivos en pacientes con LLA refractaria o en recaída tratados con terapia CAR-T 19, objetivando una supervivencia a un año libre enfermedad del 50%, y global del 76%. La primera publicación en España respecto a la experiencia con este tratamiento reproduce los resultados obtenidos en los ensayos clínicos. Se exponen los resultados obtenidos en el HNJS en el año 2020 en 8 pacientes tratados con CAR-T 19, objetivando remisión completa en el 87.5% al mes desde la infusión y una supervivencia global en el momento del análisis del 75% (media de duración de seguimiento 7.6 meses). Hasta hoy los efectos secundarios más frecuentes descritos con el uso de esta terapia a corto plazo son el síndrome de liberación de citoquinas y la neurotoxicidad. Esta innovadora terapia supone un cambio en el paradigma de la supervivencia de los pacientes pediátricos con LLA refractaria o en recaída. Aun se precisan estudios y evidencia de su efectividad, y el seguimiento de los pacientes tratados con esta terapia a largo plazo, siendo los resultados hasta hoy, alentadores.
Abstract
Acute lymphoblastic leukemia (ALL) continues to be the most frequent neoplasm in childhood, with a 5-year survival rate ranging from 78 to 91%. The increase in the survival rate in the last 40 years has been 30 to 80%, with no comparable improvement in the case of relapsed or refractory ALL. It is for this very reason that there is currently research into innovative treatments, such as CAR-T cell therapy. This treatment involves the ex vivo genetic modification of the patient’s own T cells, enhancing their specificity and cytotoxicity against antigens present in the majority of blasts, such as CD19. In clinical trials carried out worldwide, positive results have been obtained in patients with refractory or relapsed ALL treated with CAR-T 19 therapy, with disease-free survival at one year in up to 50% of patients, and overall survival at one year of 76%. The first published report in Spain with respect to this treatment reproduces the results obtained in clinical trials. The results were reported in HNJS in 2020 involving 8 patients treated with CAR-T 19. Complete remission was observed in 87.5% of patients one month after infusion followed by an overall survival of 75% at the time of analysis (7.6 months mean follow-up duration across all the patients). To date, the most frequent side effects described with the use of this therapy in the short term are cytokine release syndrome and neurotoxicity. This innovative therapy, therefore, represents a paradigm shift in the survival of pediatric patients with relapsed or refractory ALL. Further studies and evidence of its effectiveness and the long-term follow-up of patients treated with this therapy are still needed, but the results to date are encouraging.
Palabras clave: Leucemia aguda Linfoblástica; tisagenlecleucel; Terapia CAR-T 19.
Keywords: Acute lymphoblastic Leukemia; tisagenlecleucel; CAR-T 19 therapy.
Introducción
La leucemia linfoblástica aguda (LLA) supone el 75-80% de las leucemias agudas en la edad pediátrica y es la neoplasia más frecuente en la infancia (1). El tratamiento de la LLA es dirigido y específico para los diferentes grados de riesgo. De forma general consiste en ciclos de quimioterapia que difieren en intensidad y duración, incluidos en tres fases de tratamiento -inducción, consolidación y mantenimiento-.
Las tasas de supervivencia alcanzadas a 5 años en la LLA varían entre un 75 y 90% (2). Entre un 10 y 15% presentarán una recaída postratamiento quimioterápico de primera línea (2). Los factores de riesgo para presentar una recaída son: presentar al diagnóstico una cifra alta de leucocitos, una edad menor de 1 año o mayor de 10, alteraciones citogenéticas y moleculares o una falta de respuesta al tratamiento medido por la Enfermedad Mínima Residual (EMR).
Actualmente, el tratamiento tras una primera recaída se basa en quimioterapia intensiva seguida de trasplante alogénico de progenitores hematopoyéticos (alo-TPH), alcanzado en estos casos remisiones en el 70-90%. La supervivencia global (SG) tras el TPH en primera recaída es de alrededor de un 40% a los 5 años. Se estima que alrededor del 30% de estos pacientes sufrirá una segunda recaída, siendo la supervivencia inferior al 30% tras un segundo trasplante (2).
TRATAMIENTOS BASADOS EN INMUNOTERAPIA EN LA LLA EN LA ACTUALIDAD
En las últimas décadas la inmunoterapia ha cambiado el paradigma del tratamiento de pacientes con escasas expectativas terapéuticas por fracaso del tratamiento previo o por no considerarse apto para el tratamiento convencional de recaída.
La inmunoterapia surge como consecuencia de ser las células T del sistema inmune las responsables del ataque inmunológico frente a células extrañas. Para que esto ocurra, la célula diana debe presentar, por un lado, el complejo mayor de histocompatibilidad (MHC) que contiene el fragmento proteico o antígeno para su reconocimiento, y, por otro lado, el ligando que actúe como coestimulador para la activación del linfocito T.
Así, las células tumorales pueden escapar de la citotoxicidad de los linfocitos T, bien, dejando de expresar el MHC o bien expresando coestimuladores aberrantes (2,3).
Por otro lado, los avances en el estudio de inmunofenotipo de las células tumorales han permitido la detección de posibles antígenos diana para el desarrollo de la inmunoterapia. La selección del antígeno diana se realiza buscando en las células tumorales aquel más específico, siendo en la LAL de células B el CD19 (2,3,4).
En los últimos años se han desarrollado estrategias de inmunoterapia celular con las que se pretende, a través de la manipulación genética, optimizar la función del sistema inmune propio contra el cáncer. Específicamente hablamos de la inmunoterapia celular adoptiva con células T anti-receptor de antígeno quimérico (CAR-T). Además, se pretende aumentar la especificidad de unión con un antígeno de superficie seleccionado en función de la célula tumoral diana (5). Y, por otro lado, capacitar al linfocito T para activarse, proliferar y ejercer su citotoxicidad sin requerir la intermediación del MHC y el ligando coestimulador (3,6).
En su lugar se ha creado a través de ingeniería genética una molécula sintética, denominada receptor quimérico de antígeno (chimeric antigen receptor, CAR), diseñada para reconocer un antígeno de superficie previamente expresado por las células tumorales, y de producir una auto activación del linfocito T. El gen que codifica el CAR se introduce en el genoma del linfocito T in vitro a través de un vector lentiviral. De esta forma, al producirse su activación y transducción se expresa el CAR en el linfocito T (2,5,7).
Los CAR de primera generación constaban de tres dominios, un dominio de reconocimiento extracelular de cadena sencilla que se une al antígeno, un dominio de unión transmembrana y otro dominio de señalización intracelular CD3-ζ. Desde 2006 se han realizado ensayos clínicos con las células CAR-T como terapia contra el cáncer obteniendo en un principio baja efectividad, debida a una escasa citotoxicidad y proliferación de las células T modificadas del paciente (8,9).
Desde entonces se ha evolucionado creando las células CAR de segunda generación en las que se añade un segundo dominio intracelular de coestimulación que incluye un dominio de las moléculas CD28 o CD137 (4-1BB) (8). Se demostró entonces que la utilización de células CAR CD3/4-1BB era determinante para una supervivencia más duradera in vivo, con citotoxicidad y proliferación suficientes como para conseguir resultados satisfactorios en primera instancia en pacientes con leucemia linfática crónica en adultos (3).
En los últimos años se han desarrollado un CAR de tercera generación en la que se incluyen dos moléculas en tándem en el dominio intracelular coestimulante, utilizando además del CD28 y CD137 (4-1BB), el CD27 y OX40.
El siguiente paso en la evolución de los CAR ha sido la creación de receptores duales con doble especificidad antigénica (3).
El proceso de la terapia de células T CAR (CAR-T) en la práctica clínica implica en primer lugar, la extracción mediante leucoaféresis de células T extraídas del propio paciente (autólogo), o en algunas ocasiones de otro sujeto (alogénico), en segundo lugar la manipulación genética ex vivo descrita y, en tercer y último lugar, la infusión de nuevo al paciente de las células T modificadas (2,5). Previa a la infusión se realiza terapia de linfodepleción basada en quimioterapia (10).
En la actualidad y con el objetivo de tratar las formas refractarias de la LLA precursora de células B y del Linfoma No Hodgkin (LNH) de células grandes, el antígeno utilizado de forma mayoritaria es el CD19 presente en las células B de forma exclusiva (2,3).
EVIDENCIA DEL USO DE TERAPIA CAR-T 19 HASTA HOY EN LLA REFRACTARIA O EN RECAÍDA
La FDA (Administración de Alimentos y Medicamentos de los Estados Unidos) aprobó en 2017 la utilización de CAR-T 19 para casos de LLA de células B refractaria o en recaída en adultos y niños, siendo la primera terapia de modificación genética celular aprobada por esta entidad (4,6,11).
El tisagenlecleucel es el primer fármaco comercializado, a nivel mundial, de carácter autólogo y con CAR-T de tercera generación (12). En los últimos años esta terapia se ha utilizado de forma global como tratamiento de rescate en la LLA refractaria a tratamiento quimioterápico inicial detectada de forma precoz por la EMR, en recaídas postratamiento quimioterápico o post -alo-TPH en LLA de alto riesgo, y en pacientes que requieren alo-TPH según el protocolo pero que no son candidatos al mismo (2).
Desde el inicio de su utilización se han publicado casos con resultados alentadores con tasas de remisión completa del 93% y de supervivencia global a un año de alrededor del 76% con el uso de CAR-T en recaídas post-alo-TPH (2,13).
En 2013 se publicaron los primeros resultados con el uso de terapia con CAR-T 19 (9). Posteriormente a nivel mundial se han realizado ensayos clínicos controlados y revisiones sistemáticas que mantienen unos resultados positivos en términos de remisión y supervivencia.
En 2018 Maude y cols publicaron los resultados de un ensayo clínico en fase II multicéntrico con la participación de 11 países denominado ELIANA. En él se incluyeron 75 niños con LLA en recaída a los que se administró tratamiento con tisagenlecleucel. Se obtuvo remisión en el 81% de pacientes, una supervivencia libre de enfermedad del 73% a 6 meses, y del 50% a 12 meses, siendo la supervivencia global del 90% a 6 meses, y del 76% a 12 meses (14).
En este estudio se describe también una persistencia de las células CAR-T en médula ósea y sangre periférica hasta los 20 meses postinfusión, siendo esta una duración similar a la descrita en otros estudios (4,12,14).
En 2020 se publicaron los datos de los resultados obtenidos con el uso de tisagenlecleucel en EEUU y Canadá en la “vida real” en 255 pacientes con LLA refractaria entre 2017 y 2020 con una duración de seguimiento de 13.4 meses. Estos datos provienen del CIBMTR (Center for International Blood and Marrow Transplant Research). Los resultados muestran una remisión en el 85.5% de los pacientes, con una supervivencia libre de enfermedad a los 12 meses del 52.4%. En este estudio se reproducen los datos sobre la eficacia del tisagenlecleucel obtenidos en los ensayos clínicos (5).
Se ha realizado un primer metaanálisis sobre el uso de terapia con CAR-T en LLA refractaria o en recaída tanto en población adulta como en población pediátrica. Se incluyeron 35 estudios publicados entre 2012 y 2018 en el que se describen altas tasas de respuesta de forma global (11).
En los artículos referentes a la población pediátrica, (un total de 11), se analizaron 346 pacientes, obteniendo remisión en el 81% de ellos. Se evidencio una menor tasa de remisión estudiada por detección de la EMR, en los pacientes que utilizaron un CAR-T 19 alogénico así como en los pacientes de mayor edad, con respecto a la utilización de CAR-T 19 autólogo y a la población infantil, respectivamente. La supervivencia libre de enfermedad al año desde la infusión es de alrededor del 35% similar en ambas poblaciones estudiadas (11).
En España la AEMPS (Agencia Española de Medicamentos y Productos Sanitarios) ha aprobado el uso de CAR-T 19 para la LLA en 2021, siendo el tisagenlecleucel y axicabtagene y ciloleucel, los fármacos disponibles en el momento actual (15).
En nuestro país la terapia con CAR-T 19 está indicada en pacientes pediátricos y adultos jóvenes de hasta 25 años con LLA de células B que han sufrido al menos una recaída tras un TPH o una segunda o tercera recaída con otras terapias.
Recientemente Urbano ha publicado los resultados obtenidos en una serie de 40 pacientes tratados con CAR-T 19 en el hospital Clinic de Barcelona. Se obtuvo una SLE al año del 50% de los pacientes (5). En este artículo se citan datos sobre estudios que objetivan supervivencia libre de enfermedad a dos años entre el 35 y 50%.
Aun con todos los resultados exitosos obtenidos hasta hoy con CAR-T 19, se precisan ensayos clínicos con distintos brazos de tratamiento para valorar su beneficio frente al tratamiento de rescate con un segundo trasplante u otras terapias utilizadas actualmente en la LLA refractaria o en recaída (2).
En 2020 se publicó el primero en el que se analizan datos comparativos sobre las tasas de remisión y supervivencia en la LLA refractaria y en recaída alcanzadas con la terapia CAR-T 19 y los tratamientos utilizados hasta la actualidad: blinatumumab, clofarabina en monoterapia o en régimenes de poliquimioterapia intensiva que incluyen clofarabina-ciclofosfamida-etopósido, seguida de alo-TPH o tratamiento paliativo. Utilizan la comparación indirecta ajustada (Matching-Adjusted Indirect Comparison, MAIC) diseñada para hacer comparables las poblaciones de los distintos estudios.
La conclusión del estudio es que el tratamiento con CAR-T 19 supone una mayor probabilidad de alcanzar remisión completa y el doble de posibilidades de supervivencia global a un año (16).
Recaídas tras tratamiento con CAR-T 19
Se han descrito tasas de recaída postCAR-T 19 entre el 30 y 60% de los pacientes (5). En estos casos se han observado dos escenarios atendiendo al inmunofenotipo de las células blásticas. En el primer escenario, se observaron recaídas con células blásticas con inmunofenotipo CD19 positivas, lo que sugiere la pérdida precoz de los linfocitos CAR-T antiCD19 (3,5). En un segundo escenario, se objetivaron recaídas con células blásticas con inmunofenotipo CD22 positivo predominantes, y baja o nula expresión de CD19, lo que sugiere la selección de dichas células tras terapia con CAR-T 19. Este último es el escenario más frecuente en las recaídas (17).
En el ensayo clínico publicado por Maude y cols mencionado con anterioridad, se evidencio que las recaídas postCAR-T 19 eran CD 19 negativas en el 76% (14).
Se han descrito distintos mecanismos a través de los cuales esto puede ocurrir, como es el splicing alternativo, la aparición de nuevas mutaciones o la reprogramación celular (3). Esta situación determinó que comenzaran a estudiarse nuevos antígenos diana, como el CD20, CD38, BCMA, obteniéndose remisiones inferiores al 50%.
El primero que ofreció tasas de proliferación, expansión y permanencia similares a la terapia CAR-T 19, fue el tratamiento con células CAR-T antiCD22 con evidencia en ensayos clínicos preliminares la obtención de tasas de remisión equiparables (18). Aun así, se objetivaron recaídas tras terapia CAR-T 22, con fenotipos de baja expresión de CD19 y CD22, lo que apoya la teoría de la selección por presión inmune como mecanismo de escape. Esta última situación promueve la preocupación de recaídas sin tratamiento dirigido posible y, por tanto, la necesidad de encontrar nuevos antígenos diana (2,5,17).
Una de las propuestas que existen en este momento para obviar los mecanismos de escape es el desarrollo de un CAR-T multiantígeno, que disminuya la posibilidad de que las células blásticas sigan limitando el tratamiento, dirigido exclusivamente a expresar antígenos diana susceptibles.
Otra posibilidad terapéutica como consecuencia de la alta tasa de remisión completa inicial con terapia CAR-T 22, pero con posterior recaída, es su utilización como terapia puente a un TPH de rescate en pacientes en segunda o tercera recaída y que previamente han recibido otro tipo de inmunoterapia dirigida (anticuerpos monoclonales, CAR-T 19) (19). Existen ensayos clínicos donde se objetiva una supervivencia libre de enfermedad significativamente más larga en pacientes con alo-TPH de consolidación tras terapia con CART-19 (6,20).
En estudios muy recientes se han detectado en el suero de pacientes no respondedores a terapia con CAR-T 19, un mayor número de linfocitos T CD4 y CD8 con expresión de receptores inhibidores. Por tanto, se está valorando la utilización de inhibidores de ¨check point¨ (ej. anticuerpos anti-PDL1) tras la terapia con CAR-T 19 (3).
Efectos secundarios observados tras tratamiento con CAR-T 19
Con esta terapia, se describen principalmente dos tipos de efectos secundarios de aparición precoz tras la infusión, el denominado síndrome de liberación de citoquinas (SLC), así como los derivados de la neurotoxicidad. Ambos síndromes aparecen de forma menos grave y frecuente en el caso de terapia con CAR-T 22 (18,19). En España en 2019 el CISNS (Consejo Interterritorial del Sistema Nacional de Salud) aprobó el protocolo de actuación y tratamiento frente a los efectos secundarios manifestados a corto plazo en pacientes que reciben CAR-T 19 (15).
El SCL se observa hasta en el 82% de los pacientes que reciben terapia con CAR-T 19 (11,21), aunque se describen tasas menores, del 55% en algunas series (7). Existe un consenso de gradación de la gravedad diseñado por la ASBMT (American Society for Blood and Marrow Transplantation), alcanzando grados altos en el 16-26% de casos (7,14,21). Suele presentarse en los primeros 10 días postinfusión -mediana de inicio 3 días- con una duración de hasta 10 días -mediana de duración de 8 días- (14). Se manifiesta como taquicardia, escalofríos, fiebre alta, mialgia, artralgias, náuseas, vómitos, diarrea, prurito, anorexia, fatiga, cefalea, hipotensión, disnea, taquipnea e hipoxia. En la mayoría de los casos se precisa hospitalización en planta, y una minoría de ellos ingreso en la unidad de cuidados intensivos pediátricos (UCIP) (2,14,15). El tratamiento del SLC es de soporte, incluyendo ventilación mecánica y vasopresores, hasta en el 9.3% y 22.1% respectivamente, en algunas series (7). Como terapia antiinflamatoria se han utilizado los corticoides de forma general y el tocilizumab de forma dirigida, al encontrarse en el suero de los pacientes niveles elevados de IL6. En la mayoría de los estudios publicados que describen la utilización de tocilizumab no se observan interacciones con la expansión y permanencia de las células T anti-CD19 (7,12,14). Existen ensayos clínicos en los que se propone el uso preventivo de agentes como el tocilizumab (8).
El síndrome de neurotoxicidad se ha observado en el 29% de los pacientes que reciben terapia con CAR-T 19, siendo grave en el 12% (11). Suele aparecer en conjunto con el SLC o de forma inmediata tras su resolución, existiendo una correlación entre ambos. EL aumento de citoquinas aumenta la permeabilidad de la barrera hematoencefálica, con el consecuente paso de proteínas y células observadas en el líquido cefalorraquídeo de los pacientes (22). A través de resonancia magnética se han podido ver cambios a nivel cerebral entre los días 6 y 15 postinfusión, aún sin poder determinar la causalidad por la multitud de factores a los que atribuir los cambios, como es el uso de quimioterapia previa a la terapia con CAR-T 19, el metrotexate intratecal, entre otros (22). Un estudio reciente mediante secuenciación del transcriptoma de células individuales ha encontrado que el CD19, considerado principalmente como un antígeno de superficie específico de la célula B, se expresa en las células murales del cerebro humano que son críticas para la integridad de la barrera hematoencefálica, lo que sugiere que esta población celular puede contribuir a la neurotoxicidad vista con el uso de CAR-T (23). Los síntomas incluyen encefalopatía, delirio, somnolencia o confusión. El tratamiento, al igual que el SCL, es de soporte observando una buena evolución en las siguientes semanas a la infusión. En el registro prospectivo del CIBMTR se recogieron casos de convulsiones hasta en el 18.8% de los pacientes (7). Se ha planteado el uso de levetiracetam durante 30-60 días postinfusión como prevención (2).
Como efectos secundarios a largo plazo se prevé, por el propio mecanismo de acción del tratamiento, la aplasia de células B. Se ha detectado en algunas series en el 83% de pacientes hasta al menos 6 meses postinfusión, tratándose de forma exitosa con inmunoglobulinas (14). Por otro lado, se ha descrito el potencial riesgo oncogénico de las células T autólogas transducidas con vector lentiviral, por lo que se hace hincapié en el seguimiento a largo plazo de los pacientes que reciben terapia con CAR-T para detección precoz de posibles neoplasias (7,12).
Con el tiempo se detectarán otros efectos a largo plazo, que aún son inciertos por la corta experiencia con este tratamiento, además de la dificultad de buscar causalidad ante pacientes que han recibido varios tratamientos con potencial toxicidad (2,6).
Resultados iniciales del uso de terapia CAR-T 19 en el Hospital Niño Jesús de Madrid (HNJS)
En España existen cuatro centros pediátricos y uno de reserva seleccionados por el sistema nacional de salud para el tratamiento con tisagenlecleucel (Kymriah). En 2019 se designó al Hospital Infantil Universitario Niño Jesús (HNJS) como el primer centro pediátrico para la administración y seguimiento de terapias CAR-T en la Comunidad de Madrid.
En el año 2020 hubo 25 solicitudes en toda España para la utilización de CAR-T 19 en pacientes menores de 25 años con diagnóstico de LLA, de ellas 9 (36%) provenían del HNJS.
La media de edad de los nueve pacientes tratados con Kymriah en el HNJS fue de 8.8 años (13 meses-20 años y 10 meses), siendo 6 mujeres (67%). En 8 de ellos la enfermedad estaba limitada a la médula ósea, solo 1 presentaba además afectación del sistema nervioso central (SNC). Respecto a la situación de la enfermedad en el momento de la solicitud, 2 (22%) presentaban refractariedad primaria, 3 (33%) se encontraban en primera recaída y los 4 (45%) restantes en segunda recaída. Habían recibido entre 2 y 4 líneas de tratamiento, y 4 (45%) de ellos habían sido sometidos a TPH con una mediana de tiempo postrasplante de 13 meses (12-27).
La mediana de tiempo que se tardó desde la aprobación de su uso por parte del comité CAR-T hasta la infusión fue de 60 días, el tiempo trascurrido desde la aféresis hasta la infusión fue de 44 días. La mediana del tiempo de ingreso hospitalario fue de 26.5 días.
Se realizaron 11 aféresis, puesto que en dos no se consiguieron resultados óptimos en el primer intento de recogida celular en un caso por fallo de la criopreservación y en el otro porque el aspirado de médula ósea fue hipocelular.
Respecto a la celularidad obtenida en las linfoaféresis, fue de una media de 8,382 x 109 (2,26-19,63) células nucleadas totales y 3,465 x 109 (1,83 – 8,46) linfocitos CD3+, cumpliendo los criterios de la realización de la técnica >/= 2 x 109 y >/= 1 x 109 respectivamente. Se requiere >3% de células nucleadas con CD3+, obteniéndose como media en nuestra experiencia un 48,33% (18-89).
Posterior a la aféresis se administró una quimioterapia puente, en 6 de los casos, basada en el protocolo de la SEOHP que incluía en un paciente una “inducción IA like”, en 2 casos una “inducción IB like” y en un caso un esquema MYOFLAG asociando en los 9 casos terapia intratecal y en uno de ellos además se administró radioterapia craneoespinal. Como complicaciones durante esta fase se observó en uno de ellos una sepsis por BGN y una infección herpética en otro caso.
De los nueve pacientes, finalmente fueron ocho los que ingresaron para infusión de células CAR-T con linfodepleción previa. Se estudió la EMR en el aspirado de medula ósea previo al ingreso observándose un 23.7% (0.46-76.7) de células con inmunofenotipo blástico.
El 25% de ellos obtuvieron remisión completa morfológica. El esquema de linfodepleción consistió en fludarabina 4 días y ciclofosfamida 2 días precisando en dos, como profilaxis antimicrobiana se utilizó levofloxacino, aciclovir y micafungina. En 3 de los casos de administró proxilaxis con levetirazetam.
Se infundieron una media de 3.8 x 106 / kg de células CAR-T, con una viabilidad de la celularidad total del 88.9%, y del 99.9% de los linfocitos T, ajustándose a los criterios establecidos por Novartis 0.5-2 x 106 /kg, 70% y 85% respectivamente. La media de porcentaje de células viables CAR-T fue del 16.3%, por encima del criterio necesario >3%. El volumen medio de infusión fue de 15 ml, en 5 de los casos una bolsa y en 3 de ellos 2.
Respecto a las complicaciones, se observó SLC en el 62% e ICANS en el 37% de los pacientes. El tiempo medio de aparición del SCL fue de 1 día tras la infusión, con una duración media de 5 días. El 37% cumplieron criterios de SLC grado 3, precisando el 50% ingreso en UCI, falleciendo un paciente. En cuanto al uso de fármacos dirigidos, el 50% recibió tocilizumab y el 25% otros fármacos anti interleuquinas (siltuximab/anakinra) y corticoides. Como tratamiento de soporte el 37% precisó inotrópicos y ventilación mecánica invasiva, y un 25% hemofiltro. El 25% sufrió coagulopatía de consumo como manifestación del SLC.
En referencia a los casos de síndrome de neurotoxicidad, el 25% cumplía criterios de grado 3, precisando ingreso en UCI de forma específica por esta complicación en el 12% de los casos. El tiempo medio de aparición desde la infusión fueron 6 días, con una duración media de 4 días. Todos los pacientes en los que se observó neurotoxicidad habían padecido SCL, el 66% había recibido tocilizumab, y el 25% corticoides u otros fármacos anti interleuquina (siltuximab).
Los pacientes con neurotoxicidad manifestaron temblores (37%), somnolencia/alteración de conciencia (25%), crisis epiléptica (12%) y alteración de los pares craneales (25%). Se administró profilaxis anticonvulsiva en el 66% de los pacientes. Otros efectos adversos fueron hipogammaglobulinemia (87%), recibiendo tratamiento con inmunoglobulinas el 74% y desarrollaron infecciones graves el 12% de los casos. Se detectaron citopenias en el día +30 postinfusión en el 25% de los pacientes, reduciéndose éste a un 12% en el día +90. En el 25% de pacientes se alcanzó toxicidad orgánica grado ¾.
Hasta el momento del análisis de los datos, no se han detectado segundas neoplasias.
En resumen se obtuvo una tasa de remisión completa del 87.5% al mes desde la infusión y una supervivencia global en el momento del análisis del 75% -media de duración de seguimiento de estos pacientes en ese momento de 7.6 meses-. La mortalidad global del procedimiento fue de 2 pacientes (25%).
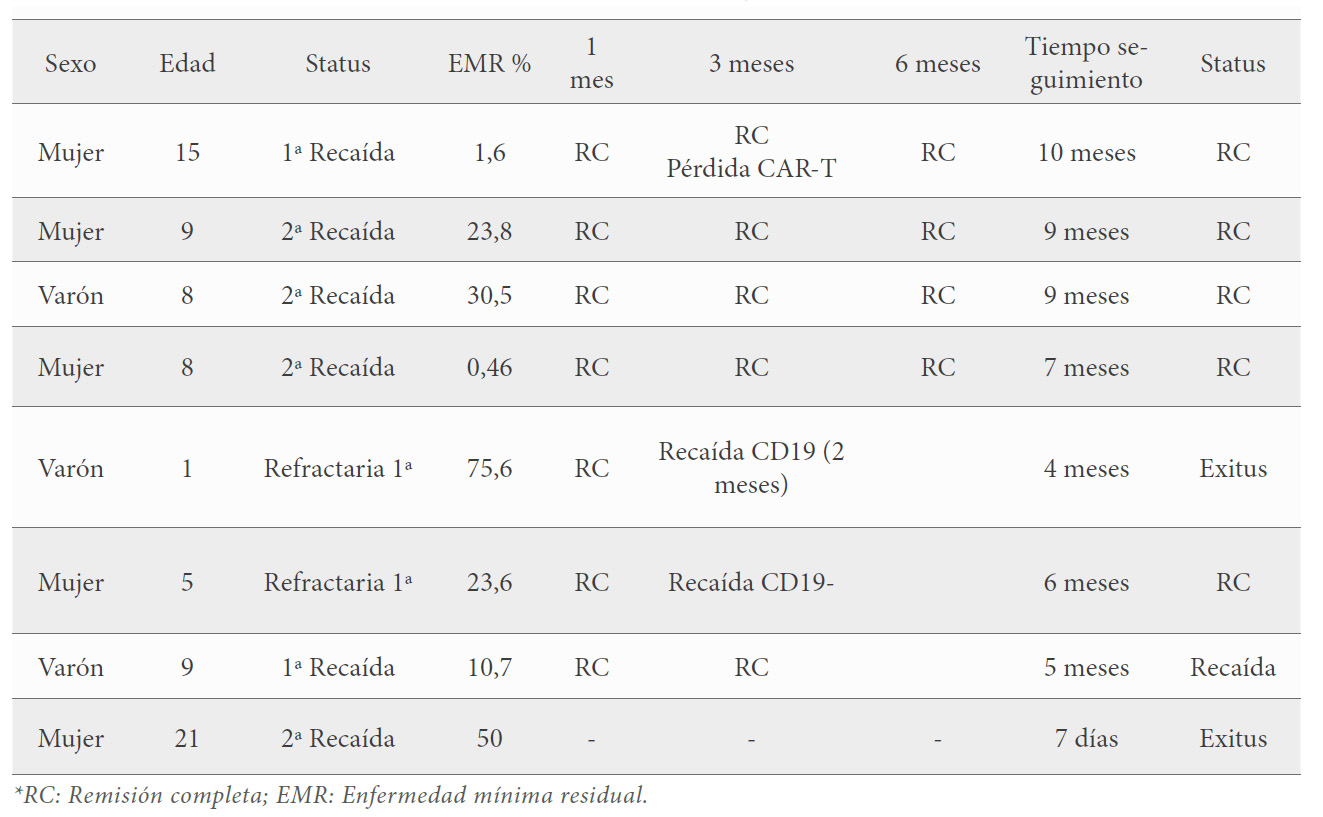
Un resumen de estos datos puede verse en la tabla 1.
DISCUSIÓN
Aunque las tasas de supervivencia alcanzadas en la LLA pediátrica han sufrido grandes avances desde la década de los 70 hasta hoy -de un 30% a más del 80% -, esto no es así en el caso de la LLA refractaría o en recaída (8,10). Estos casos suponen aun hoy, la primera causa de muerte por cáncer en edad pediátrica. Y es por esto por lo que los resultados obtenidos con la inmunoterapia han generado tantas expectativas en el tratamiento de la LLA refractaria o en recaída en pediatría.
Supone además una terapia dirigida, lo que disminuye la actual preocupación por la toxicidad y por los efectos secundarios derivados de la quimioterapia intensiva y el alo-TPH (5,10).
Se precisa el desarrollo de estos nuevos tratamientos que no solo buscan ampliar el arsenal terapéutico si no evitar toxicidades que incluso pueden acarrear la muerte del paciente (5,10,13). La inmunoterapia celular consigue un ataque inmunológico independiente de MHC y ligando coestimulador, preservando la función de citotoxicidad y de memoria de los linfocitos T (3)3.
Hasta la actualidad los resultados de los ensayos clínicos con terapia CAR-T 19 demuestran tasas de remisión y de supervivencia que no solo son comparables con el tratamiento utilizado actualmente en LLA refractaria o en recaída, si no que los superan al menos en la comparación al año postratamiento (16).
Aun así, el foco de preocupación e investigación continúan siendo las recaídas, por lo que se han realizado ensayos clínicos preliminares con terapia CAR-T 22 obteniendo resultados positivos (18). Actualmente se centra la atención en el desarrollo de células CAR multiantígeno para minimizar el riesgo de selección por presión inmune de células blásticas sin antígeno diana susceptible (17,18,19).
La inclusión de la terapia CAR-T 19 como parte del protocolo del tratamiento de primera línea ante determinados tipos de LLA o pacientes, aún está en estudio. Se beneficiarían de esta opción entre otros, aquellos pacientes con factores predictores de presentar LLA quimiorresistente, como pudiera ser el caso de LLA Ph positiva. En estudios recientes, se ha demostrado una tasa de remisión y SLE a un año con CAR-T 19 similar a la que se obtiene en LLA Ph negativa (11). Igualmente se beneficiarían los pacientes con síndromes genéticos con predisposición al cáncer como es el caso del síndrome Li Fraumeni, u otras alteraciones cromosómicas en los que el tratamiento con quimioterapia intensiva y radioterapia no sea posible, o que éste pueda derivar en consecuencias de mayor riesgo de futuras neoplasias.
En las recaídas extramedulares en el SNC se ha objetivado una menor respuesta al tratamiento de rescate con alo-TPH, planteándose la inmunoterapia celular una posibilidad de mejora en la supervivencia en estos casos (2).
Una de las limitaciones para incluir la terapia CAR-T 19 en los protocolos de tratamiento de primera línea es la toxicidad postinfusión, incluyendo el SLC y el síndrome de neurotoxicidad (21). Se ha de tener en cuenta al mismo tiempo las complicaciones que pueden surgir en el proceso de la terapia CAR-T. En primer lugar, no siempre es viable o exitosa la leucoaféresis, ya sea por la quimioterapia intensiva recibida o por encontrarse el paciente en los meses siguientes a un alo-TPH (2). Otra de las limitaciones es el tiempo necesario para la manipulación genética in-vitro, precisando por tanto de una cierta estabilidad o quimiosensibilidad en este tiempo (11). Por último, estudios actuales destacan la limitación económica que este tratamiento innovador aún tiene (8), defendiendo algunos su adecuado coste-efectividad con las tasas alcanzadas en cuestión de remisión y supervivencia hasta el momento actual (13).
En definitiva, se concluye la necesidad de realizar ensayos clínicos randomizados que comparen a largo plazo las diferentes estrategias terapéuticas disponibles en la LLA refractaría o en recaída para conseguir alcanzar mayores tasas de supervivencia. Se deberán recoger los datos sobre los pacientes que reciben terapias con CAR-T 19 para demostrar su seguridad a corto y largo plazo.
Plantear esta terapia en protocolos de tratamiento de primera línea aún debería probablemente posponerse, hasta que la eficacia y seguridad sean comprobadas a más largo plazo. El desarrollo de terapias dirigidas debe continuar, dado que son las deseadas en cuanto a disminuir las secuelas de la toxicidad de la quimioterapia y TPH a largo plazo en la población pediátrica ampliamente conocidas.
BIBLIOGRAFÍA
- López LM, Atienza AL, Navarro JS et al. Hematología y Oncología pediátricas.Majadahonda, Madrid: Ergon; 2015.
- Hucks G, Rheingold SR. The journey to CAR T cell therapy: the pediatric and young adult experience with relapsed or refractory B-ALL. Blood Cancer J. 2019; 9(2).doi:10.10387s41408-018-0164-6.
- Feins S, Kong W, Williams EF, Milone MC, Fraietta JA. An introduction to chimeric antigen receptor (CAR) T‐cell immunotherapy for human cancer. Am J Hematol. 2019; 94(S1): S3-S9.
- Greenbaum U, Mahadeo K, Kebriaei P, Shpall E, Saini N. Chimeric antigen receptor T-cells in B-acute lymphoblastic leukemia: state of the art and future directions. Front Oncol.2020; 10: 1594.
- Urbano-Ispizua A. Estado actual del tratamiento con células CAR-T en la leucemia aguda linfoblástica. An RANM. 2020; 137(01): 8-9.
- Kansagra AJ, Frey NV, Bar M et al. Clinical utilization of chimeric antigen receptor T-cells (CAR-T) in B-cell acute lymphoblastic leukemia (ALL)–an expert opinion from the European Society for Blood and Marrow Transplantation (EBMT) and the American Society for Blood and Marrow Transplantation (ASBMT). Bone Marrow Transpl. 2019; 54(11): 1868-1880.
- Pasquini MC, Hu Z-H, Curran K et al. Real-world evidence of tisagenlecleucel for pediatric acute lymphoblastic leukemia and non-Hodgkin lymphoma. Blood Adv. 2020; 4(21): 5414-5424.
- Taraseviciute A, Broglie L, Phelan R, Bhatt NS, Becktell K, Burke MJ. What is the role of hematopoietic cell transplantation (HCT) for pediatric acute lymphoblastic leukemia (ALL) in the age of chimeric antigen receptor T-cell (CART) therapy? J Pediatr Hematol Oncol. 2019; 41(5): 337-344.
- Vairy S, Lopes Garcia J, Teira P, Bittencourt H. CTL019 (tisagenlecleucel): CAR-T therapy for relapsed and refractory B-cell acute lymphoblastic leukemia. Drug Des Devel Ther. 2018; 12: 3885-3898.
- Jasinski S, De Los Reyes F, Yametti G, Pierro J, Raetz E, Carroll W. Immunotherapy in pediatric B-cell acute lymphoblastic leukemia: advances and ongoing challenges. Pediatr Drugs. 2020; 22(5): 485-499.
- Anagnostou T, Riaz IB, Hashmi SK, Murad MH, Kenderian SS. Anti-CD19 chimeric antigen receptor T-cell therapy in acute lymphocytic leukaemia: a systematic review and meta-analysis. Lancet Haematol. 2020; 7(11): e816-e826.
- Ali S, Kjeken R, Niederlaender C et al. The European Medicines Agency Review of Kymriah (Tisagenlecleucel) for the treatment of acute lymphoblastic leukemia and diffuse large B‐Cell lymphoma. Oncologist. 2020; 25(2): e321-e327.
- Sarkar RR, Gloude NJ, Schiff D, Murphy JD. Cost-Effectiveness of Chimeric Antigen Receptor T-Cell Therapy in Pediatric Relapsed/Refractory B-Cell Acute Lymphoblastic Leukemia. J Natl Cancer Inst. 2019; 111(7): 719-726.
- Maude SL, Laetsch TW, Buechner J et al. Tisagenlecleucel in children and young adults with B-Cell lymphoblastic leukemia. N Engl J Med. 2018; 378(5): 439-448.
- 20190508_Protocolo_manejo_efectos_adversos_CAR_T.pdf (mscbs.gob.es) Protocolo clínico para el manejo de los efectos adversos graves en pacientes tratados con medicamentos que contienen células T CAR (chimeric antigen receptor) ANTI-CD 19 (CART-19): desarrollado por el grupo de expertos en la utilización de medicamentos CAR del Plan de abordaje de las terapias avanzadas en el SNS: medicamentos CAR.
- Ma Q, Zhang J, O’Brien E, Martin AL, Agostinho AC. Tisagenlecleucel versus historical standard therapies for pediatric relapsed/refractory acute lymphoblastic leukemia. J Comp Eff Res. 2020; 9(12): 849-860.
- Ahmad A. CAR-T cell therapy. Int J Mol Sci. 2020; 21(12):4303. Doi.10.3390/ijms21124303.
- Fry TJ, Shah NN, Orentas RJ et al. CD22-targeted CAR T cells induce remission in B-ALL that is naive or resistant to CD19-targeted CAR immunotherapy. Nat Med. 2017; 24(1): 20-28.
- Shah NN, Highfill SL, Shalabi H et al. CD4/CD8 T-Cell selection affects chimeric antigen receptor (CAR) T-Cell potency and toxicity: updated results from a phase I anti-CD22 CAR T-Cell trial. J Clin Oncol. 2020; 38(17): 1938-1950.
- Jiang H, Li C, Yin P et al. Anti‐CD19 chimeric antigen receptor‐modified T‐Cell therapy bridging to allogeneic hematopoietic stem cell transplantation for relapsed/refractory B‐Cell acute lymphoblastic leukemia: an open‐label pragmatic clinical trial. Am J Hematol. 2019; 94(10):1113-1122.
- Curran KJ, Margossian SP, Kernan NA et al. Toxicity and response after CD19-specific CAR T-cell therapy in pediatric/young adult relapsed/refractory B-ALL. Blood. 2019; 134(26): 2361-2368.
- Tan AP. CAR-T cell therapy-related neurotoxicity in pediatric acute lymphoblastic leukemia: spectrum of imaging findings. Pediatr Neurol. 2020; 111: 51-58.
- Parker KR, Migliorini D, Perkey E et al. Single-Cell Analyses Identify Brain Mural Cells Expressing CD19 as Potential Off-Tumor Targets for CAR-T Immunotherapies. Cell. 2020;183(1): 126-142.
DECLARACIÓN ÉTICA
La aprobación de este estudio fue obtenida por el Comité de Ética local (Hospital Universitario Infantil Niño Jesús, Madrid, España).
DECLARACIÓN DE TRANSPARENCIA
Los autores/as de este artículo declaran no tener ningún tipo de conflicto de intereses respecto a lo expuesto en el presente trabajo.
ranm tv
Carlos Jiménez Romero.
Unidad de Cirugía HBP y Trasplante de Órganos Abdominales
H. Universitario Doce de Octubre. Ctra de Andalucia Km 5,4 · 28041 Madrid
Tlf.: +34 913 908 294 | E-Mail: carlos.jimenez@inforboe.es
An RANM. 2021;138(02): 157 – 167
Enviado*: 01.06.21
Revisado: 07.06.21
Aceptado: 18.06.21
* Fecha de lectura en la RANM


