Resumen
La enfermedad de Chagas se encuentra dentro de las Enfermedades Tropicales Desatendidas (ETD), según la clasificación de la OMS, y de las Enfermedades Infecciosas Desatendidas (EID) que la OPS incluye en sus planes de eliminación. La enfermedad de Chagas es la más común de las ETD (o EID) en amplias zonas de América, donde habita el vector que transmite el parásito Trypanosoma cruzi y donde se encuentra la mayoría de los pacientes y personas infectadas. Dados los movimientos de población, se ha convertido en un problema de salud pública global que afecta también a países sin transmisión vectorial como Estados Unidos o España. Se ha progresado mucho en el control de la transmisión vectorial y por transfusiones de sangre. Otras vías de transmisión, como la oral y la materno-infantil, continúan presentando grandes desafíos para el control y el acceso a la atención de los pacientes. En los países sin transmisión vectorial, la principal vía es la congénita. Considerando que hay un gran déficit de personas diagnosticadas y tratadas por la enfermedad de Chagas, el control y detección tempranos de casos en mujeres en edad fértil, embarazadas y niños, así como en otras personas asintomáticas puede acelerar la lucha contra esta enfermedad, potencialmente mortal. Para ello deben aplicarse todas las herramientas disponibles. Existen varios países y regiones que ya utilizan con eficacia el enfoque citado en mujeres y niños. Los avances realizados gracias a la colaboración entre instituciones públicas y privadas evidencian el éxito, pero se necesita un mayor compromiso político para eliminar la enfermedad como problema de salud pública en 2030, tal y como establece la estrategia ETMI-Plus promovida por la OPS, la nueva Hoja de Ruta para las ETD aprobada por la OMS, los Objetivos de Desarrollo Sostenibles (ODS) e incluso el programa de la SEGIB «Ningún bebé con Chagas».
Abstract
Chagas disease is grouped among the Neglected Tropical Diseases (NTD), according to the classification of WHO and among the Neglected Infectious Diseases susceptible to be eliminated according to PAHO (EID). Chagas disease is the most common NTD (or EID) in wide areas of South and Central America where the vector – an insect, which transmits the parasite Trypanosoma cruzi via its bite – and the great majority of patients live. However, due to population movements, this disease has now become a global problem, especially in the USA and Spain. The control of transmission by the vector or by blood transfusions has progressed considerably. However, transmission by other routes, namely oral and mother-to-child are still a challenge in regards of control and access to health care. In the countries where transmission by the vector doesn’t take place, vertical transmission is the main route of transmission. Taking into account that there is a huge gap in diagnosing and treating patients suffering from Chagas disease, early diagnosis and treatment of infected women in childbearing age, pregnant women and children, as well as asymptomatic infected people, is an important contribution towards the control of this disease which is potentially fatal if left untreated. Aiming for this objective, all available tools should be optimized and implemented. There are several countries and regions already implementing this strategy in this particular group of women and children. The advances achieved are a good example of the collaboration between organizations and institutions in the public and private sectors, although a greater political commitment is needed in order to achieve Chagas elimination as a public health problem by 2030 as promoted by the ETMI-Plus strategy established by PAHO, the new WHO-NTD road map, the UN sustainable development goals (SDG) and the program «No baby with Chagas» launched by the SEGIB.
Palabras clave: Enfermedad de Chagas; Transmisión materno-infantil; Control.
Keywords: Chagas disease; Mother-to-child transmission; Control.
INTRODUCCIÓN
Junto a las características biomédicas intrínsecas de cada enfermedad, los condicionantes sociales y ambientales son claves en el control de las enfermedades, pero en el grupo de las «desatendidas» (1), las características intrínsecas de la pobreza como las barreras de acceso a la educación, la vivienda inapropiada, el deterioro medioambiental, la falta de recursos económicos y el acceso a los servicios de salud, suponen factores adicionales de dificultad insoslayables para su control y eliminación como problema de Salud Pública (2). La enfermedad de Chagas, tradicionalmente asociada a entornos rurales, remotos y de escasos recursos, es hoy un problema de salud pública global, tanto en áreas rurales como urbanas (3). Para acelerar el control de esta enfermedad, se necesita poner en marcha y reforzar enfoques integrados, diferentes e innovadores, como la atención y el control de la transmisión materno-infantil. Con el acceso a las herramientas de control, diagnóstico y tratamiento actuales es posible prevenir y reducir los daños que causa esta enfermedad. Con nuevas herramientas será posible acelerar el camino para alcanzar las metas de eliminación propuestas para 2030, de acuerdo con la nueva Hoja de Ruta de las Enfermedades Desatendidas (ETD) (4) aprobada por la OMS y en línea con la meta 3.3 de los Objetivos de Desarrollo Sostenibles (ODS).
La enfermedad de Chagas o tripanosomiasis americana es causada por el parásito Trypanosoma cruzi (T. cruzi), que se transmite al ser humano cuando un insecto triatomino deposita sus heces infectadas junto al orificio de entrada de la picadura y se facilita la entrada con el rascado. Esta transmisión por vía vectorial ha sido históricamente el principal mecanismo de transmisión en zonas endémicas de América. A ello se suman las vías de transmisión siguientes: congénita; oral, a través de la ingestión de alimentos y bebidas contaminados por triatominos infectados; mediante donaciones de órganos y transfusión sanguínea de donantes portadores del parásito; y por accidentes de laboratorio.
La enfermedad presenta una fase aguda de una duración aproximada de dos meses, que puede ser asintomática de forma predominante o con síntomas leves e inespecíficos. En esta fase, el parásito es detectable en el torrente sanguíneo mediante técnicas parasitológicas o moleculares y si se hace el diagnóstico, el tratamiento es sumamente eficaz para alcanzar la cura del paciente. Si las personas no son diagnosticadas y tratadas en la fase aguda, pasan a una fase crónica asintomática que puede durar muchos años o décadas y en la que se hace muy difícil realizar el diagnóstico, entre otros motivos porque la falta de expresión clínica evita que acudan a consulta. Cuando el diagnóstico se realiza en esta etapa, el tratamiento es menos eficaz y la probabilidad de alcanzar la cura es mínima. En cualquier caso, aproximadamente el 30 % de las personas infectadas desarrolla en plena edad productiva manifestaciones clínicas y complicaciones de tipo cardíaco, y un 10 %, de tipo digestivo, neurológico o mixtas (5). Así mismo, pueden ocurrir episodios de muerte súbita asociada a los trastornos del ritmo cardíaco. Por este conjunto de circunstancias se considera una enfermedad desatendida, silenciosa e «invisible». En esta fase, el parásito se acantona y multiplica en las fibras musculares cardíacas y/o digestivas. Por lo tanto, el diagnóstico precoz y el tratamiento oportuno (previo a la fase crónica), son necesarios para evitar los efectos irreversibles a largo plazo (6).
La enfermedad es endémica en 21 países de América en los que habita el vector que la transmite (insectos hemípteros de la subfamilia Triatominae), conocido por diferentes nombres vernáculos como vinchuca, pitos, barbeiros o chinche besucona, entre otros, según las diferentes zonas del continente. La descripción inicial del ciclo de transmisión y de la enfermedad se debe a los trabajos del doctor brasileño Carlos Chagas en 1909 (7) y posteriormente a varios colaboradores del Instituto de Manguinhos, como el Dr. Salvador Mazza.
Actualmente la enfermedad de Chagas se considera una de las enfermedades infecciosas transmisibles de interés para la salud pública más comunes de América. La mayoría de las personas con la infección (entre 6 y 7 millones según las estimaciones oficiales) (5), así como las fallecidas (más de 10 000 al año) y las que están en riesgo de infección (75 millones, aproximadamente) (5) se concentran en países de Sudamérica como Argentina, Bolivia, Brasil, Colombia, así como en Centroamérica y México (5). Sin embargo, debido a los movimientos de población y a las vías de transmisión secundarias, la enfermedad se ha expandido a países de todo el mundo, entre los que destacan, por la cantidad estimada de casos, Estados Unidos (300 000) (8) o España (más de 68 000, de los cuales más de 22 000 son mujeres en edad fértil) (9).
HACIA EL CONTROL DE LA TRANSMISIÓN MATERNO-INFANTIL
Los programas de control de los países endémicos trabajan de forma articulada desde 1992 y de forma progresiva en Iniciativas Regionales con el objetivo de eliminar la transmisión vectorial y por transfusiones de sangre (10). Los avances realizados en los países endémicos desde principios de la década de los 90 en el control vectorial han reducido la incidencia de la transmisión por el vector en amplias zonas de América (11). Además, se ha incorporado el tamizaje universal en los bancos de sangre de todos los países considerados endémicos por la presencia del algún tipo de vector transmisor. El gran desafío en el control de la enfermedad sigue siendo la detección temprana y el tratamiento de las personas con la infección.
Actualmente, los dos fármacos tripanocidas disponibles (benznidazol y nifurtimox), tienen una altísima eficacia en las formas agudas de la infección en todas las edades, una elevada eficacia en las formas crónicas en jóvenes y niños, y menor eficacia en adultos que estén cursando la fase crónica (6). A pesar de que el diagnóstico temprano es vital para alcanzar la mayor eficacia terapéutica antiparasitaria, la mayoría de las personas que han contraído la infección lo desconocen porque alrededor del 70 % de todas las infecciones crónicas se tornan asintomáticas, lo cual anula la necesidad de que las personas busquen los servicios médicos. A lo anterior se agrega la falta de conocimiento social de la enfermedad y los niveles muy bajos de cobertura en cuanto a diagnóstico y tratamiento (12).
Se estima que entre 8000 y 15 000 recién nacidos contraen la infección durante la gestación, la mayor parte de ellos en América Latina, lo que hace que la vía congénita sea actualmente una de las principales formas de transmisión en muchos países y cause la tercera parte de las infecciones nuevas observadas (13). Por ello, centrar la atención en prevenir esta vía de transmisión es esencial para acelerar los avances en el control y la eliminación de la enfermedad a nivel global (6).
La detección temprana de infecciones en niñas y mujeres en edad fértil y su tratamiento para prevenir la transmisión congénita en futuros embarazos, así como el diagnóstico de mujeres embarazadas ofrecen una posibilidad estratégica para reducir la transmisión que, según la nueva Hoja de Ruta para las ETD de la OMS, se espera lograr en un 37 % de los países afectados en la década actual. Además, este esfuerzo permitirá detectar, tratar y curar a todos los niños nacidos de mujeres que tengan la infección. Así mismo, la detección temprana en este grupo de personas permite ampliar el universo de cobertura de atención integral a toda la población afectada. La hoja de ruta de la OMS señala la meta de que un 75 % de toda la población afectada tenga tratamiento en 2030. Además, la OPS establecía en 2019 la meta de eliminar el Chagas congénito como «problema de salud pública».
Esa meta incluye también los objetivos del Marco para la Eliminación de la Transmisión Materno-infantil del VIH, la sífilis, la hepatitis y Chagas, (ETMI-Plus), impulsado por la OPS en 2017 (14). La inclusión de una enfermedad desatendida entre los tamizajes rutinarios de otras enfermedades prevalentes fue uno de los primeros pasos en la tendencia global a impulsar iniciativas integradas que faciliten el acceso al diagnóstico y el tratamiento de varias enfermedades prioritarias para que estas puedan ser eliminadas. Con la ETMI-Plus se aspira a alcanzar a que un 90 % de las madres y sus hijos reciba los cuidados pertinentes, incluidos diagnóstico, tratamiento y vigilancia (15).
El diagnóstico y la participación de las mujeres cobra especial relevancia por el papel activo que suelen desempeñar en el cuidado de la salud a nivel familiar y comunitario, especialmente en las zonas remotas más afectadas.
Para materializar los avances, tanto en el control materno-infantil como en el acceso a la atención integral de toda la población afectada, son necesarias estrategias y herramientas adaptadas a contextos de difícil acceso para el personal y las estructuras de salud (16).
Con las herramientas actuales de diagnóstico y tratamiento, se puede llegar a la población que necesita dichos avances, pero sin duda, la mejora en la aplicación de diagnósticos de alta calidad, rápidos y confirmatorios, así como una reducción en el régimen de tratamiento (de los dos meses actuales a quince días) puede facilitar el manejo de la enfermedad de forma descentralizada y en el primer nivel de atención, el cual debe contar con infraestructura adecuada y recursos humanos capacitados (17).
Actualmente se están ensayando formas de simplificar el diagnóstico en mujeres, comparando las actuales pruebas serológicas en unidades sanitarias hospitalarias con el uso de dos pruebas rápidas en los centros de salud de primer nivel (18). De la misma forma, se están ensayando técnicas moleculares para incrementar las posibilidades de diagnosticar la infección congénita en el recién nacido (13).
El diagnóstico de mujeres en edad fértil o embarazadas exige acciones proactivas dada la prevalencia de la forma clínica (asintomática) de la infección en la fase crónica, sin patología demostrada. La detección precoz del recién nacido exige también la búsqueda activa, ya que alrededor del 65 % de los niños nacidos con infección congénita también son asintomáticos u oligosintomáticos. Esto implica perder la oportunidad de realizar un diagnóstico clínico. Alrededor del 35 % de los recién nacidos puede presentar formas clínicas evidenciables, algunos de ellos con formas graves y/o fatales tales como una meningoencefalitis o una miocarditis si no se diagnostica oportunamente (19). El diagnóstico y tratamiento oportunos reducen este perfil clínico, aproximadamente, al 10 % (20).
EL LIDERAZGO DE LOS PAÍSES JUNTO A LA SOCIEDAD CIVIL
Los compromisos adquiridos por los países e instituciones internacionales en las reuniones quedan vacíos cuando no se materializan en acciones concretas. Por su parte, no es posible que la enfermedad de Chagas tenga la relevancia que necesita en la agenda de salud global si los países no cumplen los compromisos. En los últimos años, el liderazgo de países como Brasil, Argentina o Paraguay, en los que se ha puesto en marcha la notificación obligatoria de todos los casos, agudos y crónicos, o de Colombia, donde se está avanzando en el acceso al diagnóstico y al tratamiento en zonas que estaban fuera de la cobertura del Ministerio de Salud durante los años de conflicto, son solo ejemplos de grandes avances (21). Estos se suman a los avances ya logrados en materia de control de la transmisión vectorial en las diferentes regiones de América o al tamizaje universal en donantes para interrumpir la transmisión mediante transfusiones sanguíneas (y trasplantes de órganos), en prácticamente todos los países endémicos.
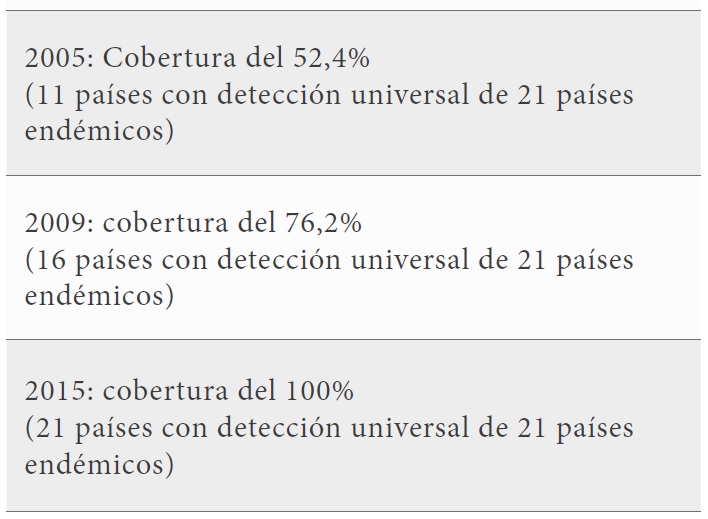
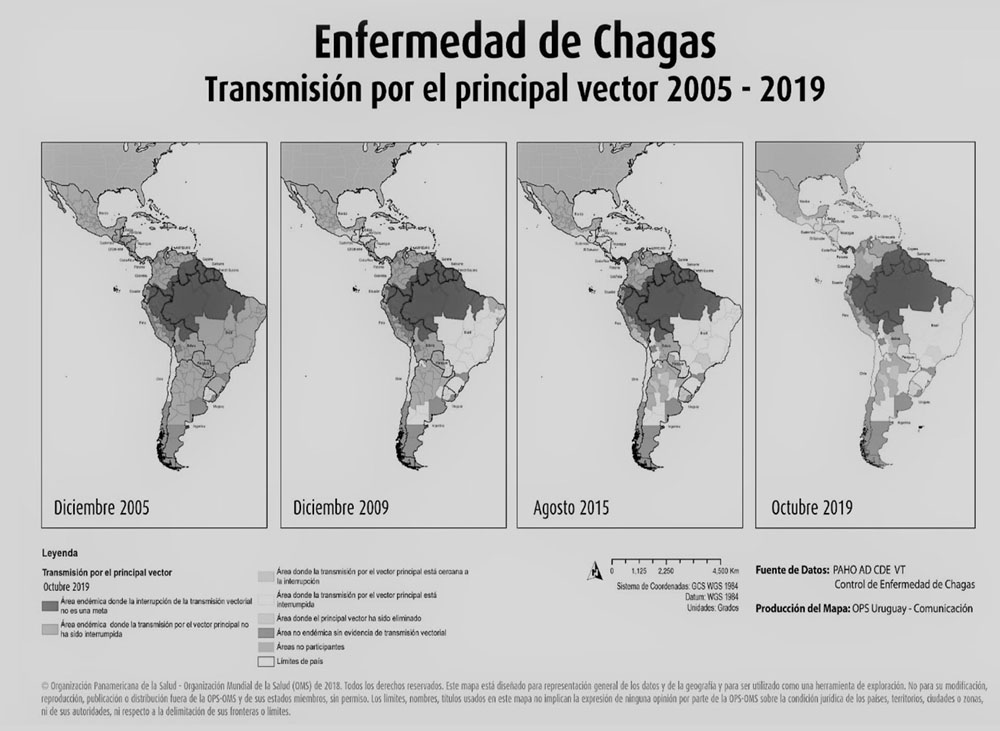
En cuanto al control de la transmisión materno-infantil de T. cruzi, pocos países tienen formalmente establecido en sus sistemas de salud la obligatoriedad de realizar el control de la transmisión congénita. Estos son, en concreto, Argentina, Bolivia, Uruguay y, parcialmente, Brasil en Goiás y Mato Grosso do Sul, además de Chile (10). La iniciativa ETMI-Plus se encuentra en una fase inicial, retardada más allá de lo esperado dados los efectos negativos de la pandemia de COVID-19 y su impacto en los países de América. Es por eso por lo que aún pasará algún tiempo antes de que estén disponibles los resultados preliminares de su implementación en algunos de esos países. Por otro lado, puesto que la transmisión congénita es la principal vía en países no endémicos, requiere especial atención. En España, varias comunidades autónomas realizan controles rutinarios a mujeres y niños de origen latinoamericano, como en Cataluña, Valencia o Galicia. Solo en la Comunidad de Murcia (22) se ha logrado interrumpir la transmisión congénita, sin que se haya notificado ningún caso en los dos últimos años. Actualmente, las autoridades sanitarias del Estado están trabajando (23) para incorporar el tamizaje prenatal de la enfermedad de Chagas en la cartera común de los servicios prestados por el Sistema Nacional de Salud, de forma que todas las mujeres embarazadas pertenecientes a los grupos de riesgo definidos tengan acceso a esta prestación y que el tamizaje se oferte de forma homogénea en todo el territorio.
La colaboración de los institutos de investigación, universidades y las ONG, sumada al esfuerzo de los Ministerios de Salud, contribuye a crear evidencia científica, pues refuerzan los programas y subprogramas nacionales de prevención y control de la enfermedad de Chagas. Una vez más, las alianzas institucionales, como la Coalición Global de Chagas (24) o la Plataforma de Chagas para la investigación (25), son claves para el trabajo en red. Junto con las asociaciones de personas afectadas, estos grupos de la sociedad civil han colaborado estrechamente con los gobiernos de países endémicos y no endémicos para luchar contra la invisibilidad de esta enfermedad.
Las alianzas público-privadas tienen el valor añadido de multiplicar el impacto de las iniciativas individuales. Un ejemplo es la Coalición Chagas, que tiene como objetivo fortalecer las alianzas y avances de todos los miembros de la comunidad de organizaciones e instituciones que trabajan con Chagas para acelerar el acceso a la atención integral de la enfermedad y darle más visibilidad en la agenda de salud global. Así mismo, sus fundadores: Fundación Mundo Sano, DNDi, ISGlobal, el Centro para el Desarrollo de Vacunas del Hospital Infantil de Texas y Baylor College, y CEADES, en conjunto y también con sus propios socios, apoyan y/o lideran programas de acceso e investigaciones para nuevos regímenes de tratamientos o nuevas entidades químicas, trabajos para encontrar biomarcadores que atestigüen la eficacia de los tripanocidas en casos crónicos y/o investigaciones para desarrollar una futura vacuna.
Las empresas farmacéuticas se están integrando cada vez más en estas alianzas público-privadas, lo que resulta en una comprensión más integral de la problemática y una mejor oferta adaptada a las necesidades. El programa de Bayer para la donación de nifurtimox a través de la OMS/OPS, así como el acuerdo para el acceso al benznidazol entre Mundo Sano y la OMS (26), incluyen ya las formulaciones pediátricas, que sin duda influirán en la aceleración del tratamiento que se utilice en los programas de detección materno-infantiles.
Otro ejemplo de estas iniciativas de colaboración, no menos importante por lo que supone para la visibilidad de la enfermedad, es fruto de la colaboración entre los grupos de personas afectadas, las organizaciones privadas, las instituciones públicas y las plataformas internacionales, que logró la aprobación del Día Mundial de Chagas por parte de la OMS, en 2018. Su celebración estimuló el entusiasmo y promesas de nuevos compromisos políticos y financieros, pero la inmediata llegada de la pandemia por la COVID-19 desaceleró ese momento prometedor. El entusiasmo que se vivía en la comunidad de expertos y afectados por la enfermedad desatendida se eclipsó. Aún más, la coinfección entre la COVID-19 y la enfermedad de Chagas supuso un doble riesgo de agravamiento de la patología cardíaca y digestiva (27).
CONCLUSIONES
La pandemia de COVID-19 ha dejado evidencias incuestionables de que el compromiso político y la cooperación internacional están detrás de cualquier avance en temas de salud, que debe traducirse en una inyección económica para nuevos programas. Entre 2000 y 2015, a través de la Agencia de Cooperación Internacional para el Desarrollo (AECID), España se convirtió en el principal donante bilateral de toda la OCDE en la lucha contra Chagas, seguido por la cooperación canadiense, con contribuciones específicas, principalmente en Bolivia, Honduras, El Salvador y Paraguay, entre otros países endémicos (28). El primer Día Mundial de Chagas, en 2018, ayudó a colocar la problemática en la agenda pública a nivel intercontinental y diferentes países y organizaciones dieron a conocer nuevos compromisos orientados al control de la transmisión materno-infantil, como el programa de financiación de UNITAID (29). Así mismo, posteriormente se anunció un nuevo programa iberoamericano de control materno-infantil que fue aprobado por los países que forman parte de la Secretaría General Iberoamericana (SEGIB) en 2021 (30).
Todas estas iniciativas exigen programas de capacitación y adopción de las estrategias en los sistemas de salud de los países afectados. Esto incluye facilitar las condiciones necesarias para las acciones específicas y la actitud favorable de los equipos de salud para la implementación de las mismas.
Es necesario recordar la importancia de contribuir al fortalecimiento de los servicios nacionales de salud de forma integrada en todos los niveles de atención para avanzar hacia la cobertura sanitaria universal (ODS 3.8), prioridad de la cooperación española. La cobertura universal es imprescindible para que todos los países puedan aplicar el conocimiento y la evidencia científica que existe, así como para poner en práctica los hallazgos de las investigaciones, lo que contribuye a prevenir, diagnosticar y tratar todo tipo de patologías y enfermedades.
Sin embargo, los recursos siguen siendo muy limitados ante las dimensiones de los desafíos impuestos por la enfermedad de Chagas y la masiva dotación presupuestaria que supone la pandemia por la COVID-19 en detrimento de otros programas. Lo positivo es que conocemos bien cómo alcanzar las metas de eliminación como objetivo de salud pública en 2030: el trabajo colaborativo, intersectorial, interdisciplinario, interregional e internacional con las personas afectadas en el centro de las decisiones y con la visión de no dejar atrás a nadie.
En un lúcido ensayo, La enfermedad y sus metáforas, Susan Sontag apuntaba que, en el mundo, finalmente, solo hay dos clases de ciudadanías, la de la salud y la de la enfermedad, pero a algunos les resulta más costoso vivir y cruzar de un territorio a otro según en qué zona del planeta les haya tocado nacer. La enfermedad de Chagas puede y debe controlarse y eliminarse como problema de salud pública global, independientemente de lo lejos o cerca que se encuentren las poblaciones afectadas. No existen ya enfermedades que no sean incumbencia de todos. El enfoque de la detección de casos a través de programas dirigidos a mujeres en edad fértil, embarazadas y niños arrojará grandes éxitos relacionados con la interrupción de la transmisión, como ya se ha observado en algunas zonas que han logrado el compromiso de todos los actores necesarios. Está en nuestras manos hacerlo posible en esta década.
BIBLIOGRAFÍA
- Organización Panamericana de la Salud. Plan de acción para la eliminación de las enfermedades infecciosas desatendidas y las medidas posteriores a la eliminación 2016-2022. Washington, D.C. 2016. [Internet] https://www.paho.org/hq/dmdocuments/2016/CD55-15-s.pdf
- Alvar, J. Pobreza y enfermedad. Debate y embate de las enfermedades tropicales. Madrid: Real Academia Nacional de Medicina de España; 2021.
- Coura, JR, Viñas PA. Chagas disease: a new worldwide challenge. Nature 2010; 465(7301):S6-S7.
- World Health Organization. Ending the neglect to attain the sustainable development goals: a sustainability framework for action against neglected tropical diseases 2021-2030. Geneva; 2021.
- Organización Mundial de la Salud. Enfermedad de Chagas. [Internet]. https://www.who.int/es/news-room/fact-sheets/detail/chagas-disease-(american-trypanosomiasis
- Organización Panamericana de la Salud. Guía para el diagnóstico y el tratamiento de la enfermedad de Chagas. [Internet] http://iris.paho.org/xmlui/handle/10665.2/49653
- de Oliveira, RB, Ballart C, Abràs A, Gállego M, Marin-Neto JA. Chagas Disease: An Unknown and Neglected Disease. En: Pinazo Delgado M-J, Gascón J, editores. Chagas Disease: A Neglected Tropical Disease. Cham: Springer International Publishing; 2020. p. 1-26.
- US Centers for Disease Control and Prevention. American Trypanosomiasis (also known as Chagas Disease). [Internet] https://www.cdc.gov/parasites/chagas/epi.html
- Imaz Iglesia, I, García San Miguel L, Blasco Hernández T, et al. Evaluación económica de distintas estrategias de cribado de la enfermedad de Chagas en España. IPE 2015/72. Madrid: Agencia de Evaluación de Tecnologías Sanitarias (AETS) – Instituto de Salud Carlos III; 2015.
- Antonieta Rojas de Arias, Carlota Monroy, Felipe Guhl, et al. Chagas disease control-surveillance in the Americas: the multinational initiatives and the practical impossibility of interrupting vector-borne Trypanosoma cruzi transmission. Mem Inst Oswaldo Cruz 2021; 116 (e210130).
- Organización Panamericana de la Salud. Enfermedad de Chagas. [Internet] https://www.paho.org/es/temas/enfermedad-chagas
- Costa Chaves, G, Abi-Saab Arrieche M, Rode J, et al. Estimación de la demanda de medicamentos antichagásicos: una contribución para el acceso en América Latina. Rev Panam Salud Públ 2017; 41:e45.
- Picado, A, Cruz I, Redard-Jacot M, et al. The burden of congenital Chagas disease and implementation of molecular diagnostic tools in Latin America. BMJ global health 2018; 3(5):e001069.
- Organización Panamericana de la Salud. ETMI Plus. Marco para la eliminación de la transmisión maternoinfantil del VIH, la sífilis, la hepatitis y la enfermedad de Chagas Washington, D.C.: OPS; 2017.
- Organización Panamericana de la Salud. Iniciativa para la eliminación de enfermedades: política para aplicar un enfoque integrado y sostenible de las enfermedades transmisibles en la región de las Américas Washington, D.C., EUA: 57.o Consejo Directivo. 71.a Sesión del Comité Regional de la OMS para las Américas; 2019.
- Carlier, Y, Altcheh J, Angheben A, et al. Congenital Chagas disease: Updated recommendations for prevention, diagnosis, treatment, and follow-up of newborns and siblings, girls, women of childbearing age, and pregnant women. PLoS Negl Trop Dis 2019; 13(10):e0007694.
- Torrico, F, Gascón J, Barreira F, et al. New regimens of benznidazole monotherapy and in combination with fosravuconazole for treatment of Chagas disease (BENDITA): a phase 2, double-blind, randomised trial. Lancet Infect Dis 2021; 21(8):1129-1140.
- Lozano, D, Rojas L, Méndez S, et al. Use of rapid diagnostic tests (RDTs) for conclusive diagnosis of chronic Chagas disease – field implementation in the Bolivian Chaco region. PLoS Negl Trop Dis 2019; 13(12):e0007877.
- Freilij, H, Altcheh J. Congenital Chagas’ disease: diagnostic and clinical aspects. Clinical infectious diseases: an official publication of the Infectious Diseases Society of America 1995; 21(3):551-555.
- Bisio, MMC, Rivero R, Gonzalez N, et al. Diagnostic Accuracy of Two Molecular Tools for Diagnosis of Congenital Chagas Disease. Mol Diagn Therapy 2021:1-11.
- Marchiol, A, Forsyth C, Bernal O, et al. Increasing access to comprehensive care for Chagas disease: development of a patient-centered model in Colombia. Rev Panam Salud Públ 2017; 41:e153.
- Consejería de Salud de la Región de Murcia. El SMS incluirá la prueba de detección de la enfermedad de Chagas a todas las mujeres en el primer trimestre del embarazo Murcia2021. [Internet] http://www.murciasalud.es/principal.php
- Stillwaggon, E, Perez-Zetune V, Bialek SR, Montgomery SP. Congenital Chagas Disease in the United States: Cost Savings through Maternal Screening. Am J Trop Med Hyg 2018; 98(6):1733-1742.
- Coalición Chagas. [Internet] http://www.coalicionchagas.org/
- DNDi. Plataforma de Chagas. [Internet] https://www.dndial.org/es/enfermedades/enfermedad-chagas/plataformadechagas/
- Mundo Sano. Mundo Sano refuerza su compromiso con la OMS para acelerar la eliminación del Chagas congénito. [Internet] https://www.mundosano.org/es/mundo-sano-refuerza-su-compromiso-con-la-oms-para-acelerar-la-eliminacion-del-chagas-congenito/
- Zaidel, EJ, Forsyth CJ, Novick G, et al. COVID-19: Implications for People with Chagas Disease. Glob Heart 2020; 15(1):69.
- Instituto de Salud Global Barcelona. Una batalla por la salud de todos. El liderazgo de España en la lucha contra el Chagas. 2017. https://www.isglobal.org/-/el-liderazgo-de-espana-en-la-lucha-contra-el-chagas
- Unitaid. Unitaid commemorates World Chagas Day with a new initiative to prevent mother-to-child transmission of the disease 2021. [Internet] https://unitaid.org/news-blog/unitaid-commemorates-world-chagas-day-with-a-new-initiative-to-prevent-mother-to-child-transmission-of-the-disease/#en
- XXVII Cumbre Iberoamericana de jefes de Estado y de Gobierno de Andorra 2021. [Internet] https://www.segib.org/wp-content/uploads/PdA_ANDORRA-ES.pdf
DECLARACIÓN DE TRANSPARENCIA
Los autores/as de este artículo declaran no tener ningún tipo de conflicto de intereses respecto a lo expuesto en el presente trabajo.
ranm tv
Sergio Sosa-Estani
Drugs for Neglected Diseases initiative – Rio de Janeiro, Brasil
Tlf.: +55 21 25 29 04 39 | E-Mail: ssosa@dndi.org
Año 2021 · número 138 (03) · páginas 202 a 208
Enviado*: 30.06.21
Revisado: 04.07.21
Aceptado: 20.07.21
Publicado Online: 21.12.21
* Fecha de lectura en la RANM


