Resumen
En el presente artículo, se analizan los retos que el creciente desarrollo de la ingeniería tisular está generando en la Universidad y en el Sistema de Salud. Con el objeto de estimular la articulación institucional necesaria en esta área entre ambos organismos, se analiza la experiencia de colaboración existente entre el Departamento de Histología de la Universidad de Granada y el Sistema de Salud Pública de Andalucía. Se describen las bases de esta colaboración, especificando las contribuciones de ambas organizaciones a las funciones de su contraparte y las actividades conjuntas que ambos organismos pueden ejecutar en el campo de la ingeniería de tejidos para favorecer la aplicación clínica como medicamento de los tejidos artificiales generados.
Abstract
In this article, we analyze the challenges that the growing development of tissue engineering is generating in the University and in the Health System. In order to stimulate the necessary institutional articulation in this area between both organizations, the experience of collaboration between the Department of Histology of the University of Granada and the Public Health System of Andalusia is analyzed. The bases of this collaboration are described, specifying the contributions of both organizations to the functions of their counterpart and the joint activities that both organisms can carry out in the field of tissue engineering to favor the clinical application as a medicine of the artificial tissues generated.
Palabras clave: Ingeniería tisular; Universidad; Sistema de salud.
Keywords: Tissue engineering; University; Health System.
INTRODUCCIÓN
La publicación en 1993 del artículo Tissue Engineering en la revista Science por Robert Langer y Joseph Vacanti constituye el punto de partida del desarrollo y la posterior expansión de la Ingeniería tisular en los últimos veinticinco años. Aunque previamente, y muy especialmente desde finales de los años ochenta del pasado siglo, se venía trabajando en la elaboración de sustitutos biológicos viables para su posible uso terapéutico fue el artículo de Langer y Vacantí el que sistematizó el nuevo campo de conocimiento y el que abrió por tanto las puertas a la investigación en los distintos ámbitos que marcaron sus autores (1, 2).
En dicho artículo los citados autores definen la ingeniería tisular como “un campo interdisciplinario que aplica los principios de ingeniería y ciencias de la vida al desarrollo de sustitutos biológicos que restauran, mantienen o mejoran la función de los tejidos o de un órgano completo”. Desde entonces los diferentes procedimientos, instrumentos, materiales y elementos celulares utilizados para la generación de tejidos artificiales han sido extraordinarios y las instituciones académicas, los sistemas asistenciales, la industria e incluso los gobiernos se han visto afectados por la presencia de esta nueva rama del saber no solo en lo que atañe al ámbito estrictamente científico y sanitario sino también al propiamente económico y regulatorio (3, 4, 5)
En el presente trabajo vamos a considerar la implementación de la ingeniería tisular en el ámbito de la Universidad y del Sistema de Salud en el contexto español y, en concreto, en relación con la experiencia desarrollada en la Universidad de Granada (UGR) y el Sistema Sanitario Público de Andalucía (SSPA). Aunque la vinculación de la ingeniería tisular con la industria será objeto de mención en el trabajo no constituye sin embargo un objetivo fundamental del mismo. El análisis que pretendemos ha de insertarse en lo que Miguel de Unamuno denomina la intrahistoria de un proceso, esto es el relato de aquello que ocurre pero que no aparece en la superficie de los acontecimientos, el análisis de aquellas condiciones que sin embargo son necesarias para que surjan los datos y los hechos que justifican la existencia de una determinada realidad (6); en nuestro caso, la presencia de la ingeniería tisular en el escenario científico de nuestro medio y de nuestro tiempo (7). En el trabajo nos ocuparemos en primer lugar de la Ingeniería tisular en la Universidad, en segundo lugar de la ingeniería tisular en el Sistema de Salud y en tercer lugar de la colaboración desarrollada entre ambos organismos para la implementación y desarrollo de dicha materia.
INGENIERÍA TISULAR Y UNIVERSIDAD
Tres son los retos que debe abordar la universidad en relación con la irrupción de la ingeniería tisular: un reto conceptual que permita su inserción en el contexto de la ciencia médica y la cultura de nuestro tiempo, un reto investigador que haga posible su avance y su progreso y, finalmente, un reto docente que permita a los alumnos adquirir los conocimientos, habilidades y destrezas necesarias en dicha materia para poder abordar conceptual y profesionalmente las numerosas demandas que en este ámbito han comenzado a generarse.
Reto conceptual y cultural
En el Departamento de Histología de la Universidad de Granada se asume a finales de los años noventa del pasado siglo el reto conceptual y cultural de incardinar la ingeniería tisular, generadora de tejidos artificiales, en el contexto de la ciencia histológica y en el contexto general de la ciencia médica y del resto de las ciencias de la salud. La primera aportación innovadora en esta orientación por parte del Departamento se produjo en el X congreso Nacional de Histología de Alicante celebrado en 1999 y dos años más tarde se explicitó en un capítulo del libro “Nuevos retos de la Docencia y la investigación en la Histología”, publicado en México en 2001 y editado por la Sociedad Mexicana de Histología (8). Con posterioridad el desarrollo conceptual tanto en su orientación básica como terapéutica se abordó en sendos discursos impartidos por el Profesor Antonio Campos, catedrático de histología de la Universidad de Granada: el discurso de Ingreso en la Real Academia Nacional de Medicina, en 2004, titulado “Cuerpo Histología y Medicina. De la descripción microscópica a la Ingeniería tisular” (9) y el Discurso de apertura de la Universidad de Granada, en 2013, titulado “La célula y el tejido como medicamento. De la médula ósea al Sistema Nervioso” (10). Más recientemente la aportación conceptual que incardina la ingeniería tisular en la ciencia histológica y a su través en la ciencia médica se ha completado con la defensa de una tesis doctoral (11) y la publicación de dos artículos de investigación bibliométrica en 2018 y 2019 en la revista Tissue Engineering (3, 12)
La aportación conceptual básica que permite insertar e incardinar la ingeniería tisular en el contexto cognitivo médico y universitario existente implica la aceptación de un cambio de paradigma para la ciencia histológica.
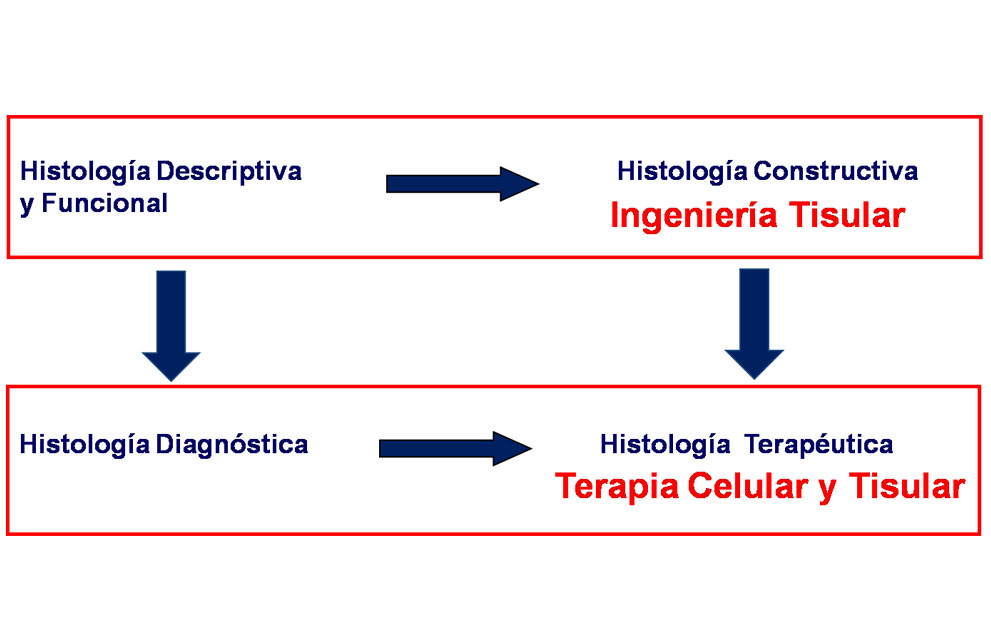
La histología desde su configuración como disciplina en el siglo XIX, se ha ocupado y ocupa del conocimiento de las estructuras corporales en los niveles de organización microscópicos y en los distintos estados euplásico, proplásico y retroplásico para ofrecer una aportación descriptiva y funcional que resulta decisiva para poder llevar a cabo el diagnostico microscópico de las lesiones (13) . La ingeniería tisular que se ocupa de la generación de tejidos artificiales sustitutos de los tejidos nativos ha dado origen a una nueva histología constructiva que, a su vez, conduce a una histología terapéutica y no solo a una histología diagnóstica (Fig. 1) . Por otra parte estos tejidos artificiales con función terapéutica, objeto de la nueva histología, se incardinan asimismo en el paradigma constructivo de la medicina para sustituir a las estructuras histológicas lesionadas a las que busca reemplazar al igual que sucede, por ejemplo, con el corazón o el hígado a nivel anatómico o con los genes a nivel molecular.
Para analizar la evolución conceptual y cognitiva de la ingeniería tisular se realizó una investigación bibliométrica de la producción global de documentos científicos en la base de datos de la web of Science entre 1991 y 2016 y una investigación de la estructura cognitiva de la ingeniería tisular mediante mapas con el programa SciMAT (3, 12). En el primer caso de los 41.588 documentos que recogen dicha denominación el 55.1% están relacionados con el ámbito de la tecnología y la ingeniería, el 27.26% con ciencias de la vida y biomedicina y un 17.64% con las ciencias físicas. En la última década se incrementan progresivamente los trabajos en el ámbito de la biomedicina más relacionados con las aplicaciones terapéuticas que los propiamente vinculados con los métodos de fabricación.
Durante el periodo analizado se observan variaciones entre distintos conceptos vinculados con la ingeniería tisular que pueden subdividirse en conceptos motores, emergentes, transversales o aislados. Sin embargo puede inferirse que en los tres vectores básicos de la ingeniería tisular -el celular, el de los biomateriales y el de los factores de crecimiento- existe una evolución muy definida (Fig.2) que debe tenerse en cuenta a la hora de establecer la orientación conceptual de la Ingeniería tisular de nuestro tiempo y su proyección en la investigación y la docencia universitaria.

Reto investigador
Resulta evidente que incorporar la ingeniería tisular en la Universidad implica asumir no solo el reto conceptual y cultural que ello supone, y hemos descrito en el apartado anterior, sino el reto investigador que asimismo lleva implícito. En este sentido el Departamento de Histología de la UGR, de cuya experiencia en este ámbito se está dando cuenta, conformó un grupo de investigación en ingeniería tisular (GIT) que inició, a finales de los años noventa del pasado siglo, una línea de investigación con dos grandes objetivos: la generación, por un lado, de tejidos artificiales biomiméticos con los tejidos nativos y el establecimiento, por otro, de los controles de calidad necesarios para su traslación a la clínica. En el primer caso y según el tejido artificial a construir se seleccionaron distintos tipos de células, diseñaron nuevos biomateriales y desarrollaron procesos de biofabricación innovadores con el fin de lograr los modelos de tejidos artificiales que tuvieran un mayor potencial terapéutico. En el segundo caso se investigaron nuevos protocolos de control calidad a nivel histológico, histoquímico, inmunohistoquímico, reológico, óptico y genético con el fin de garantizar la necesaria aprobación sanitaria para su uso clínico. En la actividad investigadora sobre algunos protocolos de calidad se ha requerido la colaboración de otros departamentos universitarios.
Fruto de esta actividad investigadora ha sido la generación de distintos tejidos artificiales como córnea (14) , piel (15, 16), mucosa oral (17), nervio periférico (18), paladar (19), cartílago (20), etc. utilizando distintos tipos celulares, biomateriales , procesos de biofabricación (21, 22, 23) y protocolos de control de calidad de los que se ha dado cuenta en publicaciones científicas (24, 25, 26, 27, 28, 29, 30).
Reto Docente
El reto docente para la universidad es transferir al alumnado del grado de medicina y del postgrado en ciencias de la salud y ciencias afines, formación en el ámbito de la ingeniería tisular y, por tanto, hacer posible el logro de competencias académicas básicas y profesionales, en su caso, para la utilización y aplicación de los contenidos vinculados a dicha materia. En el contexto de la reformas de planes de estudio que tuvo lugar en el tránsito del siglo XX al XXI, la Facultad de Medicina de la Universidad de Granada incorporó la formación en Ingeniería tisular como materia optativa asignando su enseñanza al Departamento de Histología, que desde entonces viene impartiendo dicha materia . En relación con el postgrado se aprobó asimismo un master oficial en Ingeniería tisular desde 1999 que igualmente viene impartiendo con regularidad dicha materia y en el que han participado como alumnos un elevado número de médicos residentes de especialidades, fundamentalmente médico-quirúrgicas, en cuyo horizonte terapéutico la ingeniería tisular esta cada vez más implicada. Más recientemente la materia ingeniería tisular se ha implantado en el grado de biotecnología aunque no en el de farmacia, grados ambos muy relacionados con la elaboración de los productos tisulares, especialmente en lo que se refiere a su elaboración con grado de calidad farmacéutica.
INGENIERÍA TISULAR Y SISTEMA DE SALUD
Los tejidos artificiales generados por ingeniería tisular han constituido desde su aparición, y su posterior eclosión mediática, un problema de salud de primer orden. Tres son, en este sentido, los retos que debe abordar un sistema de salud que pretenda afrontar con rigor la posible actividad terapéutica de dichos productos: identificar pertinentemente que tejidos artificiales pueden alcanzar la condición de medicamento, implementar su posible prestación asistencial en el contexto de las denominadas terapias avanzadas y, finalmente, garantizar la formación de profesionales especializados en dicha materia que puedan participar en su elaboración con grado de calidad farmacéutica y en su aplicación clínica y seguimiento.
Identificación de tejidos artificiales como medicamentos
El posible uso terapéutico de los tejidos artificiales elaborados por Ingeniería tisular fue objeto de extraordinario interés a partir de los años noventa del pasado siglo al generar grandes expectativas con las que abordar terapéuticamente problemas médicos carentes de solución o con muy limitada respuesta terapéutica (13, 31, 32). En relación con este tipo de terapia, junto a la aplicación de productos tisulares y celulares con eficacia clínicamente probada, se han aplicado también células madre y tejidos artificiales no probados ni aprobados, sin ninguna evidencia de seguridad o eficacia, en distintos países del mundo (33, 34). Este fenómeno que ha fomentado el conocido como turismo médico de terapias avanzadas o células madre ha sido y es todavía objeto de un gran debate y preocupación por parte de las autoridades sanitarias (35, 36).
En Europa hasta el año 2003 la utilización de células vivas para cualquier tipo de tratamiento se regulaba por la normativa utilizada para el trasplante sin que las células ni los tejidos tuviesen la consideración de medicamentos. A partir de entonces y debido a la publicación de la Directiva Europea 2003/63/EC (37), la legislación se modificó significativamente al establecer la normativa europea en qué casos las células y tejidos debían considerase o no medicamentos. (5, 10). Una importante contribución a dicha regulación fue la reunión de expertos y representantes gubernamentales organizada en España en 2002 con motivo de la Presidencia europea de la Unión bajo el titulo “Usos terapéuticos de células y tejidos en el marco comunitario”. En el momento presente y de acuerdo con la legislación europea vigente (38, 39) se identifican como medicamentos de terapias avanzadas la terapia génica, la terapia celular somática, los productos generados por ingeniería tisular y la combinación de ellas. Un producto de ingeniería tisular, que es el caso que nos ocupa, se considera medicamento cuando un conjunto determinado de células (autólogas o alogénicas) y biomoléculas (biomateriales y factores de crecimiento) son manipulados sustancialmente “ex vivo” para uso terapéutico y este está dirigido a regenerar, restaurar o reemplazar un tejido humano. Su utilización en seres humanos ha de regirse, además, por la misma legislación que rige la investigación, la autorización y la comercialización de los fármacos para uso humano.
Identificar los productos generados por ingeniería tisular que puedan ser potencialmente catalogados como medicamentos constituye sin duda una responsabilidad del sistema público de salud para poder garantizar una correcta aplicación terapéutica en este nuevo y emergente campo de la medicina.
Prestación del servicio asistencial
Las etapas para que un tejido artificial generado por ingeniería tisular pueda aplicarse como medicamento son cuatro (10, 40). La primera consiste en realizar una investigación preclínica pormenorizada de los mismos que garantice ex vivo e in vivo la idoneidad del producto con carácter previo a su aplicación; la segunda consiste en la aprobación del producto por la Agencia española del Medicamento y Productos Sanitarios (AEMPS) de acuerdo con los criterios establecidos por la Agencia Europea del Medicamento (EMA) para una indicación clínica concreta; la tercera consiste en la elaboración del producto en una instalación que cumpla las normas GMP (Good Manufacturing Practice) para la producción de medicamentos de terapia avanzada, la cual debe contar también con acreditación específica de la AEMPS para dicho producto y la cuarta consiste en la aplicación clínica por exención hospitalaria o tras superar un ensayo clínico. Este último debe contar con la autorización en su protocolo de los Comités Éticos de investigación clínica de los hospitales participantes y también, de nuevo, de la AEMPS previo informe preceptivo de la Organización Nacional de Trasplante.
Tras finalizar el ensayo clínico, el tejido artificial puede registrarse como medicamento de uso humano. Dicho registro no puede realizarse en ninguna agencia de los Estados Miembro de la Unión Europea sino que ha de seguir un procedimiento centralizado en la EMA y asimismo debe cumplimentarse un protocolo muy preciso en relación con la seguridad del producto, el control de su proceso de fabricación, y el resultado del ensayo clínico (5, 32).
En Andalucía para el desarrollo de estas nuevas terapias en el sistema de salud la Junta de Andalucía ha creado un organismo, la Iniciativa Andaluza en Terapias avanzadas (IATA)(actualmente denominado Red Andaluza de Diseño y Traslación de Terapias Avanzadas) que desde hace diez años viene implementando la traslación a la clínica de estas terapias (32).
Formación de profesionales especializados
Para el desarrollo de las actividades señaladas como la elaboración de los productos generados por ingeniería tisular en las instalaciones GMP, la capacitación en la posible aplicación de estas terapias por parte de facultativos de distintas especialidades y la educación sanitaria de la población en este campo, especialmente por los médicos de familia, es necesario desarrollar programas formativos específicos a distintos niveles (41, 42). En el primer caso, y de acuerdo con la normativa europea, es importante señalar que para la elaboración estos nuevos medicamentos tisulares son necesarios profesionales que posean una determinada cualificación específica como director técnico, responsable de control de calidad, responsable de producción y responsable de garantía de la calidad (43).
COLABORACIÓN UNIVERSIDAD Y SISTEMA DE SALUD
La nueva situación creada en las dos últimas décadas en las que conviven, por un lado, un desarrollo creciente de la investigación en ingeniería tisular, fundamentalmente en al ámbito universitario y, por otro, una demanda también creciente de aplicación terapéutica para estos productos, regulados solo muy recientemente en algunos países, exige la articulación de ambas realidades al mejor servicio de la sociedad. Ello es importante no solo por la significativa contribución económica que ello supone, sobre todo para la universidad y la sanidad pública, sino por la necesidad social de promover una accesibilidad equitativa por parte de los pacientes en el sistema público de salud. (41)
La experiencia de colaboración entre el Departamento de Histología de la UGR y su grupo de investigación GIT y el SSPA a través de la IATA ha resultado fructífera respecto a la ingeniería tisular en relación con los retos que tienen planteados ambos organismos y a los que se ha hecho referencia en apartados anteriores. Dicha colaboración puede esquematizarse del siguiente modo: aportación de la Universidad al Sistema de Salud, aportación del Sistema de Salud a la Universidad y aportación conjunta de ambos organismos.
Aportación de la Universidad al Sistema de Salud
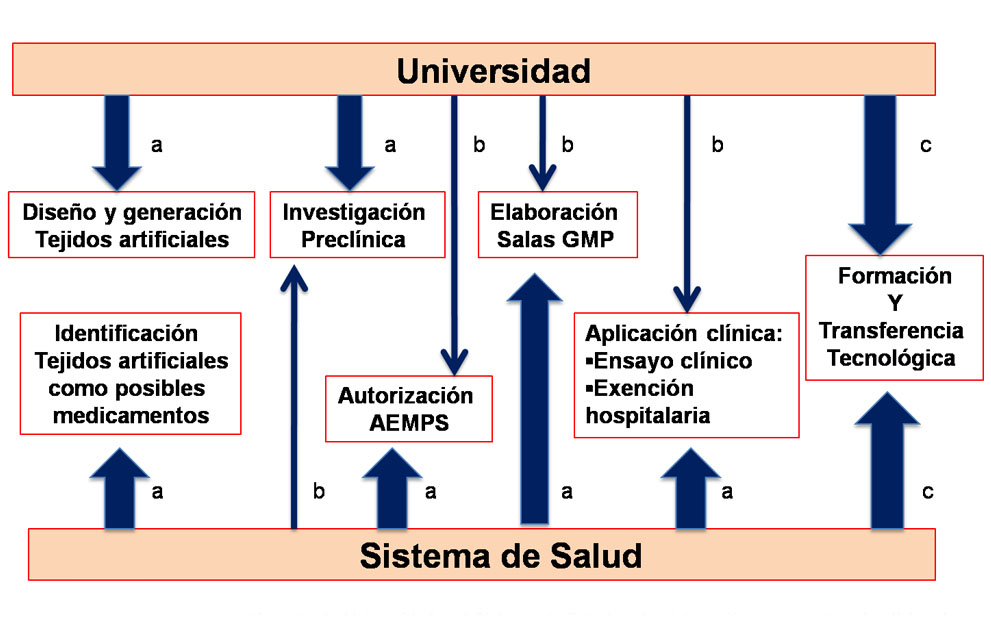
La UGR, a través de su Departamento de Histología y su grupo de investigación GIT, realiza su aportación al SSPA a tres niveles. En primer lugar proporciona, tras un largo proceso de investigación e innovación, nuevos modelos de tejidos artificiales biomiméticos susceptibles de posibles aplicaciones terapéuticas. En segundo lugar, aporta todo el desarrollo de la investigación preclínica ex vivo e in vivo imprescindible para la aprobación del producto como medicamento de terapia avanzada por la AEMPS, lo que exige una costosa investigación técnica y experimental y, en tercer y último lugar, aporta una triple colaboración en el proceso de traslación a la clínica: primero, en la participación de los investigadores como miembros del equipo de la IATA que elabora y debate los documentos a presentar con la AEMPS; segundo, en el asesoramiento, como diseñadores del prototipo, de su proceso de elaboración en grado de calidad farmacéutica en las instalaciones GMP y, tercero, participando en el ensayo clínico al realizar el control histológico tanto de los productos elaborados en la salas GMP como de las biopsias de control tras la implantación.
A nivel internacional es importante señalar que aunque la producción científica es muy elevada, con dos polos fundamentales en Estados Unidos y China como se deriva del estudio bibliométrico realizado (3), la transferencia a la clínica es escasa en relación con dicha producción al menos en lo que a ensayos clínicos se refiere pues solo se registran 84 en https://clinicaltrials.gov/ de los que 52 están vinculados a universidades.
Aportación del Sistema de Salud a la Universidad
El SSPA, a través de la IATA, realiza su aportación la Universidad a varios niveles. En primer lugar identificando los productos de ingeniería tisular que tras la investigación preclínica realizada en la Universidad pudieran transferirse a la clínica. En el caso que nos ocupa la IATA ha identificado hasta el presente tres productos del Departamento de Histología de la Universidad de Granada: la cornea artificial, actualmente en ensayo clínico; la piel, actualmente en uso por exención hospitalaria en grandes quemados y el paladar artificial en fase de aprobación por la AEMPS. (44). En segundo lugar, el SSPA, también a través de la IATA, lleva a cabo todo el procedimiento de solicitud y gestión documental para la autorización de los productos de ingeniería tisular por la AEMPS como ha ocurrido con los tres productos arriba indicados. En tercer lugar desde el SSPA se ha apoyado la generación e implementación de redes y consorcios para la captación de recursos de investigación por un lado y de Instalaciones GMP y equipos sanitarios del propio Sistema de Salud para desarrollar la transferencia mediante ensayo clínico o exención hospitalaria así como la tramitación que ello conlleva. En cuarto y último lugar la aportación se ha concretado en la búsqueda de nuevas aplicaciones para los productos generados en la Universidad. En este sentido el biomaterial desarrollado en el Departamento de Histología de la Universidad de Granada, ha sido utilizado por otros grupos vinculados al Sistema de Salud para nuevas aplicaciones por ejemplo en hemostasia, retina o vías biliares (45, 46)
Aportación conjunta de la Universidad y del Sistema de Salud
La aportación conjunta de ambos organismos se ha materializado en dos niveles. Por un lado en la generación de patentes conjuntas para la transferencia tecnológica y búsqueda de retornos. Hasta el presente en la colaboración que se analiza en el presente trabajo se han desarrollado siete patentes nacionales e internacionales. Por otro lado, la necesidad de formar profesionales especializados en las áreas anteriormente comentadas ha dado origen a la creación de un master conjunto de carácter profesional para la formación de dicho personal. El master que desde 2010 se imparte en ingles en la red con actividad presencial práctica se titula “Master in manufacturing advanced therapy medicinal products” y capacita para la obtención de las titulaciones requeridas por la normativa europea que son “qualified person”, “manufacturing manager” “quality control manager y “quality assurance manager”.En última edición el 47% han sido alumnos extranjeros procedentes de Europa, América, Asia y Oceanía y el 53% españoles procedentes de distintas comunidades autónomas.
Tras el análisis realizado puede afirmarse, en primer lugar, que la ingeniería tisular constituye, en el momento presente, una materia emergente que de acuerdo con su tasa de crecimiento se encuentra en fase de consolidación y que conceptualmente se inserta en la ciencia histológica, disciplina a la que aporta un nuevo paradigma; en segundo lugar, que la traslación a la clínica de los medicamentos generados por ingeniería tisular en Europa, Estados Unidos y algunos otros países, requiere la aplicación de una regulación muy estricta para su aprobación, elaboración y utilización terapéutica con el objeto de garantizar la seguridad clínica frente a aplicaciones indiscriminadas no probadas y, en tercer lugar, que la institucionalización para la transferencia clínica y formativa en ingeniería tisular entre las Universidades y los Sistema de Salud no está articulada, lo que posiblemente impide potenciar la transferencia y el desarrollo de unidades de producción para la aplicación terapéutica de estos medicamentos .
En el presente trabajo además de sistematizar la creciente presencia de la Ingeniería tisular en el ámbito universitario y en el ámbito sanitario se ha relatado la experiencia de colaboración en este campo entre un Departamento universitario, el de Histología de la Universidad de Granada y su grupo de investigación de ingeniería tisular, y el Sistema Sanitario Público de Andalucía y su organismo para las terapias avanzadas. En el mismo y con el objeto de estimular la necesaria articulación institucional en esta área científica y sanitaria, se describen las bases de dicha colaboración especificando las aportaciones de ambos organismos a las funciones de su contraparte y las actividades conjuntas que ambos organismos pueden ejecutar en el ámbito de la Ingeniería tisular para favorecer la traslación a la clínica como medicamentos de los tejidos artificiales generados.
BIBLIOGRAFÍA
- Langer R, Vacanti JP. Tissue engineering. Science 1993; 260: 920-926.
- Vacanti CA. The history of tissue engineering. J Cell Mol Med 2006; 10 (3): 569-576.
- Santisteban-Espejo A, Campos F, Martín-Piedra L et al. Global tissue engineering trends: a scientometric and evolutive study. Tissue Eng Part A 2018; 24(19-20): 1504-1517.
- Lysaght MJ, Nguy NA, Sullivan K. An economic survey of the emerging tissue engineering industry. Tissue Eng 1998; 4(3): 231-238.
- Cuende N, Izeta A. Clinical translation of stem cell therapies: a bridgeable gap. Cell Stem Cell 2010; 6(6): 508-512.
- Unamuno M de. En torno al casticismo. Madrid: Alianza Editorial; 2017.
- Cuende N, Rasko JEJ, Koh MBC, Dominici M, Ikonomou L. Cell, tissue and gene products with marketing authorization in 2018 worldwide. Cytotherapy 2018; 20(11): 1401-1413.
- Campos A. Histología médica: de la descripción microscópica a la ingeniería tisular. En: Uribe MC, Lorenzana MG, eds. Nuevos retos de la docencia y la investigación en histología. México: Sociedad Mexicana de Histología; 2001.
- Campos A. Cuerpo, histología y medicina : Discurso de ingreso. Madrid: Real Academia Nacional de Medicina; 2004.
- Campos, A. La célula y el tejido como medicamento : de la médula ósea al sistema nervioso: discurso de apertura Universidad de Granada, curso académico 2013-2014. Granada: Universidad de Granada; 2013.
- Santisteban-Espejo A. De la medicina descriptiva hacia la medicina constructiva: modelo de análisis bibliométrico en ingeniería tisular: tesis doctoral. Granada: Universidad de Granada; 2019.
- Santisteban-Espejo A, Campos F, Chato-Astrain J et al. Identification of cognitive and social framework of tissue engineering by science mapping analysis. Tissue Eng Part C Methods 2019; 25(1): 37-48.
- Campos A. Histología médica. Med Clinica-Barcelona 1985; 85: 63-65.
- Alaminos M, Sánchez-Quevedo MC, Muñoz-Avila JI et al. Construction of a complete rabbit cornea substitute using a fibrin-agarose scaffold. Invest Ophthalmol Vis Sci. 2006; 47(8): 3311-3317.
- Carriel V, Garzón I, Jiménez JM et al. Epithelial and stromal developmental patterns in a novel substitute of the human skin generated with fibrin-agarose biomaterials. Cells Tissues Organs 2012; 196(1): 1-12.
- Martín-Piedra MA, Alfonso-Rodríguez CA, Zapater A et al . Effective use of mesenchymal stem cells in human skin substitutes generated by tissue engineering. Eur Cell Mater 2019; 29(37): 233-249.
- Sánchez-Quevedo MC, Alaminos M, Capitán LM et al. Histological and histochemical evaluation of human oral mucosa constructs developed by tissue engineering. Histol Histopathol 2007; 22(6): 631-640.
- Carriel V, Scionti G, Campos F et al. In vitro characterization of a nanostructured fibrin agarose bio-artificial nerve substitute. J Tissue Eng Regen Med 2017; 11(5): 1412-1426.
- Liceras-Liceras E, Garzón I, España-López A et al. Generation of a bioengineered autologous bone substitute for palate repair: an in vivo study in laboratory animals. J Tissue Eng Regen Med 2017; 11(6): 1907-1914.
- García-Martínez L, Campos F, Godoy-Guzmán C et al. Encapsulation of human elastic cartilage-derived chondrocytes in nanostructured fibrin-agarose hydrogels. Histochem Cell Biol 2017; 147(1): 83-95.
- Scionti G, Moral M, Toledano M et al. Effect of the hydration on the biomechanical properties in a fibrin-agarose tissue-like model. J Biomed Mater Res A 2014; 102(8): 2573-2582.
- Campos F, Bonhome-Espinosa AB, García-Martínez L et al. Ex vivo characterization of a novel tissue-like cross-linked fibrin-agarose hydrogel for tissue engineering applications. Biomed Mater 2016; 11(5).
- Campos F, Bonhome-Espinosa AB, Vizcaino G et al. Generation of genipin cross-linked fibrin-agarose hydrogel tissue-like models for tissue engineering applications. Biomed Mater 2018; 13(2).
- Alaminos M, Sánchez-Quevedo MC, Muñoz-Avila JI et al. Evaluation of the viability of cultured corneal endothelial cells by quantitative electron probe X-ray microanalysis. J Cell Physiol 2007; 211(3): 692-698.
- Alaminos M, Garzón I, Sánchez-Quevedo MC et al. Time-course study of histological and genetic patterns of differentiation in human engineered oral mucosa. J Tissue Eng Regen Med 2007; 1(5): 350-359.
- Garzón I, Pérez-Köhler B, Garrido-Gómez J et al. Evaluation of the cell viability of human Wharton’s jelly stem cells for use in cell therapy. Tissue Eng Part C Methods 2012; 18(6): 408-419.
- Garzón I, Carriel V, Marín-Fernández AB et al. A combined approach for the assessment of cell viability and cell functionality of human fibrochondrocytes for use in tissue engineering. PLoS One 2012; 7(12): 51-61.
- Ionescu AM, de la Cruz Cardona J, González-Andrades M et al. UV absorbance of a bioengineered corneal stroma substitute in the 240-400 nm range. Cornea 2010; 29(8): 895-898.
- Chato-Astrain J, Campos F, Roda O et al. In vivo Evaluation of nanostructured fibrin-agarose hydrogels with mesenchymal stem cells for peripheral nerve repair. Front Cell Neurosci 2018;12: 501-520.
- Rodríguez IA, López-López MT, Oliveira AC et al. Rheological characterization of human fibrin and fibrin-agarose oral mucosa substitutes generated by tissue engineering. J Tissue Eng Regen Med 2012; 6(8): 636-644.
- Schneider CK, Salmikangas P, Jilma B et al. Challenges with advanced therapy medicinal products and how to meet them. Nat Rev Drug Discov 2010; 9(3): 195-201.
- Cuende N. Andalusian initiative for advanced therapies: Fostering synergies. Stem Cells Transl Med 2013; 2(4): 243-245.
- Zarzeczny A, Caulfield T, Ogbogu U et al. Professional regulation: a potentially valuable tool in responding to “stem cell tourism”. Stem Cell Reports 2014; 3(3): 379-384.
- Julian K, Yuhasz N, Hollingsworth E, Imitola J. The “growing” reality of the neurological complications of global “stem cell tourism”. Semin Neurol 2018; 38(2): 176-181.
- Gunter KC, Caplan AL, Mason C et al. Cell therapy medical tourism: Time for action. Cytotherapy 2010; 12(8): 965-968.
- Ogbogu U, Du J, Koukio Y. The involvement of Canadian physicians in promoting and providing unproven and unapproved stem cell interventions. BMC Med Ethics 2018; 19(1): 32-39.
- Directiva 2003/63/CE de la Comisión de 25 de junio de 2003, que modifica la Directiva 2001/83/CE del Parlamento Europeo y del Consejo por la que se establece un código comunitario sobre medicamentos para uso humano. Diario Oficial de la Unión Europea de 27 de junio de 2003.
- Directiva 2009/120/CE de la Comisión de 14 de Septiembre de 2009 que modifica la Directiva 2001/83/CE del Parlamento Europeo y del Consejo, por la que se establece el código comunitario sobre medicamentos para uso humano, en lo que se refiere a los medicamentos de terapia avanzada. Diario Oficial de la Unión Europea de 15 de Septiembre de 2009.
- Reglamento (CE) No 1394/2007 del Parlamento Europeo y del Consejo de 13 de Noviembre de 2007 sobre medicamentos de terapia avanzada y por el que se modifica la Directiva 2001/83/CE y el Reglamento (CE) no 726/2004. Diario Oficial de la Unión Europea de 10 de Diciembre de 2007.
- Pascual M. Regulatory aspects of human somatic cell therapy. En:. García-Olmo D, García-Verdugo JM, Alemany J et al, eds. Cell Therapy. Madrid : McGraw Hill; 2008.
- Sola García M. Identificación de actitudes y percepciones en médicos residentes y especialistas de medicina familiar y comunitaria para el diseño e implementación de programas de educación sanitaria en medicina regenerativa y terapias avanzadas : Tesis doctoral. Granada: Universidad de Granada; 2019.
- Sola M, Sánchez-Quevedo C, Martín-Piedra MA et al. Evaluation of the awareness of novel advanced therapies among family medicine residents in Spain. PLoS One 2019; 14(4).
- Directiva 2003/94/CE de la Comisión de 8 de octubre de 2003 por la que se establecen los principios y directrices de las prácticas correctas de fabricación de los medicamentos de uso humano y de los medicamentos en investigación de uso humano.
- Rico-Sánchez L, Garzón I, González-Andrades M et al. Successful development and clinical translation of a novel anterior lamellar artificial cornea. J Tissue Eng Regen Med 2019 Aug.
- Campos-Cuerva R, Fernández-Muñoz B, Farfán López F et al. Nanostructured fibrin agarose hydrogel as a novel haemostatic agent. J Tissue Eng Regen Med 2019; 13(4): 664-673.
- García Delgado AB, de la Cerda B, Alba Amador J et al. Subretinal Transplant of Induced Pluripotent Stem Cell-Derived Retinal Pigment Epithelium on Nanostructured Fibrin-Agarose. Tissue Eng Part A 2019; 25(9-10): 799-808.
DECLARACIÓN DE TRANSPARENCIA
El autor/a de este artículo declara no tener ningún tipo de conflicto de intereses respecto a lo expuesto en la presente revisión.
ranm tv
Antonio Campos
Real Academia Nacional de Medicina de España
C/ Arrieta, 12 · 28013 Madrid
Tlf.: +34 91 159 47 34 | acampos@ugr.es
Año 2019 · número 136 (02) · páginas 124 a 130
Enviado*: 07.05.19
Revisado: 12.05.19
Aceptado: 08.06.19
* Fecha de lectura en la RANM


