Resumen
El trasplante hepático ortotópico (THO) es el tratamiento de elección en hepatopatía crónica terminal y fallo hepático fulminante. Los excelentes resultados han llevado a un aumento de los pacientes en lista de espera, mientras que el número de donantes permanece estable. Por tanto, la principal limitación del THO es el acceso a un injerto hepático.
La manera de conseguir más injertos hepáticos es utilizar donantes marginales, grupo no bien definido donde se incluyen donantes >60 años, con hipernatremia o macroesteatosis hepática >30%, donantes con infección viral VHC o VHB, isquemia fría >12 h, donantes después de muerte circulatoria e injertos procedentes de bipartición hepática o donante vivo. Actualmente, la medida más práctica y frecuente para aumentar el número de injertos hepáticos, y así reducir la mortalidad en lista de espera, es utilizar los injertos de edad avanzada.
El objetivo de este trabajo es revisar el proceso de envejecimiento hepático y revisar las experiencias referidas en la literatura en cuanto a utilización de injertos añosos para ver si se debe establecer un límite de edad para THO.
Actualmente, hay suficientes estudios que acreditan el uso de injertos sexagenarios y septuagenarios para THO en comparación con donantes más jóvenes. Respecto al uso de donantes octogenarios hay menos experiencias y con menos casos, aunque su utilización está progresivamente aumentando por la necesidad de disminuir la mortalidad de los pacientes en lista de espera.
Para obtener buenos resultados utilizando injertos hepáticos sin límite de edad, debe hacerse una selección cuidadosa de los donantes (función hepática normal, buenas condiciones y estabilidad hemodinámica, estancia en UCI<72 h, isquemia fría <8 h, isquemia caliente <1 h, macroesteatosis <30%, ausencia de ateromatosis en arteria hepática y alteraciones histológicas), biopsia hepática en donantes >80 años y evitar implantar estos injertos en receptores con mala función hepática (puntuación MELD alta).
Abstract
Orthotopic liver transplantation (OLT) is the treatment of choice for patients with end-stage chronic liver diseases and acute liver failure. The excellent results of OLT have led to an increasing number of patients on the waiting list, while the number of liver donors remains stable. Thus, the main limitation of OLT is having access to a liver graft.
The way to get more liver grafts is to use marginal donors, a not well defined group where mainly are included donors > 60 years, donors with hypernatremia or macrosteatosis >30%, donors with HCV or HBV positive serologies, cold ischemia time >12 h, donors after circulatory death, and grafts from split-liver technique or living-related donation. At present, the most practical and frequent measure to increase the liver pool, and thus to reduce the waiting list mortality, is to use the older livers. The aim of this paper is to briefly review the aging process of the liver and reported experiences using old livers to see if there is a limit for using these aged grafts.
Currently, there are enough studies regarding the use of sexagenarian and septuagenarian donors that demonstrate similar results in comparison with the use of younger donors. With respect to the use of octogenarian donors there are less and short experiences, but their utilization is progressively increasing because of the necessity to decrease the waiting list mortality. In order to get good results using old liver grafts with no age limit, careful donor selection must be performed (normal liver function, hemodynamic and preharvesting good conditions, ICU <72 hours, CIT<8 hours, WIT<1 hour, macrosteatosis <30%, and absence of atherosclerosis in hepatic artery and histological alterations in biopsy), also avoiding recipient risk factors such as advanced liver disease (high MELD scores). A liver biopsy should be performed in octogenarian livers.
Palabras clave: Envejecimiento hepático; Donantes de edad avanzada; Donantes hepáticos octogenarios; Trasplante hepático.
Keywords: Liver aging; Old donors; Octogenarian liver donors; Liver transplantation.
INTRODUCCIÓN
El trasplante hepático ortotópico (THO) es el tratamiento de elección en pacientes con hepatopatía crónica en fase terminal, fallo hepático fulminante y varias enfermedades metabólicas. El problema actual sigue siendo la escasez de donantes, lo cual limita el acceso al trasplante y, por tanto, la mortalidad del candidato en lista de espera.
Por otro lado, los mejores resultados con el THO se obtienen cuando se utiliza un injerto ideal, es decir un donante <40 años, fallecido por un traumatismo craneoencefálico, estable hemodinámicamente en el momento de la extracción de órganos, y ausencia de esteatosis, hepatopatía crónica y enfermedad transmisible (1). Asumiendo estas características, el donante ideal es cada vez menos frecuente, fundamentalmente debido al progresivo y significativo descenso de los accidentes de tráfico. Así, en España, en el año 2000, el 22% de los donantes hepáticos habían fallecido por accidente de tráfico, mientras que en el 2017 solo lo hicieron el 4,7% (2).
Según el Registro Español de Trasplante Hepático, durante el año 2000, la edad media de los donantes hepáticos era de 47 años, mientras que el 2017 la edad media global fue de 60,8 años (2).
La escasez de órganos ha conducido a utilizar los donantes con criterios expandidos, también denominados marginales o subóptimos, donde normalmente se incluyen los donantes >60 años, con hipernatremia, esteatosis >30% o serologías positivas para VHC o VHB, injertos hepáticos con isquemia fría >12 horas, injertos procedentes de donantes en asistolia controlada o no controlada, injertos procedentes de bipartición hepática (split-liver) o de donante vivo (3-11).
La medida más frecuente y práctica para aumentar el número de injertos hepáticos es aumentar la edad del donante (4,12-16). No obstante, esta ampliación de la edad del injerto hepático para THO está sujeta a debate, en base a que varios grupos refieren un impacto negativo sobre la supervivencia del paciente con THO (17-20). Por otro lado, otros equipos de trasplante han obtenido similares resultados cuando utilizan injertos hepáticos >60 años, e incluso >70 y >80 años (13, 15, 21-26).
PROCESO DE ENVEJECIMIENTO DEL HÍGADO
El envejecimiento se caracteriza por un progresivo deterioro en las funciones que disminuye la capacidad de las células y órganos para responder a los estímulos intrínsecos y extrínsecos. Los cambios funcionales desarrollados en el proceso de envejecimiento van a desembocar en alteraciones significativas en la práctica clínica.
Los cambios sintéticos, excretores y metabólicos de la función hepática se asocian a la edad teniendo por tanto una influencia clínica relevante (27). Aunque el proceso de envejecimiento no causa la muerte, sí parece contribuir al inicio de las enfermedades, incluyendo las hepatopatías (28).
Los cambios fundamentales sobre el hígado relacionados con la edad son la reducción de la masa hepática y el flujo sanguíneo. No obstante, las principales diferencias con otros órganos y, por tanto, las mayores ventajas del hígado son el mantenimiento de una buena reserva funcional, capacidad regenerativa y buen flujo sanguíneo, argumentos de peso para la utilización de los injertos hepáticos de edad avanzada para THO (29, 30).
Cambios morfológicos
Los hígados añosos son de tamaño más pequeño, de coloración oscura, que generalmente presentan atrofia marrón, atribuible ésta a la acumulación de lipofucsina y fibrosis por engrosamiento de la cápsula de Glisson (30-32). Con la edad, en el hígado se presentan pocos cambios macroscópicos y microscópicos, siendo el más frecuente la disminución del peso (27).
En población sana, el hígado supone el 2,5% del peso total del cuerpo hasta los 50 años. Sin embargo, gradualmente el hígado es cada vez más pequeño, de modo que a los 90 años representa alrededor del 1,6% del peso total (33). Existen cambios de forma en la superficie hepática (surcos, protuberancias) debidos a la compresión de estructuras adyacentes (costillas) (33).
Cambios morfométricos y ultraestructurales
Mediante el examen de muestras de hígados humanos tomadas en autopsias, se ha observado un 60% de engrosamiento del endotelio y un 80% de descenso en el número de fenestraciones de células endoteliales con el aumento de la edad (34).
Con el envejecimiento se objetivan varios cambios morfológicos de los hepatocitos: aumento en el volumen medio y mayor variación en el tamaño de las células hepáticas, descenso del número de hepatocitos, aumento del tamaño del núcleo celular y del volumen del DNA nuclear. También hay un aumento de la aneuploidía y un descenso del número de mitocondrias aunque aumento en el volumen (35). Estos cambios morfológicos sugieren que los hepatocitos con el envejecimiento se hallan en estado hiperfuncionante posiblemente tratando de compensar su descenso absoluto en número (33). Mediante biopsia en sujetos sanos y con enfermedad hepática crónica, se ha observado una progresiva disminución en la longitud de los telómeros asociada al proceso de envejecimiento (36). Recientemente también se han identificado cambios en los sinusoides hepáticos probablemente relacionados con la edad que pueden repercutir sobre la función hepática (37).
Cambios en el volumen y flujo sanguíneo
Entre los 30 y los 100 años de edad se observa una pérdida de un tercio del volumen y del flujo sanguíneo hepático (31, 38). Este proceso comienza a los 25 años, a un ritmo de 0,3-1,5 por año (39), llegando a los 65 años hasta una reducción del 40-45% (40).
Este descenso del volumen y flujo sanguíneo asociado al envejecimiento contribuye a una caída en el aclaramiento de muchos fármacos cuyas farmacocinéticas se han alterado con la edad (31). La enfermedad ateroesclerótica oclusiva de las ramas arteriales viscerales de la aorta (tronco celiaco y ramas, arterias mesentéricas y renales) se presenta en el 2,6% de todos los casos, y tiende a localizarse en las vertientes proximal o media del lecho arterial, siendo quirúrgicamente abordable, pero no en ocasiones donde la ateroesclerosis se sitúa en la vertiente o trayecto distal (41) donde la arteria hepática puede estar afectada (42, 43).
Función sintética y cambios funcionales
La tasa global de síntesis de proteínas es <37% en personas entre 69-91 años en comparación con personas entre 20-23 años, y la síntesis hepática de los factores de coagulación presumiblemente empeora en pacientes añosos (33).
Parece ser que las pruebas de función hepática (bilirrubina, fosfatasa alcalina y transaminasas) no se alteran con la edad, y realmente reflejan más una lesión hepática que una marcada mala función (29, 33).
La pérdida de la masa hepática funcional quizás sea el cambio más importante del hígado en el proceso de envejecimiento normal, aunque los hepatocitos cambian poco (29). Así, parece que el envejecimiento tiene un efecto limitado sobre las funciones hepáticas, pero sí sobre la respuesta a los factores extrahepáticos (44), enfermedades o demandas metabólicas aumentadas ante las cuales la población envejecida tiene disminuida la capacidad de respuesta (29, 33). Una hipótesis defiende que mientras que los enzimas responsables del metabolismo normal o detoxificación son adecuados en el hígado añoso, el sistema es incapaz de responder al aumento de sobrecarga o estrés de un agente hepatotóxico externo (33). Por otro lado, el envejecimiento parece comprometer la regeneración hepática influenciando varias vías, siendo el resultado la reducción de la tasa de regeneración, pero no la capacidad de restaurar el órgano a su volumen original (45). El envejecimiento no aumenta la susceptibilidad a la lesión de hipoxia-reoxigenación en el hígado de rata, y aunque hay limitaciones de extrapolación al hombre, este hallazgo apoya la utilización de injertos añosos para THO en humanos (46).
EVALUACIÓN Y MANEJO DE LOS DONANTES HEPÁTICOS
La definición de injerto ideal es diferente a la de donante ideal. Así, el injerto ideal puede estar influenciado por variables que aparecen después de la extracción multiorgánica como el tiempo prolongado de isquemia fría (TIF) o isquemia caliente (TIC), injertos parciales o de bipartición (47). Los donantes se consideran marginales si tienen algún riesgo de función inicial pobre (FIP) o de fallo primario (FPI). La disfunción primaria se define como “pobre” función después del THO y el FPI como el injerto que fracasa en el mantenimiento de la vida del paciente durante la primera semana pos-THO, falleciendo o precisando un retrasplante para su supervivencia, habiendo previamente descartado factores extrahepáticos. Se define como FIP la presencia de GOT >2.000UI/l, tiempo de protrombina <16 segundos y nivel de amonio > 50 micmol/l entre los días 2-7 pos-THO en el contexto de mantenimiento de medidas de soporte (48).
Actualmente no hay una definición clara de donante hepático marginal. Entre los factores más importantes de los donantes que pueden influir sobre el desarrollo de FPI o FIP en el receptor se han señalado: edad avanzada del donante (>70-80 años), hipernatremia >155 mEq/l, macroesteatosis >30%, isquemia fría >12 horas, parada cardiaca, obesidad, elevación de transaminasas, hipotensión y uso de inotrópicos, estancia prolongada en UCI> 5 días, donantes de asistolia controlada o no controlada, injertos de donante vivo o de bipartición hepática (1, 3, 7, 49, 50-52).
Evaluación y soporte de los donantes de edad avanzada
Entre el 70-88% de los donantes mayores de 70 años fallecen por enfermedad cerebrovascular (13, 23, 53-55). Cuando se declara la muerte cerebral y se considera la donación hepática, el objetivo principal es el mantenimiento de la viabilidad de los órganos. Así, las medidas de protección del injerto hepático serán: resucitación cardiopulmonar en caso de parada cardiaca, mantenimiento de una circulación efectiva para prevenir la lesión de isquemia, terapia de la volemia para mantener una tensión arterial sistólica (TAS) o presión venosa central <10 cm de H2O, transfusión sanguínea cuando el hematocrito es <25%, oxigenación para mantener una presión arterial de O2 entre 70-100 y una saturación de O2 del 95%, prevención de la infección y mantenimiento de la normotermia y la diuresis > 1 ml/kg/h. Una TAS entre 80-100 mmHg, mantenida durante >1 hora, se considera por algunos autores como un criterio de donante marginal (13). Algunos grupos definen como criterio de marginalidad una dosis de dopamina >15 mcg/kg/min (13, 49). La parada cardiaca durante un periodo de 15 minutos no influye significativamente sobre la disfunción o FPI, aunque hay autores que no utilizan los injertos hepáticos de los donantes septuagenarios que han presentado parada cardiaca.
La estancia prolongada en UCI de los donantes puede modificar la función hepática debido a las alteraciones hemodinámicas, hormonales y nutricionales y las producidas por los fármacos vasopresores. Para algunos autores las tasas de FPI y disfunción del injerto aumentan a partir de una estancia media en UCI >3 días. Más recientemente, se ha considerado que una estancia en UCI >4 días constituye un criterio marginal debido a la asociación de una mayor tasa de lesión de preservación. Según varias series que han utilizado injertos hepáticos >70 años, la estancia media en UCI es >3,5 días (13,23,26,53,55). El mecanismo del efecto deletéreo de la hipernatremia (pico de Na>155 mEq/l) sobre la función del injerto se piensa que es por la inflamación celular y exacerbación de la lesión de isquemia-reperfusión (7). La hipernatremia se asocia a una marcada disfunción del injerto, e incluso se asocia con una supervivencia significativamente menor del injerto a 1 mes. No obstante, el sodio sérico del donante muestra valores normales en 5 series donde se han utilizado donantes >70 años (23,53, 55). La elevación de enzimas hepáticos (GOT, GPT y GGT) en donantes puede reflejar un proceso de citolisis, colostasis, hipoperfusión debida a la hipovolemia o parada cardiaca, y los niveles de enzimas hepáticos pueden alcanzar hasta 400 UI/l durante periodos cortos de asistolia o isquemia. Se han considerado criterios marginales la presencia de valores de GOT >150 UI/l y GPT >170 UI/l, y GGT >100 UI/l en donantes >70 años (13). En estudios donde se han utilizado injertos hepáticos de donantes >70 años los valores medios de GOT, GPT y GGT se hallan entre los límites normales (26,30,53,55). En ausencia de enfermedad hepato-biliar, la presencia de hiperbilirrubinemia en el donante puede ser debida a hemólisis, y no se ha demostrado que la bilirrubina >2 mg/dl se asocie a una menor supervivencia del injerto o disfunción en comparación con valores menores de bilirrubina (49). En varios trabajos publicados, los valores medios de bilirrubina de donantes >70 años oscilan entre 0,7-0,95 mg/dl (13,23,53,55). En series comparativas que analizan los donantes >70 años, los parámetros de función hepática son más favorables en donantes añosos, un hallazgo que refleja la selección meticulosa de estos donantes (23,30,53,55) para neutralizar los riesgos asociados al proceso de envejecimiento (55).
En el proceso de evaluación de los donantes >70 años se recomienda utilizar una ecografía para descartar enfermedades hepatobiliares benignas y malignas, esteatosis u otros tumores abdominales. Durante el proceso de extracción de órganos también es necesario explorar la cavidad abdominal para descartar tumores o abscesos. Se recomienda realizar una biopsia hepática en donantes octogenarios (30,53), así como en septuagenarios para excluir enfermedad hepática (esteatosis, colestasis, hepatitis o fibrosis).
La consideración de un injerto hepático como marginal en función de la edad avanzada ha cambiado en base a los mejores resultados por la experiencia acumulada relacionada con la selección y mantenimiento de los donantes en UCI, selección de receptores y cuidados posoperatorios, emparejamiento entre donante y receptor, manejo anestésico, técnica quirúrgica e introducción de inmunosupresores más potentes.
Esteatosis del injerto hepático
La esteatosis se clasifica como leve (10-30%), moderada (30-60%) y grave (>60%), pero se considera que puede desaparecer después del trasplante. La esteatosis hepática se asocia más frecuentemente al desarrollo de una lesión de preservación, recomendándose un tiempo corto de isquemia para prevenir dicha lesión.
Nosotros hemos observado una alta tasa de esteatosis en donantes >60 años, sobre todo a expensas de microesteatosis (55), aunque los injertos hepáticos con cualquier grado de microesteatosis aislada pueden utilizarse de forma segura debido a que no aumenta el riesgo de peor supervivencia del paciente o del injerto, exceptuando el riesgo inicial de disfunción (5). La experiencia del cirujano es esencial para la evaluación de la esteatosis durante la extracción del injerto, que tiene que confirmarse mediante examen histológico. Se ha observado que mediante la combinación del IMC, elevación de GOT, presencia de diabetes II, historia de consumo importante de alcohol y signos ecográficos, se puede identificar una esteatosis <30. El THO con injertos con macroesteatosis <30% tiene resultados similares a los obtenidos con injertos no esteatósicos, asumiendo la concomitante ausencia de otros factores de riesgo del donante o del receptor (3,7).
El implante de un injerto hepático con macroesteatosis moderada-grave precipita una lesión de isquemia-reperfusión grave situando al paciente en un riesgo aumentado de FIP (48), FPI y menor supervivencia del paciente y del injerto. Los injertos hepáticos con macroesteatossis >30% se pueden utilizar en pacientes con bajo riesgo, pero deben evitarse en pacientes con puntuaciones altas de MELD (Model for End-Stage Liver Disease). Otros investigadores refieren una supervivencia del paciente a 3 años comparable entre el grupo control de receptores y el de estudio de macroesteatosis >60%, concluyendo que los injertos con esteatosis grave deben considerarse para THO en pacientes de bajo riesgo, debiendo tener en cuenta un tiempo corto de isquemia y una optimización del manejo perioperatorio de los injertos esteatósicos.
En series de donantes >70 años, la incidencia de esteatosis oscila entre 16-50% y los hepatocitos están afectados en <30% de los casos (13,23,53-55). En todos los estudios de donantes octogenarios se evita el uso de injertos hepáticos con macroesteatosis >30% (14,24,30,53).
Tiempos de isquemia
La prolongación del TIF del hígado causa lesión microvascular, llamada lesión de isquemia-reperfusión (LIR), que puede llevar al FPI o FIP y aumento de la tasa de rechazo y morbilidad. La LIR del injerto hepático se desarrolla en 4 fases: lesión en el donante antes de la preservación, durante la preservación fría, recalentamiento y lesión de reperfusión. Hay una serie de factores relacionados con la historia médica del donante, tales como la edad >60 años, el tiempo prolongado en UCI, la ingesta de alcohol, consumo de drogas, esteatosis hepática, inestabilidad hemodinámica después de la muerte cerebral, hipotensión, dosis altas de fármacos inotrópicos, TIF prolongado y trauma quirúrgico durante el proceso de extracción de órganos (7). En series que comparan donantes menores y mayores de 65 años, no se ha observado un impacto significativo de la edad del donante o el TIF (< o >8 horas) sobre la incidencia de LIR, función hepática a corto plazo y supervivencia del paciente e injerto a 1 año. No obstante, se sabe que los receptores de injertos hepáticos añosos son proclives a la LIR, como se manifiesta por un notable patrón colostásico después del THO (23, 53). Por lo tanto, el TIF de los donantes añosos debe mantenerse lo más corto posible para conseguir una buena función pos-THO (13,53,55), entre 5-8 horas en series de donantes septuagenarios (23,26,53-55). Los injertos añosos con TIF >8 horas presentan mayor riesgo de FPI, siendo el doble cuando el TIF es >12 horas. La prolongación del tiempo de isquemia caliente (TIC) aumenta la lesión de isquemia fría y consecuentemente empeora la función hepática pos-THO. Se han referido efectos deletéreos sobre la supervivencia del injerto cuando el TIC es >45 minutos, pero habitualmente la mayoría de las series de donantes >70 años reportan un TIC medio entre 45-65 minutos (13,53,55).
Asignación de injertos hepáticos de edad avanzada a receptores
La puntuación MELD se ha utilizado como medida del riesgo de mortalidad en pacientes con enfermedad hepática terminal y se ha estimado adecuada como índice de gravedad ayudando a la prioridad en la distribución de los injertos hepáticos. La mortalidad en lista de espera aumenta proporcionalmente con la puntuación MELD. El implante de donantes marginales en receptores subóptimos constituye una mala combinación. Actualmente hay una cierta tendencia a implantar injertos hepáticos añosos en pacientes estables (7). Además, un donante octogenario puede implantarse en un receptor sexagenario, pero otros autores no aceptan su utilización en receptores infantiles.
Teniendo en cuenta que los pacientes más graves tienen que trasplantarse antes, los injertos hepáticos de donantes de alto riesgo deben utilizarse en receptores de bajo riesgo, mientras que los receptores de alto riesgo deben trasplantarse con injertos hepáticos de bajo riesgo. Hasta ahora, antes de la introducción de los nuevos antivirales para tratar el VHC, los injertos hepáticos de donantes jóvenes se utilizaban preferentemente para receptores VHC+, y los injertos añosos para receptores VHC-, en base a la peor supervivencia del paciente e injerto relacionadas con la recidiva del VHC cuando los injertos hepáticos eran >40-50 años, y los injertos >70 años eran trasplantados en receptores VHC+ (7,14,53), con la excepción de la serie de Doyle et al y nuestra propia serie (55) donde no hemos hallado diferencias significativas en términos de supervivencia del paciente e injerto, a 1, 3 y 5 años, entre los receptores VHC+ de injertos hepáticos <60 años y los receptores VHC+ de injertos >60 años. No obstante, la tendencia de nuestro estudio es al descenso de la supervivencia del paciente a 5 años, teniendo en cuenta que nuestra tasa de pacientes VHC+ era significativamente más alta en receptores de donantes >60 años (55). Desde la introducción de los antivirales para tratar el VHC, el escenario ha cambiado radicalmente en cuanto a la utilización de injertos añosos en receptores con cirrosis por VHC, ya que con el tratamiento antiviral, antes o después del THO, la tasa de recidiva es <5%, con lo cual es factible la generalización del uso de injertos añosos en cualquier tipo de receptor, sea o no portador del VHC+.
En algunas series el hepatocarcinoma y la cirrosis etílica fueron las indicaciones más frecuentes de trasplante donde se utilizaron injertos hepáticos >70 años (13,27). Por otro lado, las puntuaciones de MELD han sido similares en las diferentes series donde se han utilizado donantes >70 años (26,55).
EVOLUCIÓN POSTRASPLANTE Y COMPLICACIONES EN RECEPTORES DE INJERTOS HEPÁTICOS DE EDAD AVANZADA
La incidencia de FPI se ha reportado entre 2,7-8% en 5 series de receptores de donantes >70 años (13,54), mientras que en otras 4 series no se observó ningún caso de FPI (23,26,55).
La colostasis no relacionada con el rechazo pos-THO se ha observado significativamente más frecuente en receptores de donantes >70 años en comparación con los receptores de donantes más jóvenes (23). Los parámetros de síntesis (albúmina sérica y tiempo de tromboplastina) se normalizan a la semana del THO, mientras que los parámetros de función hepática (GOT,GPT) y la bilirrubina presentan valores normales a los 3 meses del trasplante. En nuestra experiencia, los valores séricos de GOT, GPT, GGT y bilirrubina, al mes del THO, fueron similares en receptores de donantes jóvenes y en receptores de donantes >70 años. Además, la actividad de protrombina y niveles de albúmina sérica fueron significativamente menores al mes del THO en receptores de donantes >70 años (55), y estos hallazgos se atribuyen a un descenso de la síntesis de proteínas y factores de coagulación que corren paralelos al proceso de envejecimiento hepático.
La estancia en UCI (entre 4-7 días) y hospitalaria (entre 20-25 días) fueron similares entre receptores de donantes jóvenes y >70 años (23,53,55). Igualmente, las tasas de rechazo agudo y crónico no son diferentes entre receptores de donantes mayores y <70 años (23,53).
En varios estudios no se han observado diferencias en la tasa de complicaciones biliares o de la arteria hepática (23,53), aunque recientemente se ha publicado un aumento significativo de la tasa de lesiones de isquemia en los receptores de donantes >70 años. En una publicación americana reciente (United Network Organ Sharing) se ha detectado que el riesgo de pérdida del injerto por trombosis de la arteria hepática (TAH) aumenta progresivamente con cada década de edad del donante >50 años (riesgo aumentado del 61% de pérdida del injerto relacionada con la TAH asociada al uso de donantes >70 años). Recientemente, una experiencia con donantes >70 años ha reportado una baja incidencia de TAH (4,7%), atribuyéndose la mejora de resultados a un apropiado manejo técnico, mientras que las variaciones anatómicas y el uso de injertos arteriales han constituido factores de riesgo independientes de la TAH.
La incidencia de infecciones es similar o incluso menor en receptores de injertos hepáticos >70 años(55). La mayoría de los estudios presentan similares tasas de retrasplante comparando los receptores de donantes >70 años con los de donantes más jóvenes(13,23,55).
Las causas más frecuentes de mortalidad en receptores de donantes >70 años se relacionan con complicaciones médicas, tumores de novo y cirrosis por recidiva del VHC(53,55).
SUPERVIVENCIA DEL PACIENTE E INJERTO EN RECEPTORES DE INJERTOS HEPÁTICOS DE EDAD AVANZADA
Receptores de injertos hepáticos menores de 70 años
En los años 90, los injertos hepáticos >50 años se consideraban añosos o de edad avanzada. Con la experiencia, en varios estudios comparativos entre receptores de injertos mayores y menores de 50 años se demostró que no había diferencias significativas entre ambos grupos respecto a las tasas de FPI, retrasplante y supervivencia del paciente e injerto.
Las dos primeras series comparativas utilizando injertos hepáticos >60 años mostraron una supervivencia del injerto al año, y a 2 años significativamente menor en receptores de injertos añosos, la cual fue atribuida a la más frecuente lesión de isquemia en dicho grupo(12). En dos series posteriores comparando receptores de injertos hepáticos mayores y menores de 60 años, las tasas de supervivencia del paciente y del injerto, FPI y disfunción del injerto fueron similares en ambos grupos con una oscilación del TIF entre 5-6,3 horas (22). Se ha establecido que el TIF prolongado empeora la función del injerto, y cuando este tiempo es >14 horas la lesión de preservación del injerto se duplica.
En una serie comparativa de 5 grupos dividida según la edad de los donantes (<50 años; entre 50-59 años; entre 60-69 años; entre 70-79 años; y > 80 años), los factores predictivos de supervivencia del injerto fueron: edad del donante entre 60-79 años, pacientes VHC+, MELD >25 y urgencia del trasplante(26).
En dos estudios comparativos utilizando injertos hepáticos mayores y menores de 65 años, la supervivencia del injerto fue menor en el grupo de receptores de injertos >65 años y la tasa de disfunción del injerto fue más alta cuando el injerto presentaba esteatosis. Sin embargo, dos recientes experiencias utilizando injertos mayores y menores de 65 años no han hallado diferencias significativas entre los grupos en cuanto a la supervivencia del paciente e injerto. Estas y otras experiencias que han utilizado injertos hepáticos >60 años se muestran en la Tabla 1 (12,15,20,22,55).

Receptores de injertos hepáticos mayores de 70 años
La mayoría de los autores concluye que la utilización de los injertos hepáticos procedentes de donantes septuagenarios no constituye per se una contraindicación de uso para THO(13,23,26,54,55). No obstante, un número menor de estudios refieren peor supervivencia del paciente y del injerto cuando se utilizan este tipo de injertos(19). (Tabla 2).

La solución para obtener buenos resultados cuando se utilizan injertos >70 años es realizar una buena selección, evitando en lo posible el uso de injertos con criterios de marginalidad en receptores de riesgo (edad avanzada, enfermedad renal, cirrosis VHC, retrasplante), relacionados con aumento de la pérdida del injerto y mortalidad (14,23,54,55). Cuando se utilizan injertos hepáticos >70 años en receptores seleccionados (primer trasplante, BMI<35, TIF<8 horas y hepatocarcinoma u otra indicación diferente a la cirrosis por VHC), los resultados son similares a los obtenidos con injertos hepáticos más jóvenes)(25).
La utilización de injertos hepáticos >70 años conlleva una supervivencia del paciente al año entre 66-95,4%, a los 3 años entre 57,5-90,6% y a los 5 años entre 46,2-84 % (13,23,25,26,55). Asimismo, la supervivencia del injerto al año varía entre 73,9-92,6%, a los 3 años entre 64,6-89,4% y a los 5 años entre 40,7-79% (13,23,25,26).
Receptores de injertos hepáticos mayores de 80 años
Desde el primer injerto hepático de 86 años utilizado para trasplante, se han publicado varias series de donantes octogenarios(24,26,30) (Tabla 3), e incluso casos aislados de injertos hepáticos nonagenarios. Las enfermedades cerebrovasculares son las causas de exitus entre el 73-81,7% de los donantes octogenarios (26,53). Los criterios generales de aceptación de los donantes octogenarios son: aspecto macroscópico y consistencia normales, no alteración de los parámetros de función hepática, estabilidad hemodinámica con utilización de bajas dosis de vasopresores (<10 mcg/kg/min) antes de la extracción de órganos, estancia en UCI <3 días, ausencia de alteraciones histológicas relevantes en la biopsia pretrasplante, tales como fibrosis, hepatitis, colestasis, macroesteatosis (<30%) y TIF <10 horas (30,53). Generalmente, se recomienda realizar una biopsia hepática antes de aceptar el injerto hepático para trasplante (14,26,30).
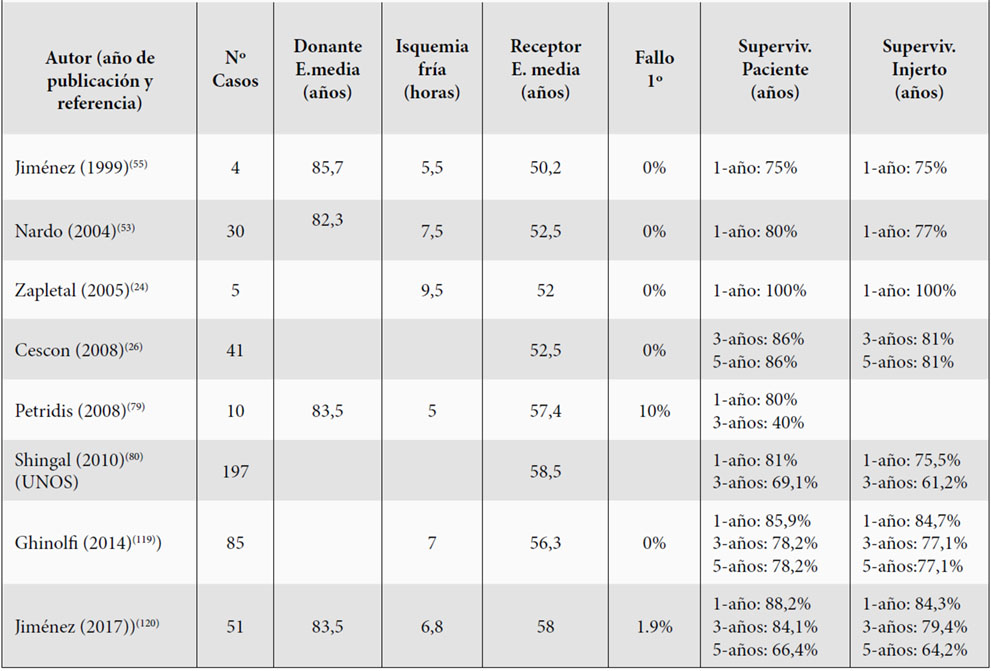
La tasa de descarte de injertos hepáticos octogenarios para THO es significativamente más alta que entre los donantes más jóvenes y las principales razones son la esteatosis moderada-masiva, cirrosis por VHC y tumores(53). En series comparativas de donantes octogenarios frente a donantes de menor edad no se han observado diferencias significativas con respeto a la estancia en UCI >5 días, IMC >35, utilización de noradrenalina, prevalencia de esteatosis, bilirrubina total, alteración de la función hepática, sodio sérico, episodios de hipotensión o uso de vasopresores(26,53).
Recientemente, otras 2 series con utilización de injertos hepáticos de donantes octogenarios, la de Ghinolfi et al, con 85 casos y la nuestra de 51 casos, no han hecho sino confirmar los resultados expuestos previamente con menos casos. Al cabo del mes del THO, al comparar receptores de donantes <65 años frente a receptores de donantes >80 años, no se observan diferencias significativas en cuanto a los parámetros de función hepática (bilirrubina, transaminasas, actividad de protrombina y albumina).
Antes de la introducción de los nuevos fármacos anti-VHC (sofosbuvir, daclatasvir, ledipasvir, ombitasvir), la utilización de los injertos hepáticos añosos, fundamentalmente mayores de 65 años, en receptores con cirrosis por VHC se asociaba a una alta incidencia de recurrencia de la hepatitis VHC, motivo por el cual dichos injertos se implantaban preferentemente en receptores con hepatocarcinoma o cirrosis etílica, evitando el VHC (26). El escenario ha cambiado radicalmente, ya que la utilización de injertos de donantes añosos en receptores con cirrosis por VHC tratados con dichos antivirales, antes o después del trasplante, se asocia a una tasa de recidiva del VHC menor del 5%. Por tanto, actualmente puede ampliarse su utilización en receptores por cirrosis VHC.
En las series publicadas, la utilización de injertos hepáticos octogenarios se ha asociado a una supervivencia actuarial del paciente a 1 año entre 75-100%, a 3 años entre 40-86% (24,26,30,53), y a 5 años entre 66,4-86% (26), mientras que la supervivencia actuarial del injerto a 1 año se ha reportado entre 75-100 %, a 3 años entre 61,2-81 % (24,26,30,53), y a 5 años entre 64,2-81% (26).
Se ha especulado sobre la “fecha de caducidad” del injerto hepático. En nuestra experiencia hemos observado que 4 injertos octogenarios implantados en otros 4 pacientes han superado la barrera de los 100 años. Esto confirma la excelente reserva funcional del hígado en comparación con otros órganos.
CONCLUSIONES
En base a lo anteriormente referido, creemos que los injertos hepáticos octogenarios, después de una selección cuidadosa, podrán utilizarse en cualquier receptor incluyendo los receptores con cirrosis por VHC, siempre que los receptores no presenten un deterioro grave de la función hepática y sean tratados antes o después del THO con los nuevos antivirales.
ABREVIATURAS
FIP: Función inicial pobre
FPI: Fallo primario del injerto
GGT: Gamma glutamil transaminasa
GOT: Glutámico oxaloacético transferasa
GPT: Glutámico pirúvico transpeptidasa
IMC: Indice de masa corporal
LIR: Lesión de isquemia-reperfusión
MELD: Model for End Liver Disease
TAH: Trombosis de arteria hepática
TAS: Tensión arterial sistólica
THO: Trasplante hepático ortotópico
TIC: Tiempo de isquemia caliente
TIF: Tiempo de isquemia fría
UCI: Unidad de cuidados intensivos
VHB: Virus de la hepatitis B
VHC: Virus de la hepatitis C
BIBLIOGRAFÍA
- Feng S, Goodrich NP, Bragg-Gresham JL, et al. Characteristics associated with liver graft failure: the concept of a donor risk index. Am J Transplant 2006;6:783-790.
- Dossier del Registro Español de Trasplante Hepático 2017 (ONT) http://www.ont.es
- Strasberg SM, Howard TK, Molmenti EP, Hertl M. Selecting the donor liver: risk factors for poor function after orthotopic liver transplantation. Hepatology 1994;20:829-838.
- Adam R, Sánchez C, Astarcioglu I, Bismuth H. Deleterious effect of extended cold ischemia time on the posttransplant outcome of aged livers. Transplant Proc 1995; 27:1181-1183.
- Ureña MAG, Colina F, Moreno E, et al. Assessing risk of the use of livers with macro and microsteatoosis in a liver transplant program. Transplant Proc 1998;30:3288-3291.
- López-Navidad A, Caballero F. Extended criteria for organ acceptance. Strategies for achieving organ safety and for increasing organ pool. Clin Transplant 2003,17:308-324.
- Busuttil RW, Tanaka K. The utiliy of marginal donors in liver transplantation. Liver Transplant 2003;9:651-663.
- Yersiz H, Renz JF, Farmer DG, Hisatake GM, McDiarmid SV, Busuttil RW. One-hundred in situ split-liver transplantation: A single center experience. Ann Surg 2003; 238:496-505.
- Renz JF, Kin C, Kinkhabwala M, et al. Utilization of extended donor criteria liver allografts maximizes donor use and patient access to liver transplantation. Ann Surg 2005;242:556-565.
- Tector AJ, Mangus RS, Chestovich P, et al. Use of extended criteria livers decreases wait time for liver transplantation without adversely impacting posttransplant survival. Ann Surg 2006;244:439-450.
- Bernat JL, D’Alessandro AM, Port FK, et al. Report of a National Conference on Donation after cardiac death. Am J Transplant 2006;6:281-291.
- Marino IR, Doyle HR, Doria C, et al. Outcome of liver transplantation using donors 60 to 79 years of age. Transplant Proc 1995;27:1184-1185.
- Emre S, Schwartz ME, Altaca G, et al. Safe use of hepatic allograft from donors older than 70 years. Transplantation 1996;62:62-65.
- Cescon M, Grazi GL, Ercolani G, et al. Long-term survival of recipients of liver grafts from donors older than 80 years: is it achievable? Liver Transpl 2003;9:1174-1180.
- Anderson CD, Vachharajani N, Doyle M, et al. Advanced donor age alone does not affect patient or graft survival after liver transplantation. J Am Coll Surg 2008;207:847-852.
- Ravaioli M, Grazi GL, Cescon M, et al. Liver transplantation with donors aged 60 years and above: the low liver damage strategy. Transplant Int 2009;22:423-433.
- Marino IR, Doyle HR, Aldrighetti L, et al. Effect of donor age and sex on the outcome of liver transplantation. Hepatology 1995;22:1754-1762.
- Hoofnagle JH, Lombardero M, Zetterman RK, et al. Donor age and outcome of liver transplantation. Hepatology 1996;24:89-96.
- Busquets J, Xiol X, Figueras J, et al. The impact of donor age on liver transplantation: influence of donor age on early liver function and on subsequent patient and graft survival. Transplantation 2001;71:1765-1771.
- Moore DE, Feurer ID, Speroff T, et al. Impact of do nor, technical, and recipient risk factors on survival and quality of life after liver transplantation. Arch Surg 2005;140:273-277.
- Grande L, Matus D, Rimola A, et al. Expanded liver donor age over 60 years for liver transplantation. Clin Transplant 1998;12:297-301.
- Rodríguez F, Jiménez C, Romano D, et al. Orthotopic liver transplantation with 100 hepatic allografts from donors over 60 years old. Transplant Proc 2002;34:233-234.
- Gastaca M, Valdivieso A, Pijoan J, et al. Donors older than 70 years in liver transplantation. Transplant Proc 2005;37:3851-3854.
- Zapletal C, Faust D, Wullstein C, et al. Does the liver ever age? Results of liver transplantation with donors above 80 years of age. Transplant Proc 2005;37:1182-1185.
- Segev DR, Maley WR, Simpkins CE, et al. Minimizing risk associated with elderly liver donors by matching to preferred recipients. Hepatology 2007;46:1907-1918.
- Cescon M, Grazi GL, Cucchetti A, et al. Improving the outcome of liver transplantation with very old donors with updated selection and management criteria. Liver Transpl 2008;14:672-679.
- Mooney H, Roberts R, Cooksley WGE, Halliday JW, Powell LW. Alterations in the liver with ageing. Clin Gastroenterol 1985; 14:757-71.
- Schmucker DL. Age-related changes in liver structure and function: Implications for disease? Exp Gerontol 2005;40:650-659.
- Winne HA, James OFW. The ageing liver. Comentary. Age Ageing 1990; 19:1-3.
- Jiménez C, Moreno E, Colina F, et al. Use of octogenarian livers safely expands the donor pool. Transplantation 1999; 68:572-576.
- Winne HA, Cope LH, Mutch E, Rawlins MD, Woodhouse KW, James OFW. The effect of age upon liver volume and apparent liver blood flow in healthy man. Hepatology 1989;9:297-301.
- Jung T, Bader N, Grune T. Lipofuscin: formation, distribution, and metabolic consequences. Ann NY Acad Sci 2007;1119:97-111.
- James OFW. Gastrointestinal and liver function in old age. Clin Gastroenterol 1983; 12:671-89.
- McLean AJ, Cogger VC, Chong GC, et al. Age-related pseudocapillarization of the human liver. J Pathol 2003;200:112-117.
- Watanabe T, Tanaka Y. Age-related alterations in the size of human hepatocytes. A study of mononuclear and binucleate cells. Virchows Arch (Cell Pathol) 1982;39:9-20.
- Aikata H, Takaishi H, Kawakami Y, et al. Telomere reduction in human liver tissues with age and chronic inflammation. Exp Cell Res 2000;256:578-582.
- Le Couteur DGL, Warren A, Cogger VC, et al. Old age and the hepatic sinusoid. Anat Rec 2008;291:672-683.
- Regev A, Schiff ER. Liver disease in the elderly. Gastroenterol Clin North America 2001;30:547-563.
- Landowne M, Stanley J. Aging of the cardiovascular system. In: Shock NW, editor. Aging some social and biological aspects. Washington: American Association for the advancement of the Science 1960;159-187.
- Bender AD. The effect of increasing age on the distribution of peripheral blood in man. J Am Geriatr Soc 1965;13:192-198.
- DeBakey ME, Lawrie GM, Glaeser DH. Patterns of atheroesclerosis and their surgical significance. Ann Surg 1985;101:115-131
- Sato T, Miwa T, Tauchi H. Age changes in the human liver of the different races. Gerontologia 1970;16:368-380.
- Findor J, Pérz V, Igartua EB, Giovanetti M, Fiovaranti N. Structure and ultrastructure of the liver in aged persons. Acta Hepatogastroenterol 1973;20:200-204.
- Popper H. Coming of age. Hepatology 1985;5:1224-1226.
- Schmucker DL, Sanchez H. Liver regeneration and aging: A current perspective. Curr Gerontol Geriatr Res 2011;2011:526379:1-8
- Le Couteur DG, Rivory LP, Pond SM. The effects of aging nutritional state on hipoxia-reoxygenation injury in the perfused rat liver. Transplantation 1994;54:531-536.
- Durand F, Renz JF, Alkofer B, et al. Report of the Paris consensus meeting on expanded criteria donors in liver transplantation. Liver Transpl 2008;14:1694-1707.
- Ploeg RJ, D’Alessandro AM, Knechtle SJ, et al. Risk factors for primary dysfunction after liver transplantation: a multivariate analysis. Transplantation 1993;55:807-813.
- Mor E, Klintmalm GB, Gonwa TA, et al. The use of marginal donors for liver transplantation. Transplantation 1992; 53:383-386.
- Mirza DF, Gunson BK, Da Silva RF, Mayer AD, Buckels JA, McMaster P. Policies in Europe on marginal quality donor livers. Lancet 1994;344:1480-1483.
- Cameron AM, Ghobrial RM, Yersiz H, et al. Optimal utilization of donor grafts with extended criteria. A single-center experience in over 1000 liver transplants. Ann Surg 2006;243:748-755.
- Briceño J, Solórzano G, Pera C. A proposal for scoring marginal liver grafts. Transpl Int 2000;13 (Suppl 1):S249-S252.
- Nardo B, Masetti M, Urbani L, et al. Liver transplantation from donors aged 80 years and over: pushing the limit. Am J Transplant 2004; 4:1139-1147.
- Kim DY, Cauduro SP, Bohorquez HE, Ishitani MB, Nyberg SL, Rosen CB. Routine use of livers from deceased donors older than 70: is it justified? Transplant Int 2005; 18:73-77.
- Jiménez-Romero C, Clemares M, Manrique A, García-Sesma A, Calvo J, Moreno E. Long-term results using old liver grafts for transplantation: sexagenarian versus liver donors older than 70 years. World J Surg 2013;37:2211-2221.
- Briceño J, Marchal T, Padillo J, Solórzano G, Pera C. Influence of marginal donors on liver preservation injury. Transplantation 2002; 74:522-6.
- Busuttil RW, Shaked A, Millis JM, et al. One thousand liver transplants. The leasons learned. Ann Surg 1994;219:490-499.
- Darius T, Monbaliu D, Jochmans I, et al. Septuagenarian and octogenarian donors provide excellent liver grafts for transplantation. Transplant Proc 2012;44:2861-2867.
- Novitzky D, Cooper DKC, Wicomb WN. Endocrine changes and metabolic responses. Transplant Proc 1988;20(Suppl 7):33-38.
- Greig PD, Forster J, Superina RA, et al. Donor-specific factors predict graft function following liver transplantation. Transplant Proc 1990;22:2072-2073.
- Fouzas I, Sgourakis G, Nowak KM, et al. Liver transplantation with grafts from septuagenarians. Transplant Proc 2008;40:3198-3200.
- Lai Q, Melandro F, Sandri GBL, et al. Use of elderly donors for liver transplantation: has the limit been reached. J Gastrointestin Liver Dis 2011;20:383-387.
- Avolio AW, Agnes S, Magalini SC, Foco M, Castagneto M. Importance of donor blood chemistry data (AST, serum sodium) in predicting liver transplant outcome. Transplant Proc 1991;23:2451-2452.
- González FX, Rimola A, Grande L, et al. Predictive factors of early postoperative graft function in human liver transplantation. Hepatology 1994;20:565-573.
- Figueras J, Busquets J, Grande L, et al. The deleterious effect of donor high plasma sodium and extended preservation in liver transplantation. Transplantation 1996;61:410-413.
- Klintmalm GBC. The liver donor: especial considerations. Transplant Proc 1988;20(Suppl 7):9-11.
- Markin RS, Wisecarver JL, Radio SJ, et al. Frozen section evaluation of donor livers before transplantation. Transplantation 1993;56:1403-1409.
- Karayalcin K, Mirza DF, Harrison RF, et al. The role of dynamic and morphological studies in the assessment of potencial liver donors. Transplantation 1994;57:1323-1327.
- D´Alessandro AM, Kalayoglu M, Sollinger HW, et al. The predictive value of donor liver biopsies on the development of primary nonfunction after orthotopic liver transplantation. Transplantation 1991;51:157-163.
- García-Ureña MA, Colina F, Moreno E, et al. Hepatic steatosis in liver transplant donors: common feature of donor population? World J Surg 1998;22:837-844.
- Adam R, Astarcioglu I, Azoulay D, et al. Age greater than 50 years is not a contraindication for liver donation. Transplant Proc 1991; 23:2602-2603.
- Fishbein TM, Fiel MI, Emre S, et al. Use of livers with microvesicular fat safely expands the donor pool. Transplantation 1997;64:248-251.
- Verran D, Kusyk T, Painter D, et al. Clinical experience gained from the use of 120 steatotic donor livers for orthotopic liver transplantation. Liver Transpl 2003; 9:500-505.
- Cucchetti A, Vivarelli M, Ravaioli M, et al. Assessment of donor steatosis in liver transplantation : is it possible without liver biopsy? Clin Transplant 2009;23:519-524.
- Moreno C, Jiménez C, Moreno E, et al. Disfunción primaria del injerto en el trasplante hepático ¿Es posible predecir esta complicación? Rev Esp Enferm Dig 1999;91:401-410.
- McCormack L, Petowsky H, Jochun W, Mullhaupt B, Weber M, Clavien PA. Use of severely steatotic grafts in liver transplantation. A matched case-control study. Ann Surg 2007;246: 940-948.
- Deroose JP, Kazemier G, Zondervan P, Ijzermans JNM, Metselaar HJ, Alwayn PJ. Hepatic steatosis is not always a contraindication for cadaveric transplantation. HPB 2011; 13:417-425.
- Nocito A, El-Bardy AM, Clavien PA. When is steatosis too much for transplantation? J Hepatol 2006;45:494-499.
- Petridis I, Gruttaduria S, Nadalin S, et al. Liver transplantation using donors older than 80 years: a single-center experience. Transplant Proc 2008;40:1976-1978.
- Singhal A, Sezginsoy B, Ghuloom AE, Hutchinson IV, Cho YW, Jabbour N. Orthotopic liver transplant using allografts from geriatric population in the United States: is there any age limit? Exp Clin Transplant 2010;8:196-201.
- Martins PN, Chang S, Mahadevapa B, Martins AB, Sheiner P. Liver grafts from selected older donors do not have significantly more ischemia reperfusion injury. HPB 2011;13:212-220.
- Yersiz H, Shaked A, Olthoff K, et al. Correlation between donor age and the pattern of liver graft recovery after transplantation. Transplantation 1995; 60:790-4.
- Wall WJ. Predicting outcome after liver transplantation. Liver Transpl Surg 1999;5:458-459.
- Cassuto JR, Patel SA, Tsoulfas G, Orloff MS, Abt PL. The cumulative effects of cold ischemia time and older donor age on liver graft survival. J Surg Research 2008;148:38-44.
- Piratvisuth T, Tredger JM, Hayllar KA, Williams R. Contribution of true cold and rewarming ischemia times to factors determining outcome after orthotopic liver transplantation. Liver Transpl Surg 1995;1:296-301.
- Ghobrial RM, Gornbein J, Steadman R, et al. Pretransplant model to predict posttransplant survival in liver transplant patients. Ann Surg 2002;236:315-322.
- Wiesner RH, McDiarmid SV, Kamath PS, et al, MELD and PELD: application of survival models to liver allocation. Liver Transpl 2001;7:567-580.
- Kamath PS, Wiesner RH, Malinchoc M, et al. A model to predict survival in patients with end-stage liver disease. Hepatology 2001;33:464-470.
- Burra P, Porte RJ. Should donors and recipients be matched in liver transplantation? J Hepatol 2006;45:488-494.
- Avolio AW, Nardo B, Agnes S, et al. The mismatch choice in liver transplantation: a suggestion for the selection of the recipient in relation to the characteristics of the donor. Transplant Proc 2005;37:2584-2586.
- Berenguer M, Prieto M, San Juan F, et al. Contribution of donor age to the recent decrease in patient survival among HCV-infected liver transplant recipients. Hepatology 2002;36:202-210.
- Wali M, Harrison RF, Gow PJ, Mutimer D. Advancing donor liver age and rapid fibrosis progression following transplantation for hepatitis C. Gut 2002;51:248-252.
- Russo MW, Galanko JA, Zacks SL, Beavers KL, Fried MW, Shrestha R. Impact of donor age and year of transplant on graft survival in liver transplant recipients with chronic hepatitis C. Am J Transplant 2004;4:1133-1138.
- Lake JR, Shorr JS, Steffen BJ, Chu AH, Gordon RD, Wiessner RH. Differential effects of donor age in liver transplant recipients infected with hepatitis B, hepatitis C and without viral hepatitis. Am J Transplant 2005; 5:549-557.
- Condron SL, Heneghan MA, Patel K, Dev K, McHutchison JG, Muir AJ. Effect of donor age on survival of liver transplant recipients with hepatitis C virus infection. Transplantation 2005; 80:145-148.
- Mutimer DL, Gunson B, Chen J, et al. Impact of donor age and year of transplantation on graft and patient survival following liver transplantation for hepatitis C virus. Transplantation 2006;81:7-14.
- Iacob S, Cicinnati VR, Hilgard P, et al. Predictors of graft and patient survival in hepatitis C virus (HCV) recipients: model to predict HCV cirrhosis after liver transplantation. Transplantation 2007;84:56-63.
- Doyle M, Anderson C, Vachharajani N, et al. Liver transplantation for hepatitis C virus. Effect of using older donor grafts on short- and medium-term survival. Arch Surg 2008;143:679-685.
- Borchert DH, Glanemann M, Mogl M, Langrehr, Neuhaus P. Adult liver transplantation using liver grafts from donors over 70 years of age. Transplant Proc 2005;37:1186-1187.
- Faber W, Seehofer D, Puhl G, et al. Donor age does not influence 12-month outcome after orthotopic liver transplantation. Transplant Proc 2011; 3789-3795.
- Winger DJ, Sponsilli EE. Concentrations of serum protein fractions in white women: effects of age, weight, smoking, tonsillectomy and other factors. Clin Chem 1977;23:1310-1317.
- Shepherd AM, Hewick DS, Moreland TA, Stevenson IH. Age as a determinant of sensitivity to warfarin. Br J Pharmacol 1977;4:315-320.
- Stewart ZA, Locke JE, Segev DL, et al. Increased risk of graft loss from hepatic artery thrombosis after liver transplantation with older donors. Liver Transpl 2009;15:1688-1695.
- Cescon M, Zanello M, Grazi GL, et al. Impact of very advanced donor age on hepatic artery thrombosis after liver transplantation. Transplantation 2011; 92:439-445.
- Wall WJ, Mimeault R, Grant DR, Bloch M. The use of older donor livers for hepatic transplantation. Transplantation 1990; 49:377-81.
- Washburn WK, Johnson LB, Lewis WD, Jenkins RL. Graft function and outcome of older (>60 years) donor livers. Transplantation 1996; 61:1062-1066.
- Grande L, Rull A, Rimola A, et al. Outcome of patients undergoing orthotopic liver transplantation with elderly donors (over 60 years). Transplant Proc 1997; 29:3289-3290.
- Markmann JF, Markmann JW, Markmann DA, et al. Preoperative factors associated with outcome and their impact on resource use in 1148 consecutive primary liver transplants. Transplantation 2001; 72:1113-1122.
- Rull R, Vidal O, Momblan D, et al. Evaluation of potential liver donors: limits imposed by donor variables in liver transplantation. Liver Transpl 2003; 9:389-393.
- Rauchfuss F, Voigt R, Dittmar Y, Heise M, Settmacher U. Liver transplantation utilizing old donor organs: a German single-center experience. Transplant Proc 2010;42:175-177.
- Neipp M, Bektas H, Lueck R, et al. Liver transplantation using organs from donors older than 60 years. Transpl Int 2004;17:416-423.
- Sampedro B, Cabezas J, Fábrega E, Casafont F, Pons-Romero F. Liver transplantation with donors older than 75 years. Transplant Proc 2011;43:679-682.
- Caso O, Jiménez C, Justo I, et al. Analizing predictors of graft survival in patients undergoing liver transplantation with donors aged 70 years and over. World J Gastroenterol 2018;24:5391-5402.
- Wall W, Grant D, Roy A, Asfar S, Block. Elderly liver donor. Lancet 1993;341:121
- Romagnoli J, Urbani L, Catalano G, et al. Liver transplantation using a 93-year-old donor. Transplant Proc 2001;33:3797.
- Grazi GL, Cescon M, Ravaioli M, Corti B, Pinna AD. Successful liver transplantation from a 95-year old donor to a patient with MELD score 36 and delayed graft arterialization. Am J Transplant 2008;8:725-726.
- Karpen SJ. Growing old gracefully: caring for the 90-year-old liver in the 40-year-old transplant recipient. Hepatology 2010;51:364-365.
- Watt KD, Lyden ER, Gulizia JM, McCashland TM. Recurrent hepatitis C posttransplant: early preservation injury may predict poor outcome. Liver Transpl 2006;12:134:139.
- Ghinolfi D, Marti J, De Simone P,et al. Use of octogenarian donors for liver transplantation: a survival analysis. Am J Transplant 2014;14:2062-2071.
- Jiménez-Romero C, Cambra F, Caso O, et al. Octogenarian liver grafts: is their use for transplant curently justified? World J Gastroenterol 2017;23:3099-3110.
- Jiménez-Romero C, Caso O, Cambra F, et al. Octogenarian liver grafts reaching centennial age after transplantation. Transplantation 2017;101:e218-e219.
DECLARACIÓN DE TRANSPARENCIA
El autor/a de este artículo declara no tener ningún tipo de conflicto de intereses respecto a lo expuesto en la presente revisión.
ranm tv
Carlos Jiménez Romero
Real Academia Nacional de Medicina de España
C/ Arrieta, 12 · 28013 Madrid
Tlf.: +34 91 159 47 34 | carlos.jiménez@inforboe.es
Año 2019 · número 136 (03) · páginas 239 a 248
Enviado*: 02.04.19
Revisado: 12.04.19
Aceptado: 08.05.19
* Fecha de lectura en la RANM


