Resumen
En esta conferencia analizamos el impacto de la tomografía de coherencia óptica en la oftalmología, describiendo sus principales aplicaciones con ejemplos e ilustraciones. El estudio detallado del segmento anterior del ojo, la posibilidad de la biometría, el estudio de la retina con su gran cantidad de alteraciones, asi como el estudio de la capa de fibras nerviosas de la retina y del nervio óptico, han cambiado en las últimas decadas dramáticamente la especialidad. El diagnóstico y seguimiento del glaucoma de una manera eficaz y no invasiva, ha sido de vital importancia en el manejo de esta patología. Los avances como el OCT funcional, y los cambios en el futuro inmediato son la mejor prueba de la gran importancia y necesidad de esta tecnología en la oftalmología.
Abstract
In this conference we analyzed the impact of optical coherence tomography on ophthalmology, describing its main applications with examples and illustrations. The detailed study of the anterior segment of the eye, the possibility of biometrics, the study of the retina with its large number of alterations, as well as the study of the nerve fiber layer of the retina and optic nerve, have changed in recent decades dramatically the specialty. The diagnosis and monitoring of glaucoma in an effective and non-invasive way, has been of vital importance in the management of this pathology. Advances such as functional OCT, and changes in the immediate future are the best proof of the great importance and need of this technology in ophthalmology.
Palabras clave: Tomografía de coherencia óptica; Oftalmología.
Keywords: Optical coherence tomography; Ophthalmology.
INTRODUCCIÓN
Desde su invención en los años 1990, la tomografía de coherencia óptica, ha cambiado dramáticamente el concepto y el entendimiento de muchos temas en salud. Y es en efecto, en el campo de la medicina en donde ha producido mayor impacto este equipo es la oftalmología.
En el área de la retina, ha demostrado ser eficaz para producir una biopsia in vivo, al obtener imágenes con una discriminación de 10 micras, con el Stratus OCT 3 y hasta 3 micras con el OCT HD. En la actualidad se obtiene una resolución cercana a la micrometría.
A través de un algoritmo de colores, puede obtenerse la información que se desee en una imagen que es posible entender sin conocer demasiado de física, ya que la tomografía de coherencia óptica, combina exitosamente diversos campos de la ciencia.
ORÍGENES DE LA TOMOGRAFÍA DE COHERENCIA ÓPTICA
La mejor comparación que puede establecerse es entre el OCT y el ultrasonido, entendiendo que el primero utiliza luz y el segundo, como su nombre indica emplea sonidos.
La idea del OCT surge de los trabajos en Interferometria. Este concepto fue desarrollado en el siglo XIX por un físico de origen judío, Albert Michelson (premio Nobel de física en 1907) quien realizó sus experimentos en el laboratorio de Hermann Von Helmholtz, el inventor del oftalmoscopio.
La interferometria se utilizó inicialmente para medir distancias, y en el siglo XX, su creador pudo calcular con precisión el ángulo de inclinación de una estrella. Por tanto este concepto permite mensurar e interpretar distancias, mediante la respuesta o no respuesta a una señal luminosa.
El sistema clásico e inicial de la interferometría y la tomografía de coherencia óptica, se establecía mediante la emisión luminosa de un diodo superluminoscente, cuya luz, se dividía en dos haces de luz coherentes, esto es que todos sus puntos luminosos estuvieran en el mismo sitio de la onda al mismo tiempo. Uno de los haces se enviaba a la muestra o tejido a estudiar, y el otro haz se dirigía a un espejo de referencia. Luego esas dos señales luminosas eran recogidas por un receptor y luego un ordenador, analizaba las diferencias entre ambos haces de luz.
Desde 1987 el profesor Adolf Wrexler en Viena, propuso la medición de la distancia anteroposterior del globo ocular mediante la interferometría (1). Pero es en 1991, cuando se publicó en la revista Science, el primer articulo sobre la tomografía de coherencia óptica, firmado por David Huang, Eric Swanson y Joel Schuman, entre otros que marca el punto de partida de la incesante evolución de esta técnica diagnostica que ha revolucionado prácticamente todos los campos de la medicina (2). En unos cinco años, ya contabamos con protocolos de análisis de glaucoma desarrollados por Schuman y los de retina desarrollados por Carmen Puliafito. En los primeros 10 años la mayoría de los trabajos eran sobre oftalmología, pero a partir del 2000, la canitdad de trabajos publicados en todo tipo de revistas de investigación médica creció de forma exponencial. Hacia el 2019 se han publicado más de 10,000 trabajos sobre la tomografía de coherencia óptica. Contamos en la actualidad con 50 empresas, 100 grupos de investigación, dedicados a estudiar y llevar más adelante esta tecnología y se han registrado más de 1000 patentes. (3)
ANALIZANDO LAS IMÁGENES
Debemos analizar la resolución axial y la transversal. La resolución Axial, determinada por la fuente de luz, determina cuales capas de la retina se pueden distinguir con claridad. Mientras que la resolución transversal determina la precisión con la que pueden ser definidas y separadas diversas estructuras. La resolución transversal está determinada por el sistema óptico del ojo, puede ser afectada por el diámetro pupilar y es corregida de forma activa por el sistema de escáner. A medida que disponemos de mejores fuentes de luz, tales como láseres de fentosegundo o de picosegundo, mejoramos en profundidad las estructuras que podemos analizar, y la mejoría en los equipos, en su hardware, nos permite conseguir cada vez mejores y más claras imágenes. El cambio ha sido dramático. En 1998 conseguíamos 100 escáner por segundo, en la actualidad llegamos a 95,000. La resolución axial en 1998 era de 15 micras y en la actualidad estamos por debajo de las 3 micras. Esto en poco más de dos décadas. El sistema origina, se conoció como de dominio tiempo, y dependía de que cada señal era analizada una por una y tenía la limitante de tiempo de la velocidad en que cada imagen se procesaba. Cuando en 2008 ya se introducen los equipos de alta definición, se basaban en un espectrómetro que, al descomponer todas las longitudes de onda, mediante un dispositivo, producía una enorme cantidad de información que era procesada mediante las transformaciones de Fourier. Este nuevo concepto se conoce como OCT de dominio Fourier, o espectral, y permitió un aumento significativo en nuestra capacidad de análisis. Se hace la comparación de que antes era un avión de hélice y se convirtió en todo un avión a reacción.
DE LA ESTRUCTURA A LA FUNCIÓN
La casa pionera en el desarrollo de la tomografía de coherencia óptica fue la casa Zeiss, con sus diversos modelos. En la actualidad existen múltiples equipos fabricados por casas tan prestigiosas como la Topcon o Nidek de Japón, la Heidelberg de Alemania o la tan interesante casa Optopol de Polonia. Como hemos visto estos equipos tenían una excelente capacidad de análisis de la estructura retiniana de inicio, luego de todo el segmento anterior del ojo y a partir de ahí diversas especialidades médicas utilizaron esta tecnología. Hacia el 2013, el concepto de análisis de estructuras cambio con la introducción de los tomógrafos de coherencia óptica capaces de estudiar funciones. El primero fue el doppler OCT. Forma más usada de OCT funcional. Requiere poca adaptación del hardware y es tan sólo una mejoría en la capacidad de procesamiento. Se toman scans sucesivos en una misma localización, y se puede medir la diferencia en las fases. La limitación que presenta es que todavía la cantidad de artefactos asociados al movimiento ocular es elevada. Los cada día mejores algoritmos de procesamiento han ido paliando esta situación. Como hemos resaltado los sistemas actuales permiten realizar 95,000 escáner por segundo. En el doppler OCT se toma un punto de la fase de la onda de luz, y se analiza durante 3.28 segundos, lo que permite obtener un flujo y un estudio funcional, de unos 2 milímetros, asumiendo un ritmo cardíaco de 73 pulsaciones por minuto. (10)
APLICACIONES EN OFTALMOLOGÍA
La oftalmología ha sido la más beneficiada entre las diferentes especialidades médicas por los avances en la tomografía de coherencia óptica. Actualmente utilizamos esta tecnología para efectuar una biometría de la longitud anteroposterior del globo ocular, en la exploración del segmento anterior del ojo, en la evaluación tanto estructural como funcional de la retina, en el estudio del glaucoma y en el análisis de la cabeza del nervio óptico.(9) (13)
BIOMETRÍA
La biometría aparece como aplicación de la tomografía de coherencia óptica en un trabajo publicado por el profesor Adolf Fercher, en marzo de 1988, con el titulo “medición de la longitud del ojo mediante interferometría con una luz parcialmente coherente”, Optics Letters, vol. 13 No. 3. En 2016 en un trabajo realizado en el Centro de física médica y de ingeniería biomédica de la Universidad médica de Viena, publicado en Invest Ophthalmol Vis Sci, firmado por el doctor Christoph Hitzenberger en que también figura el profesor Fercher, (4) vuelven a mostrar las ventajas de la medición del globo ocular con la tomografía de coherencia óptica. Esta aplicación de la tomografía de coherencia óptica tendrá mayor proyección en el futuro cuando los sistemas actuales de OCT lo incorporen a sus programas de análisis.
SEGMENTO ANTERIOR
En cuanto al estudio del segmento anterior del ojo, podemos analizar la córnea, la cámara anterior, el ángulo iridocorneal y la superficie anterior del cristalino. El OCT de segmento anterior nos permite estudiar el grosor corneal, realizar un mapa paquimétrico muy exacto, tomar medidas corneales con gran precisión, analizar la correcta colocación de anillos intracorneales y evaluar la interfase tras cirugía Lasik refractiva. Los modernos programas de análisis permiten tomas de alta definición de la córnea e incluso evaluar la película lagrimal, particularmente importante en casos de ojo seco. Los equipos de navegación del OCT, permiten colocar el punto de análisis en cualquier posición de la superficie corneal, lo que nos permite estudiar por ejemplo úlceras corneales y la evolución de su tratamiento. La capacidad de los equipos de análisis del segmento anterior del ojo, permiten tomar mediciones importantes como la longitud blanco blanco, o la profundidad de la cámara anterior del ojo. La profundidad de la cámara anterior es un indicador importante de riesgo de glaucoma por ángulo estrecho o cerrado, que el OCT realiza con gran exactitud. De igual forma la gonioscopía o goniometría realizada con la tomografía de coherencia óptica del segmento anterior, permite obtener mediciones muy precisas de dichos ángulos sin los inconvenientes de la gonioscopía tradicional, que es una técnica de contacto.
De igual forma evaluamos la presencia de sinequias anteriores, esto es las adhesiones patológicas entre la córnea y el iris, frecuentes tras episodios de inflamación intraocular. Sin gran dificultad podemos evaluar lesiones del iris, como quistes o tumores, y verificar la eficacia y permeabilidad de una iridotomía.
En la superficie anterior del cristalino es particularmente útil, y luego de cirugía de cataratas, nos es posible evaluar la correcta colocación del lente intraocular. (5)
RETINA
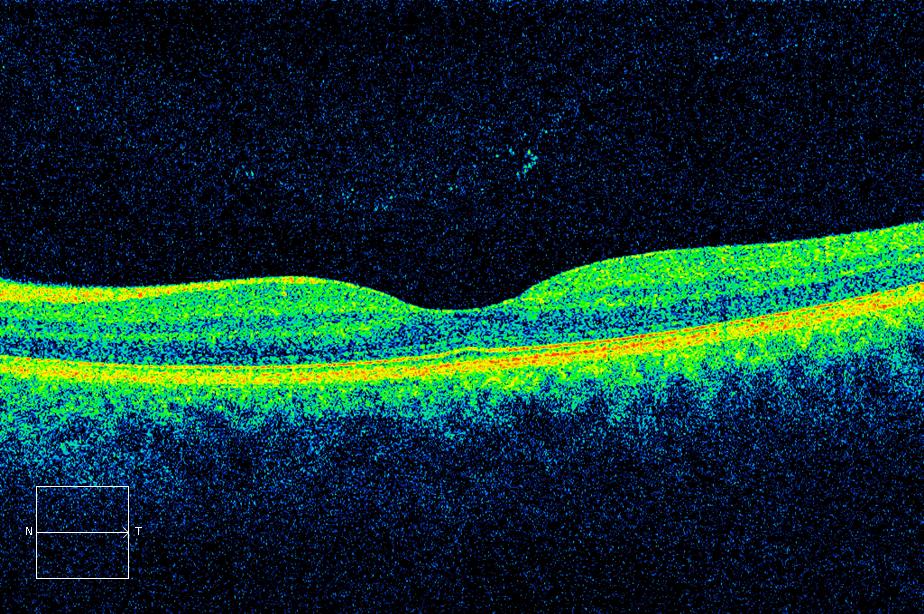
Los tomógrafos de coherencia óptica de alta definición nos ofrecen una imagen similar a la histología retiniana, permitiéndonos definir las diferentes capas retinianas. Podemos identificar edemas, distrofias, degeneración macular asociada a la edad, desprendimientos intraretinianos, agujeros maculares, alteraciones de la interfase vitreoretiniana, membranas epiretinianas, alteraciones asociadas a uveítis o inflamaciones y estudiar las estructuras coroideas.
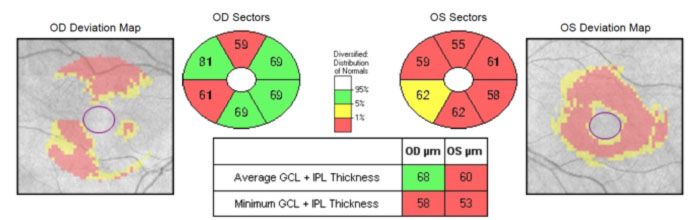
Un reporte típico de análisis macular nos ofrece los valores de grosor central expresado en micras, en una medición desde la membrana limitante interna hasta la capa de epitelio pigmentario, nos ofrece además el volumen macular expresado en milímetros cuadrados y el valor promedio del área en forma de cubo explorado también en micras. Nos ofrece además en forma gráfica los valores centrales y de los diferentes cuadrantes y además un detalle de la superficie del complejo membrana limitante- epitelio pigmentario, así como imágenes separadas de la superficie de ambas estructuras, particularmente útil en casos de degeneración macular asociada a la edad. Otro de los reportes del Cirrus 5000 de la casa Zeiss, permite evaluar el grosor macular desde la capa de células ganglionares hasta la capa plexiforme interna, que será muy interesante en la evaluación de sujetos con sospecha de glaucoma.
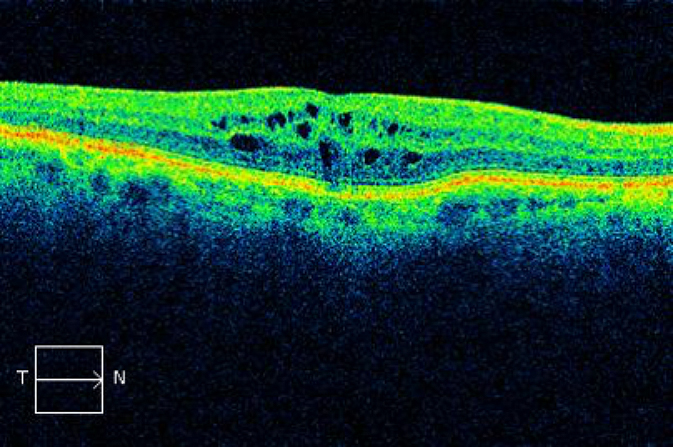
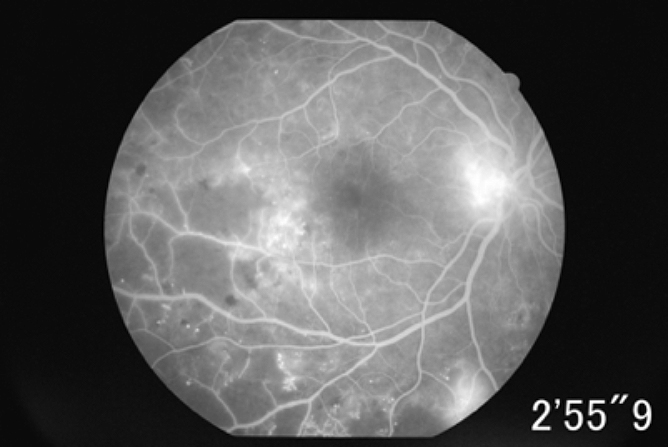
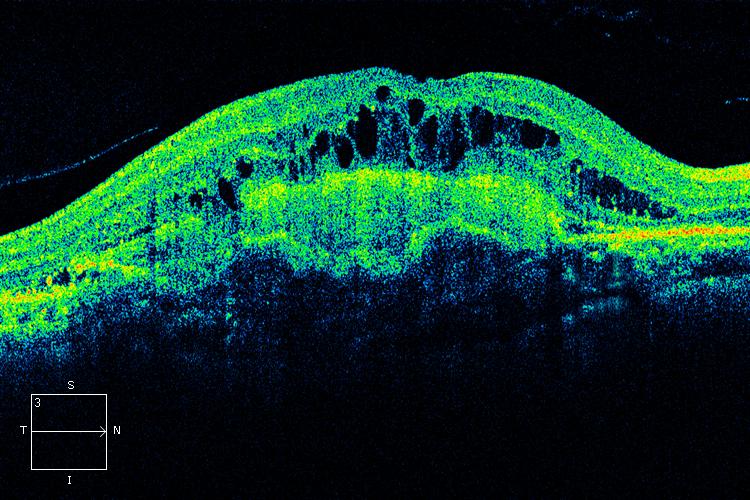
El OCT nos permite evaluar los pacientes diabéticos en búsqueda de varias patologías, tales como edema o maculopatía y además con los nuevos sistemas funcionales, realizar una angiografía que nos permite identificar los neovasos que caracterizan la retinopatía diabética proliferativa. Podemos clasificar los edemas como difusos o quísticos. Nos es muy útil esta tecnología en el seguimiento de las patologías, ya que disponemos de una herramienta de comparación de los valores retinianos en el tiempo.
En la degeneración macular asociada a la edad, tenemos la posibilidad de detectar precozmente membranas neovasculares submaculares, o alteraciones en la superficie retiniana que nos permitirán clasificar esta patología. La gran ventaja del OCT es que es una tecnología no invasiva, que ni siquiera requiere dilatación pupilar en la gran mayoría de los casos estudiados.
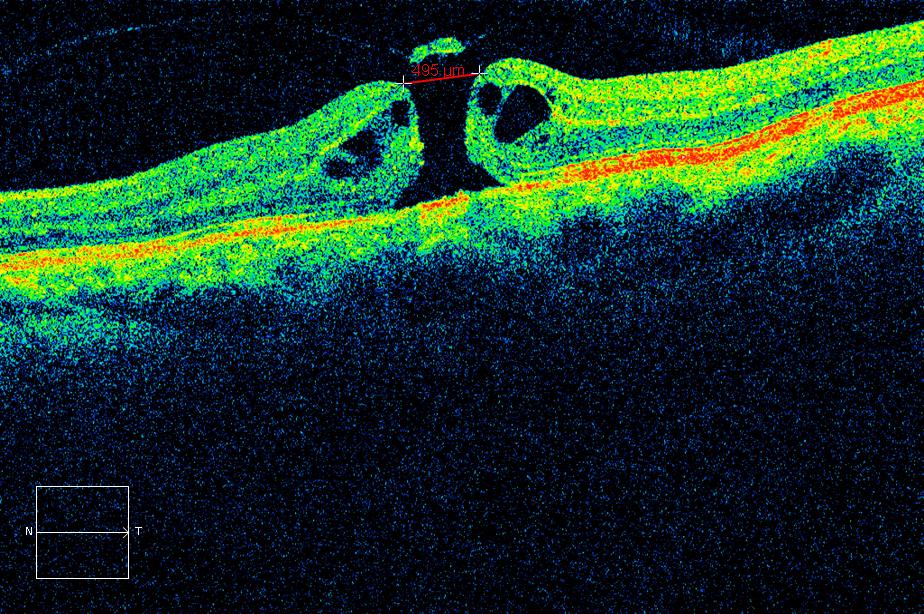
En el caso de los agujeros maculares, podemos con facilidad clasificar el estadio de los agujeros, podemos medir sus dimensiones, seguir su evolución en el tiempo y además verificar el resultado quirúrgico en aquellos casos que ameriten intervención.
Uno de los extraordinarios avances en este equipo ha sido la introducción del análisis funcional, el doppler OCT, que permite realizar angiografías con el OCT sin necesidad de uso de colorantes, tales como la fluoresceína sódica, que pueden producir lesiones renales en diabéticos. El doppler Oct nos permite evaluar las alteraciones de diferentes estructuras retinianas, además del análisis morfológico, podemos evaluar las alteraciones en la textura de la superficie estudiada. Además de los diferentes lechos vasculares retinianos, el análisis de la interfase vitreoretiniana, podremos evaluar además la coriocapilar y la coroides.
La cantidad de información de gran valor que nos ofrece este equipo, y las nuevas aplicaciones de las que cada día disponemos han convertido al OCT en la tecnología de referencia para estudios retinianos. Además, que la degeneración macular asociada a la edad, la retinopatía o maculopatía diabética o el glaucoma están entre las principales causas de aparición de nuevos casos de ceguera en el mundo. ( 6, 7)
GLAUCOMA
El OCT nos permite, con los estudios del ángulo iridocorneal, confirmar si el glaucoma es de ángulo abierto o cerrado. Luego tendremos los análisis de la cabeza del nervio óptico y de las fibras que le nutren, que son de vital importancia en el estudio de los pacientes glaucomatosos.
El primero de los resultados muestra el Nerve Fiber Layer Map. Esta es una imágen topográfica de la disposición de las fibras. Su aspecto típico es de alas de mariposa, con sus colores rojo y amarillo, dependiendo del grosor en cada punto de la capa. Luego tenemos el mapa de desviación, RNFL Deviation Map, que muestra las desviaciones de la normativa. Vemos dos circulos rojos, uno delimita la excavación y el más externo el área de cálculo del grosor de la capa de fibras nerviosas. A continuación se presenta el grosor del anillo neurosensorial, que presenta la comparación de ambos ojos. Luego por debajo nos presenta el gráfico de grosor de la capa de fibras nerviosas de la retina en la presentación TSNIT, esto es, el grosor detallado en cada uno de las zonas principales y su comparación con la normativa vigente. Luego por debajo del TSNIT presenta esta misma data en forma de cuadrantes y horaria. Esta infomación se estudia comparandola con la normativa. Es importante destacar que la zona más sensible a cambios en las sospechas de glaucoma es la zona horaria de las VII horas. A ambos lados nos presenta scaners vertivales extraídos del cubo de información del nervio óptico. Los bordes del disco y de la capa de epitelio pigmentario se marcan en negro y los de la limitante interna y la excavación en rojo.
De acuerdo a los estudios utilizados para la normativa, el valor normal del promedio de grosor de la capa de fibras nerviosas con el Cirrus son de 75 a 107.2 micras. La simetría entre ambos ojos debe estar entre el 76% al 95%. El área del anillo neurosensorial se considera normal entre 1.015 y 1.615 mm2.
Que podemos obtener con el OCT en el glaucoma?
- Medición de la capa de fibras nerviosas
- Seguimiento del tratamiento médico o quirúrgico del glaucoma
- Estudios morfométricos de la papila óptica
- Confirmar o no la sospecha de glaucoma,
- Realizar una adecuada evaluación del tratamiento, confirmar o no la presencia de cambios en el nervio óptico y saber si se ha conseguido o no la meta de la estabilidad.
- El analisis de la capa de celulas ganglionares es una herramienta de gran importancia para detectar cambios tempranos que en la evolución del glaucoma.
Nuestro objetivo es detener lo mas temprano posible la apoptosis en el nervio óptico.
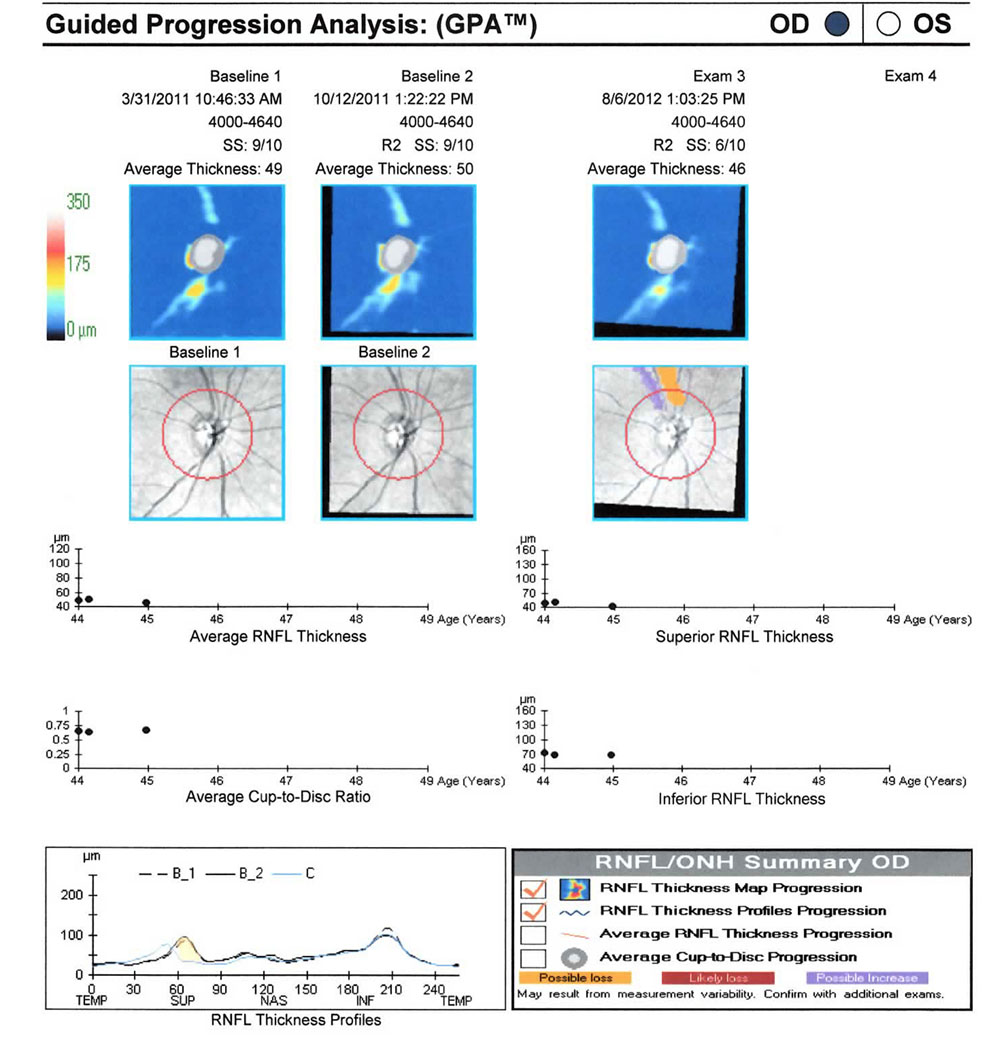
El OCT de alta definición Cirrus nos ofrece además el Guided Progression Analysis ( GPA ), el análisis guiado de la progresión en el glaucoma, que tras disponer de dos analisis de base y con 3 en total permite estudiar las variaciones de deterioro o de progreso del mapa del grosor de la capa de fibras nerviosas de la retina, del promedio del grosor de la capa de fibras nerviosas de la retina y del promedio de la relación excavación-disco. Estos valores nos permiten además realizar un análisis de regresión que nos permitirá de un pronóstico en la evolución de la patología. (8, 9, 10, 11)
CABEZA DEL NERVIO ÓPTICO
Además de su utilidad en el glaucoma, en patologías tales como edema papilar o lesiones tipo neuritis, la exploración de la relación de los valores de la cabeza del nervio óptico con los valores de la capa de fibras nerviosas de la retina, son de gran utilidad en las patologías que afectan la morfología y morfometría de la cabeza del nervio óptico. (12)
NOVEDADES EN EL OCT
En poco tiempo dispondremos de nuevos tipos de OCT como el Swept Source, que ya está disponible en algunos equipos y que pese a su gran capacidad de analisis coroideo no ha impactado aún en la práctica como esperabamos. De igual forma el OCT de polarización, que será particularmente importante para el estudio de la córnea y sus alteraciones. El OCT mmolecular, que utiliza protones de segunda generación harmónica para ofrecer imágenes cada vez de mayor y mejor calidad y resolución. Los equipos de que dispondremos en un futuro no muy lejano llegarán a 250,000 escaners por segundo.
En otras especialidades médicas como cardiología, gastroenterología, dermatología, neumología, urología el OCT es hoy una herramienta valiosa. En el area de la neurología, el uso del OCT para analizar la capa de fibras nerviosas de la retina, se ha identificado como de alto valor para predicción y seguimiento de la enfermedad de Parkinson, de la Esclerosis múltiple entre otras alteraciones neurológicas. (13, 14)
CONCLUSIONES
La facilidad en la realización de este estudio, no invasivo y que no requiere largo tiempo para su ejecución han convertido a la tomografía de coherencia óptica en el herramienta diagnóstica más importante en la oftalmología moderna.



BIBLIOGRAFÍA
- Fercher A, Mengedoht K, Werner W. Eye-length measurement by interferometry. Opt Lett 1988; 13(3): 186-192.
- Huang D, Swanson E, Puliafito C et al. Optical coherence tomography. Science 1991; 254: 1178-1181.
- Arevalo JF, Lasave AF, Arias JD, Serrano MA, Arevalo FA. Clinical applications of optical coherence tomography in the posterior pole: the 2011 José Manuel Espino Lecture. Clin Opthtalmol 2013; 7: 2181-2206.
- Hitzenberger C, Drexler W et al. Key developtmentes for partial coherence biometry and optical coherence tomography in the human eye made in Vienna. Invest Ophthalmol Vis Sci 2016; 57(9): 460-474.
- Stern H. Tomografía de coherencia óptica. Maestría de Oftalmología organizada por el Consejo Argentino de Oftalmología; 2008.
- Townsend KA, Wollstein G, Schuman JS. Imaging of the retinal nerve fiber layer in glaucoma. Br J Ophthalmol 2009; 93(2): 139-143.
- Stern H. El OCT en el edema macular. En: Tomografía de coherencia óptica. Highlights of Ophthalmology, Jaypee; 2011.
- Schuman JS, Hee MR, Arya AV, Pedut-Kloizman T, Puliafito CA, Fujimoto JG, Swanson EA. Optical coherence tomography: a new tool for glaucoma diagnosis. Curr Opin Ophthalmol 1995; 6(2): 89-95.
- Giovaninni A. The macular thickness and volume in glaucoma: an analysis in normal and glaucomatous eyes using OCT. Acta Ophthalmol Scand Suppl 2002; 236: 34-36.
- Wollstein G, Paunescu LA, Ko TH, Fujimoto JG, Kowalevicz A, Hartl I et al. UHR OCT in glaucoma. Ophthalmology 2005; 112(2): 229-237.
- Stern H. El OCT de alta definición en el Glaucoma. En: Modern trends in ophthalmology. Highlights of Ophthalmology, Jaypee; 2012.
- Stern H. El OCT en la evaluación del Nervio Óptico. En: Tomografía de coherencia óptica. Highlights of Ophthalmology, Jaypee; 2011.
- Functional optical coherence tomography: principles and progress. Kim J, Brown W, Maher JR, Levinson H, Wax A. Phys Med Biol 2015; 60(10): R211-R237.
- Adhi M, Duker JS. Optical coherence tomography: current and future applications. Curr Opin Ophthalmol 2013; 24(3): 213-221.
DECLARACIÓN DE TRANSPARENCIA
El autor/a de este artículo declara no tener ningún tipo de conflicto de intereses respecto a lo expuesto en la presente revisión.
ranm tv
Herbert Stern Diaz
Real Academia Nacional de Medicina de España
C/ Arrieta, 12 · 28013 Madrid
Tlf.: +34 91 159 47 34 | Email de correspondencia
Año 2019 · número 136 (03) · páginas 268 a 274
Enviado*: 22.10.19
Revisado: 07.11.19
Aceptado: 30.11.19
* Fecha de lectura en la RANM


