Resumen
La hibernación es un sustrato fisiopatológico miocitario reversible que puede detectarse mediante técnicas de imagen. Sin embargo, el impacto real de la cuantía del miocardio viable sobre la dinámica contráctil ventricular izquierda ha sido poco evaluado. OBJETIVO: Analizar la correlación del miocardio viable con la disincronía mecánica intraventricular izquierda en individuos con enfermedad coronaria residual postintervencionismo percutáneo. MÉTODOS: Del histograma de fase en reposo se obtuvieron desvío estándar (DEF) y ancho de banda de fase (ABF) en una muestra retrospectiva de pacientes derivados a SPECT gatillado. Se excluyeron los pacientes en ritmo no sinusal, con QRS ancho, disfunción renal, miocardiopatía hipertrófica y enfermedad valvular. La muestra se dividió en dos grupos según la presencia (n=25) o ausencia (n=90) de enfermedad epicárdica residual tras un evento coronario agudo. Los índices del análisis de fase (AF) se correlacionaron con la cuantía de miocardio viable para dos umbrales de captación (40% y 50%) mediante el coeficiente de Pearson (r). RESULTADOS. Los grupos de pacientes con y sin lesiones epicárdicas no difirieron en edad, FEVI ni volúmenes cavitarios basales. La cuantía del miocardio no viable se correlacionó mejor con los índices del AF en presencia de lesiones epicárdicas residuales. Esta correlación fue más potente para el ABF (r=0.82, IC95%: 0.63-0.91, p<0.0001) que para el DEF (r=0.77, IC95%: 0.53-0.89, p<0.0001) y disminuyó a r=0.73 y 0.77, respectivamente, cuando se utilizó un mayor umbral de viabilidad (50%). La correlación más potente se observó en aquellos con lesiones residuales y defectos fijos sugestivos de infarto (r=0.93 para ABF, p<0.0001). CONCLUSIONES: En pacientes con estenosis residual postintervencionismo, la cuantía del miocardio hibernado se correlaciona estrechamente con la disincronía mecánica intraventricular. La correlación mayor se observa con un umbral de captación miocárdica basal >40%, especialmente cuando coexiste tejido cicatrizal.
Abstract
Hibernation is a reversible myocyte pathophysiological substrate that can be detected by several imaging techniques. However, the true impact of the amount of viable myocardium on left ventricular contractile dynamics has been poorly evaluated. OBJECTIVE: To analyze the correlation of viable myocardium with left ventricle mechanical dyssynchrony in subjects with residual stenosis after percutaneous coronary intervention. METHODS: Phase standard deviation (PSD) and phase bandwidth (PBW) at rest were obtained in a retrospective sample of patients referred to gated-SPECT. Patients in non-sinus rhythm, wide QRS, renal dysfunc tion, hypertrophic cardiomyopathy and valvular heart disease were excluded. The sample was divided into two groups according to the presence (n=25) or absence (n=90) of residual epicardial disease after an acute coronary event. Phase analysis (PA) indexes were correlated with the amount of viable myocardium applying two uptake thresholds (40% and 50%) using Pearson coefficient (r). RESULTS. Both groups of patients did not differed in age, basal LVEF or cavitary volumes. The amount of nonviable myocardium was better correlated with PA indexes in the presence of residual epicardial lesions. This correlation was more powerful for PBW (r=0.82, 95% CI: 0.63-0.91, p<0.0001) than for PSD (r=0.77, 95% CI: 0.53-0.89, p<0.0001) and decreased to r=0.73 and 0.77, respectively, when a higher viability threshold was considered (50%). The best correlation was observed in those with residual lesions and fixed perfusion defects suggestive of scar (r=0.93 for ABF, p <0.0001). CONCLUSIONS: In patients with residual stenosis after percutaneous coronary intervention, the amount of hibernated myocardium correlates closely with mechanical ventricular dyssynchrony. The best correlation is observed when using a baseline myocardial uptake threshold of at least 40%, especially when scar tissue coexists.
Palabras Clave: Hibernación; Disincronía; Enfermedad coronaria.
Keywords: Hibernation; Dyssynchrony; Coronary disease.
INDICE DE ABREVIATURAS, SIGLAS Y ACRÓNIMOS
AF: análisis de fase
ABF: ancho de banda de fase
DEF: desviación estándar de fase
DMVI: disincronía mecánica del ventrículo izquierdo
ESD: escore de suma diferencial
ESR: escore de suma en reposo
FEVI: fracción de eyección del ventrículo izquierdo
Gated-SPECT: Tomografía por Emisión de Fotón Unico gatillada
PET: Tomografía por Emisión de Positrones
RMN: Resonancia Magnética Nuclear
TRC: terapia de resincronización cardíaca
VSF: volumen sistólico final del ventrículo izquierdo.
INTRODUCCIÓN
La arquitectura muscular cardíaca que garantiza una función sisto-diastólica normal es compleja. Tras décadas de meticuloso trabajo con piezas de disección, F. Torrent-Guasp demostró que el corazón humano está formado por una única banda muscular plegada sobre sí misma en forma helicoidal (“el hélix”), bombeando la sangre hacia la periferia y a la vez succionando el volumen de la precarga a través de una torsión sobre sí misma. (1) Esta disposición única posibilita una secuencia contráctil ventricular caracterizada por un movimiento circunferencial y un acortamiento longitudinal simultáneos, que transcurre desde el vértice a la base. La RMN de fusión marcada ha confirmando los hallazgos de Torrent-Guasp; una orientación en dos grandes disposiciones circunferencial y longitudinal, en transición gradual desde una dirección a otra, es el sustrato anatómico moderno de la función contráctil normal (2) Debido a esta compleja arquitectura, diferentes regiones del miocardio deben ser activadas en una secuencia temporal exacta para desencadenar un ciclo contráctil normal. En efecto, la normal activación eléctrica a través del sistema His-Purkinje avanza en un frente de onda con disparidades regionales que duran apenas 80-100 milisegundos de principio a fin (sincronía eléctrica). Esta complejidad permite comprender que, incluso el corazón de estructura y función normal pueda exhibir una mínima DMVI. (3)
El clínico suele afrontar dificultades en el manejo de la cardiopatía isquémica crónica. En estos casos, la toma de decisiones suele ser difícil, pues las evidencias disponibles sobre los beneficios individuales y sinérgicos de distintas modalidades terapéuticas son heterogéneas y/o contradictorias. Como casi la mitad de los pacientes con QRS prolongado y disfunción sistólica severa sintomática son portadores de cardiopatía isquémica, y debido a que no se obtiene una respuesta favorable en una proporción considerable de los que reciben TRC, (4) explorar los efectos de la revascularización sobre la dinámica contráctil del VI es una cuestión relevante.
Algunos factores que contribuyen a la DMVI en la enfermedad coronaria crónica, como las características del tejido cicatrizal, la severidad de la isquemia y la presencia y extensión del miocardio viable, pueden ser evaluados mediante la gated-SPECT. La hibernación y el aturdimiento (o atontamiento) son los dos sustratos fisiopatológicos que exhibe el miocardio viable en la enfermedad coronaria crónica; a menudo coexistiendo en un mismo paciente. El término hibernación miocárdica se refiere a un estado adaptativo del músculo cardíaco en el que se ha producido una reducción crónica del flujo coronario que conduce a una disminución de su capacidad contráctil, pero es reversible y se recupera parcial o totalmente con la revascularización coronaria. (5) El aturdimiento miocárdico, en cambio, se define como el deterioro de la función contráctil del miocardio, producido por una isquemia o una oclusión coronaria aguda, que es reversible tras la reperfusión temprana del flujo coronario con la revascularización, percutánea o quirúrgica, de los lechos coronarios obstruidos. La recuperación de la contractilidad se difiere en días o semanas. En cualquier variante, el miocardio viable representa un sustrato metabólico potencialmente reversible y cuantificable mediante técnicas de imagen. Aunque está bien demostrado que el tejido cicatrizal (6) y la isquemia (7) ejercen un papel importante en la dinámica contráctil del VI, los impactos del miocardio viable sobre la DMVI han sido poco explorados en distintas presentaciones de la enfermedad coronaria.
El AF por gated-SPECT es una herramienta no invasiva sólida, de fácil aplicación, confiable y de impacto clínico para cuantificar la DMVI. Además, las medidas de disincronía obtenidas presentan escasa variabilidad test-retest, inter e intra-examinador. (8). Sin embargo, son muy escasas las experiencias que han aplicado AF para evaluar el efecto de la hibernación sobre la DMVI, pues el área de estudio más relevante se ha dirigido a evaluar la capacidad de la técnica para predecir la respuesta a la TRC. (9,10) Aplicando AF analizamos la correlación del miocardio viable con la disincronía mecánica del VI en individuos con enfermedad coronaria residual sin disincronía eléctrica.
MATERIAL Y MÉTODOS
Diseño
Estudio observacional retrospectivo, unicéntrico.
Población de estudio
Estudiamos todos los pacientes que fueron remitidos consecutivamente a gated-SPECT, cuyo objetivo era evaluar la presencia y severidad de isquemia miocárdica inducida, a criterio del cardiólogo tratante. Se incluyeron los estudios realizados entre el 1ro de junio de 2019 y el 28 de febrero de 2020. Fueron excluidos los pacientes en ritmo no sinusal, con QRS ancho (120 ms), bloqueo aurículo-ventricular de 2do o 3er grado, extrasístolía frecuente, miocardiopatía hipertrófica, valvulopatía mitral u aórtica moderada/severa, evento coronario agudo en curso, hipertensión arterial pulmonar, insuficiencia renal moderada/severa o problemas técnicos.
Imágenes gammagráficas
La gated-SPECT se realizó en dos días estrés-reposo. La sensibilización se realizó con esfuerzo en cinta sinfín (Bruce) o fármacos vasodilatadores (adenosina, regadenoson). El radiofármaco utilizado fue 99m Tc-MIBI en dosis de 925-1110 MBq. Las imágenes se obtuvieron a los 45-60 minutos de inyectar 99mTc-MIBI en una gammacámara híbrida (GE OPTIMA NM/CT 640 y GE INFINIA Hawkeye 4), utilizando un colimador de baja energía y alta resolución. Se adquirieron 30 imágenes cada 6 grados de paradas angulares de 30 segundos cada una a 8 cuadros/ciclo cardíaco, en una matriz de 128×128. Se usó una ventana de intervalo RR dentro del 20% de la longitud promedio antes del ciclo de exploración. El procesamiento se realizó en la estación de trabajo Xeleris (GE Healthcare) a través del método iterativo OSEM. Para definir la extensión e intensidad de los defectos de perfusión se utilizó una escala visual semicuantitativa en un mapa polar de perfusión de 17 segmentos, desde 0=normal, a 4=ausencia de perfusión. La intensidad de los defectos se registró mediante los escores ESR y ESD. Además, se obtuvo el VSF (ml) y la FEVI basal (%). Tras interpretar las imágenes, dos expertos expresaron un juicio sobre la presencia, severidad y localización de la isquemia y los defectos de perfusión sugestivos de cicatriz postinfarto o miocardio viable. La cuantía del miocardio viable se expresó como % de la masa ventricular, considerando dos umbrales de captación basal del radiotrazador ( >40% y >50%, figura 1).

Angiografía coronaria
El estudio se realizó en el gabinete de hemodinámica. Se efectuaron proyecciones fluoroscópicas para identificar la/s arteria/s y lesión/es culpable/s del cuadro clínico y los hallazgos previos por imagen, cuando correpondiera. Tras un evento coronario agudo, se intervino siguiendo las recomendaciones actuales de la Sociedad Europea de Cardiología, que requiere considerar el estado clínico y comorbilidades, la significancia de la estenosis con base en el % de obstrucción luminal, los hallazgos angiográficos sugestivos de ruptura de placa, el patrón de flujo distal y, cuando fuera necesario, la significancia fisiológica medida por sonda intraarterial. La angioplastia se realizó siguiendo protocolos habituales, quedando a criterio del hemodinamista el tipo y número de stent/s a implantar. El procedimiento se consideró exitoso cuando obtuvo un flujo distal TIMI 2-3 sin complicaciones mayores. A los efectos del análisis comparativo, las lesiones residuales se definieron como aquellas que determinaban al menos una reducción luminal de 20% en vasos no culpables y no fueron sometidas a intervencionismo antes de la gated-SPECT. La decisión del hemodinamista actuante para no intervenir sobre estas lesiones se fundamentó en la clínica y el perfil de riesgo al ingreso, las características anatómicas de el/los vasos, la ausencia de relevancia funcional medida por sonda de presión intracoronarial y/o imposibilidades técnicas de proceder al intervencionismo e implante de stent/s.
Análisis de fase
El método utilizado para extraer la amplitud, que representa el grado de engrosamiento sistólico de la pared del VI, y la fase, que se refiere al tiempo de inicio de la contracción mecánica, a partir de los recuentos regionales ventriculares y sus cambios obtenidos durante la gated-SPECT ha sido descrito por J. Chen et al. (11) Para el AF se utilizó SyncTool de Emory Cardiac Toolbox® (Emory University, Syntermed, Atlanta). Dicha herramienta asigna un ángulo de fase en cada píxel de la imagen de fase desde el primer armónico de la curva de actividad de Fourier. A partir del histograma de fase en reposo obtuvimos los índices de disincronía DEF y ABF, en grados.
Estadística
La muestra se dividió en dos grupos según la presencia (n=25) o ausencia (n=90) de enfermedad coronaria residual. Las variables continuas se expresaron como media+DE o mediana, RIQ 25-75% y las discretas como frecuencias relativas (%).
Para comparar las variables continuas se utilizó test de “t” apareado o Mann-Whitney, cuando correspondiera, mientras que para comparar las variables discretas se aplicó test exacto de Fisher. En cada grupo, los índices del AF en reposo se correlacionaron con la cuantía del miocardio viable mediante el coeficiente (“r”) de Pearson con su IC 95%, definido para dos umbrales de captación (40% y 50%, figura 1).
En los pacientes con lesiones residuales, este análisis se amplió a los subgrupos que presentaron infarto y/o isquemia por imágenes, aplicando un modelo de rregresión lineal simple, y graficando el margen de error de las medidas individuales (95%) con relación a la línea que mejor representaba la distribución de los datos. Se consideró un valor de p significativo < 0.05 (dos colas). Para los análisis y gráficas se utilizó el software Graphpad Prism® Inc. 8.0.
Consideraciones éticas
Se respetaron las normas de la declaración de Helsinki, salvaguardando el anonimato y la confidencialida de los datos en toda la población. Los pacientes firmaron consentimiento informado para la gated-SPECT.
RESULTADOS
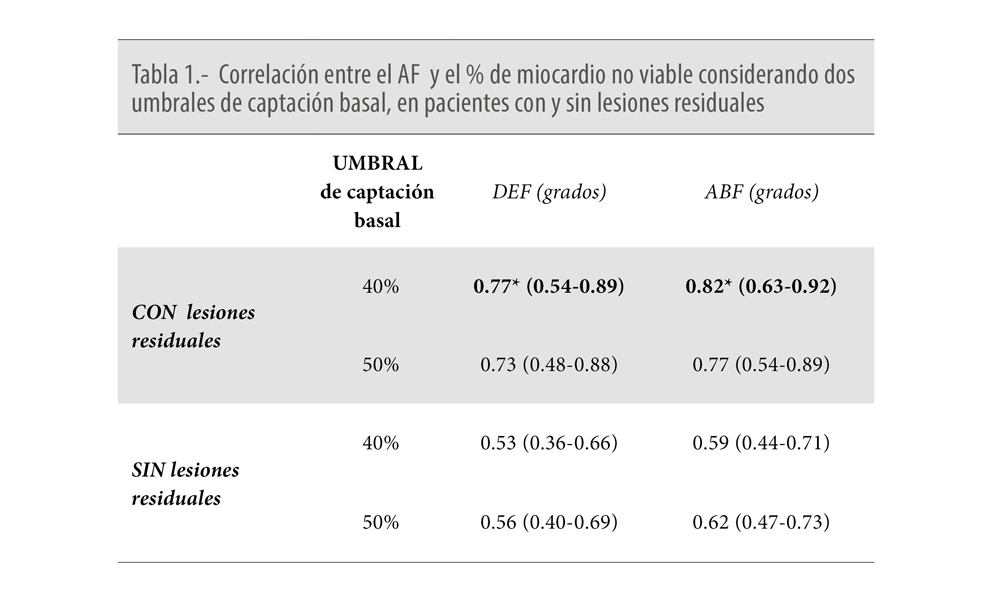
Se incluyeron 115 pacientes, de 69+13 años, la mayoría hombres (60%). Un 20% había sufrido infarto previamente, realizándose una angioplastia coronaria durante un síndrome coronario agudo con elevación de ST en el 26% de los casos. El 7% recibió cirugía de bypass. Los pacientes con lesiones residuales eran más frecuentemente hombres (40 vs. 17%, p = 0.0028). Los grupos con y sin lesiones epicárdicas residuales no difirieron significativamente en otras variables de relevancia clínica-angiográfica como edad (73, 51-75 vs. 71, 58-80 años, p=0.95), diabetes (3 vs. 10%, p>0.99), FEVI basal (63.8+9.9 vs. 63.5+13.4%, p=0.89) ni volúmenes cavitarios en reposo (VSF=36.0, 26.5-53.0 vs. 36.5, 20.8-58.8 ml, p=0.37). La cuantía del miocardio viable se correlacionó mejor con los índices del AF en presencia de lesiones residuales (tabla 1).
Análisis de subgrupos en presencia de lesiones residuales (figura 2)
En sujetos con lesiones residuales y cicatriz por imágenes (n=13), se observó una mejor correlación entre el % de miocardio no viable y la DMVI al considerar un umbral de captación de 40%, con coeficientes “r” de 0.87 (0.54-0.97) para el DEF y de 0.93 (0.79-0.98) para el ABF, respectivamente. En los pacientes con lesiones residuales, infarto e isquemia por imágenes, ya sea perilesional o remota (n=10), los coeficientes fueron de 0.87 (0.54-0.97) para el DEF y 0.86 (0.51-0.97) para el ABF al considerar un umbral de 40%, y de 0.88 (0.75-0.94) y 0.72 (0.18-0.93) para ambos índices al considerar un umbral de 50% (p<0.0001en las dos correlaciones, para ambos umbrales).

Gráficos de correlación y regresión lineal simpple entre los índices del AF en reposo con la cuantía del miocardio no viable, considerando umbrales de captación basal de 40% (paneles superiores) y 50% (paneles inferiores) en sujetos con lesiones residuales asociadas a isquemia y/o cicatriz de infarto por imágenes. En cada gráfico, el trazado lleno en negro representa la línea que estima mejor el comportamiento de los datos, y los trazados punteados en rojo superior e inferior indican el margen de error (95%) de las medidas (sombreado en gris).
DISCUSIÓN
Encontramos una muy buena correlación entre la cuantía de miocardio hibernado y la DMVI asociada a la estenosis coronaria residual, aún en ausencia de disfunción sistólica y QRS prolongado. Los resultados que arroja el análisis de subgrupos confirman una correlación aún más potente entre DMVI e hibernación asociada al tejido cicatrizal. Estos hallazgos coinciden con la escasa información experimental disponible. Zhang y col. evaluaron la DMIVI mediante AF por gated-SPECT y la cuantía del miocardio hibernado mediante la misma técnica y 18F-FDG PET, en una serie de 91 pacientes que habían sufrido infarto. Tras el análisis multivariado, encontraron que el miocardio hibernado fué un factor independiente de DMVI postinfarto. (12) Además, detectaron una mejoría en la disincronía a los 6 meses postrevascularización, en relación directa con el miocardio hibernado. Ya en pacientes con disfunción sistólica severa sintomática de etiología coronaria y complejo QRS ancho en el ECG, la mayor cuantía de miocardio hibernado se asocia con una respuesta favorable a la TRC. (10)
Durante la ruptura de placa, más aún en la oclusión trombótica en curso (infarto hiperagudo), el intervencionismo logra reestablecer el flujo coronario en el vaso culpable a expensas de un grado variable de disfunción microvascular. La gravedad de esta lesión post-reperfusión depende fundamentalmente del tiempo transcurrido tras la trombosis coronaria. (13) Además, tras restaurar efectivamente el flujo coronario mediante implante de stent suele persitir cierta carga de ateroma y un estado protrombótico. (14) Las muy escasas experiencias que describen la mecánica ventricular en pacientes con afectación multivaso sometidos a revascularización, (15) en los que el reestablecimiento del flujo es heterogéno en distintas áreas de miocardio, sugieren que podría existir una relación directa entre la presencia de la enfermedad coronaria residual y el miocardio hibernado, que confirmamos con nuestros hallazgos. Es en este sentido que nuestra experiencia muestra mayor originalidad; hasta donde sabemos, las alteraciones de la mecánica contráctil asociadas a la estenosis residual postintervencionismo no han sido evaluada más allá del período inmediato postinfarto (atontamiento postisquémico).
Demostramos que, aún en ausencia de disincronía eléctrica, la cuantía del miocardio no viable se correlaciona muy bien con el grado de DMVI, aunque esta correlación varía en función de la presencia concomitante de tejido cicatrizal e isquémico y el umbral de captación celular utilizado para cuantificar el miocardio viable.
La directa relación entre la presencia y magnitud del tejido cicatrizal y la DMVI coinciden con los descritos por estudios observacionales que aplicaron diferentes técnicas de imagen para evaluar la dinámica contráctil intraventricular. En ellos se demuestra que la presencia de una o más cicatrices de infarto transmural puede limitar la respuesta clínico-funcional (16) y la remodelación tras la TRC, (17) aplicando Doppler tisular y gated-SPECT, respectivamente. Los resultados obtenidos mediante RMN cardíaca también señalan que la combinación de DMVI y ciertas medidas de miocardio viable podrían ayudar a predecir la respuesta clínico-funcional a la TRC (18,19). Sin embargo, estos hallazgos, obtenidos con diferentes técnicas de imagen, se refieren a sujetos con indicación de TRC, por lo que difícilmente sean comparables con los resultados obtenidos en nuestra población. (6)
La reversión de algunos defectos de perfusión tras la TRC sugiere que la isquemia extensa juega un papel preponderante en la DMVI. (20,7) Esta disincronía asociada a la isquemia sería un estado potencialmente reversible que, a su vez, podría contribuir al deterioro progresivo del propio miocardio isquémico, con mayor riesgo de infarto y disfunción sistólica.
El umbral de captación basal óptimo para definir la viabilidad miocárdica en la gated-SPECT es motivo de controversia, lo cual representa una debilidad metodológica para el análisis de metadatos. (21) Los estudios de la década del 90 demostraron que la presencia de defectos de perfusión reversibles post-estrés y un umbral de captación basal de al menos 50% permitían predecir la capacidad de recuperación sistólica tras la revascularización en los pacientes con insuficiencia cardíaca isquémica. (20) Desde entonces, este umbral de captación ha sido el criterio adoptado por casi todos las investigaciones de viabilidad miocárdica que aplican SPECT. En el metanálisis de Allman y col., que incluyó 3088 pacientes con FEVI disminuida, la mortalidad anual fue casi 80% más baja con la revascularización que con la terapia médica cuando existía tejido viable en la gated-SPECT, PET o ecocardiografía. (22) Sin embargo, hubo diferencias sustanciales en la metodología, la adquisición y los criterios para definir la significancia clínica de la viabilidad en cada técnica de imagen. Debido a esto, los autores sugieren interpretar los resultados como “presencia/ausencia” de miocardio viable según las definiciones de cada estudio, y que el potencial valor pronóstico de la extensión del miocardio viable o la isquemia inducida no puede ser examinado con la información disponible. El meta-análisis de Bax y col., que comparó los resultados del SPECT mediante 201Talio y 99mTc con otras modalidades no invasivas, también consideró un umbral de captación de 50-60% como criterio de viabilidad. (23)
El gran ensayo Surgical Treatment for Ischemic Heart Failure (STICH) investigó si la terapia combinada cirugía de bypass coronario + terapia médica antiisquémica era superior a la terapia médica aislada en individuos con disfunción sistólica de causa isquémica. (24,25) Inicialmente, el diseño exigía una prueba de viabilidad preoperatoria mediante SPECT en todos los pacientes, con un umbral de viabilidad definido como una captación basal de al menos 50%. Los autores concluyen que la presencia de miocardio viable no tiene un impacto significativo sobre la mortalidad tras la revascularización, y señalan que se requieren estudios prospectivos para definir el valor clínico-terapéutico de la evaluación del miocardio viable.
Al disminuir el umbral de captación en 10% (aumentando la proporción de miocardio no viable) se observó una correlación más potente y menor margen de error entre la cuantía de miocardio hibernado y los índices de disincronía, principalmente cuando existe estenosis coronaria residual (figura 2). La mejor correlación que encontramos entre miocardio viable y DMVI asociada a un umbral de viabilidad de al menos 40% sugiere que este punto de corte se comporta mejor que el estándar de 50%. Esto podría deberse a la inclusión de más miocardio viable a forma de defectos de perfusión no intramurales (infartos subendocárdicos), que podrían contribuir a la disincronía sin generar disfunción contráctil regional detectable por imágenes, pero sí evidentes en el AF. En realidad, los diferentes umbrales de captación basal en la gated-SPECT deberían ser agregados a los índices de DMVI y contrastados con la tasa de eventos cardíacos mayores. En otras palabras, se requiere un diseño longitudinal para evaluar la hipótesis de que más miocardio hibernado se asocia con mayor DMVI y peor pronóstico.
Nuestra estudio tiene algunas limitaciones, que son inherentes al diseño retrospectivo y el tamaño muestral reducido de un ensayo piloto. Además, desconocemos el intervalo desde el intervencionismo sobre lesiones “culpables” hasta la gated-SPECT y las estrategias antiisquémicas recibidas (fármacos, rehabilitación), lo que puede alterar la cuantía del miocardio hibernado. (26,27) Por otro lado, las regiones no infartadas disfuncionantes representan áreas de miocardio aturdido, hibernado y/o remodelado. Para diferenciar estrictamente dichas variantes debería haberse medido la motilidad y engrosamiento parietal basal y post-estrés. Finalmente, la resolución espacial y los conteos regionales subóptimos son limitantes técnicas conocidas de la gated-SPECT, en particular en pacientes con ventrículos dilatados de paredes finas, sobreestimando el miocardio cicatrizal.
Aunque preliminares, los hallazgos obtenidos podrían tener implicancias clínicas importantes. En primer lugar, una dinámica contráctil que varía sustancialmente en función del miocardio hibernado representa un fundamento fisiopatológico adicional para instaurar terapias más precoces y agresivas durante los eventos coronarios agudos, intentando limitar la masa de infarto, reducir la isquemia y reclutar miocardio viable. Una intervención percutánea primaria sobre las lesiones no culpables y un inicio más precoz de la terapia antiisquémica, por ejemplo, podrían ser estrategias a considerar. En segundo lugar, las medidas de DMVI obtenidas por diferentes técnicas podrían ser nuevos marcadores pronósticos no invasivos tras un evento coronario agudo. Finalmente, nuestros hallazgos sugieren que el umbral óptimo de captación utilizado para cuantificar el miocardio viable mediante gated-SPECT debería ser reconsiderado.
CONCLUSIONES
En la enfermedad coronaria residual postintervencionismo existe una estrecha correlación entre la cuantía del miocardio hibernado y los índices de disincronía obtenidos por AF. La mejor correlación se observa al utilizar un umbral de captación miocárdica basal de 40%, especialmente cuando existe tejido cicatrizal asociado al miocardio hibernado. Una evaluación individualizada y multimodal de la DMVI asociada al miocardio viable podría ahondar el conocimiento sobre la dinámica contráctil asociada a diferentes estados metabólicos miocárdicos y, quizás, aportar a la difícil toma de decisiones clínicas en la coronariopatía crónica.
BIBLIOGRAFÍA
- Torrent-Guasp F. Structure and function of the heart. Rev Esp Cardiol 1998;51:91-102.
- Helm P, Beg MF, Miller MI, et al. Measuring and mapping cardiac fiber and laminar architecture using diffusion tensor MR imaging. Ann NY Acad Sci 2005;1047:296-307.
- Bogaert J, Rademakers FE. Regional nonuniformity of normal adult human left ventricle. Am J Physiol Heart Circ Physiol 2001;280:H610-20.
- Abraham WT, Fisher WG, Smith AL, et al; MIRACLE Study Group. Cardiac resynchronization in chronic heart failure. N Engl J Med 2002;346:1845-1853.
- Rahimtoola SH. The hibernating myocardium. Am Heart J 1989;117:211-221.
- Adelstein EC, Saba S. Scar burden by myocardial perfusion imaging predicts echocardiographic response to cardiac resynchronization therapy in ischemic cardiomyopathy. Am Heart J 2007;153:105-112.
- Brandão SCS, Nishioka SAD, Giorgi MCP, et al. Cardiac resynchronization therapy evaluated by myocardial scintigraphy with 99mTc-MIBI: changes in left ventricular uptake, dyssynchrony and function. Eur J Nucl Med Mol Imaging 2009;36:986-996.
- Trimble M, Borges-Neto S, Honeycutt E, et al. Evaluation of mechanical dyssynchrony and myocardial perfusion using phase analysis of gated SPECT imaging in patients with left ventricular dysfunction. J Nucl Cardiol 2008;15:663-670.
- Al Jaroudi W, Chen J, Jaber WA, et al. Non-echocardiographic imaging in evaluation for cardiac resynchronization therapy. Circ Cardiovasc Imaging 2011;4:334-343.
- Ypenburg C, Schalij M, Bleeker G, et al. Extent of viability to predict response to cardiac resynchronization therapy in ischemic heart failure patients. J Nucl Med 2006;47:1565-1570.
- Chen J, Garcia EV, Folks RD, et al. Onset of left ventricular mechanical contraction as determined by phase analysis of ECG-gated myocardial perfusion SPECT imaging: development of a diagnostic tool for assessment of cardiac mechanical dyssynchrony. J Nucl Cardiol 2005;12:687-695.
- Zhang F, Yang W, Wang Y, et al. Is there an association between hibernating myocardium and left ventricular mechanical dyssynchrony in patients with myocardial infarction? Hell J Nucl Med 2018;21:28-34.
- Binder A, Ali A, Chawla R, et al. Myocardial protection from ischemia-reperfusion injury post coronary revascularization. Expert Rev Cardiovasc Ther 2015;13:1045-1057.
- Alfonso F, García P, Pimentel G, et al.; Intravascular ultrasound study. Predictors and implications of residual plaque burden after coronary stenting: an intravascular ultrasound study. Am Heart J 2003;145:254-261.
- Maruskova M, Gregor P, Bartunek J, et al. Myocardial viability and cardiac dyssynchrony as strong predictors of perioperative mortality in high-risk patients with ischemic cardiomyopathy having coronary artery bypass surgery. J Thorac Cardiovasc Surg 2009;138:62-68.
- Bleeker GB, Kaandorp TA, Lamb HJ, et al. Effect of posterolateral scar tissue on clinical and echocardiographic improvement after cardiac resynchronization therapy. Circulation 2006;113:969-976.
- Sciagra R, Giaccardi M, Porciani MC, et al. Myocardial perfusion imaging using gated SPECT in heart failure patients undergoing cardiac resynchronization therapy. J Nucl Med 2003;45:164-168.
- Bilchick KC, Dimaano V, Wu KC, et al. Cardiac magnetic resonance assessment of dyssynchrony and myocardial scar predicts function class improvement following cardiac resynchronization therapy. J Am Coll Cardiol 2008;1:561-568.
- Leyva F, Foley PWX, Stegemann B, et al. Development and validation of a clinical index to predict survival after cardiac resynchronisation therapy. Heart 2009;95:1619-1625.
- Bax JJ, van der Wall EE, Harbinson M. Radionuclide techniques for the assessment of myocardial viability and hibernation. Heart 2004; 90(Suppl. V):V26-V33.
- Tajoury TH, Chareonthaitawee P. Myocardial viability imaging and revascularization in chronic ischemic left ventricular dysfunction. Expert Rev Cardiovasc Ther 2010;8:55-63.
- Allman KC, Shaw LJ, Hachamovitch R, et al. Myocardial viability testing and impact of revascularization on prognosis in patients with coronary artery disease and left ventricular systolic dysfunction: a meta-analysis. J Am Coll Cardiol 2002;39:1151-1158.
- Bax JJ, Poldermans D, Elhendy A, et al. Sensitivity, specificity, and predictive accuracies of various noninvasive techniques for detecting hibernating myocardium. Curr Probl Cardiol 2001;26:141-186.
- Velázquez EJ, Lee K, Deja MA, et al.; STICH Investigators. Coronary‐artery bypass surgery in patients with left ventricular dysfunction. N Engl J Med 2011;364:1607‐1616.
- Bonow RO, Maurer G, Lee KL, et al. Myocardial viability and survival in ischemic left ventricular dysfunction. N Engl J Med 2011;364:1617‐1625.
- Schwarz ER, Schoendube FA, Kostin S, et al. Prolonged myocardial hibernation exacerbates cardiomyocyte degeneration and impairs recovery of function after revascularization. J Am Coll Cardiol 1998;31:1018-1026.
- Beanlands RS, Nichol G, Huszti E, et al.; PARR-2 Investigators. F18-Fluorodeoxyglucose positron emission tomography imaging-assisted management of patients with severe left ventricular dysfunction and suspected coronary disease: a randomized, controlled trial (PARR-2). J Am Coll Cardiol 2007;50:2002-2012.
DECLARACIÓN DE TRANSPARENCIA
El autor/a de este artículo declara no tener ningún tipo de conflicto de intereses respecto a lo expuesto en la presente revisión.
Federico Ferrando-Castagnetto
Carlos Sainz García de Robles, 25. Apto 4i
Distrito Valdezarza · 28035 Madrid
Tlf.: +34 697 391 784 | E-Mail: federico.ferrando@gmail.com
Año 2020 · número 137 (01) · páginas 65 a 72
Enviado*: 08.04.20
Revisado: 14.04.20
Aceptado: 24.04.20
* Fecha de lectura en la RANM


