Resumen
COVID-19 (COronaVIrusDisease, año 2019) está causado el por coronavirus 2 que da lugar a un síndrome respiratorio agudo grave (SARS-CoV2). Esta enfermedad está siendo un auténtico reto para los sistemas de salud de todo el mundo. En un breve periodo de tiempo surgieron numerosas publicaciones que debieron ser interpretadas rápidamente para aclarar dudas de esta enfermedad. Las primeras descripciones de la enfermedad observada en China, describían alteraciones en parámetros de coagulación que acompañaban cuadros de tromboembolismo venoso (TEV) y trombosis en la microcirculación en bastantes pacientes hospitalizados, especialmente en los más graves. La infección por SARS-CoV2 se acompaña de una gran inflamación. La activación de la coagulación se ha asociado a las reacciones de los sistemas de defensa del organismo, vía inflamatoria y a la de la inmunidad innata, respuesta denominada inmunotrombosis o tromboinflamación. La coagulopatía asociada a la COVID-19 presenta anomalías no frecuentes en otros estados de hipercoagulabilidad que acompañan infecciones.
Revisamos los datos clínicos y los mecanismos de las anomalías de coagulación que aparecen en la COVID-19. Además mostramos varias Guías que han aparecido para aportar información útil en la profilaxis y tratamiento del TEV en pacientes hospitalizados.
El conocimiento de aspectos relacionados con el nuevo patógeno está cambiando rápidamente, también facetas de su patogenicidad y tratamiento, facilitando un mayor conocimiento y aproximación para la prevención y tratamiento de la trombosis, aspectos que continuarán cambiando.
Abstract
Coronavirus disease 2019 (COVID-19) is caused by the severe acute respiratory syndrome coronavirus 2 (SARS-CoV2). COVID-19 has been an exceptional challenge for the health system thoughout the world. Many publications have emerged in a very short time and have had to be interpreted quickly to try to clarify the doubts generated by the new disease. Evidence of abnormal coagulation parameters associated with COVID-19 appeared in early reports from China. Venous thromboembolism (VTE) and microvasculature thrombosis have been found in many of hospitalized patients, specially in more severe cases. Severe inflammation is presents in patients with SARS-CoV2 infection. The coagulation activation has been associated to reaction of host defense systems, such as immflamatory response and innate immunity pathways, a term called immunothrombosis or thromboinflammation. COVID-19-associated coagulopathy reflects unusual abnormalities present in hypercoagulable states that accompany other infections.
Here, we review clinical data and mechanisms of coagulation abnormalities that occur in association with COVID-19. Moreover we show several Guides to provide practical information for the prophylaxis and management of VTE in hospitalized patients with COVID-19.
The knowledge of this new pathogen, of its pathogenicity and treatment are evolving rapidly, and our understanding and approach for the therapy and prevention of thrombosis will continue to evolve.
Palabras clave: COVID-19; Coronavirus; Trombosis; Anticoagulación.
Keywords: COVID-19; Coronavirus; Thrombosis; Anticoagulant therapy.
En los últimos meses nos hemos visto desbordados por una enfermedad que tiene un alto nivel de contagio y que se manifiesta por un síndrome respiratorio agudo grave, expresión de una inusitada reacción inflamatoria causada por el coronavirus 2 (SARS-CoV2). La Organización Mundial de la Salud denominó este cuadro con el acrónimo COVID-19 (COronaVIrusDisease, año 2019). La irrupción abrupta en nuestro medio de esa infección y su progresión implacable nos obligó a enfrentarnos de improviso a una nueva enfermedad que desconocíamos y de la que comprobamos rápidamente su alta morbi-mortalidad.
El desconocimiento de éste proceso propició que en un corto periodo de tiempo apareciera una enorme cantidad de bibliografía, la mayor parte elaborada de forma muy rápida y tal vez de una forma no muy exigente, motivado por la urgencia de comunicar aspectos que pudieran tener utilidad clínica. La información tuvo que ser analizada y “digerida” en tiempo muy corto con el afán de buscar biomarcadores que nos ayudaran a predecir la evolución clínica, y con ello poder encontrar la mejor profilaxis y terapia para nuestros enfermos. No ha sido infrecuente vivir en este periodo cambios de actitudes e interpretaciones en las complicaciones que aparecían en la COVID-19. Si bien son muchas las interrogantes que quedan por resolver, pienso que nos encontramos en un punto donde se dispone de un conocimiento clínico-biológico suficiente que invita a profundizar en el conocimiento de la epidemiología, etiopatogenia, fisiopatología, manifestaciones clínicas, prevención y tratamiento de la COVID-19. En los próximos meses seremos testigos de nuevos avances que ayudarán a reafirmar, rectificar o profundizar en el conocimiento de la enfermedad, y este es un aspecto a tener presente cuando leamos este artículo.
Desde las primeras descripciones de la evolución de la enfermedad observada en la ciudad de Wuhan (China), donde surgió la pandemia, se describieron una serie de modificaciones del sistema hemostático que sugerían la generación de un estado de hipercoagulabilidad, expresado clínicamente por trombosis frecuentes (1). No nos vamos a detener en considerar los cambios en la interpretación de los datos que fueron apareciendo, sino que abordaremos cual es el conocimiento en el momento de escribir este documento en referencia a la etiopatogenia de la trombosis en pacientes COVID-19, la existencia de posibles biomarcadores de riesgo trombótico, su prevalencia y expresión clínica, las medidas generalmente aceptadas para la prevención y tratamiento de la complicación tromboembólica, y finalizaremos haciendo referencia a algunas de las muchas cuestiones pendientes que consideramos más relevantes.
Etiopatogenia del estado de hipercoagulabilidad en la COVID-19.
Las primeras descripciones de las alteraciones del sistema hemostático en pacientes infectados por SARS-CoV2 indicaban un ligero aumento del tiempo de protrombina, un llamativo aumento del Dímero-D, pero con niveles de fibrinógeno habitualmente normales, así como un leve descenso del recuento plaquetario. Esas pruebas se veían acompañadas de un claro aumento de clásicos marcadores de respuesta inflamatoria, como la IL-6, PCR, ferritina, y niveles de troponina. Curiosamente el incremento notable en los niveles de esos marcadores, especialmente Dímero-D fue considerado como un indicador de gravedad (1, 2).
En un primer momento la tendencia protrombótica que aparece en pacientes con la COVID-19 hacía pensar que era una situación similar a la activación que se genera en el sistema hemostático tras un cuadro de sepsis, situación denominada como Coagulación Intravascular por Sepsis (CIS) y que es preludio de la Coagulación Intravascular Diseminada (CID). Es por ello que se preconizó utilizar el score de la International Society of Thrombosis and Haemostasis (3, 4) para establecer el riesgo de la coagulopatía. Poco a poco se van acumulando evidencias que sugieren que el estado de hipercoagulabilidad que aparece en pacientes con la COVID-19 tiene diferencias sustanciales con la CIS y con la CID. A diferencia de la activación del sistema hemostático que aparece tras una infección de un patógeno que lleva a una situación de CIS o CID, el virus SARS-CoV2 no parece disponer de un efecto “per se” de activación del sistema hemostático. Las tasas plasmáticas de fibrinógeno, inhibidores naturales como la antitrombina y el recuento plaquetario en la CIS o CID son bajas mientras que en pacientes con infección por el virus SARS-CoV2 no lo suelen estar. Es por ello, junto con otras evidencias que abordamos más adelante, la alteración del sistema hemostático que vemos en pacientes con la COVID-19 se está considerado como una entidad diferente a la CIS y CID, proponiendo su denominación con el acrónimo de Coagulopatía Asociada a COVID-19 (CAC), donde el papel de la inflamación como primer y gran inductor de la activación del sistema hemostático juega un papel muy relevante (5) (Figura 1).
Es conocido que determinadas infecciones víricas, bacterianas y fúngicas pueden desembocar en una respuesta inflamatoria, como parte de la inmunidad innata. El concepto de la existencia de interacción de sistemas enzimáticos complejos, como los sistemas de la coagulación sanguínea, complemento y respuesta inflamatoria, implicados todos ellos en mecanismos de defensa del organismo es un concepto bien establecido desde hace años, pero que readquiere un valor y realce propio cuando en 2012 Engelman y Massberg acuñan el término de inmunotrombosis o tromboinflamación (6, 7)
La inmunotrombosis explica la activación del sistema hemostático a través de diferentes vías por una exagerada respuesta inflamatoria. La tormenta inflamatoria propicia la activación de plaquetas, neutrófilos y monocitos, activación de la vía intrínseca de la coagulación por activación de proteínas de la fase de contacto, así como liberación de ADN de neutrófilos, con la consiguiente presencia plasmática de Trampas Extracelulares de Neutrófilos (NET) (8). Todo ello condiciona un estado de tromboinflamación, a la que se debe sumar el efecto de la activación del sistema del complemento para potenciar una mayor activación del sistema hemostático (9) (Figura 1).
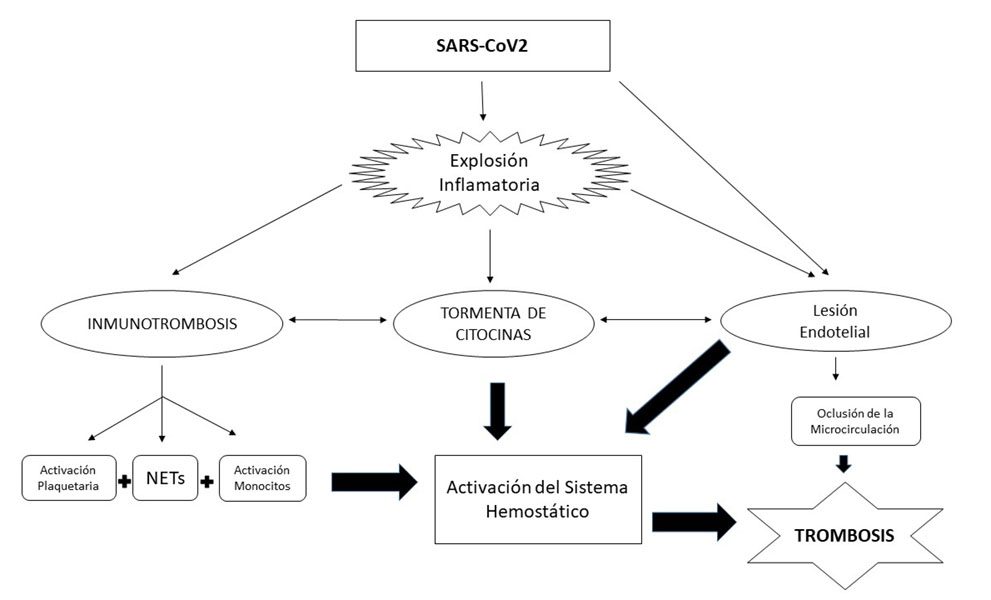
Por otra parte, las citocinas generadas en la respuesta inflamatoria tienen una reconocida capacidad de alterar el endotelio vascular generando un estado de vulnerabilidad en la pared de los vasos que conlleva a una situación protrombótica, pudiendo ocasionar también un descenso de plaquetas. No hay que olvidar que el receptor que condiciona la adhesión del virus a la célula es un receptor de la enzima angiotensina convertasa 2 que se encuentra en la superficie endotelial. La replicación viral es responsable de apoptosis endotelial y tiene un efecto protrombótico. (10)
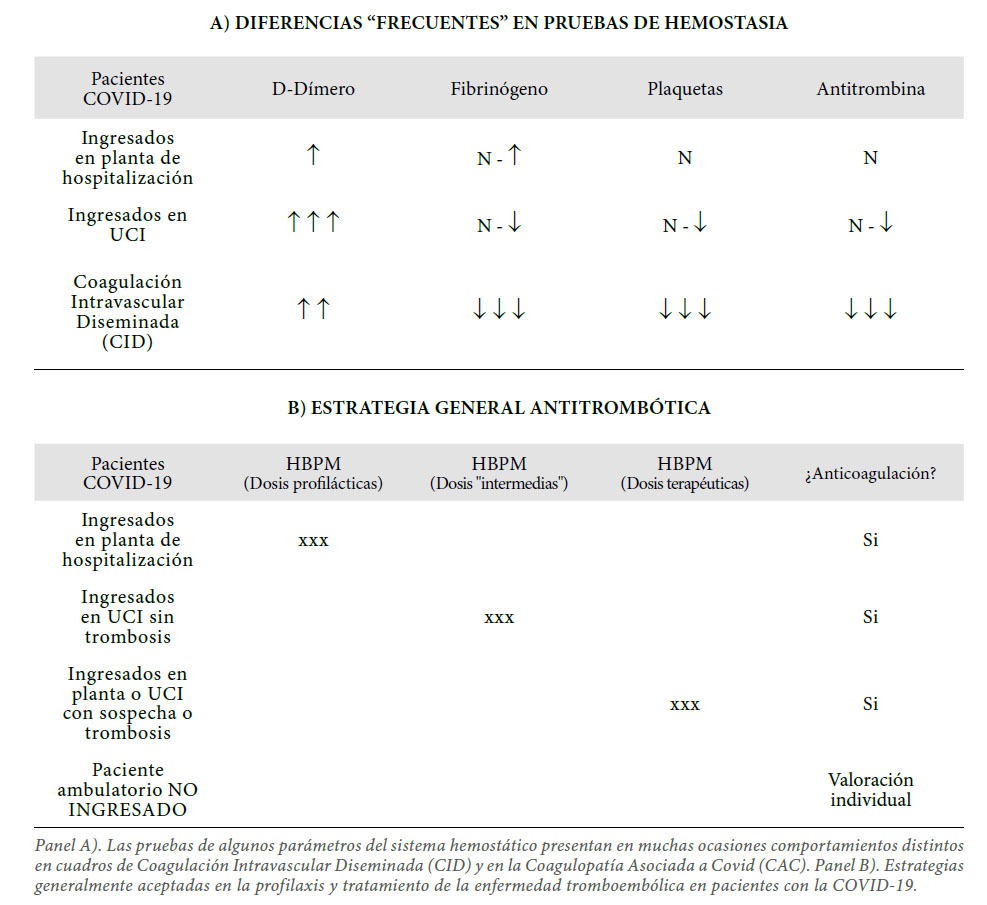
Los estudios de autopsias que van apareciendo en un número ya significativo vienen a avalar poderosamente lo indicado previamente. Patólogos de la Universidad de Basilea, en estudio realizado en 21 fallecidos por la COVID-19 nos muestran como hallazgos habituales un daño alveolar difuso exudativo con congestión capilar masiva, a menudo acompañada de microtrombos a pesar de la terapia anticoagulante que llevaban los pacientes. En algunos de ellos se encontraron embolismos pulmonares, vasculitis, hemorragia alveolar y signos de microangiopatía trombótica generalizada (11). Otros datos de reciente aparición muestras lesiones endoteliales severas asociadas con la presencia de virus intracelular y membranas celulares alteradas. La histopatología de los vasos pulmonares mostró trombosis generalizada con microangiopatía. Estas alteraciones eran 9 veces más prevalentes en pacientes con la COVID-19 que en pacientes que murieron por síndrome de dificultad respiratoria (SDRA) causado por la infección por influenza A (H1N1) (12). En definitiva, las lesiones que se van encontrando son la respuesta de una agresión inflamatoria al SARS-CoV2 que condiciona un estado de tromboinflamación con diferencias histológicas respecto a las que aparecen en el SDRA por el virus H1N1. A su vez, esos hallazgos presentan amplias diferencias a los encontrados en situaciones de CID relacionados con cuadros sépticos de diferente origen (12, 13) (Tabla I).
Incidencia y expresión clínica de los episodios trombóticos en pacientes con la COVID-19
Hemos asistido a una enorme heterogeneidad en la expresividad clínica de pacientes infectados por SARS-CoV2, desde pacientes totalmente asintomáticos a pacientes que han evolucionado en poco tiempo a graves insuficiencias respiratorias que han requerido ingreso en Unidad de Cuidados Intensivos (UCI). Se han iniciado numerosos estudios en búsqueda de diferencias genéticas que puedan explicar el diferente curso clínico y ayuden a desvelar la diferente agresividad de la enfermedad.
Nuestro cometido es centrarnos en la aparición de las complicaciones tromboembólicas en pacientes con la COVID-19. Al principio se comunicó la aparición de trombos en circuitos extracorpóreos y catéteres de enfermos, así como aparición de cuadros de tromboembolismo venoso. En los consecutivos estudios observacionales que iban apareciendo siempre se hacía referencia al riesgo de aparición de complicaciones tromboembólicas, asociándose con mayor frecuencia a los pacientes con mayor gravedad, especialmente a los ingresados en UCI. Ello condicionó que de forma generalizada en las Guías hospitalarias se incluyera la profilaxis de enfermedad tromboembólica en la enfermedad por SARS-CoV2.
Uno de los problemas al que nos hemos tenido que enfrentar era el de conocer la incidencia real de la oclusión vascular en esta enfermedad, pues eran datos difíciles de conseguir ante la dificultad de realizar pruebas objetivas diagnósticas de trombosis, como el eco-doppler o el angio-TAC, en pacientes en situación crítica y con alta capacidad de contagio. Una investigación holandesa acaba de aportar luz sobre esta complicada cuestión. En el hospital universitario de Amsterdam estudiaron la incidencia de casos de tromboembolismo venoso objetivamente confirmado en 198 pacientes que requirieron ingreso hospitalario por la COVID-19. 75 enfermos requirieron ventilación mecánica y el resto estuvieron en la planta de hospitalización (14). En 39 enfermos, mayoritariamente ingresados en la UCI, se diagnosticó una complicación tromboembólica venosa, pese a que todos los enfermos estaban con profilaxis antitrombótica con Heparina de Bajo Peso Molecular (HBPM). No fueron desdeñables los 14 casos de trombosis incidental que se encontraron al realizar el estudio de imagen, que corresponden al 36% de las trombosis observadas. La localización de los episodios oclusivos fueron embolismos pulmonares, trombosis venosa distal y proximal, y en un caso de extremidad superior. Este estudio clínico confirma la alta aparición de eventos tromboembólicos durante la COVID-19, especialmente en pacientes más graves, debiendo establecer un alto nivel de sospecha con los cambios clínicos, como empeoramiento agudo de la función respiratoria (14). Resultados similares han sido observados por otros grupos (15).
Biomarcadores de riesgo trombótico
El Dímero-D es un marcador que se usa habitualmente en el diagnóstico de tromboembolismo venoso, y siempre se le ha reconocido un valor predictivo negativo, es decir que su normalidad es un parámetro a considerar para descartar la existencia de trombosis. Al ser un reactante de fase aguda, su aumento coincide en circunstancias con trasfondo inflamatorio, de ahí su menor utilidad en el diagnóstico de oclusión vascular venosa en pacientes con cáncer, infecciones, embarazo, etc. En la situación de la COVID-19 la inflamación ocasiona una elevación importante del Dímero-D. En esas situaciones el valor predictivo del Dímero-D pierde en buena medida su valor, pudiéndose considerar un marcador subrogado a la inflamación presente y no estrictamente relacionado con la existencia de un trombo.
El empeoramiento de la insuficiencia respiratoria produce aumento de la IL-6, troponina y Dímero-D (16) y han sido adoptados como marcadores de mala evolución de la enfermedad, lo que conllevaba un mayor riesgo de aparición de complicaciones tromboembólicas (14,15).
Prevención y tratamiento de la complicación tromboembólica en pacientes con la COVID-19
Ante la presencia de complicaciones tromboembólicas se elaboraron rápidamente protocolos en hospitales y sociedades científicas, intentado orientar cuestiones relevantes relacionadas con el diagnóstico, profilaxis y tratamiento de los episodios tromboembólicos en los pacientes con SARS-CoV2 (17-20).
Entre las diferentes Guías hay pequeñas diferencias en cuanto a extensión y consideración dedicada a algunos problemas, pero existe bastante coincidencia en las medidas a tomar ante los pacientes ingresados. En general, a cualquier paciente hospitalizado por la COVID-19 sin mayores factores de riesgo de trombosis se ha recomendado dosis profiláctica de HBPM, y con dosis ajustadas al peso para los pacientes con índice de masa corporal > 35. Si el paciente presentaba factores de riesgo de trombosis, o estaban ingresados en UCI, en general las Guías sugieren incrementar la dosis de profilaxis ajustada a peso, o bien con el indefinido término de dosis “intermedias” (Tabla I). Estas dosis obviamente deben ser modificadas dependiendo de pacientes con pesos extremos, aparición de trombocitopenia o deterioro de la función renal (17-20).
En pacientes donde se ha diagnosticado o existe alta sospecha de tromboembolismo venoso, se debe administrar dosis terapéutica, y aunque no hay una clara recomendación de como pautar la dosis parece razonable administrarla cada 12 horas, pues evitamos los picos de anticoagulación plasmática que se pueden generar tras una sola dosis con un alto contenido de anticoagulante.
Los anticoagulantes orales de acción directa (ACOD) no están recomendados en estas circunstancias, precisamente por su administración oral, pues algunos pacientes están en estado crítico, y además desconocemos las posibles interacciones con los múltiples fármacos que se utilizan en el tratamiento de la enfermedad.
Otra cuestión es cuánto tiempo mantener la anticoagulación. Tal vez la situación más clara es en los pacientes que han tenido un episodio trombótico, pues la anticoagulación se debe mantener al menos tres meses y plantear su continuación dependiendo de la evolución clínica. En pacientes que han recibido dosis profilácticas y son dados de alta a casa, donde previsiblemente estarán un periodo de tiempo inmovilizados, debe plantearse una anticoagulación de al menos un periodo aproximado de 10-14 días, pero actualmente son solamente recomendaciones y no hay datos objetivos que resuelvan esta cuestión.
En los pacientes con la COVID-19 que no requieren ingreso hospitalario debe realizarse una valoración individualizada para indicar una profilaxis de enfermedad tromboembólica. Todo lo indicado, mucho más detallado, así como otros aspectos de interés vienen recogidos en diferentes Guías (17-20).
cuestiones pendientes
Queda todavía un tortuoso camino por andar para entender las múltiples cuestiones que merodean la asociación de trombosis y la COVID-19.
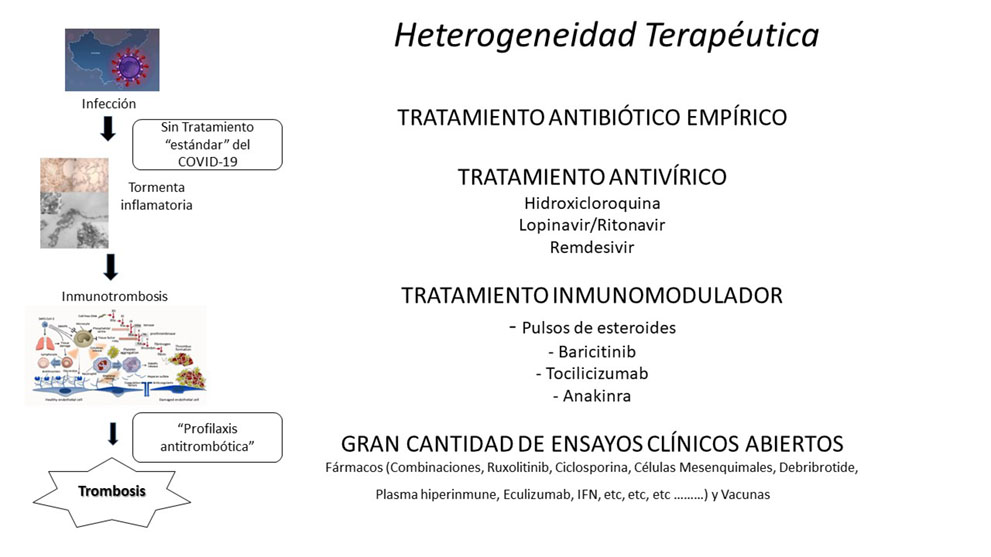
En primer lugar es necesario contar con resultados mucho más sólidos que los datos que hemos tenido disponibles. Hay en marcha numerosos estudios de carácter prospectivo, multicéntricos y multinacionales que abordan aspectos muy diferentes y ayudarán a entender mejor los motivos de la heterogeneidad en la gravedad de la presentación clínica de la COVID-19. Datos que esperemos que ayuden a contar con biomarcadores sensibles y específicos, y por supuesto para disponer de medidas profilácticas y terapéuticas que aumenten la eficacia en la prevención y tratamiento de las complicaciones tromboembólicas (Figura 2). Sin duda, conocer las diferencias en la etiopatogenia de la CAC respecto a la CIS o la CID, y sobretodo contar con medidas terapéuticas estandarizadas y eficaces para prevenir o frenar la tormenta inflamatoria, inexistentes hasta ahora, se vislumbra de crucial importancia para controlar el curso de la enfermedad, incluyendo la prevención de la trombosis.
Actualmente la terapia antitrombótica actúa en el último escalón de la enfermedad y no frena el origen y propagación de la respuesta inflamatoria (Figura 2), posiblemente por ello la mortalidad por trombosis incluso en pacientes anticoagulados con la COVID-19 sigue siendo alto.
BIBLIOGRAFÍA
- Chen N., Zhou M, Dong X et al. Epidemiological and clinical characteristics of 99 cases of 2019 novel coronavirus pneumonia in Wuhan, China: a descriptive study. Lancet 2020;395:507-513.
- Zhou F, Yu T, Du R et al. Clinical course and risk factors for mortality od adults inpatients with COVID-19 in Wuhan, China: a retrospective cohort study. Lancet 2020;395:1054-1062.
- Suzuki K, Wanda H, Imai H et al. A re-evaluation of the D-dimer cut-off value for making a diagnosis according to the ISTH overt-DIC diagnostic criteria: a communication from the SSC of the ISTH. J Thromb Haemost 2018;16:1442-1444.
- Iba T., Levy J.H., Wada H. et al. Differential diagnoses for sepsis-induced disseminated intravascular coagulation: Communication from the SSC of the ISTH. J. Thromb. Haemost. 2019;17:415–419.
- Connors JM, Levy JH. COVID-19 and its implications for thrombosis and anticoagulation. Blood;35:2033-2040.
- Engelmann B, Massberg S. Thrombosis as an intravascular effector of innate immunity. Nat Rev Immunol 2013:13:34-45.
- Jackson SP, Darbousset R, Schoenwaelder SM. Thromboinflammation: challenges of therapeutically targeting coagulation and other host defense mechanisms. Blood 2019;133:906-918.
- Noubouossie DF, Reeves BN, Strahl BD et al. Neutrophils: back in the thrombosis spotlight. Blood 2019;133:2186-2197.
- Subramaniam S, Jurk K, Hobohm L et al. Distinct contributions of complement factors to platelet activation and fibrin formation in venous thrombus development. Blood 207;129:2291-2302.
- Varga Z, Flammer AJ, Steiger P et al. Endothelial cell infection and endothelitis in COVID-19. Lancet 2020; 395:1417–1418.
- Menter T, Haslbauer JD, Nienhold R et al. Post-mortem examination of COVID19 patients reveals diffuse alveolar damage with severe capillary congestion and variegated findings of lungs and other organs suggesting vascular dysfunction. Histopathology 2020 (Pre-publicado) DOI: 10.1111/his.14134.
- Ackermann M, Verleden SE, Huehnel M et al. Pulmonary vascular endothelislitis. Thrombosis, and angiogénesis in Covid-19. N Engl J Med 2020;383:120-128.
- Hariri L, Hardin C C. Covid-19, angiogénesis, and ARDS endotypes. N Engl J Med 2020;383:182-183.
- Middeldorp S, Coppens M,. van Haaps TF et al. Incidence of venous thromboembolism in hospitalized patients with COVID-19. J Thromb Haemost 2020;18:1995-2002.
- Zhang L, Feng X, Zhang D et al. Deep Vein Thrombosis in Hospitalized Patients with Coronavirus Disease 2019 (COVID-19) in Wuhan, China: Prevalence, Risk Factors, and Outcome. Circulation 2020;142:114-128.
- Herold T, Jurinovic V, Arnreich Ch el al. Elevated levels of interleukin-6 and CRP predict the need for mechanical ventilation in COVID-19. J Allergy Clin Immunol 2020;146:128-136.
- Vivas D, Roldán V, Esteve-Pastor MA et al. Recomendaciones sobre el tratamiento antitrombótico durante la pandemia COVID-19. Posicionamiento del Grupo de Trabajo de Trombosis Cardiovascular de la Sociedad Española de Cardiología. Rev Esp Cardiol 2020;73:749-757.
- Marietta M, Ageno W, Artoni A et al. COVID-19 and haemostasis: a position paper from Italian Society on Thrombosis and Haemostasis (SISET). Blood Transfus 2020; 18: 167-169.
- Spyropoulos AC, Levy JH, Ageno W et al. Scientific and Standardization Committee Communication: Clinical Guidance on the Diagnosis, Prevention and Treatment of Venous Thromboembolism in Hospitalized Patients with COVID-19. J Thromb Haemost 2020;18:1859-1865.
- Sociedad Española de Trombosis y Hemostasia. Recomendaciones de tromboprofilaxis y tratamiento antitrombótico en pacientes con COVID-19. 2020 https://www.covid-19.seth.es/recomendaciones-de-tromboprofilaxis-y-tratamiento-antitrombotico-en-pacientes-con-covid-19/
DECLARACIÓN DE TRANSPARENCIA
El autor/a de este artículo declara no tener ningún tipo de conflicto de intereses respecto a lo expuesto en el presente trabajo.
Vicente Vicente
Real Academia Nacional de Medicina de España
C/ Arrieta, 12 · 28013 Madrid
Tlf.: +34 91 159 47 34 | Email de correspondencia
Año 2020 · número 137 (02) · páginas 140 a 146
Enviado: 06.06.20
Revisado: 10.06.20
Aceptado: 25.06.20


