Resumen
La insuficiencia cardíaca (IC) representa un importante problema socio-sanitario por su alta prevalencia, altas tasas de hospitalización y mortalidad y los importantes costos sanitarios. La IC comprende un grupo heterogéneo de síndromes con diferente fisiopatología, presentación clínica y respuesta al tratamiento. En los últimos años se han identificado múltiples dianas terapéuticas implicadas en la patogénesis de la IC y se han desarrollado numerosos fármacos frente a dichas dianas. Pero a pesar de los importantes avances en el tratamiento farmacológico de la IC con fracción de eyección reducida, ningún tratamiento ha demostrado de forma convincente hasta la fecha reducir la mortalidad de los pacientes con IC con fracción de eyección conservada. Por otro lado, la gran mayoría de los fármacos que aparecían como muy prometedores en modelos animales o en ensayos clínicos de fase 2 no han podido ser comercializados por su falta de eficacia y/o de seguridad en los grandes ensayos clínicos de fase 3. En este artículo analizamos los objetivos del tratamiento de la IC, los avances realizados en los últimos años y las posibles causas que podrían explicar nuestros repetidos fracasos.
Abstract
Heart failure (HF) represents an important healthcare problem due to its high prevalence, high rates of hospitalization and mortality, and significant healthcare costs. HF comprises a heterogeneous group of syndromes with different pathophysiology, clinical presentation, and response to treatment. In recent years, multiple therapeutic targets implicated in the pathogenesis of HF have been identified and numerous drugs have been developed against multiple targets. But despite important advances in the pharmacological treatment of HF with reduced ejection fraction, no treatment has convincingly shown to date to reduce mortality in HF patients with preserved ejection fraction. Furthermore, the vast majority of drugs that appeared very promising in animal models or in phase 2 clinical trials have not been able to be commercialized due to their lack of efficacy and / or safety in large phase 3 clinical trials. In this article we analyze the objectives of the treatment of HF, the progress made in recent years and the possible causes that could explain our repeated failures.
Keywords: Insuficiencia cardíaca; Nuevos fármacos; Ensayos clínicos; Fracción de eyección reducida; Fracción de eyección preservada.
Palabras clave: Heart failure; New drugs; Clinical trials; Reduced ejection fraction; Preserved ejection fraction.
Introducción
Las Guías de la Sociedad Europea de Cardiología definen la insuficiencia cardiaca (IC) como un síndrome clínico caracterizado por síntomas típicos (disnea, fatiga, edema de tobillos y fatiga), que puede ir acompañado de signos (como presión venosa yugular elevada, crepitantes pulmonares y edema periférico) causados por anomalías cardiacas estructurales o funcionales que conducen a una reducción del gasto cardiaco y/o una elevación de las presiones intracardiacas en reposo o durante el estrés (1,2). Clásicamente, la IC se clasifica atendiendo a la fracción de eyección del ventrículo izquierdo (FEVI) en: con FEVI preservada (≥50% o IC-FEp), reducida (<40% o IC-FEr) o intermedia (entre el 40-49% o IC-FEm) (1). La diferenciación entre IC-FEr e IC-FEp es importante, dado que presentan diferente etiología, fisiopatología, comorbilidades, pronóstico y respuesta al tratamiento.
Importancia socio-sanitaria de la insuficiencia cardiaca
La IC representa un importante problema socio-sanitario ya que: 1) representa la primera causa de hospitalización en pacientes mayores de 65 años. 2) Presenta una alta morbimortalidad y conlleva una pobre calidad de vida para el paciente. En el estudio ESC-HF, la mortalidad anual de los pacientes hospitalizados o ambulatorios con IC era del 17-23% y el 6-7% y las tasas de hospitalización del 19-44% y el 10-21%, respectivamente (3). Sin embargo, la mortalidad a 5 años puede llegar al 75%, es decir, que el pronóstico es peor incluso que muchos tipos de cáncer. 3) En los últimos 25 años, los avances terapéuticos han reducido la mortalidad y las hospitalizaciones por IC-FEr, pero no disponemos de tratamientos que reduzcan la mortalidad en pacientes con IC-FEp, que en la actualidad representa la forma de presentación de la IC en más del 50% de los pacientes y es la predominante en la mujer (1,2). 4) La prevalencia de la IC aumenta con la edad, desde un 1-4% en la población general hasta más del 10% en los mayores de 70 años (1). Por tanto, como consecuencia del aumento de las expectativas de vida de la población general, la utilización de medidas terapéuticas que prolongan la supervivencia del paciente y al marcado aumento de las comorbilidades, en los próximos años se espera un incremento en la prevalencia de la IC. 5) La IC representa la vía final de otras muchas patologías que coexisten o inducen la aparición de la IC, como cardiopatía isquémica, hipertensión arterial, fibrilación auricular, diabetes tipo 2, insuficiencia renal crónica, enfermedad pulmonar obstructiva crónica, anemia, disfunción valvular, infecciones o enfermedades pericárdicas o miocardiopatías. Las comorbilidades aumentan con la edad del paciente y es de señalar que aunque en los últimos 20 años las hospitalizaciones por causas cardiovasculares apenas si se han modificado en los pacientes con IC, las hospitalizaciones por causas no cardiovasculares han aumentado de forma progresiva y ya representan más del 60% del total (4). 6) El coste de la enfermedad es muy alto, representando casi el 2% del gasto sanitario anual en España, siendo las hospitalizaciones las responsables del 75-85% de dicho gasto (1,5). Todos estos datos justifican la búsqueda de nuevos fármacos seguros y eficaces que puedan coadministrarse con los restantes tratamientos que recibe el paciente.
Objetivos del tratamiento de la insuficiencia cardiaca
Dada su alta morbimortalidad, el tratamiento médico de la IC tiene como objetivos (Tabla 1): a) reducir la mortalidad total y/o cardiovascular; b) disminuir las hospitalizaciones debidas por IC; c) mejorar el estado clínico (utilizando biomarcadores y/o parámetros hemodinámicos), la capacidad funcional y la calidad de vida; y d) prevenir o retrasar el deterioro de la función cardiaca y del remodelado cardiaco, es decir, modificar la evolución temporal de la IC. La modificación de los factores de riesgo cardiovascular y el tratamiento agresivo y temprano de las comorbilidades que frecuentemente facilitan la progresión o desencadenan la IC (p.ej. cardiopatía isquémica, hipertensión, diabetes mellitus, etc.) es crítico para diseñar un tratamiento individualizado, retrasar la evolución de la IC, reducir las hospitalizaciones y aumentar la supervivencia.
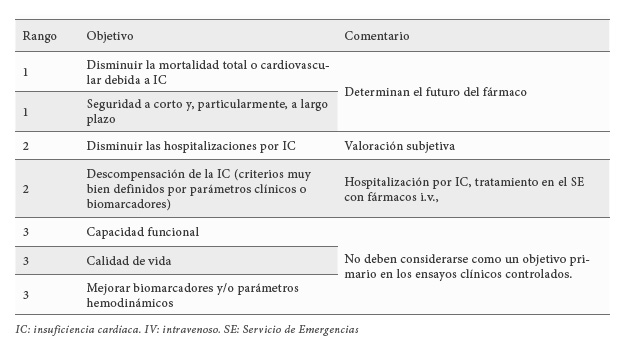
El hallazgo de que algunos fármacos inotrópicos positivos y vasodilatadores utilizados pueden producir un beneficio clínico y hemodinámico a corto plazo, pero pueden aumentar la mortalidad a largo plazo, ha llevado a la European Medicines Agency (EMA) considere que antes de aprobar un nuevo fármaco para el tratamiento de la IC éste debe de demostrar que reduce la mortalidad/morbilidad a corto y largo plazo. No obstante, reconoce que prevenir las hospitalizaciones y mejorar la capacidad funcional podrían tenerse en cuenta, siempre que el fármaco no incremente la mortalidad (6).
Avances recientes en el tratamiento de la insuficiencia cardiaca crónica
Entre 1980 y 2003 los ensayos clínicos demostraron que el tratamiento con inhibidores de la enzima de conversión (IECAs) o con antagonistas de los receptores AT1 de la angiotensina II (ARAII), de los receptores β-adrenérgicos o de los receptores de mineralocorticoides reducía significativamente la morbilidad y mortalidad de los pacientes con IC-FEr (1,7). Estos fármacos, unido a un mejor tratamiento de la cardiopatía isquémica y de las comorbilidades, ha disminuido la mortalidad y cronificado la IC, pero ha incrementado las hospitalizaciones y los gastos sanitarios. En cualquier caso, en tratamiento de la IC-FEr sigue siendo insatisfactorio y la mortalidad sigue siendo muy alta, lo que justifica la búsqueda incansable de nuevos fármacos (8).
Sin embargo, en los últimos 17 años sólo dos fármacos han sido aprobados en el tratamiento de la IC-FEr:
1) La ivabradina, un fármaco bradicardizante comercializado como antianginoso que actúa como un bloqueante selectivo de la corriente de la corriente de marcapaso (If) que controla la despolarización espontánea en las células del nódulo sinoauricular y regula la frecuencia cardíaca (7). En el estudio SHIFT (Systolic Heart Failure Treatment with the If inhibitor ivabradine trial) realizado en 6.558 pacientes con IC-FEr estable que recibían el tratamiento estándar y presentaban una frecuencia cardiaca en reposo ≥70 lpm, la ivabradina reducía significativamente, con respecto a placebo, las hospitalizaciones por IC pero no la mortalidad cardiovascular (9). Por tanto, la ivabradina sólo está indicado en pacientes en ritmo sinusal con una frecuencia cardíaca ≥70 lpm, en asociación al tratamiento estándar que incluye β-bloqueantes o cuando éstos están contraindicados o no se toleran.
2) Sabubitril-valsartan es la combinación de valsartán, un ARAII, y sacubitril, un profármaco que se metaboliza en LBQ657 que inhibe la neprilisina, enzima encargada de la degradación de diversos péptidos vasoactivos endógenos (natriuréticos, adrenomedulina, bradicinina, sustancia P, el relacionado con el gen de la calcitonina) (7). El estudio PARADIGM-HF (Prospective comparison of ARNI with ACEI to Determine Impact on Global Mortality and morbidity in Heart Failure) comparó sacubitril-valsartán con enalapril en 8.300 pacientes con IC-FEr que recibían el tratamiento estándar (10). El estudio se suspendió de forma prematura al observar que S/V reducía la mortalidad cardiovascular (20%), súbita (20%), por IC (21%) o total (16%) y la hospitalización por IC (21%) más que el enalapril, que hasta entonces se consideraba el fármaco de referencia en el tratamiento de la IC.
Si ahora analizamos los avances realizados en el tratamiento de la IC-FEp, los resultados son muy desalentadores, ya que hasta la fecha ningún fármaco ha conseguido reducir la mortalidad en los pacientes con IC-FEp, aunque dos fármacos han abierto nuevas perspectivas. En primer lugar, un análisis post-hoc no especificado del estudio TOPCAT (Aldosterone Antagonist Therapy for Adults With Heart Failure and Preserved Systolic Function), que sólo se incluía a los pacientes reclutados en América (no a los europeos), ha demostrado que en pacientes con IC-FEp, la espironolactona reducía el objetivo primario (muerte cardiovascular, hospitalizaciones por IC o muerte súbita resucitada). Sorprendentemente, este beneficio era debido exclusivamente a la reducción de la mortalidad cardiovascular, no por IC (11). Por otro lado, el estudio PARAGON-HF (Efficacy and Safety of LCZ696 Compared to Valsartan, on Morbidity and Mortality in Heart Failure Patients With Preserved Ejection Fraction) realizado en 4.822 pacientes con IC-FEp, demostró que sacubitril-valsartán no modificaba el objetivo primario compuesto de hospitalización por IC y mortalidad cardiovascular con respecto al valsartán, aunque sí se observaba un beneficio en los pacientes con IC-FEm (12). Además, en un análisis pre-especificado, sacubitril-valsartán reducía el objetivo primario en mujeres (27%), pero no en varones, un hallazgo de gran interés clínico ya que la IC-FEp predomina en las mujeres. Como consecuencia, el pasado 16 de febrero, la Food and Drug Administration de los EEUU (FDA) ha aceptado el uso de sacubitril-valsartán en determinados pacientes con IC-FEp.
Causas de nuestro fracaso
Es pues el momento de preguntarnos ¿por qué hemos fracasado repetidamente en el desarrollo de fármacos en el tratamiento de la IC?. Desde luego la causa no puede atribuirse a la incapacidad para identificar posibles dianas terapéuticas, ya que como muestra la Tabla 2 en los últimos años 15 años, se han identificado múltiples dianas potencialmente implicadas en la génesis/progresión de la IC y numerosos fármacos con muy distintos mecanismos de acción han sido valuados en ensayos clínicos controlados, la mayoría de los cuales no han conseguido reducir la mortalidad con respecto al tratamiento estándar recomendado en las guías de práctica clínica). Las principales causas que a mi entender explican los repetidos fracasos se resumen en la Tabla 3 (8,13-15). Sólo analizaré alguno de ellos:

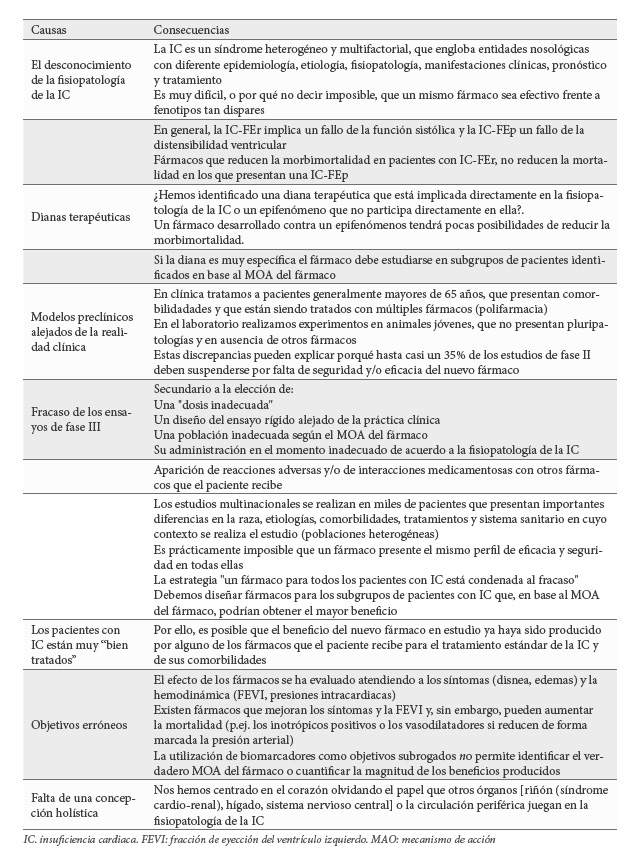
1) La primera limitación para un diseño racional de nuevos fármacos y la causa de los repetidos fracasos es nuestro desconocimiento de la fisiopatología de la IC, un síndrome heterogéneo y multifactorial, que engloba entidades nosológicas con diferente epidemiología, etiología, fisiopatología, manifestaciones clínicas, pronóstico y tratamiento y que lo único que tienen en común los pacientes es que presentan un cuadro clínico compatible con el diagnóstico de IC. Por tanto, parece lógico pensar que es muy difícil, o por qué no decir imposible, que un mismo fármaco sea efectivo frente a fenotipos tan dispares.
2) Las dianas terapéuticas identificadas en los estudios preclínicos pueden ser realmente una diana terapéutica implicada directamente en la fisiopatología de la IC o un epifenómeno. En este último caso el fármaco desarrollado tendrá pocas posibilidades de reducir la mortalidad. Otras veces identificamos una diana tan específica que la seguridad y eficacia del fármaco sólo podrá demostrarse si se estudia en subgrupos de pacientes seleccionados en base a su mecanismo de acción, algo que no sucede en los ensayos clínicos de fase II-III que habitualmente incluyen a grupos de pacientes muy heterogéneos.
3) Los modelos preclínicos utilizados para identificar nuevos fármacos seguros y eficaces están alejados de la realidad clínica. En clínica tratamos de por vida a pacientes generalmente mayores 65 años, que presentan varias comorbilidades (pluripatología) y que están siendo tratados con múltiples fármacos prescritos o no (polifarmacia). Sin embargo, en el laboratorio realizamos experimentos “limpios” para poder identificar una terminada vía de señalización, en ausencia de otros fármacos y en células o animales que no presentan comorbilidades. Esta discrepancia puede explicar porqué hasta casi un 35% de los estudios de fase II deben suspenderse por falta de seguridad y/o eficacia del nuevo fármaco.
4) En la actualidad, los pacientes con IC están muy “bien tratados” y es posible que el beneficio del nuevo fármaco en estudio ya haya sido producido por alguno de los fármacos que el paciente recibe para el tratamiento estándar de la IC y de sus comorbilidades. Esta es una de las razones por las que en el momento actual cada vez más fármacos no son superiores al tratamiento estándar en los ensayos clínicos.
5) Los estudios de fase III se realizan en miles de pacientes que presentan importantes diferencias en su raza, etiología, comorbilidades, tratamiento de éstas o el sistema sanitario en cuyo contexto se realiza en estudio. Esta heterogeneidad implica que es prácticamente imposible que un fármaco presente el mismo perfil de eficacia y seguridad en todos los pacientes. Dicho en otras palabras, no hay fármacos para todos los pacientes, sino para determinados pacientes con IC y la estrategia utilizada durante los últimos 60 años de “un fármaco para todos los pacientes está condenada al fracaso”.
6) Durante décadas la evaluación de fármacos en el tratamiento de la IC ha estado centrado en los síntomas (disnea, edemas) y la hemodinámica (FEVI, presiones intracardiacas). Sin embargo, un fármaco puede mejorar los síntomas y la fracción de eyección y no disminuir, sino aumentar, la mortalidad. Esto es lo que ha sucedido con los inotrópicos positivos o los vasodilatadores que reducen de forma marcada la presión arterial. (13-15).
7) Por último, hemos centrado nuestra mirada en el corazón, olvidando el papel que otros órganos [riñón (síndrome cardio-renal), hígado, sistema nervioso central] o la circulación periférica juegan en la fisiopatología de la IC. Es evidente que todos estos órganos diana y la circulación periférica merecen un mayor reconocimiento si queremos reducir la morbimortalidad del paciente.
Nuevos fármacos obtenidos por serendipia
Decía Albert Einstein que la serendipia es como “como salir a buscar gusanos y encontrar oro“. Algo así ha sucedido muy recientemente con algunos nuevos fármacos antidiabéticos orales. Durante 50 años el patrón estándar de evaluación los fármacos antidiabéticos estaba determinada por su capacidad para reducir los niveles plasmáticos de hemoglobina glicosilada (HbA1c) en pacientes diabéticos. Sin embargo, dos hechos que cuestionaban esta hipótesis glucocéntrica: que la reducción marcada de la HbA1c no se acompañaba de una disminución paralela en la incidencia de eventos cardiovasculares mayores (excepción hecha del infarto de miocardio) y que algunos fármacos que reducían la HbA1c podían aumentar la mortalidad cardiovascular (p.ej. la rosiglitazona). Es por ello, que en 2008 la FDA y la EMA establecieron que los nuevos fármacos antidiabéticos deberían también demostrar en estudios de fase III que no incrementaban el riesgo cardiovascular del paciente diabético. Y quiero recordar que hace ya 40 años que el Framingham Heart Study demostró que la diabetes tipo 2 duplicaba el riesgo de IC-FEr en hombres y lo quintuplicaba en mujeres (16).
El hallazgo inesperado fue que algunos nuevos antidiabéticos orales, como albiglutida (un agonista del receptor de GLP-1) y los inhibidores del cotransportador sodio-glucosa tipo-2 (SGLT2Is) del túbulo proximal renal (canagliflozina, dapagliflozina, empagliflozina, ertugliflozina), reducían significativamente las hospitalizaciones por IC-FEr en pacientes diabéticos y que este efecto aparecía ya en las primeras semanas de tratamiento (17-19). Más sorprendente ha sido el hallazgo de que dapagliflocina y empagliflozina reducen la mortalidad cardiovascular y el empeoramiento de la IC-FEr (que conduce a la hospitalización o a la visita a urgencias y obliga a un tratamiento i.v.) en pacientes con IC previa, independientemente de la presencia o no de diabetes tipo 2 (DM2) (18,19). Sin embargo, los estudios que han llevado a estos sorprendentes hallazgos no eran mecanicistas, por lo que los mecanismos implicados en la rápida reducción de las hospitalizaciones por IC son desconocidos, aunque no pueden atribuirse a los discretos cambios observados en los niveles de HbA1c, presión arterial, peso corporal o volemia (20).
En la actualidad, las guias de la Sociedad Europea de Cardiología recomiendan que se debe considerar el uso canagliflozina y empagliflozina en pacientes con DM2 y enfermedad cardiovascular establecida o con alto riesgo cardiovascular para prevenir o retrasar el inicio y las hospitalizaciones producidas por la IC (2). Sin embargo, no se realizan recomendaciones específicas para el uso de SGLT2Is en pacientes con IC-FEr establecida.
CONCLUSIONES
La IC sigue representando un desafío clínico por su alta prevalencia, morbilidad y mortalidad. Si bien disponemos de fármacos seguros que reducen la morbimortalidad en pacientes con IC-FEr, hasta la fecha ningún fármaco ha demostrado reducir la mortalidad de los pacientes con IC-FEp. El fracaso repetido de los muchos fármacos ensayados en el tratamiento de la IC es el resultado de considerar el síndrome como una entidad única, olvidando su compleja fisiopatología y sus múltiples fenotipos y de la identificación de numerosas supuestas dianas terapéuticas que, en muchos casos son simples epifenómenos. Dado que estamos hablando de múltiples síndromes con fenotipos superpuestos, la estrategia de tratar IC como una entidad única (“one size fits all approach“) está condenada al fracaso y debe ser reemplazada por el desarrollo de nuevos fármacos basados en una mejor comprensión de los mecanismos fisiopatológicos involucrados en la génesis y progresión de la IC, teniendo presente un abordaje holístico de este síndrome clínico en el que otros órganos, además del corazón, y otras frecuentes comorbilidades juegan un papel clave. El desarrollo de nuevos fármacos debe tener en cuenta las causas de los numerosos fracasos para evitar la repetición de viejos errores.
BIBLIOGRAFÍA
- Ponikowski P, Voors, AA, Anker SD, et al. 2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure: The Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC) Developed with the special contribution of the Heart Failure Association (HFA) of the ESC. Eur Heart J. 2016; 37: 2129-2200.
- Seferovic PM, Ponikowski P, Anker SD, et al. Clinical practice update on heart failure 2019: pharmacotherapy, procedures, devices and patient management: an expert consensus meeting report of the Heart Failure Association of the European Society of Cardiology. Eur J Heart Fail. 2019; 21: 1169-1186.
- Crespo-Leiro MG, Anker SD, Maggioni AP, Coats AJ, Filippatos G, Ruschitzka F, et al. European Society of Cardiology Heart Failure Long-Term Registry (ESC-HF-LT): 1-year follow-up outcomes and differences across regions. Eur J Heart Fail. 2016; 18(6): 613-625.
- Gerber Y, Weston SA, Redfield MM, et al. A contemporary appraisal of the heart failure epidemic in Olmsted County, Minnesota, 2000 to 2010. JAMA Intern Med. 2015; 175: 996-1004.
- Lesyuk W, Kriza C, Kolominsky-Rabas P. Cost-of-illness studies in heart failure: a systematic review 2004-2016. BMC Cardiovasc Disord. 2018; 18(1): 74.
- Guideline on clinical investigation of medicinal products for the treatment of chronic heart failure. 20 July 2017, CPMP/EWP/235/95, Rev.2. http://www.ema.europa.eu/docs/en_GB/document_library/Scientific_guideline/2017/09/WC500235089.pdf (acceso: 02/03/2020).
- Tamargo J, Caballero R, Delpón E., eds. Chapter 8.1 Cardiovascular drugs-from A to Z. En: Kaski JC and Kjeldsen KP, eds. The ESC Handbook on Cardiovascular Pharmacotherapy (2 edn). Oxford University Press. 2019. p. 413-812.
- Tamargo J, Caballero R, Delpón E. New drugs in preclinical and early stage clinical development in the treatment of heart failure. Expert Opin Investig Drugs. 2019; 28(1): 51-71.
- Swedberg K, Komajda M, Böhm M, Borer JS, Ford I, Dubost-Brama A, et al. Ivabradine and outcomes in chronic heart failure (SHIFT): a randomised placebo-controlled study. Lancet. 2010; 376(9744): 875-885.
- McMurray JJ, Packer M, Desai AS, et al. Angiotensin–neprilysin inhibition versus enalapril in heart failure. N Engl J Med. 2014; 371: 993-1004.
- Solomon SD, Claggett B, Lewis EF, et al. Influence of ejection fraction on outcomes and efficacy of spironolactone in patients with heart failure with preserved ejection fraction. Eur Heart J. 2016; 37(5) :455-462.
- McMurray JJ, Jackson AM, Lam CS, et al. Effects of sacubitril-valsartan versus valsartan in women compared with men with heart failure and preserved ejection fraction. Circulation 2020; 141(5): 338-351.
- Tamargo J, Amorós I, Barana A, Caballero R, Delpón E. New investigational drugs for the management of acute heart failure syndromes. Curr Med Chem. 2010; 174: 363-390.
- Tamargo J, López-Sendón J. Novel therapeutic targets for the treatment of heart failure. Nat Rev Drug Discov. 2011; 10(7): 536-555.
- Tamargo J, Rosano GM, Delpón E, Ruilope L, López-Sendón J. Pharmacological reasons that may explain why randomized clinical trials have failed in acute heart failure syndromes. Int J Cardiol. 2017; 233: 1-11.
- Kannel WB, McGee DL. Diabetes and glucose tolerance as risk factors for cardiovascular disease: the Framingham study. Diabetes Care. 1979; 2(2): 120-126.
- Zelniker TA, Wiviott SD, Raz I, et al. Comparison of the effects of glucagon-like peptide receptor agonists and sodium-glucose cotransporter 2 inhibitors for prevention of major adverse cardiovascular and renal outcomes in type 2 diabetes mellitus: systematic review and meta-analysis of cardiovascular outcomes trials. Circulation. 2019; 139(17): 2022-2031.
- McMurray JJ, Solomon SD, Inzucchi SE, et al. Dapagliflozin in patients with heart failure and reduced ejection fraction. N Engl J Med. 2019; 381: 1995-2008.
- Packer M, Anker SD, Butler J, et al; EMPEROR-Reduced Trial Investigators. Cardiovascular and renal outcomes with empagliflozin in heart failure. N Engl J Med 2020; 383(15): 1413-1424.
- Tamargo J. Sodium–glucose cotransporter 2 inhibitors in heart failure: potential mechanisms of action, adverse effects and future developments. Eur Cardiol. 2019; 14(1): 23-32.
DECLARACIÓN DE TRANSPARENCIA
El autor/a de este artículo declara no tener ningún tipo de conflicto de intereses respecto a lo expuesto en el presente trabajo.
ranm tv
Juan Tamargo
Dpto. de Farmacología y Toxicología. Facultad de Medicina. U. Complutense
IiSGM. CIBERCV · 28040 Madrid
Tlf.: +34 913 941 472 | E-Mail: jtamargo@med.ucm.es
Año 2021 · número 138 (01) · páginas 44 a 51
Enviado*: 03.03.21
Revisado: 12.03.21
Aceptado: 10.04.21
* Fecha de lectura en la RANM


