Resumen
La enfermedad de Parkinson (EP) es el segundo proceso neurodegenerativo más frecuente en la población mayor de 65 años, cuya incidencia aumentará con el progresivo envejecimiento poblacional en los próximos años. Hasta la fecha, el diagnóstico se realiza, en la mayoría de los casos, cuando la pérdida de neuronas de la sustancia negra pars compacta (SNc) alcanza un 50-60% y la pérdida de dopamina en el estriado es de un 70-80%, coincidiendo con la aparición los signos motores clásicos de la enfermedad: temblor, rigidez y lentitud de movimientos. En una proporción de pacientes se constatan síntomas no motores, generalmente asociados a la alteración de regiones no dopaminérgicas, que pueden surgir con marcada antelación (ej. 10-15 años), alrededor del diagnóstico o posteriormente. Por tanto, la EP está asociada a la afectación de grupos tanto dopaminérgicos como no dopaminérgicos, pero las manifestaciones motoras representan el motivo de consulta y causa mayor de incapacidad durante muchos años.
Dentro de los grupos neuronales dopaminérgicos existe una gran heterogeneidad en términos de morfología, metabolismo, patrones moleculares, acumulación de proteínas, niveles de inflamación, expresión de proteínas, etc. En esta revisión se exponen los hallazgos de distintos factores que podrían explicar la especial vulnerabilidad de determinadas neuronas dopaminérgicas de la SNc. Conocer los mecanismos y factores subyacentes a la vulnerabilidad selectiva de las neuronas dopaminérgicas de la región ventrolateral de la SNc es imprescindible para desarrollar terapias neuromoduladoras y/o neuroprotectoras efectivas que frenen o modifiquen el proceso neurodegenerativo en la EP.
Abstract
Parkinson´s disease (PD) is the second most frequent neurodegenerative disease affecting the population older than 65 years old. This incidence will greatly increase due to the progressive aging of the population in the coming years. PD diagnosis is made when there is a 50-60% dopaminergic cell loss in the substantia nigra pars compacta (SNc) and the striatal dopamine loss reaches around 70-80%, coinciding with the onset of classical parkinsonian motor signs: tremor, rigidity and slowness of movement. A significant proportion of patients present non-motor symptoms, generally associated to disfunction of non-dopaminergic regions, which can appear before, around or after diagnosis (10-15 years). Therefore, in PD both dopaminergic and non-dopaminergic groups are affected, but the motor manifestations are the main reason for consultation and causes the greatest disability for many years.
There is a large heterogeneity within dopaminergic neural groups in terms of morphology, metabolism, molecular pattern, protein accumulation, inflammation levels, protein expression, etc. In this review we discuss different factors that could explain the special vulnerability of certain dopaminergic neurons in the SNc. Knowledge on the mechanisms and underlying factors of this selective vulnerability of the ventrolateral dopaminergic neuros of the SNc is essential for developing neuromodulatory and/or neuroprotective therapies, leading in turn to halt or modify the neurodegenerative process in PD.
Palabras clave: Enfermedad de Parkinson; Vulnerabilidad selectiva; Calbindina; Dopamina; Sustancia negra; neurodegeneración.
Keywords: Parkinson´s disease; Selective vulnerability; Calbindin; Dopamine; Substantia nigra; Neurodegeneration.
INTRODUCCIÓN
La enfermedad de Parkinson (EP) es la segunda enfermedad neurodegenerativa más frecuente, afectando al 1-3% de la población mayor de 65 años, y la más abundante dentro de las denominadas alteraciones del movimiento (1). Debido al progresivo envejecimiento poblacional, se calcula un incremento de la prevalencia mundial de la EP desde 6,9 millones de personas en 2015 a 14 millones en 2040 (1).
La EP se caracteriza por la degeneración de las neuronas dopaminérgicas situadas en la sustancia negra pars compacta (SNc), que se asocia estrechamente a la aparición de los signos motores parkinsonianos (1). Desde el punto de vista clínico, el diagnóstico de la enfermedad se realiza, generalmente, cuando aparecen las manifestaciones motoras. No obstante, en la EP también se observa la presencia de un amplio espectro de síntomas no motores que pueden preceder incluso en décadas al desarrollo de los signos motores, como por ejemplo, alteraciones gastrointestinales, disautonomía, alteraciones sensitivas, trastornos del sueño y síntomas neuropsiquiátricos (1,2).
El tratamiento sintomático de la EP en la actualidad se centra fundamentalmente en terapias que reestablecen el déficit de dopamina (DA) estriatal, así como otras terapias más avanzadas como son la estimulación cerebral profunda o el ultrasonidos de alta intensidad (HIFU, por su siglas en inglés High Intensity Focus Ultrasound). A modo preventivo se utiliza también rehabilitación motora y cognitiva. En conjunto, las medidas terapéuticas actuales permiten controlar las principales causas de incapacidad hasta fases avanzadas de la EP. Sin embargo, el curso progresivo del proceso neurodegenerativo acaba provocando situaciones de alta incapacidad y dependencia. Por ello, un reto pendiente importante es desarrollar terapias modificadoras de la enfermedad que permitan enlentecer la progresión o frenar el proceso neurodegenerativo (3).
1.CARACTERÍSTICAS HISTOPATOLÓGICAS DE LA EP
Desde el punto de vista histopatológico, la EP se caracteriza por la degeneración de las neuronas dopaminérgicas en la SNc (1). La degeneración dopaminérgica afecta principalmente a la región caudoventrolateral de la SNc (grupo dopaminérgico A9) y progresa hacia regiones más rostrodorsomediales (4,5). Los signos motores de la EP no aparecen, sin embargo, hasta que la depleción de neuronas dopaminérgicas de la SNc es del 50-60% y la denervación dopaminérgica estriatal es del 70-80% (1,6). Además de la SNc, otros grupos dopaminérgicos, como el área retrorrubral (A8) o el área tegmental ventral (Ventral Tegmental Area, VTA, del inglés, A10), presentan una afectación dopaminérgica más leve (5). Asimismo, el proceso neurodegenerativo en la EP afecta a otros núcleos no dopaminérgicos como el locus coeruleus (LC), el núcleo basal de Meynert (NBM), el núcleo pedunculopontino (PPT), el núcleo motor dorsal del vago (NMDV), los núcleos del rafe, la amígdala y el hipocampo (7) y, por tanto, a otros sistemas como el noradrenérgico y el serotoninérgico (8).
La otra característica histopatológica de la EP es la presencia de inclusiones intraneuronales llamadas cuerpos de Lewy (Lewy bodies, del inglés) compuestos, principalmente, por el plegamiento aberrante de la proteína alfa-sinucleína, junto con otras proteínas como la ubiquitina y la proteína p62 (9). En la EP, el depósito citoplasmático de los cuerpos de Lewy no se limita solo a la SNc, sino a otras regiones del sistema nervioso central y periférico, por lo que se ha propuesto un patrón de progresión topográfico de dichos depósitos, con inicio en el bulbo raquídeo y una progresión posterior con patrón caudocraneal, afectando a múltiples estructuras cerebrales (10). Sin embargo, la relación entre la agregación de alfa-sinucleína, la neurodegeneración y los signos clínicos no ha sido esclarecida aún (7,9).
2.CARACTERÍSTICAS CLÍNICAS
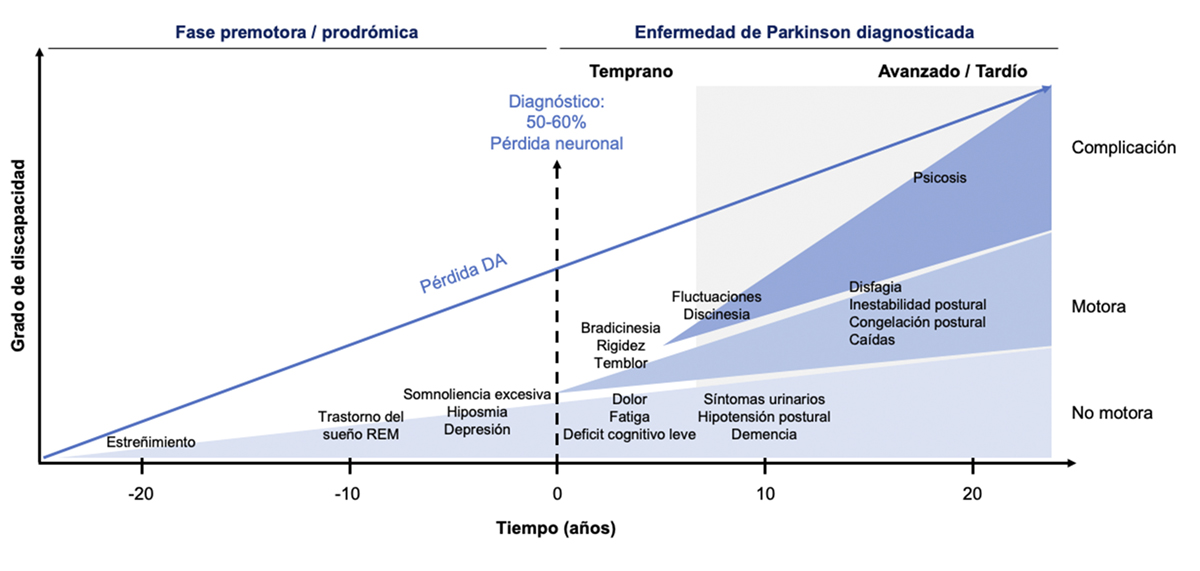
Los signos motores clásicos de la EP son un componente fundamental de la enfermedad como ya quedó expuesto en la descripción inicial que realizó James Parkinson en el siglo XX (11). Entre las manifestaciones motoras de la EP se incluyen la clásica tríada: bradicinesia, rigidez muscular y temblor de reposo. Estas manifestaciones suelen tener un inicio unilateral y asimétrico, además de tener una mejoría marcada con el tratamiento dopaminérgico (12). Tanto la progresión como la gravedad de los síntomas se relacionan estrechamente con el grado de degeneración de las neuronas dopaminérgicas de la SNc (13) (Figura 1).
Desde el punto de vista motor se puede diferenciar entre dos formas de presentación clínica: EP con predominio de temblor y EP sin predominio de temblor (aquellos en los que predomina un síndrome rígido-acinético) (14,15).
Además de los signos motores los pacientes también presentan síntomas no motores entre los que se incluyen alteraciones gastrointestinales (como estreñimiento o retraso en el vaciamiento gástrico), disautonomía (como nicturia o disfunción sexual), alteraciones sensitivas (como anosmia o dolor), trastornos del sueño (trastornos del comportamiento del sueño REM o insomnio, entre otros) y signos neuropsiquiátricos (como depresión, apatía o déficits cognitivos) (2). Los síntomas no motores suelen aparecer incluso décadas antes que los signos motores y están presentes en más del 90% de los pacientes a lo largo de la evolución de la enfermedad. Los síntomas no motores como estreñimiento, hiposmia, trastornos del sueño REM y depresión (2) caracterizan la fase premotora o prodrómica de la enfermedad, pudiendo desarrollarse décadas antes de la aparición del fenotipo motor parkinsoniano (Figura 1) pero que no son suficientes para la realización del diagnóstico clínico (16). Este periodo premotor supone una ventana temporal fundamental para el estudio del proceso fisiopatológico subyacente a la enfermedad, así como para la aplicación de tratamientos modificadores que permitan la prevención o el retraso del desarrollo y la progresión de la EP.
El número y gravedad de los síntomas no motores se incrementa con la progresión de la enfermedad (1,17) (Figura 1). Estos síntomas tienen un gran impacto negativo en la calidad de vida de los pacientes, tanto o más que los signos motores. Desde el punto de vista anatomopatológico, el desarrollo de alguno de los síntomas no motores se ha relacionado con el patrón de agregación de alfa-sinucleína, el grado de depleción dopaminérgica y la afectación de otros sistemas, especialmente el noradrenérgico y serotoninérgico (2,9).
3.PÉRDIDA NEURONAL EN LA EP
Como se ha descrito anteriormente, en la EP hay una pérdida inicial y predominante de neuronas dopaminérgicas de la SNc que proyectan al estriado, causando una depleción de DA en esta región. En los pacientes tempranos de EP se observa, mediante imágenes de tomografía por emisión de positrones (PET del inglés), que la región que primero pierde DA es la parte más dorsal del putamen postcomisural. Por tanto, de cara a desarrollar terapias neuroprotectoras en el estadio inicial de la EP debemos atender principalmente a estas dos regiones, la SNc y el putamen dorsal, para tratar de responder a dos preguntas: a) ¿Qué características tiene la SNc que la hacen tan vulnerable en la EP? y b) ¿Qué neuronas forman las conexiones nigro-estriatales y estriato-nigrales más afectadas en la enfermedad?
3.1.TERRITORIOS ANATÓMICOS VULNERABLES EN LA EP
Además de la SNc, la acumulación de LB y la muerte neuronal también afectan a otros núcleos del sistema nervioso central y periférico (7,9). Las neuronas colinérgicas del núcleo PPT, del NBM y del núcleo DMV, las neuronas noradrenérgicas del LC y las neuronas serotoninérgicas del núcleo del rafe también se ven afectadas. De la misma forma, algunos estudios muestran que algunos núcleos talámicos como el núcleo centromediano-parafascicular, el hipotálamo, el hipocampo y el bulbo olfatorio presentan alteraciones en el número de neuronas (7). Es importante destacar que la afectación de estos núcleos correlaciona con la progresión de los síntomas no motores. Por tanto, aunque los signos motores característicos de la enfermedad se relacionan con la pérdida de función o la muerte de las neuronas dopaminérgicas, los signos no motores podrían seguir el patrón de afectación de neuronas no dopaminérgicas (18) (Figura 2).
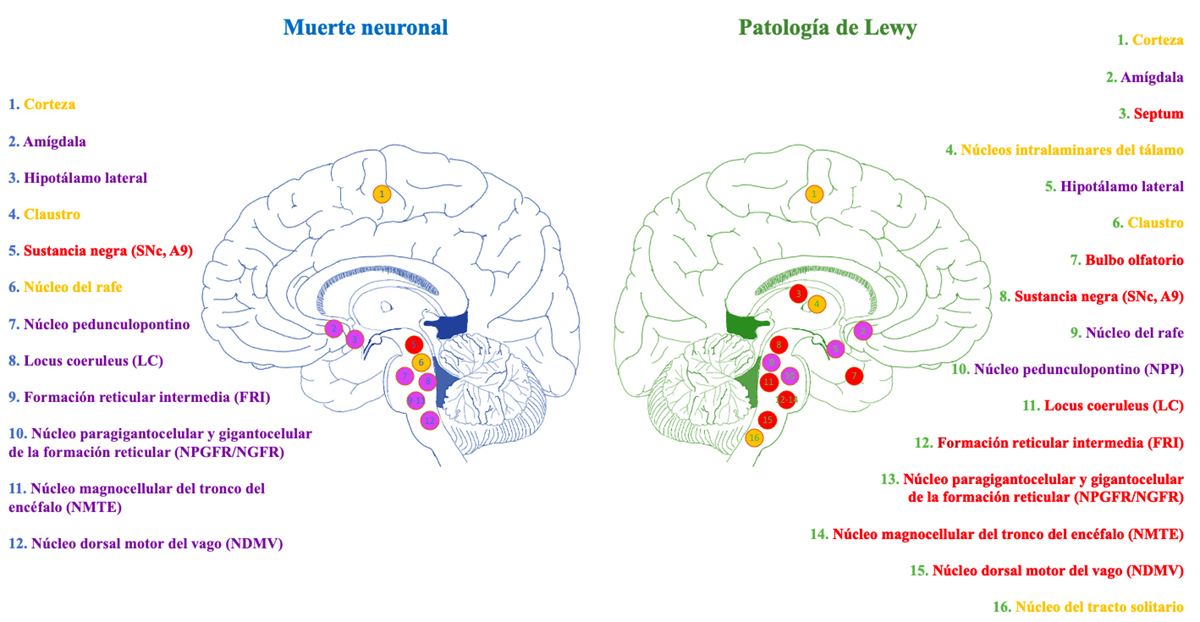
Por otra parte, como se resume en el trabajo de Surmeier y colaboradores, (7) los núcleos que presentan agregados de LB en la EP son la corteza cerebral, el hipotálamo, el núcleo basal de Meynert, la SNc, los núcleos del rafe, el LC, el DMV y los ganglios simpáticos (Figura 2).
3.2.VÍA NIGROESTRIATAL Y OTRAS PROYECCIONES DOPAMINÉRGICAS
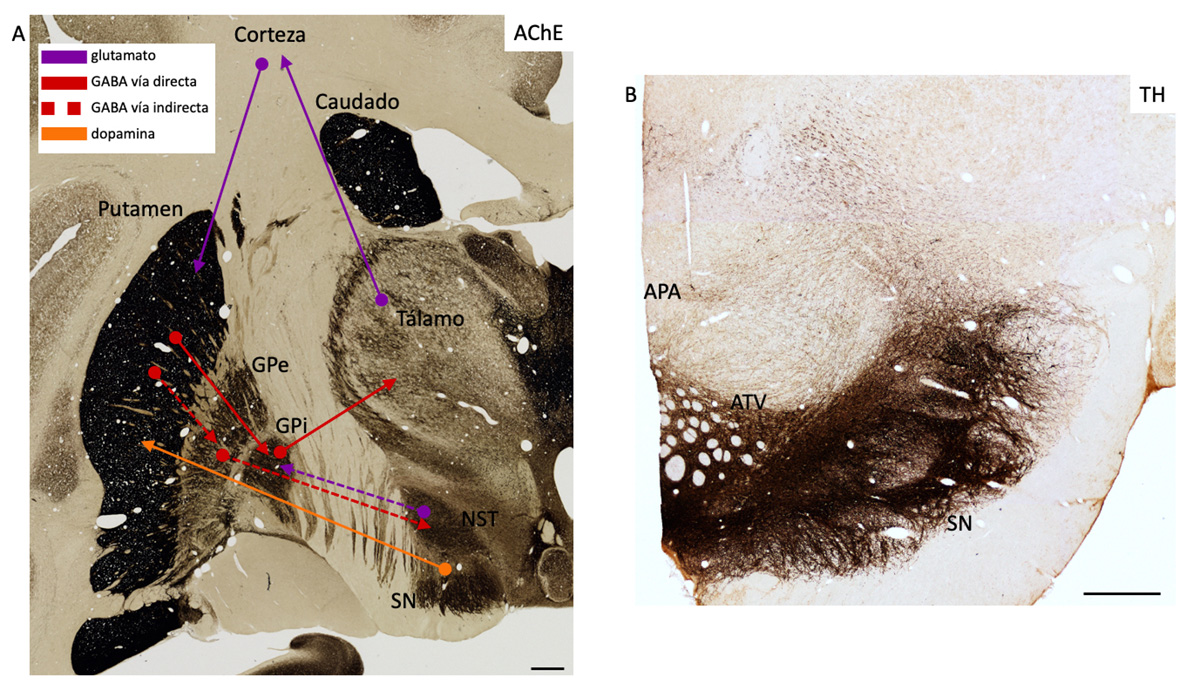
El circuito nigroestriatal está topográficamente organizado como se ha demostrado en experimentos con trazadores en primates (19–21). Las neuronas de las regiones ventrolaterales y posteriores de la SNc proyectan principalmente al putamen posterior (motor), mientras que las células más mediales de la SNc proyectan al putamen anterior y a la cabeza del caudado. Ambas proyecciones forman generalmente grupos independientes que se sobreponen en la mayoría de los planos, indicando una falta de organización topográfica precisa (Figura 3).
Haber (2000) describió en detalle la organización de la proyección nigro-estriatal en primates mediante estudios con trazadores anterógrados y retrógrados. En resumen, el estriado y la SNc forman un circuito estriato-nigro-estriatal en el que se pueden observar tres circuitos paralelos en relación a las regiones límbica, asociativa y motora del estriado (20). Estos datos se han observado de forma similar en ratones (22). Estudios recientes indican que las proyecciones nigro-extraestriatales también muestran una organización similar a las descritas en el estriado (23). Además, se ha demostrado en ratones un circuito nigro-estriato-nigral en el que los estriosomas proyectan a la región ventral de la SNc y estas proyectan de vuelta a las regiones dorsales del estriado (24).
El mayor número de neuronas dopaminérgicas se encuentra en la SNc y en el VTA (25). Teniendo en cuenta las diferencias interespecies, el número de neuronas tirosina hidroxilasa (TH) positivas en roedores en el VTA y la SNc es similar, mientras que en primates el número de neuronas en la SNc es mucho mayor que en el VTA (26). Ambos núcleos contienen neuronas GABAérgicas, sin embargo el VTA contiene también, aunque pocas, neuronas glutamatérgicas (27). En cuanto a la función, las neuronas de la SNc están involucradas en el control del movimiento y conducta, mientras que las del VTA tienen un papel importante en la regulación de la recompensa y en los procesos de emoción y adicción.
Ambos núcleos presentan proyecciones con un patrón solapante (28), aunque la mayoría de las proyecciones de la SNc inervan la parte dorsal del estriado y solo algunas proyectan al estriado ventral y a la corteza y, por el contrario, las neuronas del VTA proyectan principalmente al estriado ventral y a áreas corticales, enviando escasas proyecciones al estriado dorsal. Las dos regiones proyectan débilmente a otros territorios incluyendo el globo pálido, el núcleo subtalámico y la habénula. Además, una pequeña población del VTA envía proyecciones a la amígdala, mientras que algunas regiones del mesencéfalo proyectan al hipocampo (26).
A pesar de que todas las neuronas de la SN y del VTA comparten características moleculares, anatómicas y funcionales muy similares, como la utilización de DA como neurotransmisor, la localización en regiones próximas y la distribución parecida de sus eferencias, cada grupo exhibe una susceptibilidad diferente a la degeneración en la EP. Mientras que las neuronas del VTA se pierden en un 40%, las neuronas de la SNc alcanzan un 80%-90% de pérdida (5,8,29), siendo la parte más ventrolateral la zona más vulnerable (5,30,31).
3.3.VULNERABILIDAD DIFERENCIAL DE LA SNc EN LA ENFERMEDAD DE PARKINSON
Ya en 1991 Fearnley y Lees (32) identificaron la zona ventrolateral de la SNc como la zona selectivamente más vulnerable en la EP. La distribución de vulnerabilidad neuronal en la EP ha sido descrita en numerosos estudios patológicos (5,33,34), y ha sido observada también mediante imágenes de resonancia magnética (35). Estas observaciones de vulnerabilidad diferencial en la región ventrolateral de la SNc demuestran la importancia de entender las características de dicha zona para comprender los factores que subyacen la vulnerabilidad selectiva y muerte neuronal en la EP, e idealmente desarrollar terapias protectoras.
En general las neuronas dopaminérgicas mesencefálicas son muy heterogéneas. Los datos muestran que la pérdida de neuronas de la SNc sigue un patrón específico y sugieren que existen diferencias moleculares incluso entre subgrupos de neuronas dopaminérgicas dentro de la propia SNc. Por tanto, determinados factores protegen a las neuronas del VTA de la degeneración en comparación con las neuronas de la SNc o, por el contrario, ciertos factores aumentan la vulnerabilidad de las neuronas de la SNc a la pérdida neuronal observada en la EP.
Teniendo en cuenta todos los datos descritos hasta ahora, identificar qué características definen a cada subgrupo celular en base a su vulnerabilidad basal es de gran interés. Entre estas características se han sugerido un déficit en la proteostasis debido a defectos en la función del lisosoma o el proteosoma, la disfunción mitocondrial o el estrés oxidativo mantenido (toxicidad dopaminérgica o glutamatérgica) (36). Caben destacar cuatro hipótesis que conllevarían a una sobrecarga en las neuronas dopaminérgicas haciéndolas de base más vulnerables basadas en: 1) la toxicidad de la DA, 2) el contenido en hierro, 3) el mantenimiento de un marcapasos autónomo y 4) el gran tamaño de su árbol axónico (26). A continuación, se describen algunos factores a nivel molecular que se han relacionado con la susceptibilidad de estas neuronas a una mayor y precoz degeneración en la EP.
3.3.1.CALBINDINA: NIGROSOMA Y MATRIZ
La regulación del metabolismo del calcio en neuronas con una alta tasa metabólica es esencial. De esta forma, la calbindina (CB), una proteína ligadora de calcio cuya función es regular los niveles intracelulares de este ion, se ha propuesto como marcador de vulnerabilidad. La expresión de está proteína queda limitada en roedores a la SNc dorsal y al VTA, mientras que la SNc queda sin teñir (25). Por tanto, aquellas neuronas que expresen CB harán frente de forma más eficaz a una alta tasa metabólica o a un insulto estresante.
De hecho, Daimier y colaboradores describieron dos compartimentos en la SN humana basados en la tinción de CB (4) (Figura 3). Los autores encontraron regiones pobremente teñidas para CB a las que denominaron nigrosoma, mientras que a las zonas que sí quedaban teñidas las etiquetaron como matriz. Estas dos regiones se encuentran de igual forma en el cerebro de primate no humano (Figura 4). La combinación, por tanto, de inmunotinción frente a CB y TH permite diferenciar distintas regiones del mesencéfalo: el VTA y la SN dorsal cuyas neuronas y neuropilo son TH+/CB+, y la SNc ventral, cuyas neuronas son todas TH+/CB-. Dentro de la SNc el patrón de CB en el neuropilo permite diferenciar la matriz (CB+) del nigrosoma (CB-).

Esta última región, el nigrosoma, correspondería con la zona más vulnerable de la SNc. Numerosos trabajos han demostrado que las neuronas CB- en la SNc son más vulnerables tanto en pacientes (5) como en modelos de animales de EP (37,38,39).
Se ha publicado que las neuronas de la SNc que proyectan al estriado (región más vulnerable) no expresan CB, mientras que aquellas que proyectaban al globo pálido (región extra-estriatal) sí lo hacen (37). Esto permite sugerir una correlación entre la especial vulnerabilidad de las neuronas CB- y su correspondiente y selectiva proyección estriatal.
3.3.2.OTROS FACTORES DE VULNERABILIDAD EN LA SNc
La mayoría de los datos de identidad molecular de las neuronas dopaminérgicas se han realizado en roedores analizando diferentes genes que están involucrados en la identidad neuronal, el desarrollo o la síntesis de DA, así como genes que están ausentes, presentes o se expresan en diferentes niveles en las regiones más vulnerables (40). El conocimiento de estos datos permitiría un doble objetivo: a) definir los límites anatómicos de cada subregión dopaminérgica y b) estudiar las características particulares de aquellas regiones más o menos afectadas en la EP para el desarrollo de terapias protectoras y/o modificadoras de la enfermedad.
En el trabajo de Poulin de 2020 (41) se puede encontrar un resumen reciente de estos factores diferenciales de subpoblaciones dopaminérgicas en roedores (Figura 5). Aquí recapitulamos aquellos factores que se han relacionado más específicamente con la vulnerabilidad selectiva de la región ventral de la SNc.
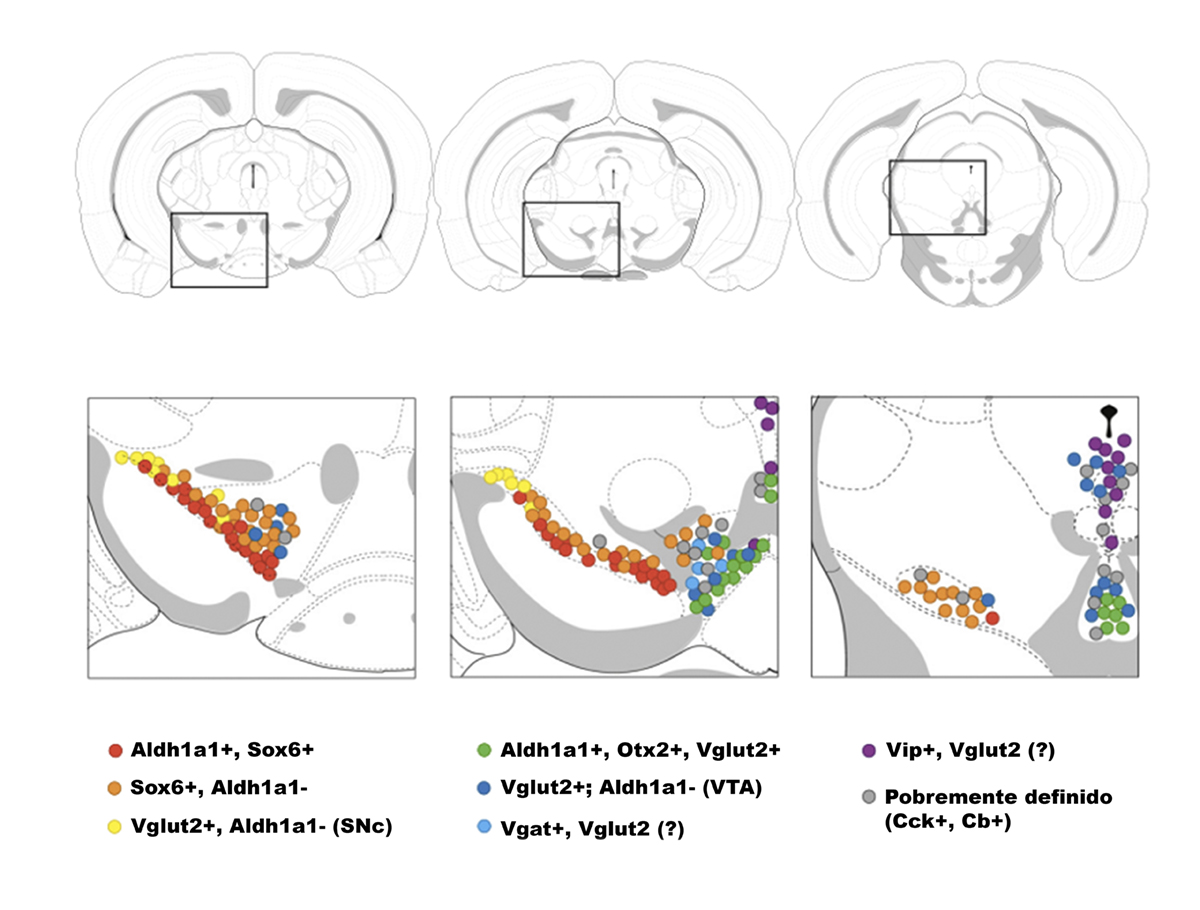
En varios trabajos se ha demostrado que la enzima ALDH1A1 (Aldehyde Dehydrogenase 1 Family Member A1), implicada en el metabolismo de DA y sus metabolitos, se expresa en las neuronas de la parte ventral y vulnerable de la SNc (42) que envían proyecciones a la zona dorsal del estriado (43–45). Esta enzima podría servir como marcador de vulnerabilidad en la EP. Asimismo, el canal de potasio GIRK2 (G-protein-activated inwardly rectifyin potassium channel 2) ha sido considerado como un factor de vulnerabilidad, ya que defectos en esta proteína se asocian con una muerte progresiva de las neuronas dopaminérgicas de la SNc en ratones (46). La expresión de ALDH1A1 y de GIRK2 en la SNc humana parece estar localizada precisamente en las neuronas de la región más ventral y vulnerable (25,47,48).
Por último, también se han propuesto otros fenómenos relacionados con una mayor vulnerabilidad de dichas neuronas entre los que se encuentran la expresión de melanina (29,49), la menor longitud de los telómeros de estas células (7) y la presencia de marcadores de inflamación en los alrededores (50).
CONCLUSIONES
La SNc presenta una vulnerabilidad selectiva de neuronas dopaminérgicas en la EP de origen multifactorial, basado en el estrés celular asociado a diferentes factores: disfunción mitocondrial, proteostasis alterada y elevado estrés oxidativo, entre otros. Sin embargo, estos factores por sí mismos no explican por qué la patología de la EP está restringida a unos núcleos cerebrales específicos. Numerosos estudios, como los descritos en esta revisión han tratado de buscar qué factores diferenciales presentan las neuronas de las regiones más afectadas en la EP. El tema clave pendiente de resolución sigue siendo qué tienen estas neuronas en común que las hacen tan sensibles y más vulnerables en comparación con otras regiones del cerebro (Figura 6).
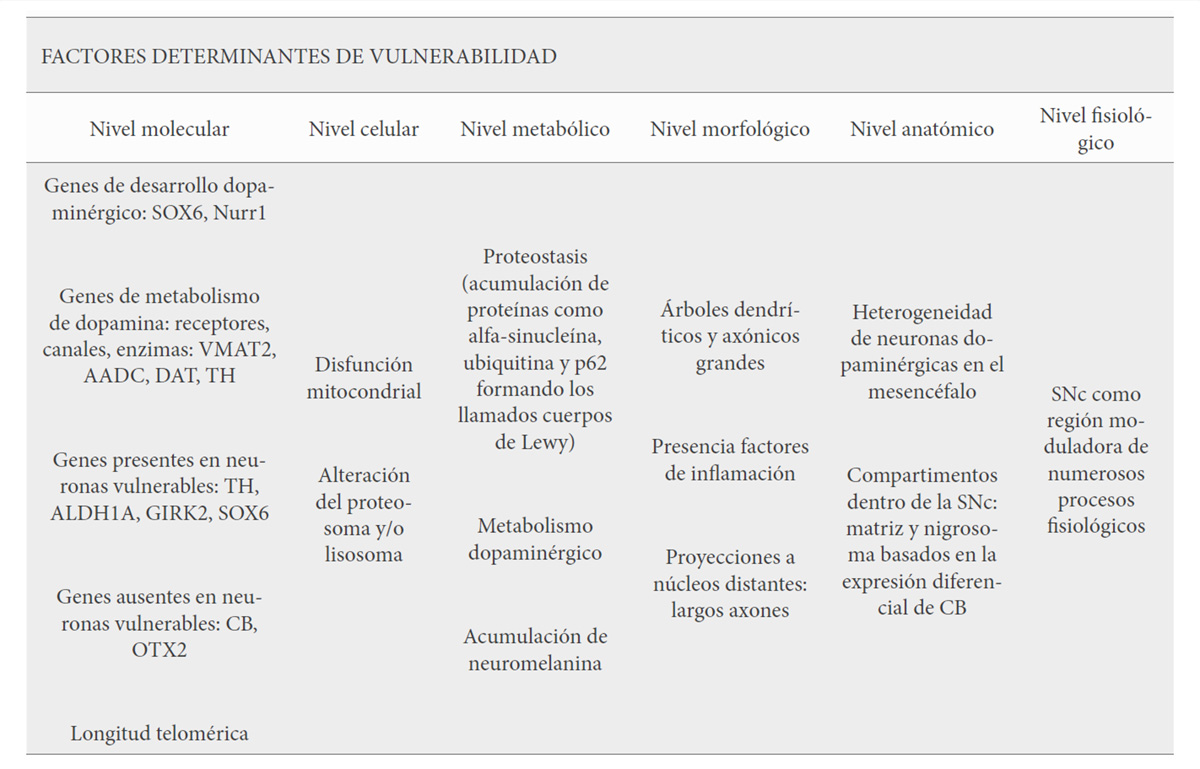
El conocimiento de la naturaleza de la muerte neuronal selectiva y la disfunción celular en el cerebro parkinsoniano es imprescindible para desarrollar estrategias terapéuticas que frenen o protejan del proceso neurodegenerativo.
BIBLIOGRAFÍA
- Kalia LV, Lang AE. Parkinson’s disease. Lancet. 2015; 386(9996): 896-912.
- Schapira AHV, Chaudhuri KR, Jenner P. Non-motor features of Parkinson disease. Nat Rev Neurosci. 2017; 18(7): 435-450.
- Del Rey NL, Quiroga-Varela A, Garbayo E, et al. Advances in Parkinson’s disease: 200 years later. Front Neuroanat. 2018; 12: 113.
- Damier P, Hirsch EC, Agid Y, Graybiel AM. The substantia nigra of the human brain. I. Nigrosomes and the nigral matrix: a compartmental organization based on calbindin D(28K) immunohistochemistry. Brain. 1999; 122(8): 1421-1436.
- Damier P, Hirsch EC, Agid Y, Graybiel AM. The substantia nigra of the human brain II. Patterns of loss of dopamine-containing neurons in Parkinson’s disease. Brain. 1999; 122(8): 1437-1448.
- Ehringer H, Hornykiewicz O. Distribution of noradrenaline and dopamine (3-hydroxytyramine) in the human brain and their behavior in diseases of the extrapyramidal system. Klin Wochenschr. 1960; 4(2):1236-1239.
- Surmeier DJ, Obeso JA, Halliday GM. Selective neuronal vulnerability in Parkinson disease. Nat Rev Neurosci. 2017; 18(2): 101-113.
- Brichta L, Greengard P, Flajolet M. Advances in the pharmacological treatment of Parkinson’s disease: targeting neurotransmitter systems. Trends Neurosci. 2013; 36(9): 543-554.
- Fares MB, Jagannath S, Lashuel HA. Reverse engineering lewy bodies: how far have we come and how far can we go? Nat Rev Neurosci. 2021; 22(2):111-131.
- Braak H, Del Tredici K, Rüb U, De Vos RAI, Jansen Steur ENH, Braak E. Staging of brain pathology related to sporadic Parkinson’s disease. Neurobiol Aging. 2003; 24(2): 197-211.
- Parkinson J. An essay on the shaking palsy. 1817. J Neuropsychiatry Clin Neurosci. 2002;14(2): 223-236.
- Postuma RB, Berg D, Stern M, et al. MDS clinical diagnostic criteria for Parkinson’s disease. Mov Disord. 2015;30(12): 1591-1601.
- Kordower JH, Olanow CW, Dodiya HB, et al. Disease duration and the integrity of the nigrostriatal system in Parkinson’s disease. Brain. 2013; 136(8): 2419-2431.
- Marras C, Lang A. Parkinson’s disease subtypes: lost in translation? J Neurol Neurosurg Psychiatry. 2013; 84(4): 409-415.
- Jankovic J, McDermott M, Carter J, et al. Variable expression of parkinson’s disease: a base-line analysis of the DATATOP cohort. Neurology. 1990; 40(10): 1529-1534.
- Berg D, Postuma RB, Adler CH, et al. MDS research criteria for prodromal Parkinson’s disease. Mov Disord. 2015; 30(12):1600-1611.
- Kordower JHH, Olanow CWW, Dodiya HBB, et al. Disease duration and the integrity of the nigrostriatal system in Parkinson’s disease. Brain. 2013; 136(8): 2419-2431.
- Pfeiffer RF. Non-motor symptoms in Parkinson’s disease. Park Relat Disord. 2016; 22: S119–S122.
- Joel D, Weiner I. The connections of the dopaminergic system with the striatum in rats and primates: an analysis 2000with respect to the functional and compartmental organization of the striatum. Neuroscience; 96(3): 451-474.
- Haber SN, Fudge JL, McFarland NR. Striatonigrostriatal pathways in primates form an ascending spiral from the shell to the dorsolateral striatum. J Neurosci. 2000; 20(6): 2369-2382.
- Fujiyama F, Sohn J, Nakano T, et al. Exclusive and common targets of neostriatofugal projections of rat striosome neurons: a single neuron-tracing study using a viral vector. Eur J Neurosci. 2011; 33(4): 668-677.
- Menegas W, Bergan JF, Ogawa SK, et al. Dopamine neurons projecting to the posterior striatum form an anatomically distinct subclass. eLife. 2015; 4: e10032.
- Rommelfanger KS, Wichmann T. Extrastriatal dopaminergic circuits of the Basal Ganglia. Front Neuroanat. 2010; 4: 139.
- Crittenden JR, Tillberg PW, Riad MH, et al. Striosome-dendron bouquets highlight a unique striatonigral circuit targeting dopamine-containing neurons. Proc Natl Acad Sci USA. 2016; 113(40): 11318-11323.
- Björklund A, Dunnett SB. Dopamine neuron systems in the brain: an update. Trends in Neurosciences. 2007; 30: 194-202.
- Brichta L, Greengard P. Molecular determinants of selective dopaminergic vulnerability in Parkinson’s disease: an update. Front Neuroanat. 2014; 8: 152.
- Nair-Roberts RG, Chatelain-Badie SD, Benson E, White-Cooper H, Bolam JP, Ungless MA. Stereological estimates of dopaminergic, GABAergic and glutamatergic neurons in the ventral tegmental area, substantia nigra and retrorubral field in the rat. Neuroscience. 2008; 152(4): 1024-1031.
- Bentivoglio M, Morelli M. Chapter I, The organization and circuits of mesencephalic dopaminergic neurons and the distribution of dopamine receptors in the brain. Handb Chem Neuroanat. 2005; 21: 1-107.
- Hirsch E, Graybiel AM, Agid YA. Melanized dopaminergic neurons are differentially susceptible to degeneration in Parkinson’s disease. Nature. 1988; 334(6180): 345-348.
- Braak H, Rüb U, Gai WP, Del Tredici K. Idiopathic Parkinson’s disease: possible routes by which vulnerable neuronal types may be subject to neuroinvasion by an unknown pathogen. J Neural Transm. 2003; 110(5): 517-536.
- Halliday GM, McRitchie DA, Cartwright H, Pamphlett R, Hely MA, Morris JGL. Midbrain neuropathology in idiopathic Parkinson’s disease and diffuse Lewy body disease. J Clin Neurosci. 1996; 3(1): 52-60.
- Fearnley JMM, Lees AJJ. Ageing and Parkinson’s disease: substantia nigra regional selectivity. Brain. 1991; 114 ( Pt 5): 2283-2301.
- German DC, Manaye K, Smith WK, Woodward DJ, Saper CB. Midbrain dopaminergic cell loss in parkinson’s disease: computer visualization. Ann Neurol. 1989; 26(4): 507-514.
- Gibb WR, Lees AJ. Anatomy, pigmentation, ventral and dorsal subpopulations of the substantia nigra, and differential cell death in Parkinson’s disease. J Neurol Neurosur Ps. 1991; 54(5): 388-396.
- Martín-Bastida A, Lao-Kaim NP, Roussakis AA, et al. Relationship between neuromelanin and dopamine terminals within the Parkinson’s nigrostriatal system. Brain. 2019; 142(7): 2023-2036.
- Giguère N, Burke Nanni S, Trudeau L-E. On cell loss and selective vulnerability of neuronal populations in Parkinson’s disease. Front Neurol. 2018; 9: 455.
- Dopeso-Reyes IG, Rico AJ, Roda E, et al. Calbindin content and differential vulnerability of midbrain efferent dopaminergic neurons in macaques. Front Neuroanat. 2014; 8: 146.
- Inoue K-I, Miyachi S, Nishi K, et al. Recruitment of calbindin into nigral dopamine neurons protects against MPTP-Induced parkinsonism. Mov Disord. 2019; 34(2): 200-209.
- Takada M, Tokuno H, Nambu A, Inase M. Corticostriatal projections from the somatic motor areas of the frontal cortex in the macaque monkey: segregation versus overlap of input zones from the primary motor cortex, the supplementary motor area, and the premotor cortex. Exp Brain Res. 1998; 120(1): 114-128.
- Brodsky M, Lahna D, Pollock J, Pettersson D, Grinstead J, Rooney W. Nigrosome 1 absence in de novo Parkinson disease. Neurology. 2018; 90(11): 522-552.
- Poulin J-F, Gaertner Z, Moreno-Ramos OA, Awatramani R. Classification of midbrain dopamine neurons using single-cell gene expression profiling approaches. Trends Neurosci. 2020; 43(3): 155-169.
- La Manno G, Gyllborg D, Codeluppi S, et al. Molecular diversity of midbrain development in mouse, human, and stem cells. Cell. 2016; 167(2): 566-580.
- Poulin J-F, Caronia G, Hofer C, et al. Mapping projections of molecularly defined dopamine neuron subtypes using intersectional genetic approaches. Nat Neurosci. 2018; 21(9): 1260-1271.
- Sgobio C, Wu J, Zheng W, et al. Aldehyde dehydrogenase 1-positive nigrostriatal dopaminergic fibers exhibit distinct projection pattern and dopamine release dynamics at mouse dorsal striatum. Sci Rep. 2017; 7(1): e5283.
- Wu J, Kung J, Dong J, et al. Distinct connectivity and functionality of aldehyde dehydrogenase 1a1-positive nigrostriatal dopaminergic neurons in motor learning. Cell Rep. 2019; 28(5): 1167-1181.
- Schein JC, Hunter DD, Roffler-Tarlov S. Girk2 expression in the ventral midbrain, cerebellum, and olfactory bulb and its relationship to the murine mutation weaver. Dev Biol. 1998; 204(2): 432-450.
- Graybiel AM, Ohta K, Roffler-Tarlov S. Patterns of cell and fiber vulnerability in the mesostriatal system of the mutant mouse weaver. I. Gradients and compartments. J Neurosci. 1990; 10(3): 720-733.
- Liu G, Yu J, Ding J, et al. Aldehyde dehydrogenase 1 defines and protects a nigrostriatal dopaminergic neuron subpopulation. J Clin Invest. 2014; 124(7): 3032-3046.
- Vila M. Neuromelanin, aging, and neuronal vulnerability in Parkinson’s disease. Mov Disord. 2019; 34(10): 1440-1451.
- Walker DG, Lue LF, Serrano G, et al. Altered expression patterns of inflammation-associated and trophic molecules in substantia nigra and striatum brain samples from parkinson’s disease, incidental lewy body disease and normal control cases. Front Neurosci. 2016; 9: 507.
DECLARACIÓN DE TRANSPARENCIA
Los autores/as de este artículo declaran no tener ningún tipo de conflicto de intereses respecto a lo expuesto en el presente trabajo.
ranm tv
José A. Obeso
Real Academia Nacional de Medicina de España
C/ Arrieta, 12 · 28013 Madrid
Tlf.: +34 91 547 03 18 | Email de correspondencia
An RANM. 2021;138(02): 114 – 123
Enviado*: 13.10.20
Revisado: 17.10.20
Aceptado: 26.11.20
* Fecha de lectura en la RANM


