Resumen
El trasplante de páncreas (TP) es considerado el único tratamiento que puede convertir a un paciente diabético en una situación de euglucemia sin necesidad de tratarlo con insulina o antidiabéticos orales. Desde el año 1966 hasta finales de 2016, en EE.UU. se realizaron más de 50.000 TP, mientras que en España se realizaron 1.730 en los últimos 10 años. En esta revisión se realizará una actualización del TP teniendo en cuenta los avances más recientes, añadiendo nuestra experiencia acumulada desde el inicio del programa en el año 1995.
Desde la realización del primer TP, en 1966, en el Hospital de la Universidad de Minnesota, se han producido mejoras significativas a lo largo del tiempo debido a los avances en técnica quirúrgica en donantes y receptores, cuidados perioperatorios de los pacientes e introducción de inmunosupresores más potentes con los que se ha conseguido reducir la tasa de rechazo por debajo del 20%. Aunque el TP es un tratamiento asociado a una alta morbilidad (trombosis del injerto, infecciones sistémicas e intraabdominales, fístulas anastomóticas, etc.), en la actualidad, los grupos de mayor experiencia han conseguido una supervivencia del paciente, a 3 años, del 93% y una supervivencia del injerto pancreático entre el 78-83%.
Asimismo, cuando la función pancreática pos-TP es normal, se consigue una mejora de la calidad de vida y de la mayoría de las complicaciones debidas a la diabetes, sin necesidad de tratar al paciente con antidiabéticos orales o insulina.
Abstract
Pancreas transplantation (PT) is considered as the only treatment that can convert a diabetic patient in a euglucemic state without the use of insulin or oral antidiabetic drugs. From 1996 to the end of 2016, more than 50,000 PT were performed in USA, and in Spain were performed 1.730 PT during the last 10 years. In this review we will perform an update of PT considering the introduction of several advances in the last years, adding our accumulated experience from the beginning of our program in the year 1995.
The first PT was carried out in the Hospital of the University of Minnesota, and from that date several significant improvements have been introduced along the time due to advances in surgical technique in pancreas donors and recipients, perioperative management of patients, and introduction of more potent immunosuppressors able to reduce the rejection rate under 20%. Although PT is a therapy associated with a higher morbidity (pancreas graft thrombosis, systemic and intraabdominal infections, anastomotic leakages, etc.), currently most of the PT teams have obtained a rate of 93% of patient survival at 3-years, and between 78% and 83% of graft survival at 3-years.
Additionally, the normal pancreas graft function is associated with an improvement of quality of life and most of complications related to diabetes, without the necessity to treat with antidiabetics drugs or insulin.
Palabras clave: Trasplante de páncreas; Diabetes; Complicaciones de la diabetes; Tratamiento de la diabetes; Nefropatía diabética.
Keywords: Pancreas transplantation; Diabetes; Diabetes complications; Treatment of diabetes; Diabetic nephropathy.
INTRODUCCIÓN
Desde el descubrimiento y aislamiento de la insulina por Banting y Best, en 1922 (1), la administración en pacientes diabéticos los mantenía con vida, aunque el desarrollo de las complicaciones evolutivas de la enfermedad (nefropatía, neuropatía, retinopatía, enfermedad cardiovascular, infecciones, etc.) constituían las causas más frecuentes de morbi-mortalidad.
Después de una fase experimental, en el hospital de la Universidad de Minnesota, el primer trasplante de páncreas-riñón simultáneo (TPRS) en humanos fue realizado, en dicho centro, en 1966, por W. Kelly y R. Lillehei (2). Con el trasplante de páncreas (TP), los pacientes recuperaban la euglucemia. Inicialmente, los resultados eran desalentadores debido a la pérdida de la función pancreática por rechazo y la mortalidad fundamentalmente debida a complicaciones infecciosas. No obstante, este procedimiento quirúrgico se fue extendiendo a otros centros, con la consiguiente mejora de la técnica quirúrgica, introducción de inmunosupresores más potentes y manejo perioperatorio de los pacientes, todo lo cual ha contribuido a una significativa mejora de los resultados. En España, el primer trasplante de páncreas con éxito se realizó en Barcelona, en 1983, y en Madrid, en el año 1995, en el H. Doce de Octubre. Desde el año 1966 hasta diciembre de 2016, se han realizado más de 50.000 TP en todo el mundo (3), mientras en España, en los últimos 10 años, se ha alcanzado la cifra de 1.730 TP (4). No obstante, en los últimos años se ha observado un descenso del TP tanto en España (4) como en EE.UU. debido a la peor calidad de los injertos pancreáticos (obesidad y de mayor edad), mejor manejo de los pacientes diabéticos y no envío de éstos desde las consultas de endocrinología a las de TP (5).
TIPOS DE TRASPLANTE DE PÁNCREAS. INDICACIONES Y CONTRAINDICACIONES
Las opciones de TP son las siguientes: 1) TPRS; 2) Trasplante de páncreas aislado (TPA): y 3) Trasplante de páncreas después del renal (TPDR).
El TPRS es el más frecuentemente realizado, siendo raramente efectuado en España el TPA. Las indicaciones varían poco entre los diferentes equipos de trasplante, exponiéndose, en la Tabla 1, las establecidas en nuestro protocolo.
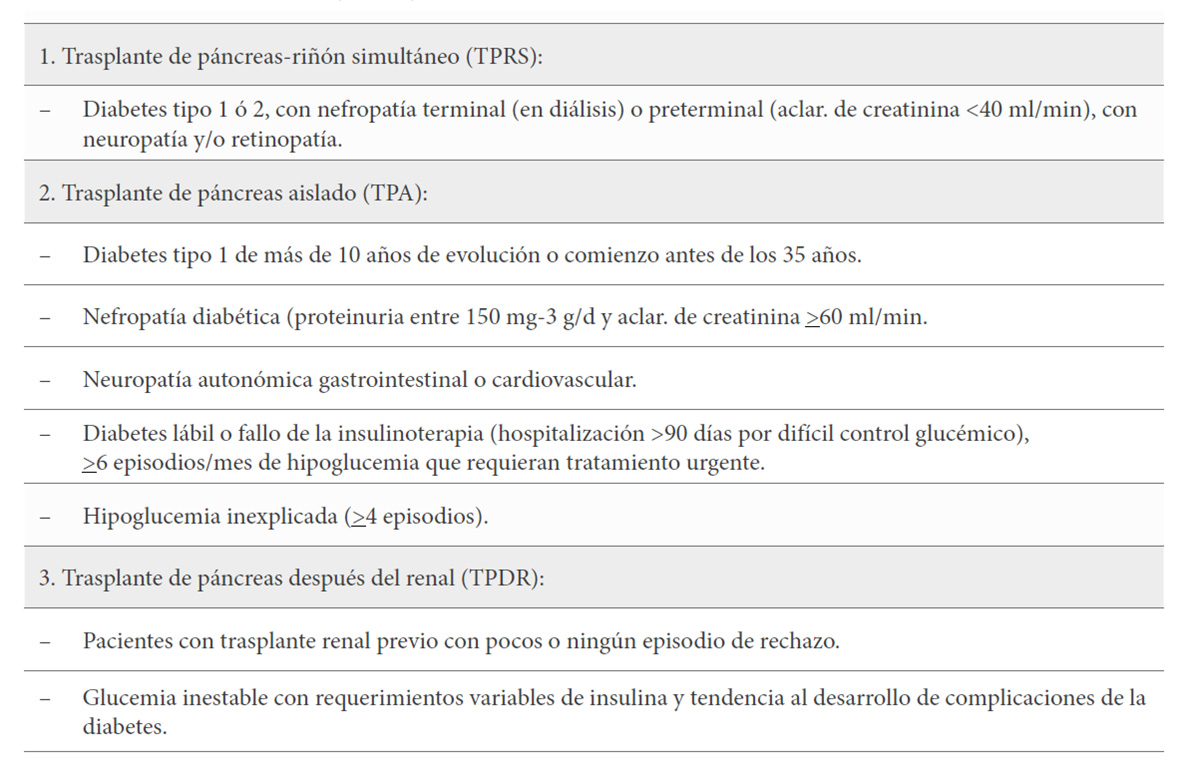
El mejor momento para realizar un TP es antes de la aparición de las complicaciones. Sin embargo, debido a la dificultad en predecir cuándo van a aparecer éstas, en la mayoría de los casos el TP se hace en una fase evolutiva avanzada, con la presencia casi constante de nefropatía, retinopatía y neuropatía (triopatía). Debido a las consecuencias irreversibles de la diabetes, se debe intentar hacer el TPRS en la fase evolutiva de prediálisis, algo que rara vez sucede en nuestra experiencia. Cuando el aclaramiento de creatinina es >60-70 ml/min se realiza el TPA, mientras que en pacientes con aclaramiento de creatinina <40 ml/min se realiza un TPRS. La mayoría de los trasplantes de páncreas se realizan con injerto renal y pancreático de donantes de muerte encefálica, y en algunos centros, sobre todo americanos, se realiza también con cierta frecuencia un trasplante renal de donante vivo y posteriormente un TP procedente de un donante cadáver.
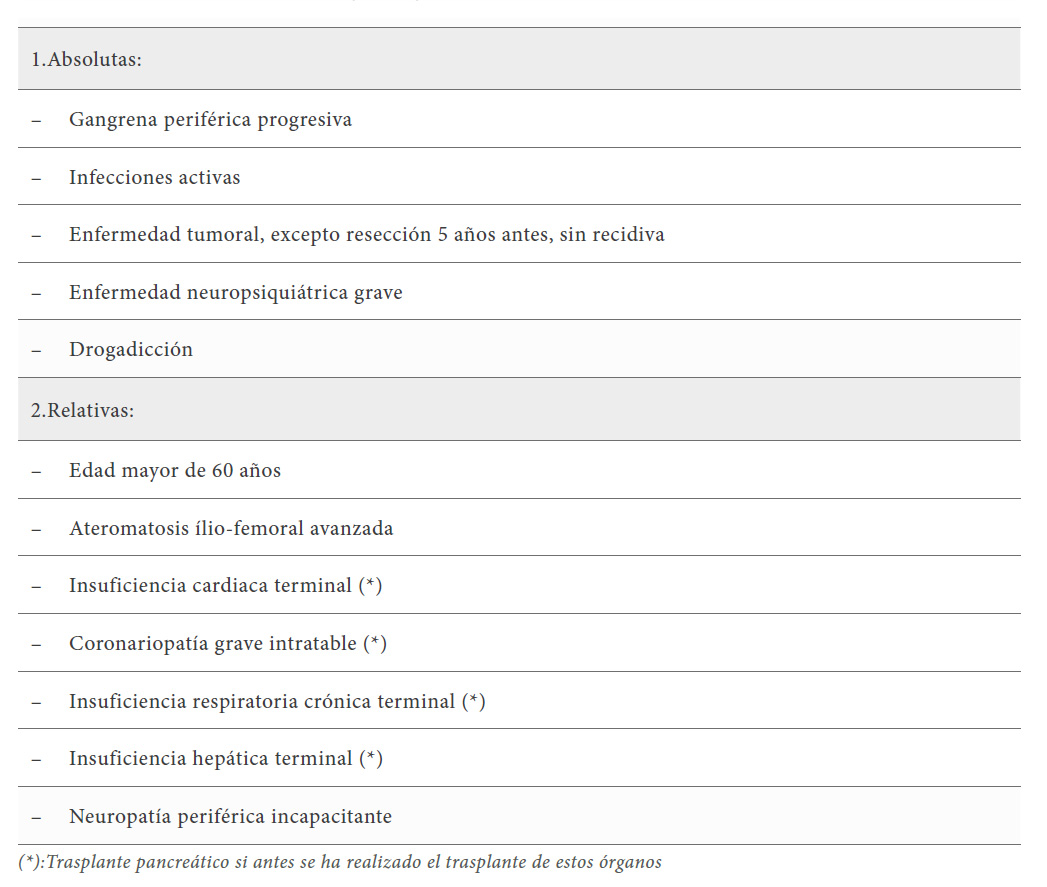
De forma general, se establece un límite de edad del receptor entre 18-60 años, aunque lo fundamental es la edad biológica. En realidad, lo que marca una contraindicación para el TP suele ser la morbilidad cardiovascular (cardiopatía y ateromatosis ílio-femoral) desarrollada por el paciente durante muchos años por el efecto de la diabetes y nefropatía (Tabla 2). Los resultados en la serie de la Universidad de Wisconsin (6) en cuanto al TP en pacientes >50 años frente a <50 años han sido similares en términos de supervivencia del paciente y del injerto, aunque la morbilidad cardiovascular fue mayor en los pacientes >50 años.
Sin embargo, si nos atenemos a la serie multicéntrica norteamericana de la United Network for Organ Sharing (UNOS), de 3.440 TP en >50 años, se aprecia una menor supervivencia del paciente y del injerto frente a los pacientes de menor edad (7).
El TP en pacientes con infección por virus de la inmunodeficiencia humana (VIH+) no está totalmente aceptado, ya que en los pocos trasplantes realizados con esta patología se ha obtenido una alta tasa de complicaciones y fallo del injerto (8).
Cuando la nefropatía diabética se asocia a una insuficiencia terminal de otro órgano, se puede realizar un TP siempre que se haga de forma simultánea con los órganos en situación terminal.
PROTOCOLO DE EVALUACIÓN DE CANDIDATOS A TRASPLANTE
Las complicaciones cardiacas e infecciosas son las más frecuentes después del TP. Durante el estudio pre-trasplante es importante descartar la enfermedad coronaria, asintomática en el 30% de los pacientes diabéticos tipo 1 con fallo renal terminal, los cuales suelen presentar estenosis coronaria (9). La primera prueba diagnóstica para descartar una lesión coronaria isquémica es una ecocardiografía de esfuerzo o con dobutamina, aunque otros autores son partidarios de realizar directamente una coronariografía en pacientes mayores de 45 años. (10). Un angio-TAC aorto-ilíaco se realiza a todos los candidatos a TP, por la importancia de descartar ateromatosis en arterias ilíacas que es la zona donde se implantan los injertos renal (fosa ilíaca izquierda) y pancreático (fosa ilíaca derecha) (Tabla 3).

CRITERIOS DE ACEPTACIÓN Y EXCLUSIÓN DE INJERTOS PANCREÁTICOS
Nuestros criterios de aceptación del injerto pancreático siguen básicamente los de la mayoría de los centros de TP (Tabla 4). Los injertos de donantes >45 años se deben aceptar con ciertas precauciones, haciendo una valoración meticulosa, ya que la mayoría de éstos suelen fallecer por enfermedad cerebrovascular, lo cual implica afectación ateromatosa generalizada que también incluye alteración vascular del injerto pancreático; habiéndose establecido una serie de factores de buen funcionamiento del injerto pancreático, como el índice de masa corporal (IMC) <30 kg/m2, sexo femenino, causa traumática del fallecimiento, estabilidad hemodinámica y corta estancia hospitalaria (11, 12). Casi la mitad de los donantes de páncreas presentan glucemias >200 mg/dl, debido a la administración de sueros glucosados y corticoides. Para descartar la presencia de una diabetes, se administran sueros sin glucosa y se repite la glucemia una hora después.

TÉCNICA DE EXTRACCIÓN DEL INJERTO Y PREPARACIÓN EN BANCO
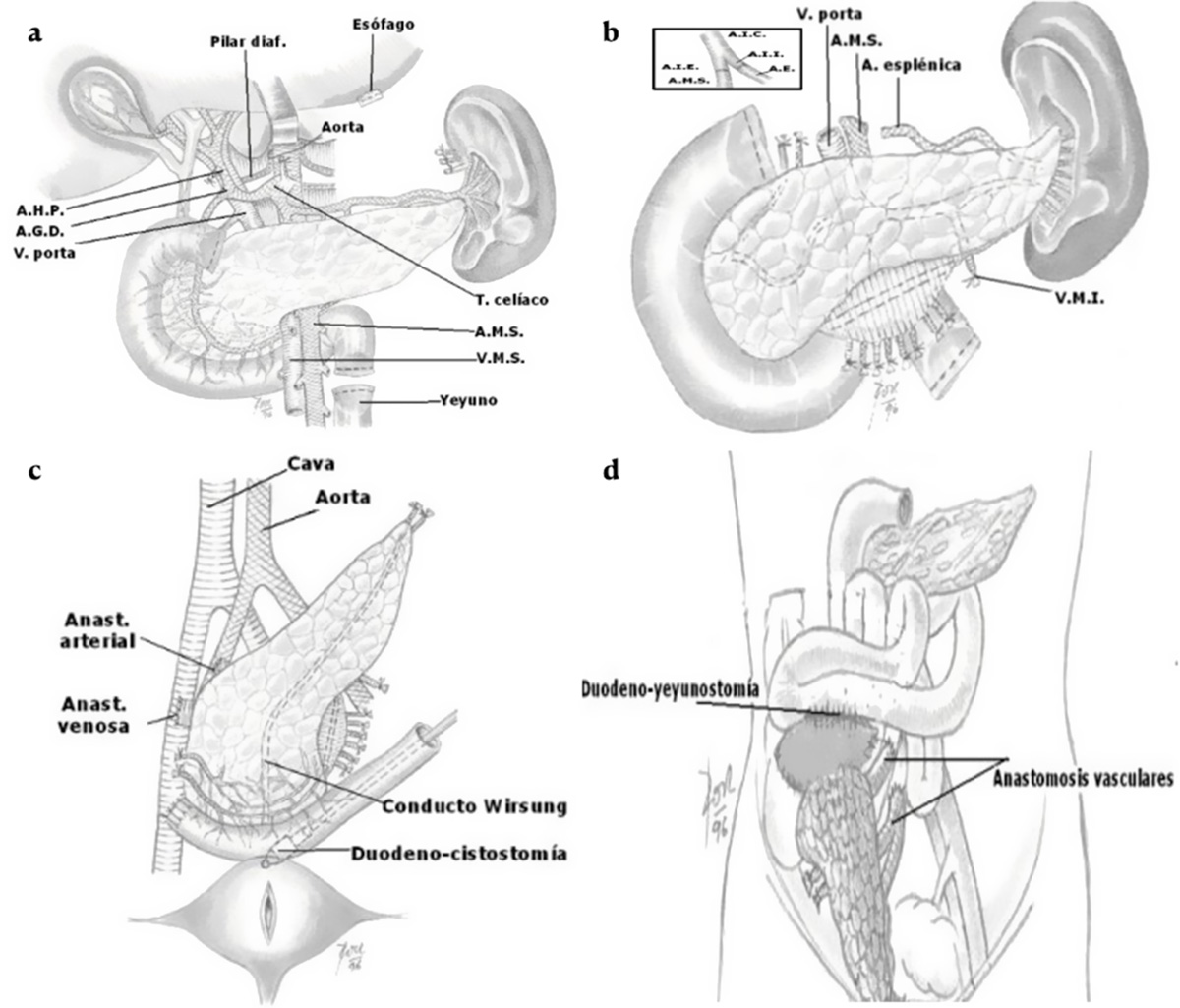
La extracción del bloque duodeno-pancreático es la técnica utilizada para el TP. Después de realizar una laparotomía cruciforme, se efectúan las siguientes maniobras: movilización del duodeno y cabeza del páncreas, sección del ligamento gastrocólico, disección y sección con grapadora de la primera porción duodenal (a 1 cm del píloro y previo lavado de la luz duodenal con solución antibiótica y antifúngica), ligadura y sección del colédoco suprapancreático, ligadura y sección de la arteria gastroduodenal por encima del duodeno, disección de la arteria esplénica, disección, ligadura y sección de los vasos coronarios, disección de la aorta supraceliaca, sección con grapadora del primer asa yeyunal y disección del bazo y cola-cuerpo del páncreas (Figuras 1a). Se canulan la aorta infrarrenal y una rama de la vena mesentérica superior (VMS), y se procede a la heparinización sistémica (3 mg/kg). Se liga la aorta por debajo de la cánula y por encima del tronco celiaco y se inicia la perfusión, a través de la cánula dentro de la aorta infrarrenal, con solución de preservación de Celsior (un total de 2 litros por la aorta, pero solo 1,2 litros para perfundir el páncreas, y 2 litros de solución a través de la VMS). La vena porta se secciona a 1,5 cm de la VMS. Al final se secciona la arteria esplénica y la arteria mesentérica superior (AMS) en sus orígenes respectivos, extrayéndose el injerto duodeno-pancreático que se coloca sumergido en una bolsa con solución de preservación a 4º C, rodeado de otra bolsa de hielo picado, donde permanecerá hasta su preparación en banco. En la cirugía de banco se realiza la esplenectomía, cierre de los extremos duodenales y las anastomosis arteriales. Así, se obtiene un injerto arterial en Y invertida de donante compuesto por la arteria ilíaca común (AIC) y sus ramas, externa (AIE) e interna (AII). La AIE se anastomosa con la AMS y la AII con la arteria esplénica (Figura 1b) (13).
TÉCNICA DEL IMPLANTE PANCREÁTICO
Se describen las técnicas de implante del injerto más habituales. En el receptor se realiza una laparotomía media infraumbilical con ampliación supraumbilical de 4-5 cm. Se diseca el ciego y colon ascendente, creando un lecho donde se situará más adelante el injerto pancreático. Se disecan 4-5 cm de la cava infrarrenal distal y 3-4 cm de la vena ilíaca común derecha proximal. Asimismo, se disecan también la AIC, AIE y AII. Si la intención es efectuar una derivación duodeno-vesical (hoy en día rara vez utilizada), se liberará la vejiga mediante sección de los ligamentos peritoneales y umbilical medio y disección de la cara vesical anterior. La primera anastomosis vascular es la de la vena porta del injerto con la vena cava abdominal distal del receptor, en posición término-lateral. A continuación, se anastomosa la rama vertical del injerto en Y invertida del donante (interpuesto en el banco) con la AIC o AIE del receptor, en posición término-lateral. Seguidamente, se procede a perfundir el injerto pancreático (primero, la vena y después, la arteria).
Las técnicas de derivación de la secreción pancreática más aceptadas son la duodeno-cistostomía (anastomosis entre el duodeno del injerto con la vejiga del receptor, actualmente menos realizada) (Figura 1c), y la duodeno-enterostomía latero-lateral (anastomosis del duodeno del injerto con el yeyuno del receptor cuando el páncreas se coloca en posición craneal (Figura 1d) y con el íleon cuando se coloca en posición caudal) (13), y la más recientemente introducida, la duodeno-duodenostomía (anastomosis latero-lateral entre el duodeno del injerto y la tercera porción duodenal del receptor).
Con esta última técnica es fácil realizar una endoscopia y biopsia duodenal en casos de sospecha de rechazo, aunque no está exenta de complicaciones (hemorragia, fístula, estenosis, etc.) (14).
La duodeno-cistostomía se ha dejado de utilizar por ser menos fisiológica que la derivación intestinal y por presentar el paciente acidosis metabólica provocada por la pérdida de bicarbonato por la orina y complicaciones urológicas y pancreatitis del injerto por reflujo. La anastomosis del injerto pancreático-duodenal con el íleon terminal se realiza a unos 100 cm de la unión íleo-cecal. Después del TP se efectúa el trasplante renal si el trasplante pancreático-renal es la indicación. Existen pacientes límites para el TP debido a la ateromatosis extensa en las arterias ilíacas comunes o externas, sitio donde se van a hacer las anastomosis arteriales del injerto pancreático y renal. En casos de gran complejidad será necesario realizar una endarterectomía e incluso una resección de un segmento arterial que se sustituye por un injerto arterial del donante o por una prótesis (15).
CUIDADOS PERIOPERATORIOS Y MONITORIZACIÓN DEL INJERTO
Durante la inducción anestésica se efectúa la profilaxis antibiótica con vancomicina y ceftazidima, y en el postoperatorio de la infección fúngica con fluconazol y del citomegalovirus (CMV) con valganciclovir y las del Pneumocystis jirovecii con trimetroprim-sulfametoxazol. Después de la perfusión del injerto pancreático se realizan determinaciones periódicas de glucemia, pudiendo encontrarse el paciente euglucémico antes de salir de quirófano sin necesidad de aporte de insulina. Si se ha realizado un TPRS, después de completar la anastomosis arterial, es conveniente aumentar el flujo renal para mejorar la diuresis mediante la administración de manitol, furosemida y dopamina. Después de finalizar el trasplante, el paciente pasa a reanimación donde es controlado analíticamente y evitando la hipotensión que se asocia a un mayor riesgo de trombosis del injerto (16). La trombosis del injerto pancreático es la causa no inmunológica más frecuente de pérdida del injerto (entre el 3,1-17% de los casos) (17), siendo la etiología multifactorial. Así, actualmente no hay un protocolo estándar seguro para prevenir esta complicación que se presenta con una incidencia alrededor del 7% con una pérdida del injerto en el 83,3% de los casos (18). Como medida preventiva de esta complicación se ha utilizado heparina i.v. a bajas dosis (300-500 U/hora) (19) o heparina de bajo peso molecular (0,4 mg/día) (20). Se ha observado una tendencia a una menor tasa de trombosis del injerto con la utilización profiláctica de heparina i.v. a bajas dosis asociada a 325 mg/día de aspirina (19, 20). En la actualidad nuestra profilaxis consiste en la administración de enoxaparina (4.000 UI/día) a las 24 horas del TP, añadiendo 100 mg/día de ácido acetilsalicílico a los 5 días del TP.
Para monitorizar el injerto pancreático se hacen determinaciones periódicas en sangre de glucosa, amilasa y creatinina (en TPRS), así como un ecodoppler al día siguiente del TP para valorar los flujos venosos y arteriales de los injertos pancreático y renal. Si el páncreas trasplantado tiene una función normal, la cifra de glucemia será menor de 200 mg/dl sin necesidad de aporte de insulina. La presencia de hiperglucemia con necesidad de administración de insulina, después de un periodo previo de normoglucemia, indica un mal funcionamiento del injerto que puede deberse a una trombosis del injerto, rechazo, disfunción, pancreatitis, lesión de preservación, etc.
La hiperamilasemia precoz puede reflejar una lesión de preservación o una pancreatitis transitoria, y con niveles más elevados una trombosis venosa del injerto, fístula anastomótica o pancreatitis. En los casos de trombosis arterial se suele observar un descenso de la cifra de amilasa.
Cuando se efectúa una derivación duodeno-vesical de la secreción exocrina del páncreas, la valoración del injerto se realiza por la determinación de la cifra de amilasa en orina de 24 horas. Si la amilasa en orina desciende en más de un 25% puede indicar un rechazo, pancreatitis o trombosis. Durante el seguimiento, en consulta se miden además los niveles de péptido C, insulina y hemoglobina glicosilada, creatinina en sangre y filtrado glomerular (en TPRS). Para evaluar la vascularización del injerto pancreático o detectar eventuales complicaciones se utilizan el angio-TAC o TAC abdominal.
Según el Scientific Registry of Transplant Recipients (SRTR), la tasa media de rechazo en TP es del 13%, con menor incidencia en TPRS que en TPDR y en TPA (21). Aunque esta tasa es baja si la comparamos con la superior al 70% en la era de la ciclosporina como inmunosupresor de base, en la actualidad en casi todos los grupos de TP se sigue utilizando la inducción con anticuerpos (timoglobulina, basiliximab) durante 7-12 días y mantenimiento con tacrolimus (dosis para mantener niveles entre 10-15 hasta el 6º mes y después entre 5-10 ng/ml), micofenolato mofetilo (500-1.000 mg/12 h) y corticoides, con tendencia a retirar estos últimos a los 3-6 meses del TP. La terapia de inducción parece estar más justificada en el TPA, asociado a mayor tasa de rechazo y dificultad diagnóstica de éste.
C0MPLICACIONES POS-TRASPLANTE
A pesar de los avances en la preservación de órganos, técnica quirúrgica (extracción e implante del páncreas), fármacos inmunosupresores más potentes, profilaxis antiinfecciosa y técnicas diagnósticas más sofisticadas, las complicaciones quirúrgicas y los fallos técnicos continúan siendo un problema grave después del TP, con frecuencia asociados a la pérdida del injerto y, a veces, al fallecimiento del enfermo. Las complicaciones postrasplante se presentan en la Tabla 5.

Los fallos o complicaciones técnicas (trombosis venosa o arterial, pancreatitis, infecciones intraabdominales, fístulas anastomóticas, hemorragia del injerto) y el rechazo agudo o crónico son las principales causas de la pérdida de los injertos pancreáticos. En una serie de 937 TP la tasa de pérdida del injerto por complicaciones técnicas fue del 13,1% (123 injertos): trombosis (52%), pancreatitis (20,3%), infecciones (18,7%), fístulas (6,5%) y hemorragia intraabdominal (2,4%) (22). Aunque se denominan complicaciones o fallos técnicos, esto no implica errores de técnica, sino que son consecuencia de la eventual presencia de factores de riesgo relacionados con el donante o con el receptor. La edad del donante mayor de 40 años y la obesidad del receptor son factores de riesgo de complicaciones quirúrgicas (trombosis, infección intraabdominal, fístulas anastomóticas, pancreatitis aguda grave). Después de un trasplante de páncreas, entre el 31-32% de los enfermos van a precisar al menos una relaparotomía por complicaciones abdominales (19,23,24). La necesidad de una relaparotomía se asocia a una supervivencia al año significativamente menor del paciente y del injerto (25).
La trombosis del injerto pancreático presenta una incidencia global entre 10-35% y supone el 52% dentro de las causas técnicas de la pérdida del injerto (19). La presencia de esta complicación añade una morbilidad considerable al TP e incluso mortalidad si ocurre en el postoperatorio inmediato y no se realiza una trasplantectomía inmediata. La trombosis precoz ocurre dentro de la primera semana y supone el 70% de los casos, relacionándose con la situación de bajo flujo del injerto, edema pancreático, alteración de la microcirculación e hipercoagulabilidad local y sistémica (16), mientras que la trombosis tardía es más rara y se asocia con mayor frecuencia al rechazo crónico. La incidencia de la trombosis oscila entre el 8,8% y el 35%, siendo múltiples los factores de riesgo (16,18,26-28) que se muestran en la Tabla 6. El cuadro clínico de esta complicación es de dolor de rápida instauración en fosa ilíaca derecha, hemoperitoneo, leucocitosis e hiperglucemia que precisa insulina. Después de la confirmación con ecodoppler o TAC se puede intentar una trombectomía o trombólisis en la fase precoz o en casos de trombosis parcial, pero prácticamente el tratamiento en cerca del 90% de los casos es la resección del injerto por la gravedad de la complicación.

La incidencia de fístulas entre la anastomosis del duodeno del injerto con el intestino delgado del receptor es del 4-10% con una pérdida asociada del injerto en el 67% de los casos (29), y los factores de riesgo son la isquemia, edema, tensión anastomótica, infección peri-injerto e inmunosupresión. Si la fístula está circunscrita, se realiza una sutura, mientras que si hay una peritonitis se recurre a una trasplantectomía por la gravedad de esta complicación.
Como factores de riesgo de la pancreatitis del injerto se han subrayado la obesidad, inestabilidad hemodinámica y el uso de vasopresores en el donante, perfusión excesiva y a gran presión del injerto, alteración de la microcirculación o isquemia del injerto durante el proceso de preservación y pos-reperfusión y bloqueo de conducto de Wirsung (30,31). La pancreatitis aguda por reflujo de orina en los pacientes con derivación duodeno-vesical se resuelve mediante la reconversión a una derivación duodeno-entérica (32).
La hemorragia intraabdominal es la causa de relaparotomía entre el 2-8% de los pacientes trasplantados (19,23) y se correlaciona con la heparinización con dosis bajas para prevenir la trombosis del injerto (19).
Las complicaciones urológicas (pancreatitis por reflujo de orina, infecciones, hematuria, cistitis, uretritis, etc.) están relacionadas con el TP cuando se realiza una derivación duodeno-vesical (32,33).
La infección es una importante causa de morbi-mortalidad después del TP con un aumento del coste del proceso y un impacto negativo en la supervivencia del paciente y del injerto (34). El riesgo de infección es directamente proporcional a la intensidad y tipo de inmunosupresión (mayor con anticuerpos mono o policlonales) y la duración de ésta. Los gérmenes más frecuentes son las bacterias gram positivas y negativas, hongos (Candida spp., y más raro el Aspergillus spp), virus o la combinación de éstos. Las infecciones bacterianas representan el 33% de las infecciones graves (35) y son frecuentes durante el primer mes postrasplante, localizándose preferentemente en el tracto urinario, área intraabdominal, pulmón y sangre (bacteriemias). Los factores de riesgo de bacteriemia son la cateterización vascular prolongada, infección urinaria, neumonía, infección intraabdominal, leucopenia y tratamiento antirechazo. En nuestra serie la incidencia de infecciones fúngicas ha sido del 28% (la mayoría por Candida spp y 2 casos de Mucor), detectándose como factores de riesgo la enfermedad arterial periférica, tiempo prolongado de isquemia del injerto y transfusión sanguínea importante. La infección fúngica ha sido un factor de riesgo independiente de disfunción grave del injerto (34). La infección por Mucor, aunque rara, es grave y típica en inmunodeprimidos y diabéticos, pudiendo causar una infección rinocerebral, pulmonar, de la piel o diseminada, tratándose con anfotericina B y drenaje quirúrgico (36). Nuestra incidencia de infección por CMV es del 17%, habiendo observado un descenso de esta infección cuando se ha realizado profilaxis universal con ganciclovir o valganciclovir (34). La diálisis peritoneal previa al TP no ha influido significativamente sobre el desarrollo de infecciones intraabdominales o supervivencia del paciente o de los injertos pancreático o renal (37). Sin embargo, la derivación de la secreción exocrina a la vejiga sí ha supuesto una incidencia más alta de infección grave, en comparación con la derivación al intestino (34).
Desde la sustitución de la ciclosporina por el tacrolimus+micofenolato mofetilo y utilización de anticuerpos (basiliximab, timoglobulina o alemtuzumab), la tasa de rechazo descendió desde el 76% hasta el 35%, según la experiencia de Wisconsin (38). En los reciente datos de TP del registro americano (21), la tasa global de rechazo agudo ha descendido hasta el 13%, siendo menor en el TPRS que en TPDR y en TPA. Los marcadores de rechazo que se utilizan son los exocrinos (amilasa, lipasa y tripsinógeno anodal) y endocrinos (glucosa y creatinina) que se pueden determinar en sangre (derivación vesical o entérica) y en orina (solo en derivación vesical. No obstante, ninguno de estos marcadores tiene especificidad o sensibilidad del 100%. La glucemia elevada es un marcador muy específico de rechazo (90-95%), aunque tardío, ya que cuando la glucemia es >300 mg/dl, la función endocrina sólo se recupera en el 2% de los casos. La actividad de amilasa en orina sólo se determina cuando se hace una derivación duodeno-vesical, sospechándose un rechazo cuando dicha actividad desciende >25%. El rechazo agudo se confirma mediante biopsia percutánea del páncreas o del duodeno (cistoscopia en derivación duodeno-vesical o endoscopia digestiva alta en derivación duodeno-duodenal). El rechazo agudo leve o moderado se trata aumentando la dosis de corticoides, tacrolimus o micofenolato mofetilo, mientras que el grave se trata con anticuerpos antilinfocitarios. En el rechazo crónico existe proliferación fibrosa de la íntima, estrechamiento luminal, isquemia y fibrosis del páncreas con pérdida completa de la función pancreática, lo que hace que no exista tratamiento eficaz.
La no función del injerto se define por la necesidad de insulina o antidiabéticos orales para poder mantener la glucemia, mientras que la recurrencia de la diabetes se define por el requerimiento de insulina y pérdida grave del péptido C en ausencia de rechazo, hecho que se presenta con una incidencia del 7,6% según una serie reciente. No obstante, a veces coexisten la diabetes y el rechazo (39).
SUPERVIVENCIA DEL PACIENTE Y DEL INJERTO PANCREÁTICO
Según el registro americano de trasplante, durante el periodo del año 2001 hasta el 2016, la supervivencia, a 3 años, del paciente con TPRS era del 93%, mientras que la del injerto pancreático era del 80% y la del riñón del 89%. En TPDR, la supervivencia del páncreas a 3 años era del 70% y en TPA era del 65% (3). En la experiencia del Doce de Octubre, de 175 pacientes con TPRS, la supervivencia del paciente a 1, 3 y 5 años fue de 95,4%, 93% y 92,4%, respectivamente, y la del injerto fue de 81,6%, 77,9% y 72,3%, respectivamente (28). Cuando en un paciente con nefropatía diabética se realiza sólo un trasplante renal la mortalidad a 10 y 20 años es un 20-30 mayor que cuando se hace un TPRS (40), lo que indica la conveniencia de realizar un TPRS.
EFECTOS DEL TRASPLANTE DE PÁNCREAS SOBRE LA DIABETES Y CALIDAD DE VIDA
El TP funcionante previene o reduce la nefropatía (41), mejora la polineuropatía periférica y autonómica (cardiaca, digestiva) (42) y mejora la enfermedad cardio-cerebro-vascular (43), aumenta el colesterol HDL y disminuye el colesterol LDL y la tensión arterial (44). Asimismo, la retinopatía se estabiliza o mejora a los 3 años del trasplante entre el 63% y 73% de los pacientes (45,46).
En estudios sobre calidad de vida, se ha observado una mejoría en varios parámetros comparados antes y después del TPRS: satisfacción, vitalidad, dolor corporal, funciones sociales, estado de salud mental, preocupación por la diabetes, y calidad de vida global (47,48). En los casos de embarazo en TP, éste llega a término con éxito en el 93,8% de las pacientes, con resultados similares a las trasplantadas sólo de riñón (49).
conclusiones
El TP con función normal restablece la glucemia normal en el paciente diabético, consiguiéndose una supervivencia del paciente del 93% y del injerto entre el 78-83% a 3 años. Asimismo, se obtiene una mejora de la calidad de vida y de la mayoría de las complicaciones debidas a la diabetes sin precisar tratamiento con insulina o antidiabéticos orales.
BIBLIOGRAFÍA
- Banting FG, Best CR. The internal secretion of the pancreas. J Lat Clin Med. 1922; 7: 251-266.
- Kelly WD, Lillehei RC, Merkel FK, Idezuki Y, Goetz FC. Allotransplantation of the pancreas and duodenum along with the kidney in diabetic nephropathy. Surgery. 1967; 61: 827-837.
- Gruessner AC, Gruessner RWG. Pancreas transplantation for patients with type 1 and type 2 diabetes mellitus in the United States: a registry report. Gastroenterol Clin N Am. 2018; 47: 417-441.
- Organización Nacional de Trasplante (ONT). Dossier de actividad en trasplante de páncreas en el año 2020. Disponible en http:/www.ont.es
- Stratta RJ, Gruessner AC, Odorico JS, Fridell JA, Gruessner RWG. Pancreas transplantation: an alarming crisis in confidence. Am J Transplant. 2016; 16: 2556-2562.
- Scalea JR, Redfield RR, Arpalli E, et al. Pancreas transplantation in older patients is safe, but patient selection is paramount. Transpl Int. 2016; 29(7): 810-818.
- Siskind E, Maloney C, Akerman M, et al. An analysis of pancreas transplantation outcomes based on age groupings-an update of the UNOS database. Clin Transplant. 2014; 28: 990-994.
- Lo DJ, Sayed BA, Turgeon NA. Pancreas transplantation in unconventional recipients. Curr Opin Organ Transplant. 2016; 21: 393-398.
- Ramanathan V, Goral S, Tanriover B, et al. Screening asymptomatic diabetic patients for coronary artery disease prior to renal transplantation. Transplantation. 2005; 79: 1453-1458.
- Manske CL, Thomas W, Wang Y, Wilson RF. Screening diabetic transplant candidates for coronary artery disease: identification of a low risk subgroup. Kidney Int. 1993; 44: 617-621.
- Boggi U, Del Chiaro M, Signori S, et al. Pancreas transplants from donors aged 45 years or older. Transplant Proc. 2005; 37: 1265-1267.
- Salvalaggio PR, Schnitler MA, Abbott KC, et al. Patient and graft survival implications of simultaneous pancreas-kidney transplantation for old donors. Am J Transplant. 2007; 7: 1561-1571.
- Jiménez C, Moreno E, López A, et al. Técnica quirúrgica del trasplante de páncreas. En: Jiménez C, Riaño D, Moreno E, Jabbour N, eds. Avances en trasplante de órganos abdominales. Madrid. Cuadecon; 1997. p. 441-453.
- Gunasekaran G, Wee A, Rabets J, Winans C, Krishnamurthi V. Duodenoduodenostomy in pancreas transplantation. Clin Transplant 2012; 26: 550-557.
- Fridell JA, Gage E, Goggins WC, Powelson JA. Complex arterial reconstruction for pancreas transplantation in recipients with advanced arteriosclerosis. Transplantation 2007; 83: 1385-1388.
- Troppmann C, Gruessner AC, Benedetti E, et al. Vascular graft thrombosis after pancreatic transplantation: univariate and multivariate operative and non-operative risk factor analysis. J Am Coll Surg. 1996; 182: 285-316.
- Scheffert TL, Taber DJ, Pilch NA, et al. Clinical outcomes associated with the early postoperative use of heparin in pancreas transplantation Transplantation. 2014; 97(6): 681-685.
- Blundell J, Shahrestani S, Lendzion R, Pleass HJ, Hawthorne WJ. Risk factors for early pancreatic allograft thrombosis following simultaneous pancreas-kidney transplantation: a systematic review. Clin Appl Thromb Hemost. 2020; 26: 1-14.
- Humar A, Kandaswamy R, Granger D, Gruessner RW, Gruessner AC, Sutherland DER. Decreased surgical risks of pancreas transplantation in the modern era. Ann Surg. 2000; 231: 269-275.
- Schenker P, Vonend O, Ertas N, et al. Incidence of pancreas graft thrombosis using low-molecular-weight heparin. Clin Transplant. 2009; 23: 407-411.
- Kandaswamy R, Stock PG, Gustafson SK, et al. OPTN/SRTR 2018 Annual Data Report: Pancreas. Am J Transplant. 2020; 20(Suppl 1): 131-192.
- Humar A, Ramcharan T, Kandaswamy R, Gruessner RWG, Gruessner AC, Sutherland DER. Technical failures after pancreas transplants: why grafts fail and the risk factors: a multivariate analysis. Transplantation. 2004; 78: 1188-1192.
- Steurer W, Tabbi MG, Bonatti H, et al. Stapler duodenojejunostomy reduces intraabdominal infection after combined pancreas kidney transplantation as compared with hand-sawn anastomosis. Transplant Proc. 2002; 34: 3357-3360.
- Manrique A, Jiménez C, López R, et al. Relaparotomy after pancreas transplantation: causes and outcome. Transplant Proc. 2009; 41: 2472-2475.
- Troppmann C, Dunn DL, Najarian JS, et al. Operative reintervention following early complications after pancreas transplantation. Transplant Proc. 1994; 26(2): 454.
- Douzdjian V, Abecassis M, Cooper JL, Smith JL, Corry J. Incidence, management and significance of surgical complications after pancreas transplantation. Surg Gynecol Obstet. 1993; 177: 451-456.
- Jiménez C, Manrique A, Herrero ML, et al. Incidence of pancreas graft thrombosis in portoiliac and portocaval venous anastomosis. Transplant Proc. 2005; 37: 3977-3978.
- Jiménez-Romero C, Marcacuzco Quinto A, Manrique Municio A, et al. Trasplante de páncreas-riñón simultáneo. Experiencia del Hospital Doce de Octubre. Cir Esp. 2018; 96: 25-34.
- Spetzler VN, Goldaracena N, Marquez MA, et al. Duodenal leaks after pancreas transplantation with enteric drainage: characteristics and risk factors. Transpl Int. 2015; 28: 720-728.
- Keck T, Banafsche R, Werner J, Gebhard MM, Herfarth C, Klar E. Desmopressin impairs microcirculation in donor pancreas and early graft function after experimental pancreas transplantation. Transplantation. 2001; 72: 202-209.
- Hanish SI, Petersen RP, Collins BH, et al. Obesity predicts increased overall complications following pancreas transplantation. Transplant Proc. 2005; 37: 3564-3566.
- Jiménez-Romero C, Manrique A, Morales JM, et al. Conversion from bladder to enteric drainage for complications after pancreas transplantation. Transplant Proc. 2009; 41: 2469-2471.
- Medina Polo J, Morales JM, Blanco M, et al. Urological complications after simultaneous pancreas-kidney transplantation. Transplant Proc. 2009; 41: 2457-2459.
- Herrero-Martínez JM, Lumbreras C, Manrique A, et al. Epidemiology, risk factors and impact on long-term pancreas function of infection following pancreas-kidney transplantation. Clin Microbiol Infect. 2013; 19: 1132-1139.
- Lumbreras C, Fernández I, Velosa J, Munn S, Sterioff S, Paya CV. Infectious complications following pancreatic transplantation: incidence, microbiological and clinical characteristics, and outcome. Clin Infect Dis. 1995; 20: 514-520.
- Jiménez C, Lumbreras C, Aguado JM, et al. Successful treatment of mucor infection after liver or pancreas-kidney transplantation. Transplantation. 2002; 73: 476-480.
- Marcacuzco A, Jiménez-Romero C, Manrique A, et al. Outcome of patients with hemodialysis undergoing simultaneous pancreas-kidney transplantation. Clin Transplant. 2018; 32: e13268.
- Freise CE, Hirose R, Feng S, et al. Minimal rejection with a steroid sparing protocol in simultaneous pancreas kidney transplantation. Am J Transplant. 2002; 2(Suppl.3): 203.
- Vendrame F, Hopfner YY, Diamantopoulos S, et al. Risk factors for type 1 diabetes recurrence in immunosuppressed recipients of simultaneous pancreas-kidney transplants. Am J Transplant. 2016; 16: 235-245.
- Esmeijer K, Hoogeveen EK, van den Boog PJM, et al. Superior long-term survival for simultaneous pancreas-kidney transplantation as renal replacement therapy: 30-year follow-up of a nationwide cohort. Diabetes Care. 2020; 43: 321-328.
- Sutherland DER, Gruessner RWG, Dunn DL, et al. Lessons learned from more than 1.000 pancreas transplants at a single institution. Ann Surg. 2001; 233: 463-501.
- Navarro X, Sutherland DER, Kennedy WR. Long term effects of pancreatic transplantation on diabetic neuropathy. Ann Neurol. 1997; 42: 727-736.
- Jukema JW, Smets YF, van der Pijl JW, et al. Impact of simultaneous pancreas and kidney transplantation on progression of coronary atherosclerosis in patients with end-stage renal failure due to type 1 diabetes. Diabetes. 2002; 25: 906-911.
- Elliott MD, Kapoor A, Parker MA, et al. Improvement in hypertension in patients with diabetes mellitus after kidney/pancreas transplantation. Circulation. 2001; 104: 563-569.
- Ulbig M, Kampik A, Thurau S, et al. Long-term follow-up of diabetic retinopathy for up to 71 months after combined renal and pancreatic transplantation. Graefe´s Arch Clin Exp Ophthalmol. 1991; 229: 242-245.
- Voglová B, Hladiková Z, Nemétová L, et al. Early worsening diabetic retinopathy after simultaneous pancreas and kidney transplantation – Myth or reality? Am J Transplant. 2020; 20: 2832-2841.
- Nathan DM, Fogel H, Norman D, et al. Long-term metabolic and quality of life results with pancreatic/renal transplantation in insulin-dependent diabetes mellitus. Transplantation. 1991; 52: 85-91.
- Gross CR, Limwattananon C, Matthees B, et al. Impact of transplantation on quality of life in patients with diabetes and renal dysfunction. Transplantation. 2000; 70: 1736-1746.
- Tang J, Gulyani A, Hewawasam E, et al. Pregnancy outcomes for simultaneous pancreas-kidney transplant recipients versus kidney transplant recipients. Clin Transplant. 2021; 35: e14151
DECLARACIÓN DE TRANSPARENCIA
Los autores/as de este artículo declaran no tener ningún tipo de conflicto de intereses respecto a lo expuesto en el presente trabajo.
ranm tv
Carlos Jiménez Romero.
Unidad de Cirugía HBP y Trasplante de Órganos Abdominales
H. Universitario Doce de Octubre. Ctra de Andalucia Km 5,4 · 28041 Madrid
Tlf.: +34 913 908 294 | E-Mail: carlos.jimenez@inforboe.es
An RANM. 2021;138(02): 157 – 167
Enviado*: 01.06.21
Revisado: 07.06.21
Aceptado: 18.06.21
* Fecha de lectura en la RANM


