Resumen
La enfermedad de Castleman, es un trastorno linfoproliferativo poco frecuente. La forma localizada es la más común y suele ser asintomática, pese a que el diagnóstico definitivo es histológico hay que conocer cómo se manifiesta en los estudios de imagen. La localización más frecuente en los casos de Enfermedad de Castleman unicéntrica es el tórax. Exponemos el caso de una paciente de nuestro centro para mejorar y profundizar sobre la interpretación de las pruebas de imagen en esta patología.
Abstract
Castleman’s disease is a rare lymphoproliferative disorder. The localized form is the most frequent and it is usually asymptomatic. Although the definitive diagnosis is histologic, it is necessary to know how it manifests in imaging studies. The most frequent location in cases of unicentric Castleman’s disease is the thorax. We present the case of a patient from our center to improve the interpretation of imaging proof in this pathology.
Palabras clave: Enfermedad de Castleman; Unicéntrica; PET/TC; 18F-FDG; TC.
Keywords: Castleman´s disease; Unicentric; PET/CT; 18F-FDG; CT.
INTRODUCCIÓN
La enfermedad de Castleman (EC) es un trastorno linfoproliferativo benigno que fue descubierto en 1954 por el Doctor B. Castleman (1).
Se clasifica en función de su morfología en dos subtipos en: EC unicéntrica (ECU) afectando a un único nódulo linfático o una sola estación linfática, mientras que la EC multicéntrica (ECM) afecta a múltiples estaciones linfáticas.
Los principales subtipos histológicos de la EC son las variantes hialino-vasculares, la de células plasmáticas y la variante mixta que comparte hallazgos patológicos de ambas (2).
En cuanto a la clínica los pacientes con ECU tienen una presentación asintomática y afectan con mayor frecuencia al tórax. Los pacientes con enfermedad multicéntrica presentan síntomas sistémicos; el alcance y la gravedad de estos síntomas pueden variar en función de coinfecciones (VIH/VHH8) o condiciones sistémicas (Síndrome de POEMS) (3).
Por todo ello la enfermedad de Castleman supone un reto diagnóstico y es importante conocer e interpretar los hallazgos por imagen.
CASO CLÍNICO
Paciente de 37 años que acude al servicio de urgencias por tos y febrícula, sin referir contacto estrecho con COVID. Se solicita una PCR siendo negativa y una radiografía de tórax PA y LAT para descartar neumonía SARS-COV2. En el estudio por imagen (Figura 1 Imagen A línea superior) se observa una masa mediastínica, por lo que se decide realizar un estudio de forma programada para valorar la lesión.
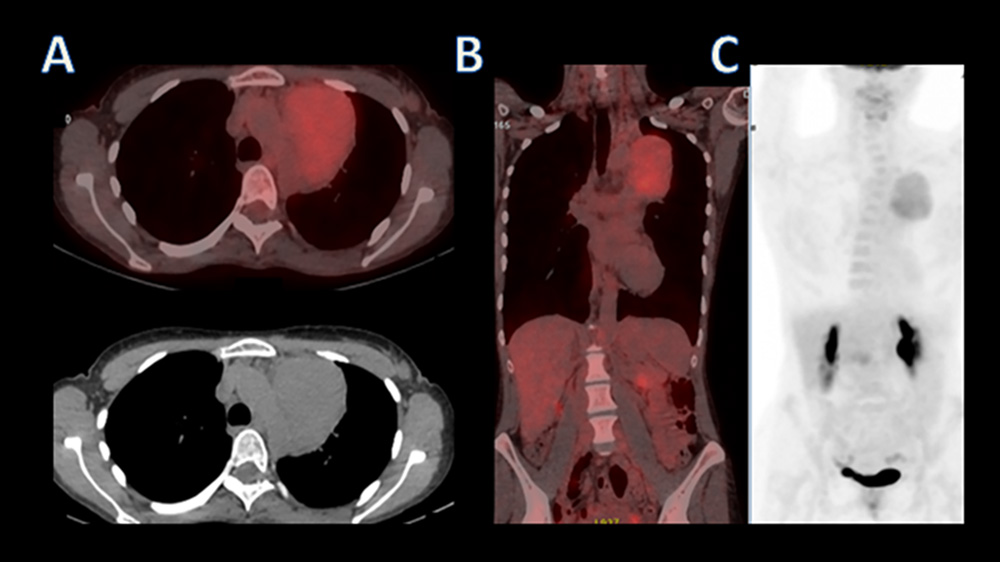
Se solicita un TC con contraste identificándose, una masa única en mediastino anterior, hipervascular (Figura 1 Imagen B línea inferior), sin otras lesiones asociadas. Ante la sospecha de un síndrome linfoproliferativo, se realiza un PET/TC para caracterizar metabólicamente la lesión. Destacando una leve captación de 18F-FDG por parte de la masa, asociando un metabolismo similar a la región referencia hepática (Figura 2). En la biopsia se identifica una tumoración de tejido linfoide, conformada por folículos linfoides que contienen centros germinales atróficos con presencia de células dendríticas y una disposición concéntrica de los linfocitos en la zona del manto, con una apariencia en «capas de cebolla». El estroma interfolicular es prominente, con frecuentes vasos hiperplásicos siendo el estudio anatomopatológico compatible con ECU variante hialino vascular.

Se completó el estudio con una analítica (LDH, VSG, PCR, IL6, inmunoglobulinas) y serología (VIH, VHH8) siendo negativa y sin hallazgos de afectación sistémica. Se decide realizar resección completa de la lesión como tratamiento curativo.
DISCUSIÓN
La Enfermedad de Castleman es una entidad poco frecuente que puede aparecer a cualquier edad, aunque lo más frecuente es que suceda en torno a la 3º-4º década de la vida en los casos de ECU, como en nuestra paciente. Sin embargo, la ECM suele aparecer en torno a los 60 años (2), este subtipo es de peor pronóstico y se subdivide en: idiopática (ECMi), asociada al VHH8 (ECM-VHH8) o al síndrome de POEMS (ECM-POEMS) (2)
La mayoría de las EC multicéntricas se relacionan con un estado de inmunodeficiencia por la infección por el VIH y el VHH-8, estos pacientes también tienen un mayor riesgo de desarrollar sarcoma de Kaposi y linfomas (4). Se sabe que el VHH8 codifica la IL6. Esta interleukina ayuda a la diferenciación de los linfocitos B a células plasmáticas y estimula la proteína C, desencadenando el síndrome inflamatorio (3) por ello ECM suele presentar afectación sistémica.
Se debe solicitar a todos los pacientes la prueba del VIH y los niveles de ADN del VHH8 porque es un marcador útil para valorar la actividad de la enfermedad y la respuesta al tratamiento (5).
Patológicamente, se reconocen dos variantes histológicas principales: el tipo hialino-vascular (HV) y el tipo de células plasmáticas (CP). La HV se da en un 90% de los casos de enfermedad de Castleman unicéntrica (4) y se caracteriza por presentar hiperplasia folicular y aumento de la vascularización a nivel interfolicular. Es frecuente observar linfocitos dispuestos en varias capas en la zona del manto «capas de cebolla» y presencia de células dendríticas como el caso de nuestra paciente.
La variante de células plasmáticas se caracteriza por la escasez de vasos hialinizados en los centros germinales con presencia de abundantes células plasmáticas en el área interfolicular ganglionar (5). (Figura 3) La enfermedad de Castleman puede imitar otras patologías, por ello destacamos las características más frecuentes de los estudios por imagen para ayudar a un correcta orientación cuando nos encontremos con esos retos diagnósticos, sobre todo centrándonos en la ECU torácica que era el caso de nuestra paciente.

La EC puede aparecer en cualquier localización, incluso en territorios extralinfáticos. Aproximadamente el 70% se localizan en el tórax (4), suele presentarse como un ganglio solitario o una masa localizada en el mediastino o en el hilio (6). En la radiografía identificamos una masa en mediastino anterior como veíamos en la (Figura 1), ampliando el estudio con un TC.
La enfermedad de Castleman torácica unicéntrica en el TC puede clasificarse según los siguientes patrones: como una masa solitaria, no invasiva (50% de los casos); una masa dominante con afectación de estructuras contiguas (40% de los casos) o con menor frecuencia como una linfadenopatía o conglomerado adenopático limitada a un compartimento mediastínico (4). La presencia de calcificaciones es muy infrecuente y puede incluir patrones puntuales o gruesos en la periferia de la lesión (6) a diferencia de otras lesiones mediastínicas como el timoma que con mayor frecuencia presentan calcificaciones y áreas quísticas(7).
Tras la administración de contraste la mayoría de los casos presentan un realce homogéneo e intenso, que refleja la hipervascularización de la de la lesión, se considera este hallazgo en el TC característico de las enfermedades de Castleman unicéntricas torácicas y abdominales (4). Este intenso realce, es secundario a la presencia de una extensa red de pequeños vasos sanguíneos en la zona interfolicular del subtipo vascular hialino, que representa la gran mayoría de los casos de ECU(8).
Nos encontramos con una paciente asintomática con una masa mediastínica anterior bien circunscrita, no invasiva e hipervascular tras la administración de contraste. Hay que hacer un diagnóstico diferencial con otras lesiones en mediastino anterior hipervasculares, (8) en estos casos los estudios PET/TC tienen en cuenta las características metabólicas de las estructuras colaborando en el diagnóstico (9).
La sospecha principal fue de síndrome linfoproliferativo, en la imagen PET/TC (Figura2). Nuestra paciente presentó una lesión mediastínica con leve metabolismo y un valor captación estandarizado (SUVmáx 4,3) no se identificaron otras lesiones hipermetabólicas, corroborando la enfermedad unicéntrica.
La Enfermedad de Castleman en la PET/TC muestra avidez por la 18F-FDG presentando un rango elevado pero variable de SUVmáx por encima de 2 (10). Se ha observado que los valores de (SUV) de los ganglios linfáticos con 18F-FDG en la EC son menores que los observados en el linfoma activo (6). Por ello ante pacientes asintomáticos en los que de manera incidental, identifiquemos una masa hipervascular en mediastino y que asocie metabolismo en la PET/TC debemos recordar esta patología.
Actualmente en las guías clínicas sólo se recomienda como alternativa al TC la PET/TC en las directrices de tratamiento publicadas para la (ECMi) (9), pero sabemos que ésta técnica de imagen molecular, puede detectar una captación anormalmente alta en los ganglios linfáticos pequeños o normales, que pasarían por alto con la TC. Además, se ha visto en los casos de ECM-VHH8 presenta una mayor captación de 18F-FDG en otras localizaciones como: el bazo y médula ósea (9). Los estudios de imagen tienen un papel fundamental a la hora de valorar el riesgo de la EC; La presencia de hepato-esplenomegalia, ascitis y derrame puede implicar afectación sistémica y asociar mayor riesgo de malignizar (3). La PET/TC ha demostrado que el aumento de captación del radiofármaco se correlaciona con la multicentricidad y este hallazgo puede ayudar como marcador de gravedad (10).
En la ECU la resección completa de la lesión es el tratamiento curativo en la mayoría de los pacientes. Pero pese a tener un mejor pronóstico y menor riesgo de malignizar que la ECM, pueden desarrollar linfomas y se ha relacionado el sarcoma de células dendríticas foliculares con la ECU (5), muchas veces se diagnostican tras el estudio histológico de la pieza o durante el seguimiento de la enfermedad. Por ello los estudios de imagen no sólo ayudan a diferenciar entre afectación unicéntrica o multicéntrica, sino que además juegan un papel fundamental para valorar la progresión, el riesgo de malignizar y hacer un correcto seguimiento. Por esta razón es fundamental conocer la Enfermedad de Castleman e interpretar y reconocer los hallazgos de esta patología en los estudios de imagen.
BIBLIOGRAFÍA
- Castleman B, Towne V. CASE records of the Massachusetts General Hospital weekly clinicopathological exercises: case 40011. N Engl J Med.1954;250(1):26-30
- Dispenzieri A, Fajgenbaum DC. Overview of Castleman disease. Blood. 2020;135(16):1353–64.
- Bonekamp D, Horton KM, Hruban RH, Fishman EK. Castleman disease: the great mimic. Radiographics. 2011;31(6):1793–1807.
- Ko S-F, Hsieh M-J, Ng S-H, et al. Imaging spectrum of Castleman’s disease. AJR Am J Roentgenol. 2004;182(3):769–775
- Soumerai JD, Sohani AR, Abramson JS. Diagnosis and management of Castleman disease. Cancer Control. 2014;21(4):266–278.
- Madan R, Chen J-H, Trotman-Dickenson B, Jacobson F, Hunsaker A. The spectrum of Castleman’s disease: mimics, radiologic pathologic correlation and role of imaging in patient management. Eur J Radiol. 2012;81(1):123–131.
- Benveniste MFK, Rosado-de-Christenson ML, Sabloff BS, Moran CA, Swisher SG, Marom EM. Role of imaging in the diagnosis, staging, and treatment of thymoma. Radiographics. 2011;31(7):1847–61; discussion 1861-1863.
- Kligerman SJ, Auerbach A, Franks TJ, Galvin JR. Castleman disease of the thorax: Clinical, radiologic, and pathologic correlation: From the radiologic pathology archives. Radiographics. 2016;36(5):1309–1332.
- Koa B, Borja AJ, Aly M, et al. Emerging role of 18F-FDG PET/CT in Castleman disease: a review. Insights Imaging. 2021;12(1):35.doi:10.1186/s13244-021-00963-1
- Lee ES, Paeng JC, Park CM, et al. Metabolic characteristics of Castleman disease on 18F-FDG PET in relation to clinical implication. Clin Nucl Med. 2013;38(5):339–342
DECLARACIÓN DE TRANSPARENCIA
Los autores/as de este artículo declaran no tener ningún tipo de conflicto de intereses respecto a lo expuesto en el presente trabajo.
Ana Utrera Costero
Hospital Universitario y Politécnico La Fe. Servicio de Medicina Nuclear
Avda. de Fernando Abril Martorell, 106 · 46026 València, Valencia
Tlf.:+34 91 547 03 18 | E-Mail: utrera_anacos@gva.es
Año 2021 · número 138 (03) · páginas 283 a 287
Enviado: 25.11.21
Revisado: 29.11.21
Aceptado: 14.12.21


