Resumen
Las lesiones de nervio periférico y plexo braquial son complejas y suponen un gran deterioro funcional. El diagnóstico precoz y la exploración y reconstrucción quirúrgicas son fundamentales en casos seleccionados, ya que la atrofia muscular generada por la denervación del músculo limita los tratamientos quirúrgicos que se pueden realizar una vez sobrepasado un determinado plazo temporal.
Las pruebas radiológicas y neurofisiológicas son cruciales para un correcto diagnóstico y seguimiento de las lesiones, y la rehabilitación es esencial para una correcta evolución postquirúrgica. Las opciones quirúrgicas incluyen la reparación primaria, reparación con injertos nerviosos, transferencias nerviosas, transferencias de músculo libre funcional y transferencias tendinosas, teniendo que adecuar a la clínica y tiempo de evolución del paciente la técnica quirúrgica a realizar. Una vez se produce la atrofia muscular, la reparación nerviosa y las transferencias nerviosas no conseguirán un buen resultado funcional.
Debido a la complejidad de estas lesiones y la necesidad de diferentes especialistas, estos pacientes deben ser tratados en unidades multidisciplinares para conseguir el mejor resultado posible.Abstract
Brachial plexus and peripheral nerve injuries are complex and suppose a great functional deficit. An early diagnostic and surgical exploration and reconstruction is essential in some cases. Muscular atrophy generated by the chronic denervation limits surgical treatments that can not be performed once overcoming a specific time frame.
Radiologic and neurophysiological tests are essential to perform a correct diagnostic and follow-up of these injuries, and rehabilitation is crucial to achieve a good postsurgical outcome. Surgical treatments include primary nerve repair, repair with nerve grafts, nerve transfers, free functional muscle transfers and tendon transfers. Each technique should be adequate to the clinic and evolution time of the injury. Once muscle atrophy is established, nerve repair and nerve transfers do not achieve a good functional result.
Due to the high complexity of these injuries and the need for different medical specialists, these patients must be treated in multidisciplinary units to achieve the best possible result.Palabras clave: Nervio periférico; Plexo braquial; Cirugía reconstructiva; Lesiones nerviosas.
Keywords: Peripheral nerve; Brachial plexus; Reconstructive Surgery; Nerve injuries.
INTRODUCCIÓN
Las lesiones del plexo braquial y nervio periférico se manifiestan como pérdida de función motora, pérdida de sensibilidad e incluso dolor neuropático. Estas lesiones pueden requerir largos periodos de recuperación, además de dejar secuelas temporales o permanentes que pueden ser limitantes para la vida diaria de las personas, afectando a su calidad de vida. En Europa, se estima una incidencia de 300.000 casos nuevos por año (1). El perfil de paciente es joven (edad media 29 años) y varón (75%)(2,3).
En esta revisión bibliográfica se describirán los principios biológicos fundamentales de estas lesiones, el tratamiento clínico y quirúrgico actual necesario para optimizar la recuperación de estos pacientes.
RESPUESTA ORGÁNICA TRAS LAS LESIONES DE PLEXO BRAQUIAL Y NERVIO PERIFÉRICO
De acuerdo con la clasificación de Sunderland, podemos encontrar diferentes tipos de daño nervioso en función de las estructuras afectadas (6):
- Tipo I: lesión de la vaina de mielina.
- Tipo II: daño axonal.
- Tipo III: daño axonal y del endoneuro.
- Tipo IV: daño axonal, del endoneuro y del perineuro.
- Tipo V: sección nerviosa completa.
- Tipo VI: las fibras nerviosas presentan en diferentes zonas diversos grados de afectación.
Salvo en las lesiones tipo I de Sunderland, los nervios sometidos a traumatismos desarrollarán un proceso de degeneración walleriana en torno a la primera semana tras la lesión, produciendo la desestructuración del cabo distal del nervio dañado (7). En el cabo proximal se produce una desestructuración limitada que alcanza, de forma típica, hasta el primer nodo de Ranvier. No obstante, si la lesión se produce muy cerca del cuerpo neuronal, se puede producir la apoptosis de la célula (7). La regeneración axonal se produce una vez se completa la degeneración walleriana. En el extremo distal del cabo proximal se forma un cono de crecimiento cuya organización se puede ver dificultada por la interposición de tejido cicatricial. La velocidad de crecimiento es de entre 2-3 mm/día en segmentos proximales, mientras que en segmentos más distales es menor, de 1-2 mm/día (7).
Tras la denervación, se producen cambios a nivel muscular. Los músculos diana se atrofian de forma gradual, pierden masa por atrofia de las fibras musculares. A partir de 3 semanas, las fibras musculares denervadas comienzan a realizar descargas espontáneas en reposo, que se registran en el EMG como fibrilaciones y ondas agudas. La hipotrofia muscular por denervación y desuso llega a su máximo en 3-4 meses. Si el músculo no se reinerva, se produce la proliferación de fibroblastos, y se deposita colágeno en el endo y perimisio, de modo que las fibras musculares atróficas son reemplazadas por tejido conectivo engrosado (8).
Cuando se produce la reparación nerviosa, se facilita el proceso de reinervación de las fibras denervadas, aumenta la masa muscular y el diámetro de las fibras musculares de manera que el músculo experimenta una recuperación funcional. No obstante, cuando la reparación nerviosa se difiere, la reinervación del músculo es menos eficaz (8).
DIAGNÓSTICO Y MANEJO QUIRÚRGICO ANTE LA SOSPECHA DE LESIONES NERVIOSAS
Una exploración física exhaustiva es crucial para determinar el nervio o nervios dañados. Es imprescindible valorar tanto, el posible déficit motor, como sensitivo en función del territorio afectado.
La sensibilidad se puede explorar con el test de sensibilidad de dos puntos o con el test de monofilamentos de Semmes-Weinstein (9).
En el caso de pérdida de función nerviosa aguda, el manejo clínico es diferente dependiendo de si son secundarias a un traumatismo que produce una solución de continuidad, o si se trata de lesiones cerradas (2). Si la clínica neurológica se presenta en el contexto de un traumatismo con solución de continuidad, se debe realizar una exploración quirúrgica urgente de las estructuras nerviosas (2).
En cuanto a las lesiones cerradas, el estudio inicial debe investigar la continuidad del nervio afectado. Si se sospecha que el nervio pudiera estar seccionado (lesión tipo V de Sunderland), es necesaria una exploración quirúrgica temprana. La recuperación nerviosa no puede darse sin una continuidad nerviosa. Sin embargo, si los estudios neurofisiológicos y las pruebas de imagen justifican la continuidad del nervio, puede realizarse un manejo conservador inicial. Será necesario un seguimiento clínico y neurofisiológico, valorando parámetros clínicos (fuerza muscular y sensibilidad) y aparición de datos de denervación o de reinervación en pruebas neurofisiológicas (2).
ESTUDIOS NEUROFISIOLÓGICOS EN LESIONES NERVIOSAS
Dentro de las pruebas que debemos realizar en la sospecha de lesiones nerviosas cerradas encontramos el estudio de conducción nerviosa y el electromiograma. En el caso de sospecha de lesiones nerviosas agudas en traumatismos con solución de continuidad, la indicación será realizar la exploración quirúrgica de las mismas de forma inmediata.
Estudio de conducción nerviosa
Los nervios y los músculos son estructuras excitables y, sus potenciales, pueden ser inducidos y capturados por electrodos externos. Cuando un nervio es estimulado, se produce un potencial de acción muscular compuesto, el sumatorio del potencial de acción de cada fibra muscular individual (CMAP), y un potencial de acción de nervioso (NAP), que pueden ser registrados en músculo y nervio respectivamente. La amplitud y la latencia de la respuesta y la velocidad de conducción son analizadas en los estudios neurofisiológicos (9).
La amplitud de las respuestas registradas estiman la cantidad de fibras motoras o sensitivas despolarizadas, mientras que la velocidad de conducción mide la velocidad de los axones mielinizados motores o sensitivos más rápidos y de mayor calibre (9).
Cuando se produce la desmielinización de los axones (Sunderland I) se produce un bloqueo de la conducción por un fallo de la conducción saltatoria (10). En los estudios de conducción nerviosa (NCS) se observa un aumento de la latencia de respuesta motora y una disminución de la velocidad de conducción nerviosa (10).
Si tenemos pérdida de fibras nerviosas (Sunderland II-V) el hallazgo mayoritario que encontraremos en los NCS es la reducción en la amplitud de CMAP, ya que un menor número de axones funcionantes se encuentra conectado a las fibras musculares (10).
Inmediatamente después de una sección completa de un nervio debido a un traumatismo, la porción del nervio distal a la lesión será normal, ya que la degeneración axonal no habrá comenzado (10). La amplitud de CMAP sólo empezará a decrecer unos días después. En este periodo de tiempo y en lesiones donde no se afecta la vaina de mielina (Sunderland II-V), podríamos esperar encontrar latencias y velocidades de conducción normales en el cabo distal (10).
Transcurridas 1 o 2 semanas, debido a la pérdida de axones motores y la pérdida de fibras de mayor velocidad de conducción, nos encontraremos una disminución en la amplitud acorde con la degeneración axonal, así como un discreto aumento de la latencia motora y discreta disminución de la velocidad de conducción (10).
Además del estudio de las fibras nerviosas motoras, también podemos hacer NCS de fibras sensitivas (10). El potencial de acción sensitivo del nervio (SNAP) se obtiene tras estimular eléctricamente las fibras sensitivas y registrar el potencial de acción en un punto alejado del mismo nervio. Este puede ser obtenido de forma ortodrómica (estimulación distal y registro proximal) o antidrómica (estimulación proximal y registro distal) (10).
Cuando se producen lesiones a niveles proximales del plexo braquial, el mantenimiento de los SNAP depende de la presencia de cuerpos celulares no dañados en los ganglios dorsales (10). En el caso de lesiones postganglionares, registramos una disminución de la amplitud o ausencia de SNAP, mientras que, en el caso de lesiones preganglionares, encontraremos un SNAP de amplitud normal a pesar de presentar el paciente clínica sensitiva (10). Es por ello que los NCS sensitivos son muy útiles para localizar una lesión como pre o postganglionar (10).
Electromiografía
Esta prueba nos da información sobre la función del músculo y sus unidades funcionales. En ella se explora la calidad y cantidad de potenciales de acción de la unidad motora (MUAP), su reclutamiento espacio-temporal de cara a generar movimientos adecuados, la presencia de denervación y el establecimiento de reinervación (9).
En el electromiograma (EMG) lo primero que se estudia es la actividad en reposo (9). Los potenciales de fibrilación y las ondas agudas positivas aparecen en torno a los 21 días tras la lesión, mientras que las descargas repetitivas complejas indican denervación crónica (9). Los potenciales de fasciculación se producen por la activación espontánea de unidades motoras (9).
Además, debemos realizar un análisis de los MUAP y sus patrones de reclutamiento y activación durante la contracción voluntaria (9).
En la lesión axonal aguda y la desmielinización pura (Sunderland I), no todas las unidades motoras pueden ser reclutadas, pero los MUAP remanentes presentan una morfología normal con aumento de la frecuencia para obtener una contracción suficiente (9).
Varias semanas tras la denervación aguda, se puede observar reinervación precoz colateral a través de los axones sanos (Sunderland VI), lo que se registra en el EMG como pequeños potenciales satélites de los MUAP (9). Posteriormente, cuando se produce un aumento de fibras musculares por unidad motora debido a la reinervación, los MUAP aumentan en amplitud, se prolongan y son polifásicos, siendo éste el patrón de denervación-reinervación (9).
Para valorar la presencia de pérdida axonal (presencia de potenciales de denervación), el tiempo óptimo para realizar el estudio electrofisiológico es a partir de las 3 semanas tras la lesión (9). Estos estudios se deben repetir en 3 meses para realizar un seguimiento de las lesiones y determinar si es necesaria una reparación quirúrgica de acuerdo al ratio de denervación-reinervación (9).
Neurofisiología intraoperatoria
Los usos de la monitorización neurofisiológica durante la cirugía incluyen: 1. identificar nervios periféricos, 2. localizar lesiones preexistentes a lo largo del transcurso de un nervio; 3. determinar la continuidad funcional a través de una lesión preexistente; 4. determinar la probabilidad de presentar una avulsión de raíces nerviosas; 5. identificar dianas para la biopsia nerviosa; 6. monitorizar y prevenir daño a estructuras nerviosas íntegras durante la cirugía (11).
Las diferentes características neurofisiológicas según en tipo de lesión nerviosa han sido resumidas en la Tabla 1.

PRUEBAS DE IMAGEN
La investigación neurofisiológica nos aporta información sobre la fisiopatología del déficit nervioso, su grado de severidad y pronóstico (9). No obstante, aunque se trata de una herramienta fundamental en la evaluación clínica, no provee información precisa respecto a la morfología, etiología o extensión de las lesiones focales en nervios periféricos frente a la afectación focal de algunos fascículos (9,11).
En casos graves con nervios no excitables y en pacientes postoperados que no muestren signos de mejoría, el electromiograma y las velocidades de conducción no pueden aportar información concluyente respecto a la presencia de sección nerviosa, distancia entre cabos nerviosos o la presencia de múltiples sitios de daño nervioso (9). La valoración por imagen, concretamente la resonancia magnética y la ecografía, pueden superar estos problemas aportando información sobre la morfología nerviosa y los tejidos adyacentes (9).
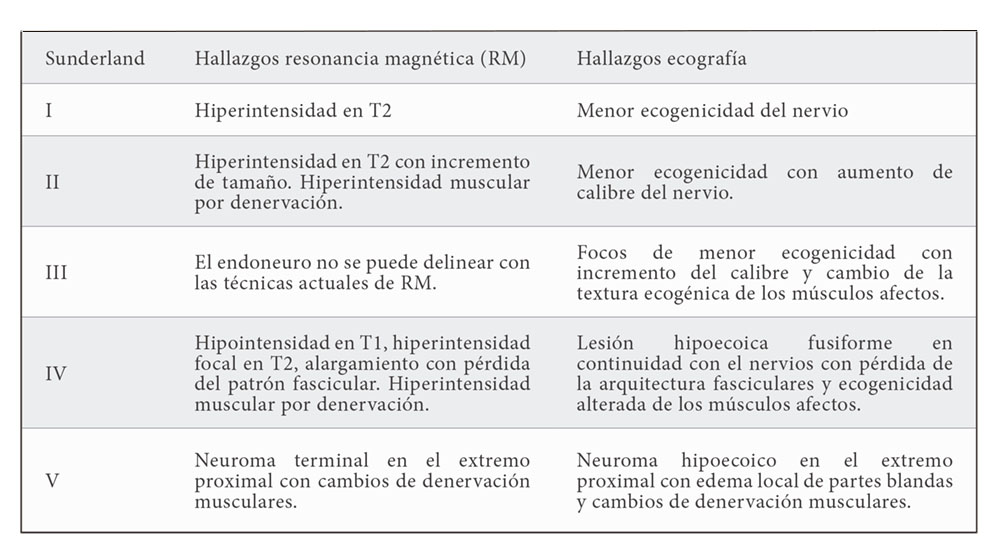
La resonancia magnética (RM) y la ecografía nos permiten determinar si existe daño en un nervio, con hallazgos diferentes en función del tipo de lesión de acuerdo a la clasificación de Sunderland (12).
En algunos estudios, se aprecia una sensibilidad similar de ambas pruebas de imagen (RM y ecografía) para la valoración de la continuidad del nervio, mientras que existe una menor sensibilidad de la ecografía en la detección de neuromas (88% frente al 100% de la RM) (12). En otros estudios (13) se observa un 93.2% de precisión a la hora de clasificar el daño traumático del nervio periférico por ecografía.
La ecografía nos permite realizar la valoración del nervio periférico en pacientes en los que la RM no puede interpretarse adecuadamente por la presencia de dispositivos que producen alteración del campo magnético (implantes metálicos, marcapasos u otros dispositivos). Otras de sus ventajas es la capacidad que presenta para examinar un territorio nervioso completo y poder realizar una exploración en tiempo real y con maniobras dinámicas.
La RM de plexo braquial es útil para valorar la afectación nerviosa extensa en algunas patologías o tumores de nervio periférico y detectar los signos de denervación muscular de manera precoz. Para ello utiliza secuencias potenciadas en T1 y secuencias sensibles al líquido (potenciadas en T2 con saturación grasa). La realización adicional de secuencias tras la administración de contraste intravenoso, son beneficiosas en casos de lesiones con características similares al nervio, tumores nerviosos y para descartar la presencia de cambios cicatriciales en los casos de neuropatía remanente o recurrente (14).
La neurografía por resonancia magnética es otra técnica que permite a través de secuencias de alta resolución en equipos con alto campo magnético, estudiar con más detalle la anatomía de los nervios periféricos y plexos, y delimitar de forma más exacta la extensión de las lesiones (14). Para ello utiliza secuencias de alta resolución y cortes muy finos, aunque su uso no está ampliamente extendido.
Las diferentes características radiológicas según el tipo de lesión nerviosa han sido resumidas en la Tabla 2.
TRATAMIENTO QUIRÚRGICO
Sutura primaria y utilización de injertos nerviosos
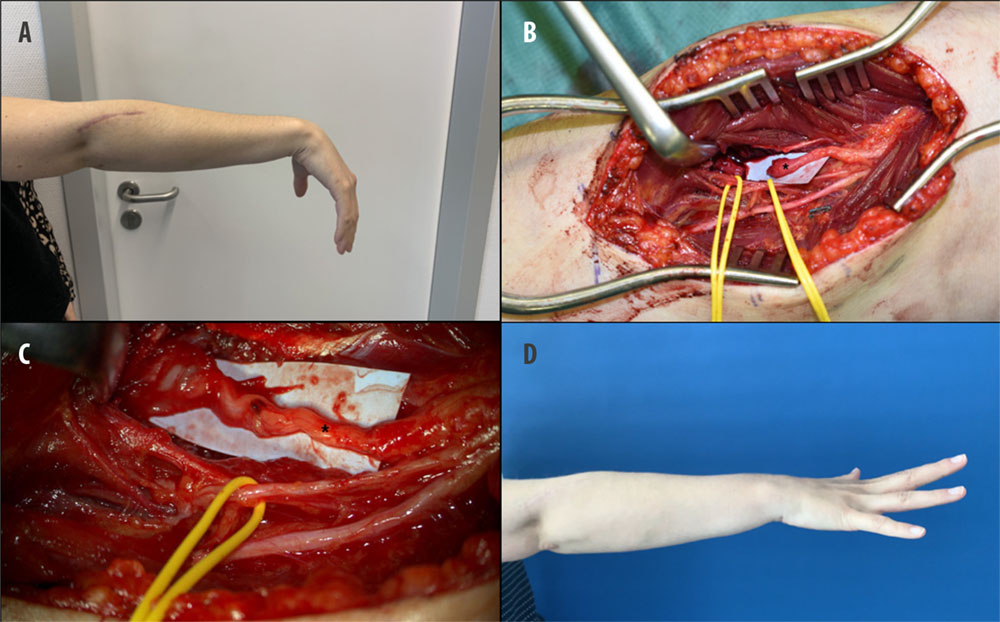
En las lesiones nerviosas agudas no cerradas se debe realizar una exploración quirúrgica de las estructuras que se puedan encontrar dañadas, realizando un desbridamiento del tejido necrótico y de los nervios afectos hasta hallar tejido viable (2,15). Los nervios seccionados deben suturarse. Al realizar la sutura primaria del nervio, en caso de nervios mixtos con componente sensitivo y motor, tendremos que tener en cuenta la disposición de las fibras para realizar una alineación correcta (15).
Siempre que sea posible se realizará una neurorrafia término-terminal sin tensión de ambos cabos del nervio lesionado (2). La exploración y reparación nerviosa se deben realizar, si es posible, en las primeras 48 horas (2). En caso de no poder realizar una sutura sin tensión, se debe interponer un injerto nervioso para realizar la neurorrafia (16). No obstante, se suele encontrar un peor resultado funcional en el uso de injertos nerviosos frente a la sutura primaria (15,17).
Los autoinjertos nerviosos aportan una estructura con factores neurotróficos y células de Schwann viables para la regeneración axonal. Estos pueden ser obtenidos de múltiples nervios donantes, siendo el nervio sural el más habitual (15).
No obstante, existen otros nervios subsidiarios de ser utilizados como donantes para obtener autoinjertos nerviosos, tal como los nervios cutáneos antebraquiales medial y lateral, la rama cutánea dorsal del nervio cubital, los nervios peroneos superficial (distal), los nervios intercostales y los nervios cutáneos del muslo lateral y posterior (15). La obtención de autoinjertos resulta en una pérdida de función del nervio utilizado, generando zonas de anestesia e hipoestesia (temporal o permanente) de los territorios inervados por el mismo, una cicatriz en la zona donante, y el riesgo de formar un neuroma doloroso en el extremo proximal del nervio (15,18). No obstante, esta morbilidad suele ser baja y aceptable para el paciente (18).
Los aloinjertos de cadáver pueden ser tratados de numerosos modos para reducir los antígenos presentes en ellos, como la liofilización, preservación en frío o irradiación (15). El uso de aloinjertos de cadáver precisa la viabilidad de las células de Schwann tanto del receptor como del aloinjerto, ya que éstas actúan como células de soporte para la remielinización y como células presentadoras de antígenos (15). Al no eliminar la presencia de antígenos del donante de forma completa, para el uso de estos, se requiere la utilización de inmunosupresión sistémica de forma temporal, hasta que las células de Schwann del paciente migren de forma efectiva hacia la zona de injerto, típicamente a los 24 meses (15).
Recientemente se ha popularizado el uso de diferentes aloinjertos acelulares que eliminan las células de Schwann, de modo que se crea un producto inmunotolerante. Se preserva la arquitectura celular y las señales de guía en forma de laminina. Sin células, no se produce la degeneración walleriana ni la degeneración de los tubos endoneurales. Aunque se han publicado resultados prometedores usando aloinjertos acelulares en nervios sensitivos e incluso mixtos (19), el nervio autólogo sigue siendo el gold standard en la reconstrucción nerviosa.
Transferencias nerviosas
Las transferencias nerviosas fueron popularizadas en 1984 por Oberlin, mejorando significativamente los resultados funcionales en lesiones complejas (20). Éstas convierten una lesión proximal en una lesión distal al transferir la función de un nervio funcionante a un nervio distal no funcionante próximo a la musculatura a reinervar (15). Las indicaciones del uso de transferencias nerviosas incluyen, entre otras: lesión del plexo braquial u otras lesiones proximales, distancia extensa desde el punto de lesión a la placa motora, pacientes que acuden a consulta de forma tardía, lesión traumática significativa de la extremidad que resulte en una pérdida segmentaria de la función nerviosa y lesión nerviosa previa con cicatrización significativa alrededor del hueso o estructuras vasculares (15).

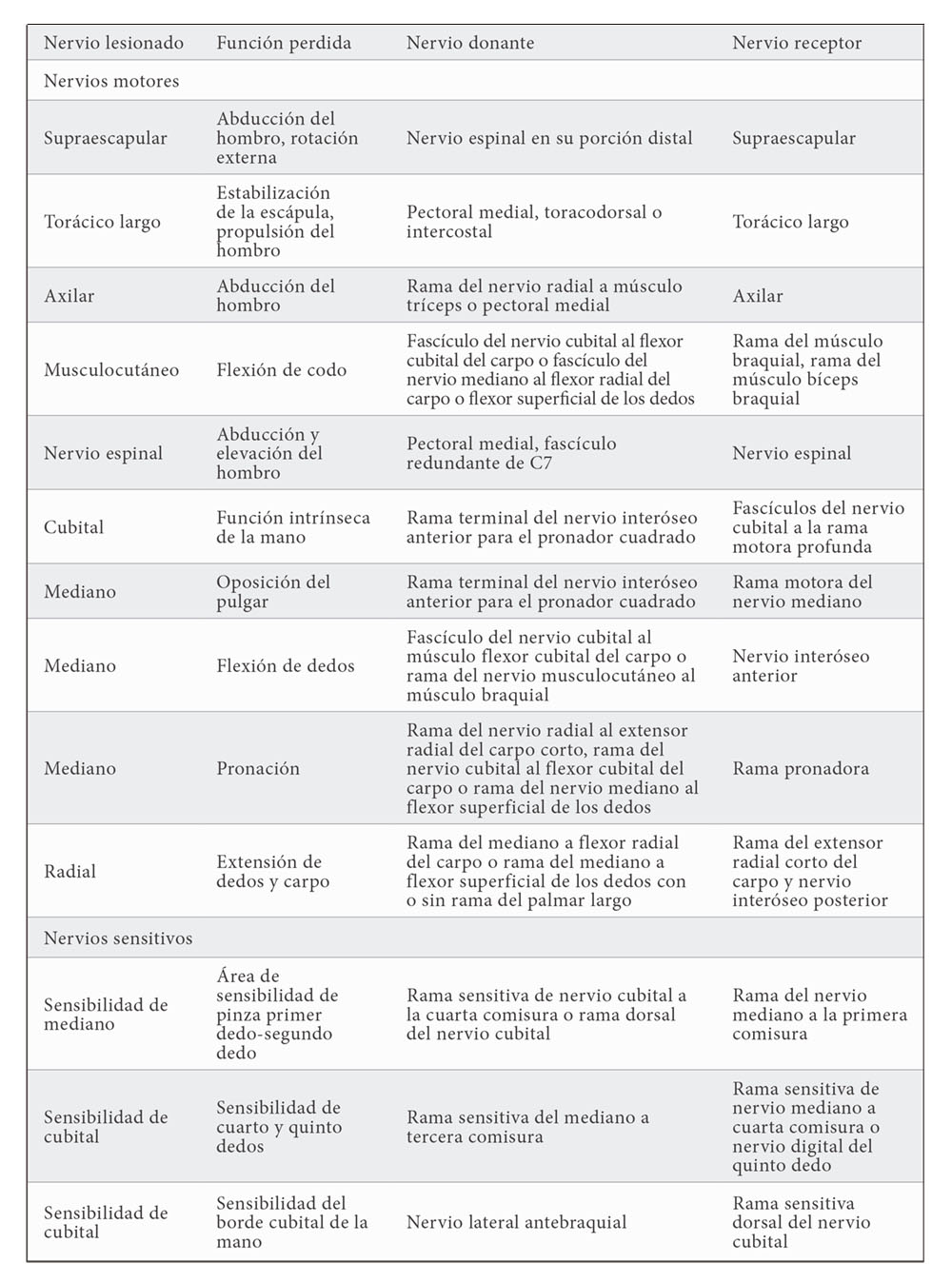
Algunas de las transferencias nerviosas más utilizadas han sido resumidas en la Tabla 3.
Colgajos musculares
La transferencia de músculo libre funcional fue descrita por primera vez por Tamai en 1970 en un modelo canino (21). La primera descripción en humanos se realizó en 1976 en China (22).
Las transferencias libres de un músculo funcional se utilizan para restaurar la flexión de codo, la función deltoidea, la extensión de codo y la flexión y extensión de muñeca y dedos (23). La transferencia libre de músculo gracilis funcional es la más utilizada con este fin (23). Otros músculos utilizados son el dorsal ancho, recto femoral, tensor de la fascia lata, gastrocnemio, serrato anterior y colgajo quimérico de músculo grácil y aductor largo (23).
La transferencia de músculo funcional libre tiene las ventajas de permitir una reinervación más rápida respecto a las transferencias nerviosas (debido a la disminución de distancia desde el nervio donante a la placa muscular), de que el músculo ha sido denervado en el momento de la cirugía, siendo el estado de éste no tiempo-dependiente (presenta la posibilidad de ser transferido en cualquier momento desde el origen de la lesión) y la posibilidad de obtener dicho músculo fuera de la zona de traumatismo (24). Por contra, dicho procedimiento quirúrgico es complejo y requiere del uso de técnicas microquirúrgicas por un equipo con experiencia en dicha disciplina.
Transferencias tendinosas
El desarrollo de un plan quirúrgico para realizar transferencias tendinosas precisa identificar aquellos músculos que se encuentran denervados, evaluar el déficit funcional y valorar qué músculos se encuentran disponibles para usarlos como donantes (25). Los tendones donantes deben proceder de músculos con un rango de movimiento similar al receptor y una fuerza mínima M4 (contracción contra resistencia) según la clasificación BMRC (British Medical Research Council)(25,26). Es posible combinar una transferencia tendinosa con la reparación nerviosa, sin embargo, la indicación para estos procedimientos combinados debe ser valorada de forma individual (26).
Prótesis mioeléctricas
Una prótesis mioeléctrica es un tipo de prótesis accionada por contracciones musculares voluntarias. Recientemente se han publicado resultados prometedores con este tipo de tecnología, Sin embargo, las prótesis mioeléctricas de miembro superior sirven, al igual que los trasplantes de mano y otras opciones reconstructivas, como un miembro no dominante, que apoya al miembro dominante (27). Incluso tras la amputación de la mano dominante, los paciente tienden a reasignar la dominancia a la mano restante, usando la reconstruida como una herramienta de soporte (27).
A pesar del gran avance en los últimos años de este tipo de dispositivos, existe una alta tasa de abandono, que puede ser de hasta el 20%. Con el sudor, edema del muñón, ganancia o pérdida ponderal, etc.; los electrodos de superficie pierden contacto, por lo que se degrada el control protésico. Además, existen inconvenientes como la duración de las baterías o el peso de dichos dispositivos (27).
Además de las limitaciones motoras, los pacientes candidatos al uso de prótesis pierden la sensibilidad. Ésta también puede ser dada de forma no invasiva mediante estimulación vibrotáctil y electrotáctil, o de forma invasiva, mediante el uso de electrodos para estimular de forma directa los nervios periféricos (27). Para ello, la prótesis debe incluir sensores propioceptivos que recojan la información sobre la actuación de la prótesis (fuerza, velocidad, etc) y la traslade en parámetros de estimulación (27). Para restaurar la sensibilidad, también se puede hacer reinervación muscular dirigida sensitiva a los nervios cutáneos de la piel de un área. Las prótesis actualmente comercializadas no poseen la habilidad de aportar sensibilidad (27). No obstante, se han realizado de forma exitosa modelos experimentales de prótesis osteointegradas con control motor y capacidad sensitiva (28).
Recientemente se ha publicado el uso de estas prótesis mioeléctricas, previa amputación electiva del miembro no funcional, para mejorar la funcionalidad del paciente (29,30). Se necesitan más estudios sobre este abordaje terapéutico.
TRATAMIENTO REHABILITADOR
La transferencia nerviosa selectiva es una técnica utilizada para restaurar la función motora y sensorial en pacientes con lesiones nerviosas graves (31). La recuperación funcional exitosa depende tanto de la re-inervación periférica como del proceso de re-aprendizaje motor que implica plasticidad cortical (31,32,33).
El procedimiento quirúrgico es una oportunidad para promover la actividad en las áreas de la corteza sensorial-motora de la parte del cuerpo sin movimiento, por esta razón los pacientes no pueden ser tratados con protocolos estándar (31). Los axones de los nervios donantes son la vía a través de la cual se transmite la información funcional necesaria para repoblar los receptores sensoriales y motores de la placa motora, para alcanzar el principal objetivo, el re-aprendizaje cortical para reparar la función periférica perdida (29,31). Este re-aprendizaje de nuevos patrones motores y sensitivos es el objetivo y mayor desafío con este tipo de técnica (31). Es esencial que el paciente comprenda, se comprometa, adhiera e implique en el tratamiento rehabilitador propuesto, así como en su recuperación (31,32, 34).
El tratamiento rehabilitador comprende dos fases: temprana y tardía (34). En la primera etapa durante las tres primeras semanas posteriores a la cirugía se debe evitar las movilizaciones del miembro intervenido. Para evitarlo, se utilizan ortesis y cabestrillos (31,34,35).
La siguiente etapa se inicia desde la cuarta semana hasta el tiempo de re-inervación precoz que puede prolongarse entre 3 y 6 meses, en función de la distancia de la reparación nerviosa hasta la placa motora. Se solicita al paciente que recuerde la función perdida que tenía previamente e imagine que está ejecutando el movimiento deseado (31,34). Se realizan técnicas de rehabilitación como la terapia de espejo, ambas actividades promueven la activación de las áreas corticales motoras y sensoriales denervadas para restablecer su representación a nivel cortical (31,34). Durante esta fase es necesario asegurar el mantenimiento del rango de movilidad articular completo de todo el miembro con cinesiterapia pasiva para prevenir las rigideces articulares (31,34). Igualmente, se inicia el tratamiento de la cicatriz para su flexibilización e incluyen ejercicios propioceptivos y el movimiento activo de las articulaciones libres. Se utilizan técnicas como el biofeedback con EMG, que permite al paciente visualizar la actividad muscular incluso cuando no es apreciable clínicamente (31,34). Los ejercicios se realizan a favor de gravedad solicitando al paciente que haga el movimiento del nervio donante para realizar el movimiento del nervio receptor (p. ej. extensión de codo para abducción de hombro en transferencia de nervio radial a axilar). De forma paralela se promueve la re-educación funcional para incentivar el uso e integración gradual de la extremidad operada (31,34,35,36).
La etapa de fortalecimiento busca lograr movimiento contra gravedad. Se puede utilizar EMG-biofeedback y estimulación eléctrica para llegar a un determinado umbral de contracción muscular que estimule al músculo comprometido. Se entrena la activación muscular con y sin EMG biofeedback hasta que la fuerza muscular sea suficiente para superar la gravedad o resistencia de los músculos antagónicos y produzca actividad concomitante de los nervios donante y receptor (31,34).
En la última etapa de la fase tardía se busca incrementar el número de unidades motoras nuevas, así como el fortalecimiento de las unidades motoras maduras. En este estadio se utiliza la estimulación eléctrica neuromuscular, los ejercicios son realizados contra gravedad, se introduce resistencia progresivamente a medida que el paciente mejora y tareas cada vez más complejas que incluyan mayor fuerza y precisión. El enfoque en esta fase es reaprender el movimiento original del nervio receptor y permitir el movimiento independiente de ambos grupos musculares (31,34).
Se pautan ejercicios terapéuticos para realizar en el domicilio y se realizan tareas para el reentrenamiento gradual de las actividades básicas de la vida diaria. Pueden quedar secuelas funcionales sensitivas y/o motrices que se deben tener en cuenta para optimizar la reinserción laboral y social del paciente (35,36).
La valoración y el abordaje precoz de la sensibilidad puede reducir el dolor y evitar complicaciones no deseadas como una distrofia simpática refleja. El tratamiento se basa en técnicas de desensibilización, reeducación de funciones discriminatorias y de sensibilidades simples y complejas, aumentando los estímulos de forma progresiva según la evolución clínica (36).
Las fases de la rehabilitación después de una reparación primaria o con injertos del nervio dañado pasa por etapas similares, sin ser necesaria la reeducación del paciente, al eliminar la variable nervio donante-nervio receptor.
VISIÓN MULTIDISCIPLINAR
Para optimizar todo el espectro de opciones diagnósticas y terapéuticas anteriormente expuestas en lesiones de nervio periférico, es fundamental el abordaje multidisciplinar del paciente. Las pruebas de imagen y de neurofisiología son imprescindibles para el diagnóstico y planificación prequirúrgica de las lesiones. Durante la cirugía, el trabajo entre cirujano y neurofisiólogo facilita la toma de decisiones para optimizar el tratamiento. Por último, la rehabilitación precoz y el manejo del dolor son esenciales para conseguir el mejor resultado posible.
CONCLUSIONES
Las lesiones del plexo braquial y nervio periférico son complejas y conllevan un déficit funcional. Sin embargo, existe un amplio espectro de tratamientos quirúrgicos (injertos nerviosos, transferencias nerviosas, tendinosas y musculares, etc.) que mejoran la calidad de vida del paciente. Valorar a estos pacientes lo antes posible en unidades con un abordaje multidisciplinar es crítico para optimizar la recuperación funcional de estos pacientes.
BIBLIOGRAFÍA
- Ichihara S, Inada Y, Nakamura T. Artificial nerve tubes and their application for repair of peripheral nerve injury: an update of current concepts. Injury. 2008; 39 (Suppl 4): 29-39.
- Neligan PC. Plastic Surgery. Oxford : Elsevier; 2017. 4680 p.
- Kim DH, Murovic JA, Tiel RL, Kline DG. Mechanisms of injury in operative brachial plexus lesions. Neurosurg Focus [Internet]. 2004 May 15 [cited 2021 Sep 27]; 16(5). Available from: https://pubmed.ncbi.nlm.nih.gov/15174822/
- Althagafi A, Nadi M. Acute Nerve Injury. En: StatPearls [Internet]. StatPearls Publishing; 2021.
- Warade AC, Jha AK, Pattankar S, Desai K. Radiation-induced brachial plexus neuropathy: a review. Neurol India. 2019; 67(7): 47-52.
- Sunderland S. A classification of peripheral nerve injuries producing loss of function. Brain. 1951; 74(4): 491-516.
- Menorca RMG, Fussell TS, Elfar JC. Nerve Physiology [Internet]. Hand Clinics. 2013; 29: 317-330. Available from: http://dx.doi.org/10.1016/j.hcl.2013.04.002
- Wu P, Chawla A, Spinner RJ et al. Key changes in denervated muscles and their impact on regeneration and reinnervation. Neural Regen Res. 2014; 9(20): 1796-1809.
- Gagliardo A, Toia F, Maggì F, Mariolo AV, Cillino M, Moschella F. Clinical neurophysiology and imaging of nerve injuries: preoperative diagnostic work-up and postoperative monitoring. Plast Aesthet Res. 2015; 2: 149-155.
- Mallik A, Weir AI. Nerve conduction studies: essentials and pitfalls in practice. J Neurol Neurosurg Psychiatry. 2005;76(suppl 2): ii23-ii31.
- Crum BA, Strommen JA, Stucky SC. Peripheral nerve stimulation and monitoring during operative procedures [Internet]. Muscle Nerve. 2007; 35: 159-170. Available from: http://dx.doi.org/10.1002/mus.20707
- Agarwal A, Chandra A, Jaipal U et al. Can imaging be the new yardstick for diagnosing peripheral neuropathy?: a comparison between high resolution ultrasound and MR neurography with an approach to diagnosis [Internet]. Insights Imaging. 2019; 10(1): 104. Available from: http://dx.doi.org/10.1186/s13244-019-0787-6
- Zhu J, Liu F, Li D, Shao J, Hu B. Preliminary study of the types of traumatic peripheral nerve injuries by ultrasound [Internet]. Eur Radiol. 2011; 21(5): 1097-1101. Available from: http://dx.doi.org/10.1007/s00330-010-1992-3
- Kollmer J, Bendszus M, Pham M. MR Neurography: Diagnostic Imaging in the PNS [Internet] [cited 2021 Sep 27].Clin Neuroradiol. 2015; 25(Suppl 2): 283-289. Available from: https://pubmed.ncbi.nlm.nih.gov/26070607/
- Wilson Z. Ray SEM. Management of nerve gaps: autografts, allografts, nerve transfers, and end-to-side neurorrhaphy. Exp Neurol. 2010; 223(1): 77-85.
- Terzis J, Faibisoff B, Williams B. The nerve gap: suture under tension vs. graft. Plast Reconstr Surg. 1975; 56(2): 166-170.
- Brophy RH, Wolfe SW. Planning brachial plexus surgery: treatment options and priorities. [Internet] [cited 2021 Sep 27]. Hand Clin. 2005; 21(1): 47-54. Available from: https://pubmed.ncbi.nlm.nih.gov/15668065/
- Martins RS, Barbosa RA, Siqueira MG et al. Morbidity following sural nerve harvesting: a prospective study. [Internet] [cited 2021 Sep 27]. Clin Neurol Neurosurg. 2012; 114(8): 1149-1152. Available from: https://pubmed.ncbi.nlm.nih.gov/22425460/
- Isaacs J, Browne T. Overcoming short gaps in peripheral nerve repair: conduits and human acellular nerve allograft. [Internet] [cited 2021 Sep 27]. Hand. 2014; 9(2): 131-137. Available from: https://pubmed.ncbi.nlm.nih.gov/24839412/
- Oberlin C, Béal D, Leechavengvongs S, Salon A, Dauge MC, Sarcy JJ. Nerve transfer to biceps muscle using a part of ulnar nerve for C5-C6 avulsion of the brachial plexus: anatomical study and report of four cases. [Internet] [cited 2021 Sep 27]. J Hand Surg Am .1994; 19(2): 232-237. Available from: https://pubmed.ncbi.nlm.nih.gov/8201186/
- Tamai S, Komatsu S, Sakamoto H, Sano S, Sasauchi N. Free muscle transplants in dogs, with microsurgical neurovascular anastomoses. [Internet] [cited 2021 Sep 27]. Plast Reconstr Surg. 1970; 46(3): 219-225. Available from: https://pubmed.ncbi.nlm.nih.gov/4247301/
- Free muscle transplantation by microsurgical neurovascular anastomoses: report of a case. [Internet] [cited 2021 Sep 27]. Chin Med J. 1976; 2(1): 47-50. Available from: https://pubmed.ncbi.nlm.nih.gov/816616/
- Seal A, Stevanovic M. Free functional muscle transfer for the upper extremity. [Internet] [cited 2021 Sep 27]. Clin Plast Surg. 2011; 38(4): 561-575. Available from: https://pubmed.ncbi.nlm.nih.gov/22032586/
- Maldonado AA, Kircher MF, Spinner RJ, Bishop AT, Shin AY. Free functioning gracilis muscle transfer versus intercostal nerve transfer to musculocutaneous nerve for restoration of elbow flexion after traumatic adult brachial pan-plexus injury. [Internet] [cited 2021 Sep 27]. Plast Reconstr Surg. 2016; 138(3): 483e-488e. Available from: https://pubmed.ncbi.nlm.nih.gov/27556623/
- Ratner JA, Peljovich A, Kozin SH. Update on tendon transfers for peripheral nerve injuries. [Internet] [cited 2021 Sep 27]. J Hand Surg Am. 2010; 35(8): 1371-1381. Available from: https://pubmed.ncbi.nlm.nih.gov/20684937/
- Loewenstein SN, Adkinson JM. Tendon transfers for peripheral nerve palsies. Clin Plast Surg. 2019; 46(3): 307-315.
- Aman M, Sporer ME, Gstoettner C et al. Bionic hand as artificial organ: current status and future perspectives. [Internet] [cited 2021 Sep 27]. Artif Organs. 2019; 43(2): 109-118. Available from: https://pubmed.ncbi.nlm.nih.gov/30653695/
- Ortíz-Catalán M, Mastinu E, Sassu P, Aszmann O, Brånemark R. Self-contained neuromusculoskeletal arm prostheses. [Internet] [cited 2021 Sep 27]. N Engl J Med. 2020; 382(18): 1732-1738 . Available from: https://pubmed.ncbi.nlm.nih.gov/32348644/
- Aszmann OC, Roche AD, Salminger S et al. Bionic reconstruction to restore hand function after brachial plexus injury: a case series of three patients. Lancet. 2015; 385(9983): 2183-2189.
- Aszmann OC, Vujaklija I, Roche AD et al. Elective amputation and bionic substitution restore functional hand use after critical soft tissue injuries. Sci Rep. 2016; 6: 34960.
- Sturma A, Hruby LA, Farina D, Aszmann OC. Structured motor rehabilitation after selective nerve transfers. [Internet]. J Vis Exp. 2019; 150. Available from: http://dx.doi.org/10.3791/59840
- Petronić I, Marsavelski A, Nikolić G, Cirović D. [Postoperative rehabilitation in patients with peripheral nerve lesions]. Acta Chir Iugosl. 2003; 50(1): 83-86.
- Tuturov AO. The role of peripheral nerve surgery in a tissue reinnervation [Internet]. Chin Neurosurg J. 2019; 5: 5. Available from: http://dx.doi.org/10.1186/s41016-019-0151-1
- Novak CB, von der Heyde RL. Rehabilitation of the upper extremity following nerve and tendon reconstruction: when and how. Semin Plast Surg. 2015; 29(1): 73-80.
- Manual SERMEF de rehabilitación y medicina física. Buenos Aires [etc]: Panamericana, 2019. 857 p.
- Noël L, Liverneaux P. Tratamiento y rehabilitación de las lesiones nerviosas periféricas. EMC – Kinesiterapia – Medicina Física. 2014; 35(2): 1-9.
- Tien Y, Couceiro J, Sánchez-Crespo M (eds). The handbook of hand emergencies. Newcastle upon Tyne: Cambridge Scholars Publisher, 2020. 440 p.
DECLARACIÓN DE TRANSPARENCIA
Los autores/as de este artículo declaran no tener ningún tipo de conflicto de intereses respecto a lo expuesto en el presente trabajo.
Andrés A. Maldonado
Unidad de Nervio Periférico y Plexo Braquial. Servicio de Cirugía Plástica
Hospital Universitario de Getafe. Carretera de Toledo Km 12.5 · 28905 Getafe, Madrid
Tlf.:+34 91 547 03 18 | E-Mail: mail@andresmaldonado.es
Año 2021 · número 138 (03) · páginas 270 a 281
Enviado: 23.06.21
Revisado: 28.06.21
Aceptado: 12.07.21


