Resumen
Desde la primera descripción de un caso de lo que hoy llamamos colitis ulcerosa, a finales del siglo XVIII, el conocimiento acerca de la Enfermedad Inflamatoria Intestinal (EII) ha cambiado radicalmente. De utilizar tuberculostáticos en la enfermedad de Crohn e irrigaciones rectales en la colitis ulcerosa, a diseñar medicamentos dirigidos a dianas moleculares específicas, nuestras armas farmacológicas, endoscópicas y quirúrgicas han evolucionado y nos han permitido tratar las formas más graves y desafiantes, previamente consideradas incluso letales. Gran parte de nuestro éxito controlando estas enfermedades se debe a una mejor comprensión de la inflamación crónica y las complejas alteraciones inmunológicas subyacentes; y quizá, uno de los mayores logros en la historia de la E.I.I. haya sido la aparición de los fármacos biológicos. Además, el desarrollo de técnicas que nos permiten detectar la actividad biológica en sangre y heces, las distintas posibilidades de detectar lesiones premalignas o tratar complicaciones de una forma mínimamente invasiva, así como las nuevas estrategias quirúrgicas, permiten individualizar cada día más el tratamiento y seguimiento y mejorar la calidad de vida de nuestros pacientes. Sin embargo, aún quedan muchos retos diagnósticos y terapéuticos en Enfermedad Inflamatoria Intestinal. Revisamos de forma sintética el manejo actual en enfermedad de Crohn, colitis ulcerosa y colitis indeterminada en 2022.
Abstract
Since the first report of a disease that today we call ulcerative colitis at the end of the 18th century, the knowledge in Inflammatory Bowel Disease (IBD) has radically changed. From using tuberculostatics to treat Crohn’s disease and rectal irrigations in ulcerative colitis, to developing specific drugs targeted to specific molecules, our pharmacological, endoscopic, and surgical tools have evolved and allowed us to treat its severe and challenging variants, traditionally considered to be fatal. Much of the credit of our success controlling these conditions comes from a better understanding of the complex underlying immune alterations and permanent inflammation that cause them; and maybe, one of the greatest achievements in IBD has been the design of the so-called biologic therapy. Moreover, the development of clinical tests to detect inflammatory activity in blood and stool, the apparition of new ways of detecting premalignant lesions and minimal invasive therapy for complications, and new surgical strategies have let us to individualize treatment and monitoring the disease and improve life quality in our patients. However, we still find lots of diagnostic and treatment challenges in IBD in our daily practice, today. We present our review of the management of Crohn’s disease, ulcerative colitis, and indeterminate colitis in 2022.
Palabras clave: Enfermedad Inflamatoria Intestinal; Colitis ulcerosa; Enfermedad de Crohn; Tratamiento.
Keywords: Inflammatory Bowel; Disease Ulcerative colitis; Crohn’s disease; Treatment.
INTRODUCCIÓN
La Enfermedad Inflamatoria Intestinal (E.I.I.), comprende dos entidades clínicas diferenciadas: la colitis ulcerosa y la enfermedad de Crohn. Ambos trastornos parecen tener una base genética compleja en la que están implicados distintos fenómenos moleculares, del complejo mayor de histocompatibilidad y epigenéticos. Sin embargo, la E.I.I. parece necesitar otros elementos para desarrollarse fenotípicamente, entre los que destacan factores tóxicos, dietéticos, infecciosos e incluso farmacológicos. En los últimos años, se intenta, dentro del marco de una susceptibilidad genética no siempre presente, poner en común estos factores ambientales con una alteración en el sistema inmunológico y de la respuesta inflamatoria. La microbiota luminal, que presenta una densidad especial en el íleon y el colon, y el mesenterio, cada vez se plantea más como partícipe esencial en la aparición y perpetuación de estas enfermedades inflamatorias mediadas por la inmunidad.
Tradicionalmente, una de las características diferenciales entre ambos trastornos ha sido su afinidad por la zona del tracto digestivo a la que afectan y la profundidad que alcanzan en la pared intestinal. La colitis ulcerosa se origina en el recto, y su extensión es continua con un ‘tope’ proximal, el ciego. Afecta exclusivamente la capa mucosa de la pared colónica. La enfermedad de Crohn puede afectar, de una forma que podríamos definir como ‘caprichosa’, a cualquier tramo del punto digestivo desde la boca hasta el ano, aunque con una predilección por el íleon terminal, el colon, o ambos. A diferencia de la colitis ulcerosa la enfermedad de Crohn puede extenderse a través de todas las capas de la pared intestinal dando lugar a ulceraciones o fístulas, lo cual explica sus distintas formas clínicas: inflamatoria, estenosante y penetrante. Estos comportamientos fenotípicos no han de entenderse como compartimentos estancos; en la mayoría de los pacientes el componente inflamatorio y el fibroso tienden a coexistir. Además, no es infrecuente la aparición de patología fistulosa compleja a nivel perianal, que va a condicionar factores pronósticos y terapéuticos.
ABORDAJE DIAGNÓSTICO
Como consecuencia de esta idiosincrasia anatómica e histológica, los síntomas atribuidos a ambas enfermedades van a diferir. En la colitis ulcerosa, la clínica predominante es la de hemorragia digestiva baja asociada a la diarrea y el síndrome rectal con urgencia y tenesmo. El dolor abdominal crónico y la diarrea líquida nos hacen sospechar en una enfermedad de Crohn, especialmente de localización ileal y en su patrón de predominio inflamatorio, si bien puede presentarse de forma suboclusiva o mediante íleo obstructivo completo si se genera una estenosis fibrótica. En sus formas penetrantes, el Crohn puede originar fístulas a otras vísceras huecas (como vejiga o vagina), hacia músculos o a la piel, así como formar abscesos intraabdominales. La clínica del Crohn dependerá en gran parte por el tramo afecto. [1]
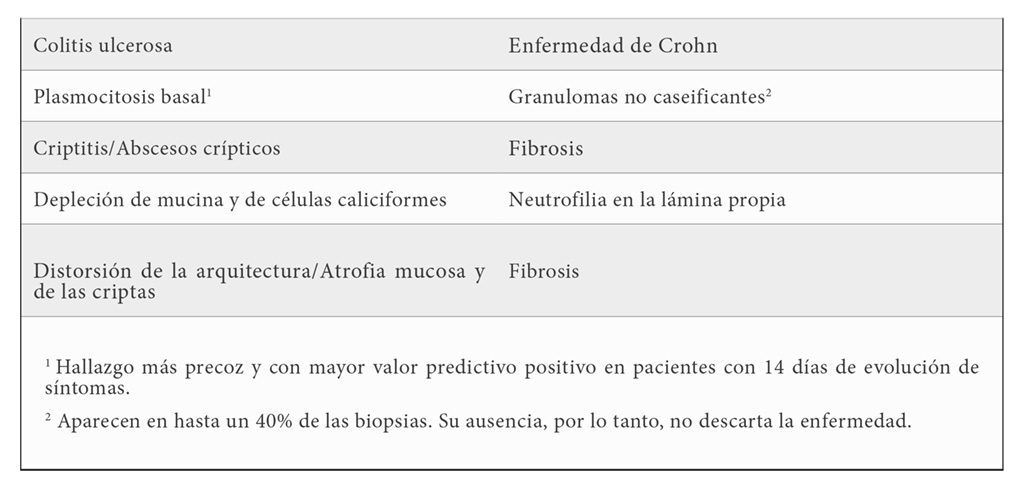
Con respecto a las alteraciones anatomopatológicas de la E.I.I., los cambios que se presentan al microscopio no son patognomónicos en ninguna de sus dos vertientes, por lo que nos deben plantear el diagnóstico diferencial con otras enfermedades infecciosas, granulomatosas, colágenas, isquémicas o incluso neoplásicas. Los aspectos histológicos diferenciales descritos entre colitis ulcerosa y enfermedad de Crohn se recogen en la tabla 1. [2]
Ante la sospecha de E.I.I., es fundamental realizar una adecuada y exhaustiva anamnesis. Además de lo obvio que supone el preguntar la edad del paciente (históricamente, se han descrito dos picos de edad de incidencia – el primero, entre los 15 y 30 años de edad, y un segundo, hacia la quinta-sexta década de la vida), interrogar acerca de hábitos diarios (tabaquismo) o antecedentes familiares, puede ayudarnos a completar una buena historia clínica y orientar el diagnóstico. No obstante, como se podía inferir del párrafo anterior, desvelar estos trastornos como causa de los síntomas se va a basar en datos clínico-analíticos, endoscópicos e histológicos para ambas enfermedades, y, en el caso de la enfermedad de Crohn, en las pruebas de imagen (que, en la colitis ulcerosa, se suelen reservar para descartar sus complicaciones más severas). Herramientas como la determinación de proteína C reactiva o calprotectina fecal (marcadores biológicos), la ileocolonoscopia con toma de biopsias o la cápsula endoscópica y la enterorresonancia magnética o la tomografía axial computarizada, van a ser de interés para el diagnóstico, seguimiento y monitorización de respuesta y/o recaída ante el tratamiento médico o quirúrgico. En los últimos años, se han creado y estandarizado guías, protocolos y escalas que nos indican cuándo intervenir en el manejo de nuestros pacientes, en función de los resultados de estas pruebas. [3]
Aun así, se estima que, entre un diez y un quince por ciento de los pacientes en los que sospechamos una E.I.I., no vamos a poder decantarnos por una de las dos opciones existentes. La denominación ‘colitis indeterminada’, surge a finales de los años 70 para aquellos pacientes en los que en la pieza quirúrgica de colectomía no era posible esclarecer si se trataba de una colitis ulcerosa o una enfermedad de Crohn, ya que, en estos especímenes, el colon presentaba un aspecto ulceroso profundo y con afectación transmural. Posteriormente, ha aparecido el concepto ‘colitis no clasificada’, en la que no logramos concluir un diagnóstico a pesar de haber realizado un estudio clínico, endoscópico, radiológico e histológico adecuado. Los distintos autores se debaten entre si se trata de una tercera entidad, o si bien es una forma de colitis ulcerosa o enfermedad de Crohn que se desenmascarará en el seguimiento a largo plazo. Actualmente, la tendencia terapéutica en estos casos es hacia un tratamiento similar al de la colitis ulcerosa. [4]
ABORDAJE TERAPÉUTICO
Aunque los esfuerzos principales de clínicos, endoscopistas, radiólogos y patólogos se dirijan a establecer las características que distinguen ambas enfermedades, también es importante señalar lo que las une. La base inmunológica a la que obedecen estos trastornos nos ha ayudado a poder entender su historia natural, así como su comportamiento clínico y tisular, pero también a comprender las afecciones en otros órganos con las que suelen coexistir (las denominadas manifestaciones extraintestinales de la E.I.I.). Pero, sin duda, la importancia del entendimiento del trastorno inmunológico en el que nace la E.I.I. radica en la revolución que ha supuesto en su tratamiento. El desarrollo inicial de fármacos inmunomoduladores ha permitido limitar la duración del uso de corticoides, fármacos potentes pero cargados de efectos adversos. Pero quizá sea más llamativo el impacto del uso de fármacos biológicos, los anticuerpos monoclonales, cuyo uso se practica desde hace ya más de dos décadas, lo cual ha permitido de una forma segura y cómoda controlar las formas más refractarias o recidivantes. Actualmente, gran parte de los esfuerzos de investigación se dirigen a generar nuevos medicamentos que se puedan emplear de una forma eficaz y cómoda para los pacientes.
Una característica común a muchas enfermedades con base inmunológica, y, especialmente, en la E.I.I., es el curso en brotes, definidos como períodos sintomáticos autolimitados en el tiempo, si bien, a nivel histológico, se han evidenciado cambios crónicos subyacentes en ambas enfermedades y cada vez se le da más importancia al ‘daño crónico’ que asienta de forma residual tras cada brote, especialmente en la enfermedad de Crohn. Lo que parece claro es que, dado que el espectro clínico de la enfermedad puede variar entre sintomatología leve y manejable desde el domicilio y una situación de riesgo vital, debemos disponer de las armas terapéuticas suficientes y adecuadas para cada escenario. Es por ello, por lo que se han creado distintas escalas de actividad y gravedad para ambas enfermedades, que incluyen datos clínicos, analíticos y, en ocasiones, endoscópicos, que nos van a ayudar a establecer la severidad del brote.
Con estos datos, y teniendo en cuenta la localización y el comportamiento de la enfermedad, las guías disponibles y la evidencia que las respaldan nos indican cómo manejar los fármacos y las técnicas endoscópicas y quirúrgicas disponibles para conseguir una adecuada remisión clínica y mantener sin nuevos episodios al paciente y así mejorar su calidad de vida.
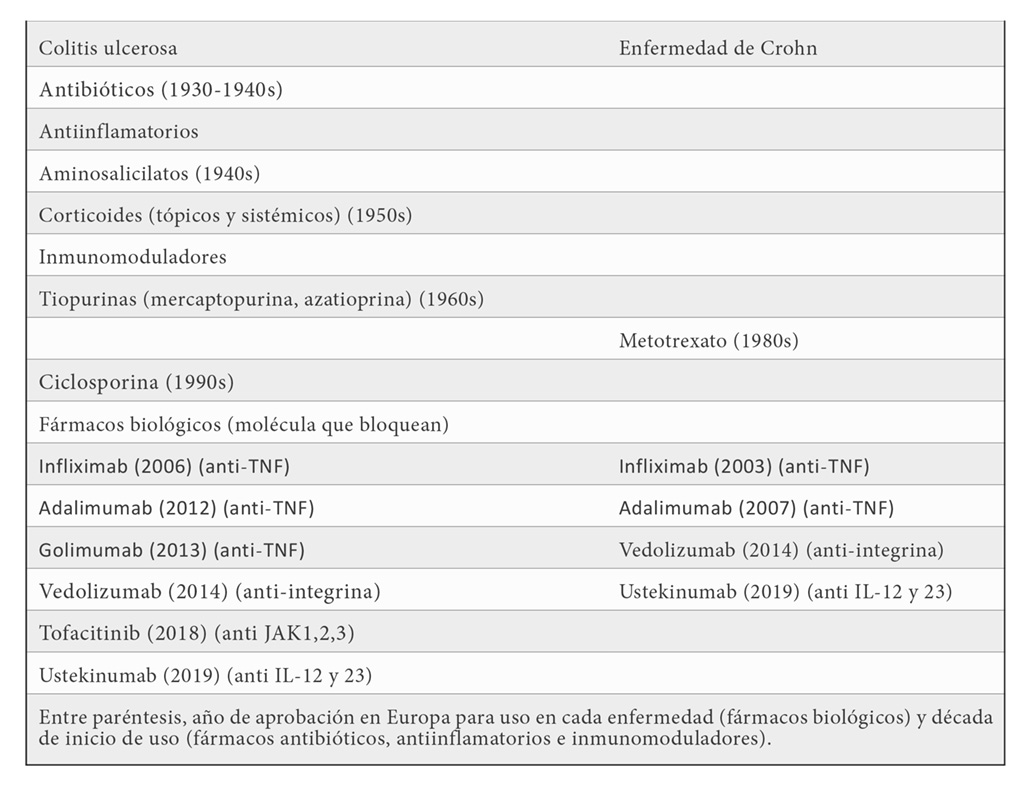
En el caso de la colitis ulcerosa, tras haber realizado un estudio exhaustivo de la anatomía afectada, debemos considerar la localización de la enfermedad y la gravedad del brote. En el caso de encontrarnos formas leves y moderadas, será de elección la administración de aminosalicilatos orales y en su forma rectal (lo cual puede hacerse de forma exclusiva en el caso de la proctitis). Estos fármacos son eficaces no sólo para inducir la remisión en el brote, sino también para el mantenimiento. En casos leves y moderados que no responden a estos fármacos, ha de pensarse en administrar corticoides sistémicos de liberación colónica (beclometasona) o corticoides sistémicos convencionales (como, por ejemplo, la prednisona o la metilprednisolona). El brote grave supone ingreso hospitalario, y la inducción de la remisión debe iniciarse con corticoides sistémicos, si bien esto no implica que se prescinda del tratamiento tópico, muy eficaz para el control de la clínica rectal. En estos pacientes, es esencial el soporte nutricional, la tromboprofilaxis y la valoración conjunta con el cirujano de forma precoz. Si, aun así, no conseguimos inducir una remisión (la llamada corticorrefractariedad), lo cual debemos pensar entre el tercer y el séptimo día de tratamiento, existen otros fármacos con otras dianas terapéuticas capaces de inducir la remisión clínica; ciclosporina, los fármacos anti-TNF (infliximab, adalimumab y golimumab), fármacos anti-integrina (vedolizumab), inhibidores de las interleucinas 12 y 23 (ustekinumab) y las llamadas pequeñas moléculas (tofacitinib, inhibidor de proteínas JAK 1, 2 y 3) (tabla 2).
En algunos casos, en función de la evolución clínica y el contexto del paciente y sus comorbilidades, se puede valorar la cirugía. [5,6]
Una vez logrado el control del brote y la remisión clínica, debemos encargarnos de que ésta se mantenga. En caso de haber logrado controlar la clínica con los aminosalicilatos, se mantienen estos a largo plazo. Si hemos inducido la remisión con cualquiera de los otros fármacos, salvo los corticoides, parece lógico continuar con los mismos, ya que también son capaces de mantener a nuestros pacientes sin brotes.
Aunque nos hemos situado en un escenario de ‘no respuesta’ a la corticoterapia, es habitual que los pacientes respondan al tratamiento esteroideo. De hecho, existe un subgrupo de pacientes en los que la suspensión o la reducción de dosis provoca una reaparición de los síntomas; estamos dentro del escenario denominado corticodependencia. No nos enfrentamos a un problema de respuesta a corticoides, sino a que no somos capaces de mantener a nuestro paciente asintomático sin tener que recibirlos. Los fármacos inmunomoduladores (azatioprina, mercaptopurina o metotrexato) ayudan a disminuir las necesidades de corticoides, lo cual les confiere su principal indicación. Estos medicamentos son capaces de inducir remisión, pero lo hacen de una forma lenta, por lo que actualmente no se recomiendan para la inducción de remisión. Sin embargo, sus aplicaciones se están expandiendo, ya que, hoy, sabemos que su asociación a algunos fármacos anti-TNF (especialmente, el infliximab) protege de la generación de anticuerpos, y, por ende, del fracaso a dicha terapia (el llamado ‘fallo secundario’). Los fármacos biológicos también pueden utilizarse para evitar la corticodependencia.
En el brote de enfermedad de Crohn, también será relevante conocer el segmento del tracto digestivo afecto y la gravedad medida por los índices de actividad de la enfermedad. Sin embargo, el factor que más va a determinar el arma terapéutica a elegir va a ser el patrón de afectación que predomine (como ya hemos mencionado, estos pueden coexistir). Las formas inflamatorias de enfermedad de Crohn se van a tratar, en función de la gravedad, con corticoides de acción local (especialmente, budesónida en las formas leves o moderadas, con afectación de íleon y/o colon ascendente) o corticoides de forma sistémica (en las formas más severas). De nuevo, en casos corticorefractarios, se debe realizar la inducción con anticuerpos monoclonales anti-TNF, ustekinumab o vedolizumab. Al igual que en la colitis ulcerosa, la inducción no debe intentarse con fármacos inmunomoduladores exclusivamente, y estos deben asociarse con el infliximab para evitar el fallo secundario. La corticodependencia de la enfermedad de Crohn se trata de forma análoga a las de la colitis ulcerosa.
En la enfermedad de Crohn no es raro que los patrones estenosantes y penetrantes, tanto al debut como a largo plazo, hagan necesario recurrir a la cirugía. Las estenosis en la enfermedad de Crohn suelen tener un componente inflamatorio y fibrótico. Si bien lo lógico es pensar que las primeras responderán a un tratamiento médico y las segundas a uno endoscópico o quirúrgico, no debemos dejar ninguno de los dos de lado. Las estenosis simples (no muy numerosas, cortas, no anguladas o bien asociadas a anastomosis quirúrgicas) suelen manejarse con dilataciones endoscópicas, si bien las complejas, que no reúnen las características previas o bien se asocian a otro tipo de complicaciones (fístulas, abscesos, bezoares…) suelen requerir la cirugía.
La forma penetrante de la enfermedad de Crohn puede tener un tratamiento conservador, como en el caso de fístulas entero-entéricas asintomáticas. Sin embargo, cuando se comunica el tracto gastrointestinal con otros órganos (vísceras huecas, músculos), el tratamiento médico debe acompañarse de una solución quirúrgica. Los abscesos generados en el seno de un brote penetrante pueden manejarse con antibioterapia (exclusiva si son pequeños e inaccesibles), acompañado de drenaje percutáneo cuando la anatomía lo favorece, o cirugía si la localización no lo permite y presentan un tamaño considerable que impida el manejo exclusivamente médico.
La enfermedad perianal compleja se ha convertido en el escenario más desafiante actualmente para el clínico dedicado a la E.I.I. En las formas simples y asintomáticas puede recomendarse la actitud expectante o incluso la fistulectomía. Para fístulas complejas, el tratamiento de elección es combinado: cirugía con una exploración bajo anestesia en la que se proceda a la limpieza de los trayectos fistulosos y la colocación de sedales (que evitaran la aparición de nuevos abscesos) junto con la administración de un fármaco anti-TNF (preferiblemente infliximab). En las formas que no acaban de curar a pesar de este tratamiento combinado, puede ser útil la terapia la terapia avanzada con administración intralesional de células madre de tejido adiposo. [7,8]
En el año 2022, quedan aún muchos interrogantes y existen diversas posiciones con respecto al manejo óptimo de la E.I.I. A pesar de que el manejo inicial en sus formas más comunes se sigue realizando con fármacos conocidos desde hace muchos años, el arsenal farmacológico, endoscópico, intervencionista y quirúrgico es cada vez mayor, con la aparición nuevas armas terapéuticas que señalizan dianas farmacológicas más específicas y técnicas menos invasivas, pero más eficaces, que nos ayudan en las formas más resistentes o complejas. Las terapias avanzadas incluidas las células madre y la terapia génica pueden ofrecer un futuro esperanzador para el tratamiento de la EII.
BIBLIOGRAFÍA
- Actis, Giovanni Clemente, et al. “History of Inflammatory Bowel Diseases.” Journal of Clinical Medicine, vol. 8, no. 11, 14 Nov. 2019, www.ncbi.nlm.nih.gov/pmc/articles/PMC6912289/, 10.3390/jcm8111970. Accessed 11 Apr. 2020.
- Sands BE. From symptom to diagnosis: clinical distinctions among various forms of intestinal inflammation. Gastroenterology. 2004 May;126(6):1518–32.
- Yr, Yu, and Rodriguez Jr. “Clinical Presentation of Crohn’s, Ulcerative Colitis, and Indeterminate Colitis: Symptoms, Extraintestinal Manifestations, and Disease Phenotypes.” Seminars in Pediatric Surgery, 1 Dec. 2017, pubmed.ncbi.nlm.nih.gov/29126502/.
- Mitchell, P. J., et al. “Indeterminate Colitis.” Techniques in Coloproctology, vol. 11, no. 2, 1 June 2007, pp. 91–96, pubmed.ncbi.nlm.nih.gov/17510748/, 10.1007/s10151-007-0337-y. Accessed 20 Mar. 2022.
- Raine, Tim, et al. “ECCO Guidelines on Therapeutics in Ulcerative Colitis: Medical Treatment.” Journal of Crohn’s and Colitis, vol. 16, no. 1, 12 Oct. 2021, pp. 2–17, 10.1093/ecco-jcc/jjab178. Accessed 20 Mar. 2022.
- Spinelli, Antonino, et al. “ECCO Guidelines on Therapeutics in Ulcerative Colitis: Surgical Treatment.” Journal of Crohn’s and Colitis, vol. 16, no. 2, 17 Oct. 2021, pp. 179–189, 10.1093/ecco-jcc/jjab177. Accessed 20 Mar. 2022.
- Torres, Joana, et al. “ECCO Guidelines on Therapeutics in Crohn’s Disease: Medical Treatment.” Journal of Crohn’s and Colitis, vol. 14, no. 1, 11 Nov. 2019, pp. 4–22, 10.1093/ecco-jcc/jjz180.
- Adamina, Michel, et al. “ECCO Guidelines on Therapeutics in Crohn’s Disease: Surgical Treatment.” Journal of Crohn’s & Colitis, vol. 14, no. 2, 10 Feb. 2020, pp. 155–168, www.ncbi.nlm.nih.gov/pubmed/31742338, 10.1093/ecco-jcc/jjz187. Accessed 18 May 2020.
DECLARACIÓN DE TRANSPARENCIA
Los autores/as de este artículo declaran no tener ningún tipo de conflicto de intereses respecto a lo expuesto en el presente trabajo.
Carlos Taxonera
Servicio Aparato Digestivo, Hospital Clínico San Carlos
Calle del Prof Martín Lagos, s/n · 28040 Madrid, España
Tlf.: +34 648 116 249 | E-Mail: carlos.taxonera@salud.madrid.org
Año 2021 · número 139 (01) · páginas 31 a 36
Enviado: 31.03.21
Revisado: 30.03.22
Aceptado: 02.04.22


