Resumen
Presentamos las imágenes correspondientes a un PET-TC hepático mediante un estudio multitrazador de un paciente portador de virus de hepatitis C crónico, en lista de espera para trasplante y con lesión sospechosa de hepatocarcinoma.o
Abstract
We present the images corresponding to a hepatic PET-CT scan through a multitraceal study of a patient with chronic hepatitis C virus, on the waiting list for transplantation and with a lesion suspected of hepatocarcinoma.
Palabras clave: PET-TC; Hepatocarcinoma; 18F-FDG; 18F-FCH.
Keywords: PET-TC; Hepatocellular carcinoma; 18F-FDG; 18F-FCH.
INTRODUCCIÓN
El fundamento de la imagen en Medicina Nuclear (MN) está constituido por la alteración del proceso que subyace en la enfermedad y que ponemos de manifiesto mediante las diferentes exploraciones. La diversidad de radiofármacos (RF) disponibles constituye el verdadero arsenal para la caracterización de lesiones estructurales, atendiendo precisamente a sus peculiaridades metabólicas y bioquímicas. El objetivo del presente trabajo es mostrar un estudio de tomografía por emisión de positrones-tomografía computarizada (PET-TC) multitrazador ([18F]-FDG y [18F]-FCH) en un caso de hepatocarcinoma y discutir, en términos metabólicos y bioquímicos, el diferente comportamiento de los radiofármacos utilizados.
CASO CLÍNICO
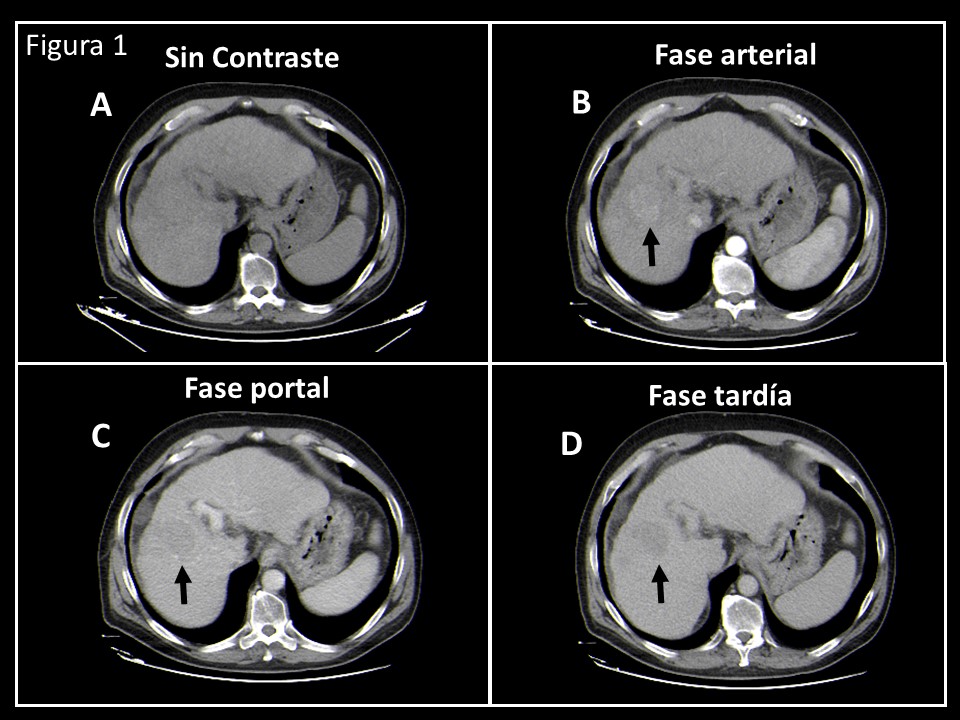
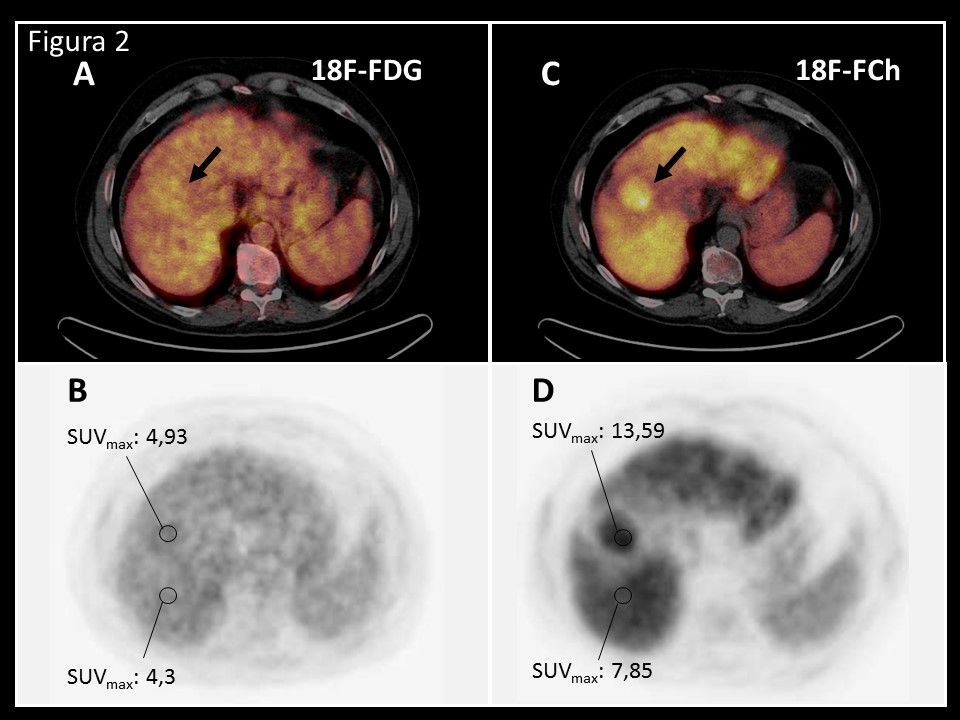
Paciente varón de 52 años portador de virus de hepatitis C y cuadro clínico de hepatopatía crónica con hipertensión portal. En una exploración TC realizada como parte de protocolo para inclusión en lista de espera para trasplante, se descubre una lesión nodular de 34 x 42 mm en el segmento IV del hígado y sospechoso de hepatocarcinoma por su patrón de vascularización en las diferentes fases (figura 1). Es remitido al servicio de MN con la finalidad de descartar enfermedad a distancia mediante la realización de un PET-TC con fluorodesoxiglucosa marcada con Flúor-18 ([18F]-FDG). En dicha exploración no se observa ningún depósito en segmento IV, aunque si se aprecia una ligera irregularidad en la distribución del RF intraparenquimatoso (figura 2A y B). Ante la sospecha previa de hepatocarcinoma y el comportamiento de la [18F]-FDG, que sugiere corresponder en una lesión con alto grado de diferenciación, se recomienda completar el estudio con fluorocolina marcada con Flúor-18 ([18F]-FCH). En la exploración con [18F]-FCH (figura 2C y D) se visualiza un foco hipercaptante que corresponde a la lesión visualizada en el TC inicial. Esta lesión presenta una mayor avidez por la [18F]-FCH, mostrando un mayor contraste con el tejido circundante y unos valores de SUV significativamente mayor que los observados con la [18F]-FDG.
DISCUSIÓN
La diferente distribución, y en consecuencia la semiología, de los diferentes radiofármacos en los estudios PET-TC posee una base metabólica (figura 3). Los hepatocitos muestran una cantidad variable y en diferentes proporciones de las enzimas que intervienen en el metabolismo, tanto de la [18F]-FDG (1) como de la [18F]-FCH (2). Ambos radiofármacos se han venido utilizando en las últimas décadas como trazadores de Medicina Nuclear en el ámbito oncológico. Por un lado, la [18F]-FDG refleja el consumo de glucosa por la célula neoplásica que se encuentra aumentado en la gran mayoría de tumores y que es necesaria para hacer frente al gran consumo energético propio de estas células (3). Por otro lado, la captación de [18F]-FCH refleja indirectamente otro fenómeno que se encuentra aumentado también en las neoplasias, como es la formación de membranas celulares (4). La colina forma parte de la molécula fosfatidil-colina, que es el componente fundamental de las membranas celulares.
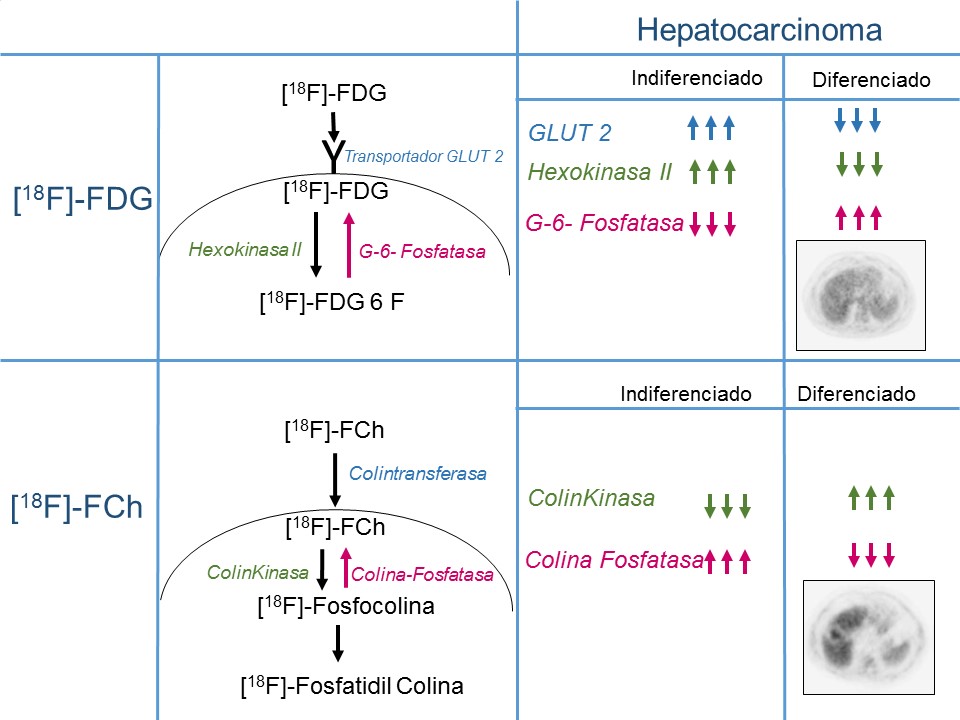
En el caso de muchas neoplasias, incluidas las neoplasias hepáticas, el grado de diferenciación tumoral también contribuye al diferente comportamiento de los diferentes radiofármcacos (5). Los hepatocarcinomas diferenciados se caracterizan por presentar una expresión disminuida de transportadores de glucosa (GLUT 2) y de la actividad de la enzima encargada de fosforilar al RF durante el primer paso de su metabolismo; al mismo tiempo que también muestran una mayor actividad de la enzima encargada de revertir el paso de la fosforilación. Todo esto conduce a un menor índice de captación tumor/fondo, disminuyendo el rendimiento diagnóstico de la molécula [18F]-FDG en la valoración de hepatocarcinomas bien diferenciados (6).
Este perfil enzimático está invertido en los hepatocarcinomas indiferenciados. La actividad de la enzima Glucosa 6-fosfatasa se encuentra muy reducida en este tipo de neoplasias, adicionalmente existe una alta concentración de transportadores de glucosa en la membrana (GLUT), contribuyendo estos dos fenómenos, a un incremento en la internalización de glucosa marcada con 18F y su posterior fosforilación en la vía metabólica de la glucosa, quedando atrapada con 18F-FDG-6-fosfato (7).
En el caso del metabolismo de la [18F]-FCH por las células neoplásicas hepáticas ocurre algo similar, pero a la inversa (figura 2). Es decir, la tasa de actividad de las enzimas favorecedoras del metabolismo del radiofármaco están aumentadas en el caso de los tumores diferenciados, favoreciendo su detectabilidad. En primer lugar, la colina es incorporada a la célula por un transportador de membrana (colinintransferasa) y posteriormente, fosforilada por la acción de la Colin Kinasa y posteriormente, en el interior del hepatocito, a través de sucesivos pasos metabólicos se sintetiza fosfatidilcolina. El paso catalítico inverso por el que se produce la desfosforilación de la colina se lleva a cabo por la Colina-fosfatasa. La actividad elevada del transportador de membrana y de la enzima colinkinasa es característico de este tipo de lesiones hepáticas diferenciadas y lo que permite al PET-TC con este trazador discriminar este tipo de lesiones (8).
El diferente comportamiento de estos dos radiofármacos también viene condicionado por alteraciones genéticas y factores humorales oncológicos. Así por ejemplo, los hepatocarcinomas con sobreexpresión de determinados oncogenes como el c-Myc tienen mayor avidez por el trazador de Glucosa (9). En cambio, un tercio de los hepatocarcinomas humanos presentan una activación de las señales de β-Catenina que condiciona una mayor avidez por el trazador de Colina(10). Este tipo de hepatocarcinomas con mutaciones de la β-Catenina tienen una escasa proliferación y altos niveles de diferenciación.
CONCLUSIÓN
El estudio con PET-TC multitrazador (18F-FDG y 18F-FCH) es una herramienta útil para el diagnóstico de lesiones sospechosas de hepatocarcinoma y caracterizar su perfil metabólico.
DECLARACIÓN DE TRANSPARENCIA
Los autores/as de este artículo declaran no tener ningún tipo de conflicto de intereses respecto a lo expuesto en el presente trabajo.
BIBLIOGRAFIA
- Gil Martínez EM, Rabadán Bujalance F, Ponce Herrera C, Martínez Obrador D, Moya García F. PET-FDG en el hepatocarcinoma: a propósito de un caso. Rev Esp Med Nucl. 2004; 23: 352-353.
- Tulin PE, Dolgushin MB, Odzharova AA et al. Perfusion CT and PET with 18F-FDG and 18F-FCh in the complex diagnosis of hepatocellular carcinoma. Eur J Hybrid Imaging. 2017; 1(1): 13. doi: 10.1186/s41824-017-0018-7. Epub 2017 Dec 1. PMID: 29782602; PMCID: PMC5954776.
- Cabrera Villegas A, García Velloso MJ, Gámez Cenzano C. Tomografía por emisión de positrones (PET) en oncología clínica (Parte III) [Positron emission tomography (PET) in clinical oncology [Part III]]. Rev Esp Med Nucl. 2002; 21: 304-320; quiz 321-3. Spanish. doi: 10.1016/s0212-6982(02)72096-x. PMID: 12206748.
- Kuang Y, Salem N, Corn DJ et al. Transport and metabolism of radiolabeled choline in hepatocellular carcinoma. Mol Pharm. 2010; 7: 2077-2092. doi: 10.1021/mp1001922. Epub 2010 Sep 21. PMID: 20698576; PMCID: PMC2992798.
- Yamamoto Y, Nishiyama Y, Kameyama R et al. Detection of hepatocellular carcinoma using 11C-choline PET: Comparison with 18F-FDG PET. J Nucl Med. 2008; 49: 1245-1248. doi: 10.2967/jnumed.108.052639. Epub 2008 Jul 16.PMID: 18632827.
- Iwata Y, Shiomi S, Sasaki N et al. Clinical usefulness of positron emission tomography with fluorine-18-fluorodeoxyglucose in the diagnosis of liver tumors. Ann Nucl Med. 2000; 14: 121-126. doi: 10.1007/BF02988591. PMID: 10830530.
- Wudel LJ Jr, Delbeke D, Morris D et al. The role of [18F]fluorodeoxyglucose positron emission tomography imaging in the evaluation of hepatocellular carcinoma. Am Surg. 2003; 69: 117-124; discussion 124-126. PMID: 12641351.
- Bansal A, Shuyan W, Hara T, Harris RA, Degrado TR. Biodisposition and metabolism of [(18)F]fluorocholine in 9L glioma cells and 9L glioma-bearing fisher rats. Eur J Nucl Med Mol Imaging. 2008; 35: 1192-1203. doi: 10.1007/s00259-008-0736-y. Epub 2008 Feb 9. PMID: 18264706; PMCID: PMC2386980.
- Yuneva MO, Fan TW, Allen TD et al. The metabolic profile of tumors depends on both the responsible genetic lesion and tissue type. Cell Metab. 2012; 15: 157-170. doi: 10.1016/j.cmet.2011.12.015. PMID: 22326218; PMCID: PMC3282107.
- Gougelet A, Sartor C, Senni N et al. Hepatocellular carcinomas with mutational activation of beta-catenin require choline and can be detected by positron emission tomography. Gastroenterology. 2019; 157: 807-822. doi: 10.1053/j.gastro.2019.05.069. Epub 2019 Jun 10. PMID: 31194980.
Antonio Cabrera Villegas
Servicio de Medicina Nuclear. Hospital Clínico San Carlos.
C/ Profesor Martín Lagos S/N · 28040 Madrid
Tlf.: +34 913 303 000 | E-Mail: acabrerav@salud.madrid.org
An RANM. 2022;139(03): 303-306
Enviado: 07.07.22
Revisado: 12.07.22
Aceptado: 22.07.22


