Resumen
Las funciones fisiológicas de las adipoquinas en el metabolismo energético o la homeostasis cardiovascular, entre otras, son bien conocidas. En los últimos años, nuestro laboratorio ha proporcionado evidencia creciente del posible papel de las adipoquinas como mediadores de daño vascular, al inducir distintos mecanismos pro-inflamatorios y pro-senescentes. La secreción de adipoquinas como visfatina y dipeptidilpeptidasa-4 (DPP4) por el tejido adiposo, especialmente el visceral, está incrementada en pacientes obesos o con diabetes tipo 2. Ambas adipoquinas son enzimas metabólicamente activas, y es precisamente esta actividad la que induce la activación de receptores específicos, como los “toll like receptors” tipo 4 (TLR4) para visfatina y los “protease activated receptor 2” (PAR2) para DPP4. La estimulación de estos receptores pone en marcha mecanismos pro-inflamatorios y pro-senescentes como el factor nuclear de transcripción-κB (NF-κB) o la activación del inflamasoma NLRP3 (“nucleotide-binding, leucin-rich-repeat, pyrin domain containing 3”), una estructura celular que transforma las formas inmaduras de citoquinas clásicas en sus formas activas, interleuquina-1β (IL-1β) o interleuquina-18 (IL-18). Es importante resaltar, por tanto, que son estas citoquinas los efectores finales de las acciones deletéreas de las adipoquinas, y el bloqueo de las mismas puede ser una aproximación terapéutica de gran importancia. En nuestros experimentos, el antagonismo específico de los receptores para IL-1 con anakinra previene las respuestas inflamatorias y senescentes inducidas por visfatina y DPP4. Este hallazgo concuerda con los datos de otros investigadores y, especialmente, con los resultados del ensayo clínico CANTOS, que demuestra un efecto cardioprotector por la acción anti-inflamatoria del anticuerpo monoclonal anti-IL-1β canakinumab. Por otro lado, también hemos proporcionado evidencia experimental sobre las acciones inducidas por posibles adipoquinas vasculoprotectoras, como la angiotensina-(1-7) que, a través de la activación de receptores Mas, induce la expresión de klotho y la activación de mecanismos antioxidantes, como la conocida vía Nrf2-HO-1 (“nuclear factor erythroid-2 y hemoygenase-1”).
Abstract
The main physiologic function of adipokines on the energy metabolism and the cardiovascular homeostasis, among others, are well known. In the last years, our laboratory is providing increasing evidence about the possible role of adipokines as mediators of vascular damage, by inducing different pro-inflammatory and pro-senescent mechanisms. The secretion of adipokines like visfatin or dipeptidylpeptidase-4 (DPP4) by adipose tissue, particularly by the visceral fat, is enhanced in obese and type 2 diabetic patients. Both adipokines are enzymes metabolically active that can induce the activation of specific receptors, namely type 4 “toll like receptors” (TLR4) for visfatin and “protease activated receptor 2” (PAR2) for DPP4. Stimulation of such receptors is triggering well known pro-inflammatory and pro-senescent mechanisms, like the nuclear transcription factor-κB (NF-κB) or the inflammasome NLRP3 (“nucleotide-binding, leucine-rich-repeat, pyrin domain containing 3”), a cell structure that transforms the immature forms of classic cytokines in their active derivates, interleukin-1β (IL-1β) or interleukin 18 (IL-18). It is worth to note that these classic cytokines are the final effectors for the harmful effects of the adipokines and its blockade can be a very relevant therapeutic approach. In our experiments, the specific antagonism of IL-1 receptors with anakinra prevents the inflammatory and senescent effects evoked by visfatin and DPP4. Moreover, this finding is in agreement with data from other researchers, as well as with the results of the CANTOS clinical trial, which demonstrate a very important cardioprotective cardiovascular effect mediated by the anti-inflammatory effect of the monoclonal antibody canakinumab. On the other hand, we have also provided experimental evidence about possible vasculopotective adipokines, such angiotensin-(1-7), which is able to induce, through activation of Mas receptors, the expression of klotho protein and the activation of antioxidant pathways, like the well known Nrf2-HO-1 (“nuclear factor erythroid-2 y hemoygenase-1”).
Palabras clave: Obesidad; Adipoquinas; Disfunción vascular; Senescencia; Visfatina; Dipeptidilpeptidasa-4.
Keywords: Obesity; Adipokines; Vascular dysfunction; Senescence; Visfatin; Dipeptidylpeptidase-4.
INTRODUCCIÓN
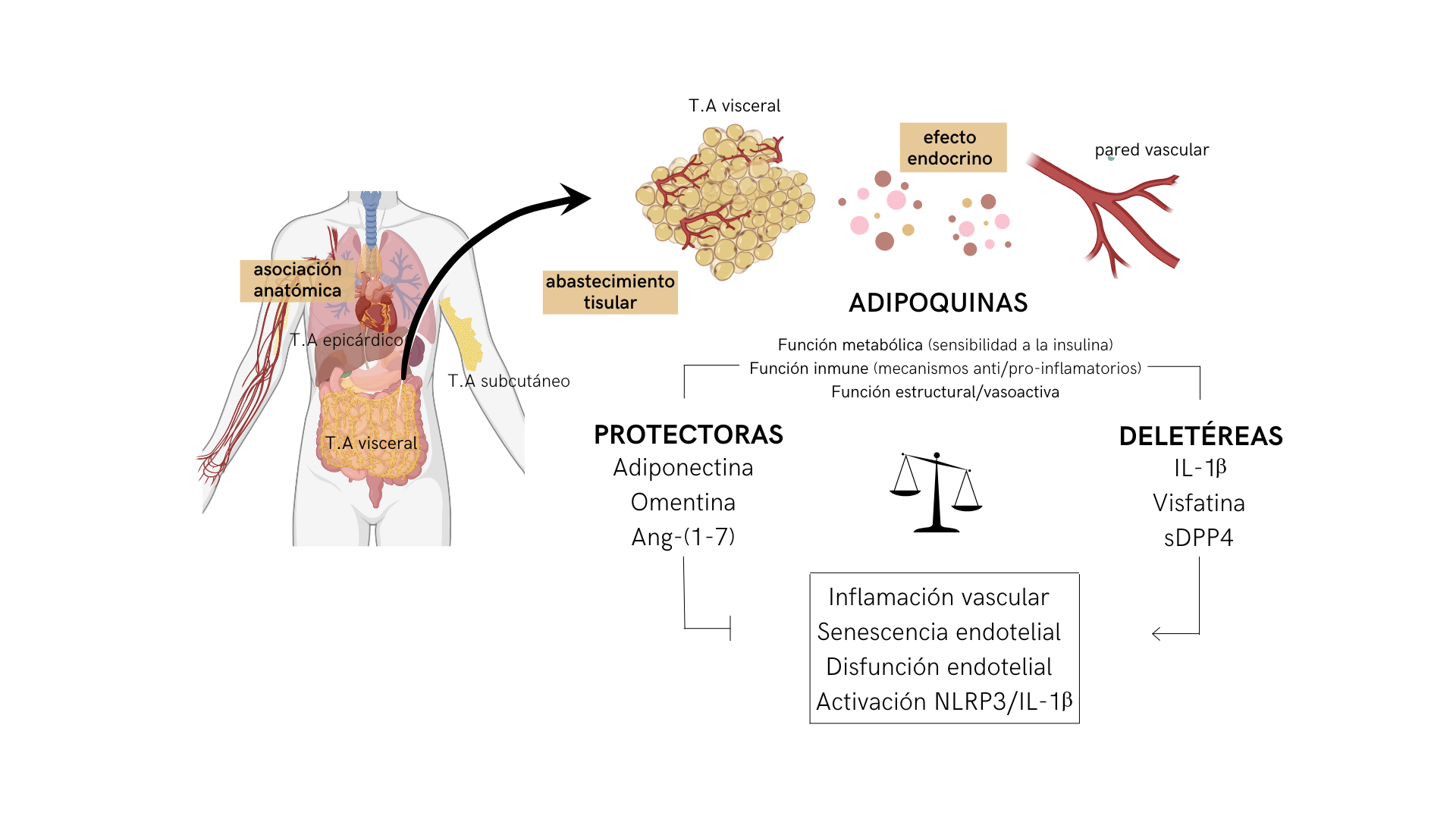
La obesidad y la diabetes mellitus tipo 2 son factores de riesgo independientes para distintas enfermedades cardiovasculares, como hipertensión o aterosclerosis, con un papel relevante en el envejecimiento vascular acelerado. Su enorme difusión mundial (son las dos únicas enfermedades no infecciosas consideradas pandémicas por la OMS) convierte la patología cardiometabólica en un objetivo prioritario de la investigación biomédica. En este sentido, existe cada vez más evidencia acerca del papel de las adipocitoquinas o adipoquinas como nexo entre el tejido adiposo y el sistema cardiovascular. Se conoce que el tejido adiposo tiene un posible papel endocrino y más probablemente paracrino o autocrino, a través de la secreción de adipoquinas, moléculas de naturaleza y mecanismos muy diferentes, que modulan la función y estructura vasculares. En condiciones fisiológicas, es bien conocida la relación anatómica y funcional estrecha que unen al tejido adiposo y la vasculatura (Figura 1). Por un lado, el tejido adiposo está muy vascularizado y el mantenimiento de un flujo sanguíneo adecuado es esencial para abastecer al tejido y regular la función metabólica, la adipogénesis y el remodelado del tejido adiposo. Por otro lado, prácticamente todos los vasos sanguíneos están rodeados de tejido adiposo que produce gran cantidad de moléculas con actividad vasocrina. Además, se conoce la conexión estrecha que existe entre el crecimiento del tejido adiposo y el desarrollo del árbol vascular intratisular. Se ha estudiado de modo particular la grasa periadventicial que rodea distintos lechos vasculares, como el epicárdico, así como el tejido adiposo subcutáneo y el visceral, los más abundantes. El perfil secretor de las adipoquinas es depósito-específico y se ha identificado al tejido adiposo visceral como el más estrechamente relacionado con alteraciones metabólicas como la resistencia a la insulina y el aumento del riesgo cardiovascular.
Se han descrito adipoquinas protectoras de la función vascular y de la sensibilidad a la insulina, secretadas por un tejido adiposo sano, como omentina y adiponectina (Figura 1), mientras que la grasa de sujetos obesos produce adipoquinas deletéreas, con capacidad pro-inflamatoria, tales como leptina, interleuquina-1β (IL-1β) o factor de necrosis tumoralα (TNFα). Existe evidencia creciente de que estas adipoquinas inflamatorias producen disfunción endotelial, que es uno de los mecanismos tempranos de mayor importancia en el desencadenamiento de patología vascular. En este trabajo se va a prestar particular atención a dos adipoquinas relativamente recientes, como son la visfatina y la dipeptidilpeptidasa-4 (DPP4), que tienen en común la característica de poseer actividad enzimática (Figura 1).
SÍNTESIS
La visfatina se describió inicialmente por Fukuara et al (1) en 2005 como una molécula incrementada en obesidad y diabetes tipo 2, con una estructura idéntica a la enzima nicotinamida fosforribosiltransferasa, capaz de transformar la nicotinamida en mononucleótido de nicotinamida y, por tanto, con un papel relevante en la producción de NAD (Nicotinamida adenina dinucleótido). Nuestro grupo demostró que esta sustancia produce inflamación en cultivos de músculo liso vascular humano (2) y disfunción endotelial en microvasos humanos y de rata (3), así como senescencia endotelial (4).
De modo interesante, nuestros datos (2) indican que la visfatina, a través de su actividad enzimática y mediante la producción de mononucleótido de nicotinamida, puede activar receptores específicos, denominados “toll like receptors” tipo 4 (TLR4) en la pared vascular, lo que activa el factor nuclear de transcripción-κB (NF-κB), que constituye un mecanismo esencial para desencadenar procesos inflamatorios.
Estudios más recientes indican asimismo la capacidad de esta adipoquina para inducir la activación del inflamasoma NLRP3 (siglas de la denominación inglesa “nucleotide-binding, leucin-rich-repeat, pyrin domain containing 3”) cuya relevancia en los procesos inflamatorios está siendo objeto de intensa investigación. Se trata de una estructura celular que tiene un papel esencial en la respuesta innata inmune, desencadenada por distintos mecanismos, y que se caracteriza por la activación de la enzima caspasa-1, que transforma las formas inmaduras de citoquinas clásicas, como pro-interleuquina 1β o pro-interleuquina 18 en sus formas activas, IL-1β o IL-18 (5).
Nuestro grupo ha comprobado la capacidad de visfatina, tanto in vitro como in vivo, para activar el inflamasoma NLRP3, lo que conduce a inflamación, senescencia y, consecuentemente, disfunción vascular (6). Desde el punto de vista farmacológico, es interesante que estos efectos patológicos pueden ser bloqueados, o al menos reducidos, tanto in vitro como in vivo, por antagonistas de los receptores para IL-1β del tipo de anakinra, así como mediante el bloqueo farmacológico del ensamblaje del inflamasoma (6), lo que sugiere que el mediador final de estos procesos es la IL-1β producida por la activación de este complejo.
Una segunda adipoquina que se ha descrito más recientemente es la DPP4, una exopeptidasa bien conocida por los farmacólogos, ya que es crucial en la degradación de las incretinas y, en base a ello, es una diana farmacológica establecida, de modo que su inhibición por las gliptinas es un abordaje terapéutico de la diabetes tipo 2. En efecto, estos fármacos constituyen un grupo claramente establecido de antidiabéticos orales, dada su capacidad de incrementar los niveles endógenos de incretinas al reducir su inactivación.
En 2011, Lamers et al. (7) describieron que la forma soluble de la enzima (sDPP4) era una nueva adipoquina secretada por el tejido adiposo, especialmente la grasa visceral. Esta secreción era significativamente más alta en sujetos obesos o con diabetes tipo 2 y se correlaciona con resistencia de los tejidos a la insulina (8).
Poco después, en colaboración con estos investigadores, comprobamos que la sDPP4 era capaz de producir inflamación en cultivos de células musculares humanas, a través de la activación de un receptor denominado PAR2 (protease activated receptor 2), que modula respuestas inflamatorias en obesidad, enfermedades metabólicas y cáncer y que actúa como un sensor de enzimas proteolíticas generadas en infecciones (9). Asimismo, demostramos que sDPP4 produce disfunción endotelial actuando sobre dichos receptores PAR2 y activando la producción y liberación de tromboxano-A2 (10). Es interesante resaltar que las acciones deletéreas de sDPP4 dependen de su actividad enzimática y pueden ser antagonizadas con bloqueantes de esta actividad como las gliptinas (10, 11).
Recientemente, hemos descrito que este mismo mecanismo está implicado en la inducción de senescencia por sDPP4 en células endoteliales humanas cultivadas (11). Nuestros datos indican asimismo que sDPP4 es capaz de desencadenar el ensamblaje y activación del inflamasoma NLRP3, produciendo IL-1β como efector final de las respuestas inflamatoria y senescente que, por tanto, son antagonizadas por el bloqueo de los receptores para IL-1β (11).
Estos resultados pueden ser aplicables también en pacientes obesos. Para estudiar este aspecto, se utilizaron biopsias de epiplon de pacientes con normopeso y obesos (con índice de masa corporal (IMC) inferior o superior a 30 kg·m-2, respectivamente) para analizar por una parte la reactividad vascular en microvasos mesentéricos humanos y, por otra, extraer RNA de la grasa visceral (11). Se observó que, en microvasos mesentéricos de pacientes con IMC< 30 kg·m-2, sDPP4 produce disfunción endotelial que puede ser antagonizada por gliptinas (es decir, depende de su acción enzimática), mientras que en los microvasos de pacientes obesos ya existe, en condiciones basales, un importante grado de disfunción endotelial que se correlaciona claramente con el índice de masa corporal y que se revierte cuando los vasos se incubaron previamente con una gliptina (11).
Conforme a lo previamente reportado (7), en la grasa visceral de estos pacientes obesos hay unos niveles aumentados de mRNA para DPP4 en comparación con los pacientes delgados. Además, estos mayores niveles del mensajero para la DPP4 presentan una clara correlación positiva con el índice de masa corporal y, de manera muy interesante, una correlación inversa con el grado de disfunción endotelial (11).
También se determinó, en la grasa visceral de estos pacientes, la expresión de mRNA para marcadores de senescencia celular, como p53, p21 y p16, así como de componentes del inflamasoma, como NLRP3, IL-1β e IL-18. Todos ellos estaban significativamente incrementados en pacientes obesos respecto del grupo control y mostraban buenas correlaciones positivas con el índice de masa corporal y negativas con la función endotelial (11).
En definitiva, los datos indican claramente que en la grasa visceral de pacientes obesos existe un aumento en la expresión de DPP4 que se asocia tanto a la disfunción endotelial como a los marcadores de senescencia o los componentes del inflamasoma NLRP3. Por tanto, de acuerdo a los resultados descritos en cultivos celulares, proponemos que estos fenómenos están relacionados, de modo que los mayores niveles de DPP4 desencadenan mecanismos pro-inflamatorios, incluyendo la activación del inflamasoma, que en última instancia libera IL-1β, induce senescencia e interfiere con la función endotelial (11).
Existen distintos trabajos que apoyan esta hipótesis. Así, en 2007 se demostró que el antagonista del receptor para IL-1 anakinra mejora distintos parámetros clínicos en pacientes diabéticos (12), aunque en este estudio no se analizó su posible beneficio en la función vascular. Un tiempo después, nuestro grupo demostró que este fármaco puede prevenir la disfunción vascular observada en un modelo experimental de diabetes mellitus, lo que estaba relacionado con una menor respuesta inflamatoria en la pared vascular (13). Posteriormente, en 2017, se publicó un importante ensayo clínico, denominado CANTOS (14), analizando el papel de canakinumab, un anticuerpo monoclonal específico contra la IL-1β, en pacientes con patología cardiovascular en los que se demostró una menor reincidencia de infarto de miocardio e ictus y una reducción de la mortalidad cardiovascular (14). Es interesante resaltar que en estos pacientes no se modificaron los niveles de LDL o HDL, pero sí se observó una disminución de la proteína C reactiva de alta sensibilidad, un marcador de inflamación. Es decir, la protección que ofrece canakinumab obedece a su capacidad para reducir la respuesta inflamatoria y no está relacionada con el control de factores clásicos de riesgo cardiovascular, como los niveles de colesterol (14) o la presión arterial (15).
Otros estudios realizados en nuestro laboratorio sugieren también la existencia de adipoquinas cardioprotectoras, entre las que cabe destacar la angiotensina-(1-7) o Ang-(1-7), un péptido del sistema renina-angiotensina-aldosterona que actúa como un antagonista fisiológico del efector final de este sistema, la angiotensina-II (Ang-II). Así, la Ang-II es vasoconstrictora, pro-fibrótica y pro-inflamatoria, mientras que la Ang-(1-7) es vasodilatadora, anti-fibrótica y anti-inflamatoria (16). En nuestro caso, hemos demostrado que la Ang-(1-7) previene la disfunción endotelial y la inflamación vascular a través de su interacción con receptores específicos asociados a proteínas G, los receptores Mas (17, 18, 19). Además, no sólo antagonizan los efectos de la Ang-II, sino que también pueden prevenir los efectos inflamatorios y pro-senescentes de citoquinas como la IL-1β (20), es decir, pueden tener un efecto protector de amplio espectro y no solamente limitado al sistema renina-angiotensina-aldosterona.
Adicionalmente, nuestros datos indican (20) que dichos efectos protectores de Ang-(1-7) pueden estar mediados por su capacidad de incrementar la expresión de una proteína con capacidad anti-envejecedora, denominada klotho (21, 22). Esta proteína, a su vez, activa la vía Nrf2-HO-1 (“nuclear factor erythroid-2 y hemoxygenase-1”), un mecanismo citoprotector frente a estímulos pro-oxidantes ampliamente descrito (20, 22).
CONCLUSIONES
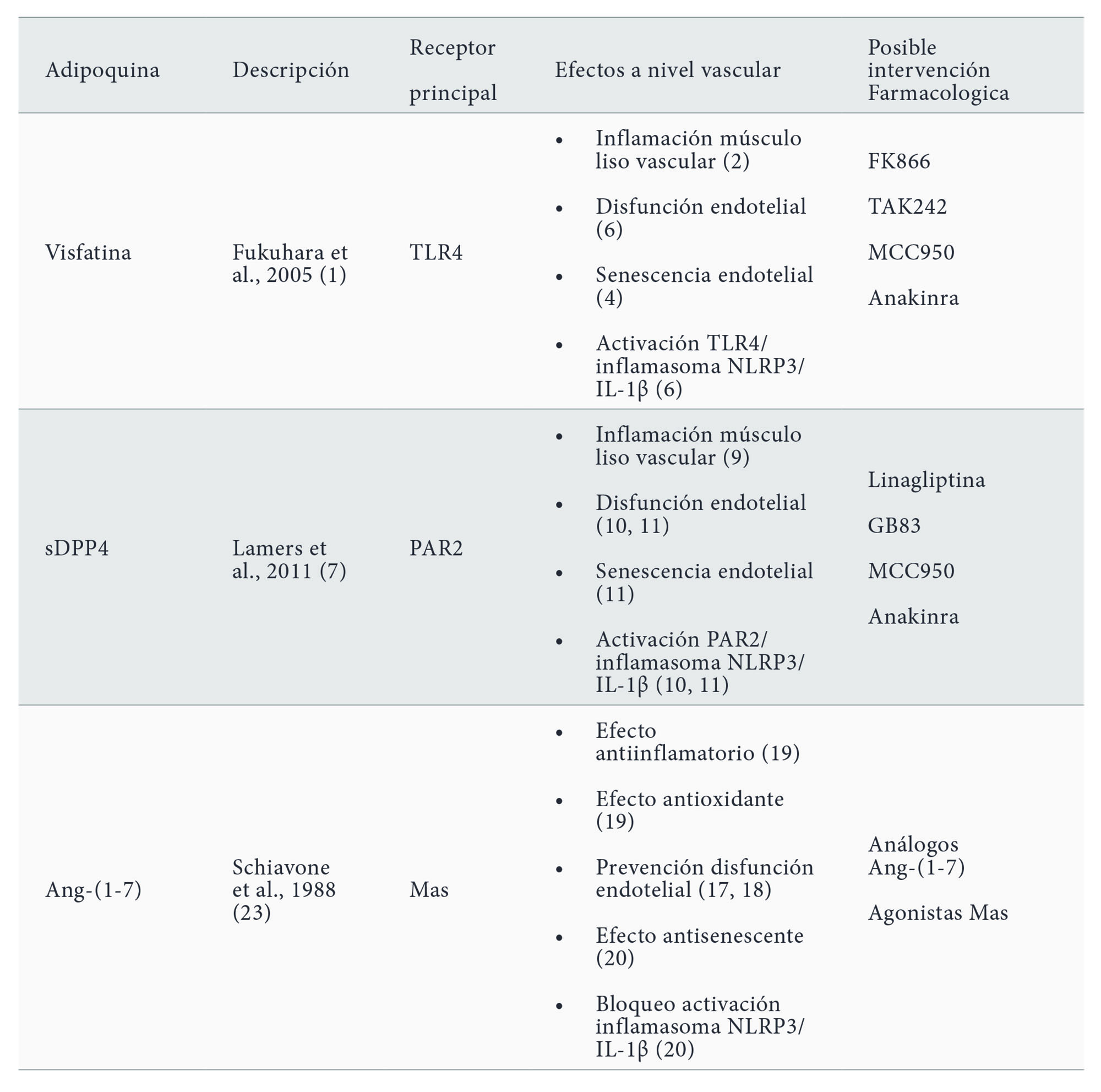
En definitiva, el trabajo de nuestro laboratorio en los últimos años ha proporcionado evidencia creciente del posible papel de las adipoquinas como mediadores de daño vascular, al inducir distintos mecanismos pro-inflamatorios y pro-senescentes. Así, la secreción de las adipoquinas visfatina y DPP4 por el tejido adiposo, especialmente el visceral, está incrementada en pacientes obesos o con diabetes tipo 2. Ambos compuestos son enzimas metabólicamente activas, y activan receptores específicos, como son TLR4 para visfatina y PAR2 para DPP4 (Tabla 1). Es la estimulación de estos receptores la que pone en marcha mecanismos pro-inflamatorios y pro-senescentes clásicos, como NF-κB, pero también desencadena la activación del inflamasoma NLRP3, una estructura celular que transforma las formas inmaduras de citoquinas clásicas, como pro-IL-1β o pro-18 en sus formas activas, IL-1β o IL-18.
Es importante resaltar, por tanto, que son estas citoquinas clásicas los efectores finales de las acciones deletéreas de las adipoquinas y, consecuentemente, el bloqueo de las mismas puede ser una aproximación terapéutica de gran importancia. En nuestros experimentos, el antagonismo de los receptores para IL-1 previenen las respuestas inflamatorias y senescentes inducidas por visfatina y DPP4. Este hallazgo que concuerda con los datos de otros investigadores y, de modo especial, con los resultados del ensayo clínico CANTOS, que demuestra un efecto cardioprotector muy importante por la acción anti-inflamatoria del anticuerpo monoclonal anti-IL-1β canakinumab.
Por otro lado, también hemos proporcionado evidencia experimental sobre las acciones inducidas por posibles adipoquinas vasculoprotectoras, como la Ang-(1-7) que, a través de la activación de receptores Mas, parecen inducir la expresión de klotho y la activación de mecanismos antioxidantes, como la Nrf2-HO-1 (Tabla 1).
AGRADECIMIENTOS
Este trabajo ha sido financiado por el Plan Nacional de I+D del Ministerio de Economía (SAF2017-84776-R y PID2020-115590RB-100/ AEI/10.13039/501100011033),Boehringer Ingelheim España S.A. el Ministerio de Educación (FPUMECD, FPU16/0261;
Juan de la Cierva Incorporación (IJCI-2015-24474), el Fondo Social Europeo y la Comunidad de Madrid (PEJ-2018-AI/SAL-9955 and PEJ-2017-AI/SAL-6867) y la Universidad Autónoma de Madrid (FPI-UAM, SFPI/2016-00981 y SFPI/2020-00053).
DECLARACIÓN DE TRASPARENCIA
Los autores/as de este artículo declaran no tener ningún tipo de conflicto de intereses respecto a lo expuesto en el presente trabajo.
BIBLIOGRAFÍA
- Fukuhara A, Matsuda M, Nishizawa M et al. Visfatin: a protein secreted by visceral fat that mimics the effects of insulin. Science. 2005; 307(5708): 426-430. doi: 10.1126/science.1097243.
- Romacho T, Azcutia V, Vázquez-Bella M et al. Extracellular PBEF/NAMPT/visfatin activates pro-inflammatory signalling in human vascular smooth muscle cells through nicotinamide phosphoribosyltransferase activity. Diabetologia. 2009; 52(11): 2455-2463. doi: 10.1007/s00125-009-1509-2.
- Vallejo S, Romacho T, Angulo J et al. Visfatin impairs endothelium-dependent relaxation in rat and human mesenteric microvessels through nicotinamide phosphoribosyltransferase activity. PLoS One. 2011; 6(11): e27299. doi: 10.1371/journal.pone.0027299.
- Villalobos LA, Uryga A, Romacho T et al. Visfatin/Nampt induces telomere damage and senescence in human endothelial cells. Int J Cardiol. 2014; 175(3): 573-575. doi: 10.1016/j.ijcard.2014.05.028.
- Rheinheimer J, de Souza BM, Cardoso NS, Bauer AC, Crispim D. Current role
- of the NLRP3 inflammasome on obesity and insulin resistance: a systematic review. Metabolism. 2017; 74: 1-9. doi: 10.1016/j.metabol.2017.06.002
- Romacho T, Valencia I, Ramos-González M et al. Visfatin/eNampt induces endothelial dysfunction in vivo: a role for Toll-Like Receptor 4 and NLRP3 inflammasome. Sci Rep. 2020; 10(1): 5386. doi: 10.1038/s41598-020-62190-w.
- Lamers D, Famulla S, Wronkowitz N et al. Dipeptidyl peptidase 4 is a novel adipokine potentially linking obesity to the metabolic syndrome.. Diabetes. 2011; 60(7): 1917-1925. doi: 10.2337/db10-1707.
- Sell H, Blüher M, Klöting N et al. Adipose dipeptidyl peptidase-4 and obesity: correlation with insulin resistance and depot-specific release from adipose tissue in vivo and in vitro. Diabetes Care. 2013; 36(12): 4083-4090. doi: 10.2337/dc13-0496.
- Wronkowitz N, Görgens SW, Romacho T et al. Soluble DPP4 induces inflammation and proliferation of human smooth muscle cells via protease-activated receptor 2. Biochim Biophys Acta. 2014; 1842(9): 1613-1621. doi: 10.1016/j.bbadis.2014.06.004.
- Romacho T, Vallejo S, Villalobos LA et al. Soluble dipeptidyl peptidase-4 induces microvascular endothelial dysfunction through proteinase-activated receptor-2 and thromboxane A2 release. J Hypertens. 2016; 34(5): 869-876. doi: 10.1097/HJH.0000000000000886.
- Valencia I, Vallejo S, Dongil P et al. DPP4 promotes human endothelial cell senescence and dysfunction via the PAR2-COX-2-TP axis and NLRP3 inflammasome activation. Hypertension. 2022; 79(7): 1361-1373. doi: 10.1161/HYPERTENSIONAHA.121.18477.
- Larsen CM, Faulenbach M, Vaag A et al. Interleukin-1-receptor antagonist in type 2 diabetes mellitus. N Engl J Med. 2007. 12; 356(15): 1517-1526. doi: 10.1056/NEJMoa065213.
- Vallejo S, Palacios E, Romacho T, Villalobos L, Peiró C, Sánchez-Ferrer CF. The interleukin-1 receptor antagonist anakinra improves endothelial dysfunction in streptozotocin-induced diabetic rats. Cardiovasc Diabetol. 2014. 18; 13: 158. doi: 10.1186/s12933-014-0158-z.
- Ridker PM, Everett BM, Thuren T et al; CANTOS Trial Group. Antiinflammatory therapy with canakinumab for atherosclerotic disease. N Engl J Med. 2017. 21; 377(12): 1119-1131. doi: 10.1056/NEJMoa1707914.
- Rothman AM, MacFadyen J, Thuren T et al. Effects of interleukin-1β inhibition on blood pressure, incident hypertension, and residual inflammatory risk: a secondary analysis of CANTOS. Hypertension. 2020; 75(2): 477-482. doi: 10.1161/HYPERTENSIONAHA.119.13642.
- Santos RA. Angiotensin-(1-7). Hypertension. 2014; 63(6): 1138-1147. doi: 10.1161/HYPERTENSIONAHA.113.01274.
- Peiró C, Vallejo S, Gembardt F. Endothelial dysfunction through genetic deletion or inhibition of the G protein-coupled receptor Mas: a new target to improve endothelial function. J Hypertens. 2007; 25(12): 2421-2425. doi: 10.1097/HJH.0b013e3282f0143c.
- Peiró C, Vallejo S, Gembardt F et al. Complete blockade of the vasorelaxant effects of angiotensin-(1-7) and bradykinin in murine microvessels by antagonists of the receptor Mas. J Physiol. 2013. 1; 591(9): 2275-2285. doi: 10.1113/jphysiol.2013.251413.
- Villalobos LA, San Hipólito-Luengo Á, Ramos-González M et al. The Angiotensin-(1-7)/Mas axis counteracts angiotensin ii-dependent and -independent pro-inflammatory signaling in human vascular smooth muscle cells. Front Pharmacol. 2016. 15; 7: 482. doi: 10.3389/fphar.2016.00482.
- Romero A, Dongil P, Valencia I et al. Pharmacological blockade of NLRP3 inflammasome/IL-1β-positive loop mitigates endothelial cell senescence and dysfunction. Aging Dis. 2022. 1; 13(1): 284-297. doi: 10.14336/AD.2021.0617.
- Takahashi Y, Kuro-O M, Ishikawa F. Aging mechanisms. Proc Natl Acad Sci U S A. 2000. 7; 97(23): 12407-12408. doi: 10.1073/pnas.210382097.
- Romero A, San Hipólito-Luengo A, Villalobos L et al. The angiotensin-(1-7)/Mas receptor axis protects from endothelial cell senescence via klotho and Nrf2 activation. Aging Cell. 2019. e12913. doi: 10.1111/acel.12913.
- Schiavone MT, Santos RA, Brosnihan KB, Khosla MC, Ferrario C.M. Release of vasopressin from the rat hypothalamo-neurohypophysial system by angiotensin-(1-7) heptapeptide. Proc Natl Acad Sci USA. 1988; 85(11): 4095-4098. doi: 10.1073/pnas.85.11.4095.
ranm tv
Carlos F. Sánchez Ferrer
Universidad Autónoma de Madrid. C/ Arzobispo Morcillo 4 · 28029 Madrid
E-Mail: carlosf.sanchezferrer@uam.es
An RANM. 2022;139(03): 223-228
Enviado*: 04.05.22
Revisado: 10.05.22
Aceptado: 17.05.22
* Fecha de lectura en la RANM


