Resumen
Las enfermedades autoinmunes sistémicas, entre las que se encuentra el lupus eritematoso sistémico (LES), presentan una mayor morbi-mortalidad de origen cardiovascular así como una mayor incidencia de una ateroesclerosis precoz y acelerada en comparación con la población general. Esta afectación no puede explicarse sólo por la presencia de los denominados factores clásicos de riesgo como la hipertensión, diabetes, hipercolesterolemia, obesidad o tabaquismo, sino que parece depender de factores no clásicos asociados a la enfermedad. El desequilibrio entre el daño y la reparación vascular juega un papel fundamental en el inicio de la lesión arterioesclerótica. Este balance entre daño y reparación puede romperse por factores no bien conocidos que se han asociado a inflamación crónica, estrés oxidativo, tratamientos farmacológicos, alteración en las células implicadas en la reparación del endotelio y en moléculas de regulación inmunitaria. Actualmente se están investigando biomarcadores que ayuden a los clínicos a identificar a aquellos pacientes que presenten un mayor riesgo de enfermedad cardiovascular.
Abstract
Systemic autoimmune diseases, such systemic lupus erythematosus (SLE), show an increased morbidity and cardiovascular mortality and a higher incidence of early and accelerated atherosclerosis than the general population that cannot be explained only by the presence of classic risk factors such arterial hypertension, mellitus diabetes, hypercholesterolemia, obesity or smoking, but it seems to depend on factors associated with the disease. The imbalance between vascular damage and repair plays a critical role in the initiation of atherosclerotic lesion. This balance may be broken by factors associated with chronic inflammation, oxidative stress, pharmacological treatments, altered molecules and cells involved in the repair of the endothelium. Research is ongoing to identify biomarkers that can help clinicians to predict which SLE patients are the greatest risk for cardiovascular disease.
Palabras clave: Ateroesclerosis; Lupus; Biomarcadores; Prevención.
Keywords: Atherosclerosis; Lupus; Biomarkers; Prevention.
INTRODUCCIÓN
Existe un riesgo bien conocido de enfermedad cardiovascular en los pacientes con lupus eritematoso sistémico (LES) que contribuye a la morbimortalidad de esta enfermedad autoinmune sistémica (1,2). El patrón bimodal de mortalidad en el lupus fue descrito inicialmente por Urowitz et al en 1976, que observó que las muertes durante el primer año del diagnóstico eran debidas a la actividad de la enfermedad, pero las producidas más de ocho años después del diagnóstico se relacionaban con episodios cardiovasculares (3).
En el LES se ha observado una mayor incidencia de episodios cardiovasculares y de la mortalidad de causa vascular, comparados con grupos de edad y sexo similares. Los pacientes con LES tienen 5-6 veces más probabilidades de presentar un síndrome coronario agudo que la población general y se ha descrito que este riesgo se incrementa hasta 50 veces en el grupo de mujeres entre 35-44 años (4).
En el desarrollo de este proceso intervienen diversos mecanismos, como los factores de riesgo tradicionales para la ateroesclerosis (tabaco, dislipemia, diabetes mellitus e hipertensión arterial), el uso de fármacos como los corticoesteroides, mecanismos inflamatorios y autoinmunes que están presentes en estas patologías, autoanticuerpos, actividad de la enfermedad, moléculas de la inflamación, el tiempo de evolución de la enfermedad y el daño crónico (1) (Tabla 1). Un aspecto de gran interés por las implicaciones terapéuticas y pronósticas que conlleva es la demostración mediante diferentes exploraciones complementarias, de la existencia de una enfermedad cardiovascular subclínica en estos pacientes.
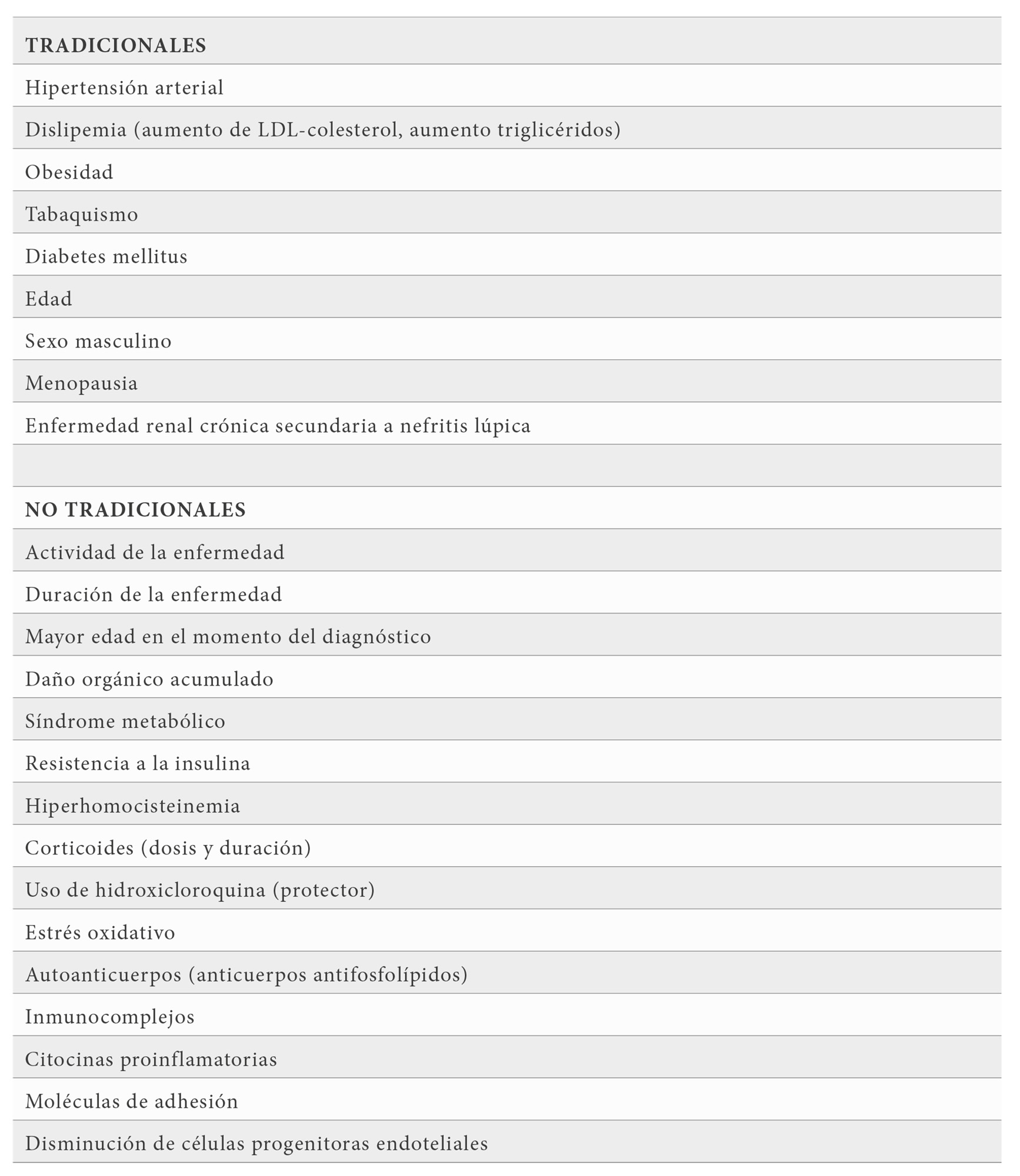
FACTORES DE RIESGO CARDIOVASCULAR EN EL LUPUS ERITEMATOSO SISTÉMICO
Hay estudios que proporcionan evidencia clínica del aumento de la incidencia de sufrir un evento coronario de los pacientes con LES, estimándose en un 10%. En concreto, Manzi et al (4) comprobaron que las mujeres con LES entre 35 y 44 años tenían 50 veces más frecuencia de padecer un infarto de miocardio que las mujeres de la misma edad y semejantes factores de riesgo de la cohorte del estudio Framingham. Estos autores concluyeron que la enfermedad cardiovascular era siete veces más frecuente en LES que en la población general. En series posteriores se ha observado una incidencia de 10,9% de eventos cardiovasculares de origen arteriosclerótico, independientemente de los factores de riesgo clásicos, enfermedad cardiovascular previa o insuficiencia renal (5,6,7).
Múltiples estudios epidemiológicos han identificado un riesgo significativamente elevado de muerte debido a enfermedades cardiovasculares. En un metaanálisis reciente con 15 artículos evaluados (8), cifra la tasa estandarizada de mortalidad por todas las causas de muerte por episodios cardiovasculares en 2,2. Moreno-Torres et al basándose en el registro nacional español de altas hospitalarias concluye que las enfermedades cardiovasculares, junto a infecciones y neoplasias son la causa principal de admisiones y de mortalidad (9).
A la vista de todos estos datos, cabe plantearse por qué el sistema cardiovascular de los pacientes con LES es tan vulnerable y cuál es la relación entre el LES y la ateroesclerosis. Existen estudios que sugerían un aumento en la prevalencia de factores de riesgo cardiovascular. Así Petri et al (10) estimaron la prevalencia de los factores “clásicos” en una cohorte de 225 pacientes con LES, demostrando que el 53% tenían 3 o más de los 7 factores de riesgo considerados. Al comparar pacientes lúpicos con afectación coronaria con aquellos que no la tenían, Manzi et al (4) observaron mayor hipercolesterolemia en los pacientes lúpicos con afectación coronaria. Del mismo modo, Petri et al (10), concluyen un aumento significativo del porcentaje de hipertensión arterial, hipercolesterolemia y obesidad en los pacientes con evidencia de patología cardiovascular frente a los que no estaban afectados.
Estos estudios sugieren que los pacientes con LES tienen más factores de riesgo que la población general y, en consecuencia, más enfermedad coronaria, aunque se ha demostrado que estos factores de riesgo por sí solos, no explican el gran incremento de incidencia de eventos vasculares (11). Al mismo tiempo se ha observado que los pacientes con LES necesitan menos factores de riesgo de los llamados clásicos para desarrollar enfermedad isquémica coronaria, por lo que debe existir una actividad aterogénica dada por la propia enfermedad (1). Los algoritmos basados solo en factores de riesgo cardiovascular tradicionales (SCORE) infraestiman el verdadero riesgo de los pacientes con LES.
ATEROESCLEROSIS SUBCLÍNICA EN EL LUPUS ERITEMATOSO SISTÉMICO
Dada la elevada incidencia de enfermedad coronaria y relevancia pronóstica de la misma en pacientes con LES, parece justificado la identificación precoz de ateroesclerosis subclínica a distintos niveles, preferiblemente con técnicas no invasivas y de fácil aplicación en la práctica diaria (Tabla 2).
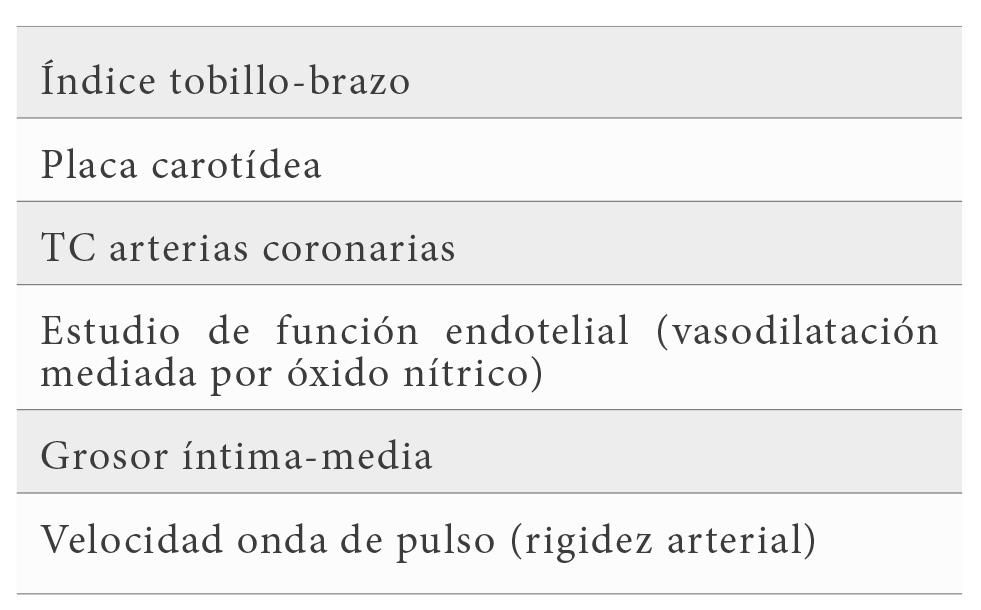
Entre estas técnicas, se encuentra el índice tobillo-brazo (ITB) que se trata de un método reproducible con una alta sensibilidad y especificidad para detectar enfermedad arterial periférica. Hay estudios como el de Papamichael et al (12) en el año 2000, que sugieren que podría ser un predictor de ateroesclerosis coronaria y eventos cardiovasculares y una herramienta útil para la detección precoz de ateroesclerosis en la población general. Respecto al LES, Theodoridou et al (13) en 2003, midieron el ITB en 91 pacientes con LES con una media de edad de 39 años y demostraron que a pesar de tratarse de pacientes jóvenes tenían una prevalencia de ITB patológico del 37%, lo que sugiere patología vascular asintomática.
Existen diversos estudios que han valorado la existencia de placa carotidea mediante ecografía modo B. Roman et al (14) compararon la prevalencia de placa carotidea en una cohorte de mujeres con LES y un grupo control ajustado por edad, sexo, raza y presión arterial. Los pacientes con LES tenían una prevalencia significativamente más alta de placa carotidea en todos los grupos de edad respecto a los controles. Hallazgos similares se encontraron en el estudio de Ahmad et al (15) con 200 mujeres con LES y 100 controles y en la cohorte de Pittsburg de Manzi et al (16), en la que determinaron la prevalencia de placa carotidea en 175 mujeres con LES. Roman et al (17), estudió la existencia de placa carotidea en 159 pacientes y analizó la existencia de nuevas placas o la progresión de estas en un seguimiento ecográfico de 3 años. Los resultados mostraron una tasa de progresión de 10% por año, dato que es más alto que el 5% de los individuos controles. En este estudio, también intentaron correlacionar la existencia de placa y la progresión de esta con diversas variables para intentar encontrar factores predictores de progresión de la ateroesclerosis y encontraron significación estadística con la edad al diagnóstico de LES, la duración de la enfermedad y los niveles de homocisteína.
Otro método empleado para detectar enfermedad coronaria asintomática es la determinación mediante tomografía computarizada (TC) del depósito de calcio en las arterias coronarias, que es un marcador de ateroesclerosis. Hay estudios que han demostrado que la calcificación coronaria y, por tanto, la ateroesclerosis asintomática, es más frecuente en pacientes con LES que en individuos sanos (18,19,20).
Trabajos realizados por Bruce et al (21) y por Nikpour et al (22) sugirieron que el estudio de la perfusión miocárdica mediante SPECT (Single Photon Emission Computed Tomography) podría ser un predictor de enfermedad coronaria, aunque al realizar una arteriografía a los pacientes con defectos de perfusión, se identificaron estenosis significativas en tan sólo el 38% de los pacientes (23).
Por otra parte, Moschetti et al (24) describe el importante papel que juega el endotelio en la patogénesis de la ateroesclerosis subclínica. Se han validado varias técnicas que determinan la función endotelial en la población general, midiendo la repuesta de la célula endotelial a estímulos farmacológicos o fisiológicos. Existen trabajos que demuestran esta disfunción endotelial determinada mediante la disminución de la dilatación mediada por flujo en pacientes con LES (25,26,27). Una de estas técnicas mide la vasodilatación endotelial mediada por óxido nítrico, en respuesta a la isquemia inducida cuando se hincha un manguito de presión, demostrando la asociación de la disfunción endotelial con la actividad de la enfermedad y la ateroesclerosis en pacientes con LES (25).
El grosor íntima-media (GIM) en arteria carótida común determinado mediante ecografía doppler ha sido aceptado como marcador precoz de ateroesclerosis subclínica (28) y parece estar asociado a incremento de riesgo de infarto de miocardio e ictus (29). En los pacientes con LES el papel del GIM ha sido más debatido. Son muchos los trabajos que han comparado las medidas de GIM en paciente con LES y en controles de características similares. Varios de estos trabajos han obtenido diferencias significativas, encontrando que el GIM era mayor en pacientes lúpicos y que aumentaba con la edad y con la mayor duración de la enfermedad, por lo que todos ellos propusieron que éste último parámetro sea utilizado para detectar estadios tempranos de ateroesclerosis subclínica (28, 30, 31 ,32, 33).
Por último, la velocidad de onda de pulso (VOP) mide elasticidad arterial, lo cual es importante porque alteraciones de la elasticidad arterial pueden traducir de forma precoz cambios que predispongan al desarrollo de patología vascular. Un metaanálisis de diecisiete estudios reveló que un incremento de la velocidad de onda pulso de 1m/s puede aumentar el riesgo cardiovascular en más de un 14% (34). Selzer et al (35) en 2001 fueron unos de los primeros en realizar un trabajo que evaluaba los factores de riesgo asociados con la pérdida de elasticidad arterial medida por VOP en mujeres con LES. Observó que la VOP estaba aumentada en los pacientes con mayor número de factores de riesgo CV previos. Posteriormente, el mismo autor demostró que la rigidez arterial estaba asociada con la edad, la presión arterial sistólica, enfermedad renal y otros marcadores como niveles elevados de C3, leucopenia e hiperinsulinemia (36). Tso et al (37) realizaron un estudio similar, cuyo objetivo era identificar la relación entre la VOP y los factores cardiovasculares, así como Shang et al (31) que evaluaron la relación entre la elasticidad arterial, la actividad de la enfermedad y el daño orgánico producido por el LES. En ambos estudios, las pacientes tenían incrementada la VOP en comparación con los controles y se correlacionaba con el índice de actividad del LES (SLEDAI) y con el índice de daño orgánico (SLICC/ACR). En un trabajo español de Sabio et al (38), se concluyó que los pacientes con LES y síndrome metabólico tenían mayor VOP comparados con aquellos sin síndrome metabólico, lo que sugiere que el síndrome metabólico debe contribuir al desarrollo de ateroesclerosis acelerada en el LES.
ATEROESCLEROSIS Y ACTIVIDAD EN EL LUPUS ERITEMATOSO SISTÉMICO
Parece claro que en el LES existe un aumento del riesgo de ateroesclerosis y aunque existen estudios que han demostrado un incremento en la prevalencia de factores de riesgo cardiovascular clásicos en estos pacientes, otros sugieren que el incremento del riesgo no es sólo atribuible a éstos y que existe un factor adicional que es la propia enfermedad y los factores relacionados con ella.
Hay trabajos importantes en los que también se relaciona un índice SLICC/ACR alto con la presencia de estenosis coronaria en angiografía y con incremento en el GIM (16,23). En el trabajo de Maksimowickz et al (39), observaron un aumento de la incidencia de placa carotidea no explicado por los factores de riesgo convencionales e identificaron la edad, la tensión arterial sistólica, los niveles de C3 elevados y una puntuación superior a 3 en el índice de daño orgánico como factores independientes para el desarrollo de arteriosclerosis. Otros estudios han relacionado el incremento de C3 con aumento de la velocidad onda-pulso (36) y con la rigidez arterial (31,37). En la población general, estudios como el de Muscari et al (40) han identificado también niveles de C3 como factor de riesgo independiente de infarto agudo de miocardio en hombres sin eventos isquémicos previos. Urowitz et al (5) identificaron como factores de riesgo relacionados con el LES, la presencia de vasculitis y de afectación neuropsiquiátrica. La enfermedad renal y el desarrollo de nefritis lúpica han sido asociadas con hipertensión e incremento del riesgo de arterioesclerosis. Muchos estudios han encontrado que la proteinuria mantenida está asociada al desarrollo de ateroesclerosis subclínica en el LES (14,41). La creatinina ha sido identificada como factor de riesgo por Maksimowickz-‐McKinnon et al (39), y en un estudio posterior de Thompson et al (42), como predictor independiente de progresión del GIM en pacientes con LES, sugiriendo que el daño renal contribuye o es un marcador de progresión de enfermedad cardiovascular.
Un factor importante a tener en cuenta en el desarrollo de ateroesclerosis en el LES es la relación con el tratamiento. El papel de los corticoides en el desarrollo de ateroesclerosis es controvertido. Por un lado, existen estudios que relacionan el tratamiento con corticoides con mayor ateroesclerosis, basándose en que la terapia con esteroides empeora los factores de riesgo clásicos, aumentando la incidencia de hipertensión, diabetes y empeorando el perfil lipídico (43) y que dosis altas de corticoides estaban asociadas a un aumento significativo del riesgo de enfermedad cardiovascular después de ajustar por la actividad y duración de la enfermedad (44). Sin embargo, otros observaron que una terapia intensiva mejoraba los mecanismos de inflamación del LES que también están implicados en el desarrollo de la ateroesclerosis (14). Por otra parte, los antipalúdicos (hidroxicloroquina) parecen ser “protectores”(1) por mejorar la afinidad entre la insulina y su receptor, mejorar el perfil lipídico y la disfunción endotelial, así como contribuir a la inhibición de la agregación plaquetaria (efecto antitrombótico).
CÉLULAS PROGENITORAS ENDOTELIALES Y LUPUS ERITEMATOSO SISTÉMICO
Un aspecto de crucial importancia para preservar la integridad del endotelio y prevenir la formación de la placa tras un daño vascular es el mantenimiento de una reparación vascular normal. La reparación vascular está mediada principalmente por las células progenitoras endoteliales (CPE) derivadas de médula ósea, que en respuesta a señales de estímulo indicativas de daño vascular son capaces de migrar a sangre periférica, proliferar y diferenciarse a células endoteliales maduras. Los individuos con disminución de CPE circulantes tienen mayor riesgo de enfermedad cardiovascular que los individuos con números normales de CPE (45) y la disminución de CPE se ha asociado con ateroesclerosis subclínica (46). En pacientes con LES existen varios estudios que describen una reducción del número de CPE e incluso una funcionalidad celular alterada (47), sugiriendo a las CPE como un posible marcador de daño endotelial (48) y de ateroesclerosis subclínica (49,50).
CONCLUSIONES
En el lupus eritematoso sistémico está demostrado que existe una ateroesclerosis precoz y acelerada que se manifiesta en forma de enfermedad cardiovascular. En la evaluación de estos pacientes se deben tener en cuenta factores de riesgo tradicionales, así como los tratamientos administrados y la actividad de la enfermedad, relacionados con la existencia de inflamación crónica. Es fundamental la demostración de enfermedad subclínica, dadas las implicaciones terapéuticas y pronósticas que plantea, a través de la investigación de biomarcadores que permitan identificar a aquellos pacientes que presenten un mayor riesgo de enfermedad cardiovascular y en los que se debe considerar el cambio de estilo de vida y el uso racional de hidroxicloroquina, ácido acetilsalicílico a dosis bajas, IECAs/ARA II y estatinas / fibratos.
AGRADECIMIENTOS
A los pacientes y profesionales de la Unidad de Enfermedades Autoinmunes Sistémicas del Servicio de Medicina Interna del Hospital Universitario Puerta de Hierro Majadahonda.
FINANCIACIÓN
Este trabajo ha sido parcialmente financiado por la Fundación Española Medicina Interna (FEMI 2020) a través del proyecto “Nutrición de precisión en pacientes con enfermedades autoinmunes sistémicas y con síndrome metabólico” y por el proyecto “Metacategorización personalizada de procesos inflamatorios asociados a síndrome metabólico, enfermedades autoinmunes y virales para medicina de precision” (METAINFLAMACIÓN, Ref: Y2020/BIO-6600) de la Comunidad de Madrid.
DECLARACIÓN DE TRANSPARENCIA
El autor/a de este artículo declara no tener ningún tipo de conflicto de intereses respecto a lo expuesto en el presente trabajo.
BIBLIOGRAFÍA
- ↑McMahon M, Seto R, Skaggs BJ. Cardiovascular disease in systemic lupus erythematosus. Rheumatol Immunol Res. 2021; 2(3): 157-172.
- ↑Abu-Shakra M, Urowitz MB, Gladman DD, Gough J. Mortality studies in systemic lupus erythematosus. Results from a single center. I. Causes of death. J Rheumatol. 1995; 22(7): 1259-1264.
- ↑Urowitz M, Bookman A, Koehler B, Gordon D, Smythe HA, Ogryzlo MA. The bimodal mortality pattern of systemic lupus erythematosus. Am J Med. 1976; 60(2): 221-225.
- ↑Manzi S, Meilahn E, Rairie J et al. Age-specific incidence rates of myocardial infarction and angina in women with systemic lupus erythematosus: Comparison with Framingham study. Am J Epidemiol. 1997; 145(5): 408-415.
- ↑Urowitz M, Ibañez D, Gladman D. Atherosclerotic vascular events in a single large lupus cohort: Prevalence and risk factors. J Rheumatol. 2007; 34(1): 70-75.
- ↑Samuelsson I, Parodis I, Gunnarson I et al. Myocardial infarctions, subtypes and coronary atherosclerosis in SLE: a case-control study. Lupus Sci Med. 2021; 8(1): e000515.
- ↑Fischer LM, Schlienger RG, Matter C, Jick H, Meier CR. Effect of rheumatoid arthritis or systemic lupus erythematosus on the risk of first-time acute myocardial infarction. American J Cardiol. 2004; 93(2): 198-200.
- ↑Lee YH, Choi SJ, Ji JD, Song GG. Overall and cause-specific mortality in systemic lupus erythematosus: an updated meta-analysis. Lupus. 2016; 25(7): 727-734.
- ↑Moreno-Torres V, Tarín C, Ruiz-Irastorza G et al. Trends in hospital admissions and death causes in patients with systemic lupus erythematosus: Spanish national registry. J Clin Med. 2021; 10(24): 5749.
- ↑Petri M, Pérez-Gutthann S, Spence D, Hochberg MC. Risk factors for coronary artery disease in patients with systemic lupus erythematosus. Am J Med. 1992; 93(5): 513-519.
- ↑Ballocca F, D´Ascenzo F, Moretti C et al. Predictors of cardiovascular events in patients with systemic lupus erythematosus (SLE): a systematic review and meta-analysis. Eur J Prev Cardiol. 2015; 22(11): 1435-1441.
- ↑Papamichael CM, Lekakis JP, Stamatelopoulos KS et al. Ankle-brachial index as a predictor of the extent of coronary atherosclerosis and cardiovascular events in patients with coronary artery disease. Am J Cardiol. 2000; 86(6): 615-618.
- ↑Theodoridou A, Bento L, D’Cruz D, Khamashta MA, Hughes GRV. Prevalence and associations of an abnormal ankle-brachial index in systemic lupus erythematosus: a pilot study. Ann Rheumatic Dis. 2003; 62(12): 1199-1203.
- ↑Roman MJ, Shanker BA, Davis A et al. Prevalence and correlates of accelerated atherosclerosis in systemic lupus erythematosus. N Engl J Med. 2003; 349(25): 2399-2406.
- ↑Ahmad Y, Bruce IN. Subclinical atherosclerosis in systemic lupus erythematosus. J Rheumatol. 2004; 31(5): 841-843.
- ↑Manzi S, Selzer F, Sutton-Tyrrell K et al. Prevalence and risk factors of carotid plaque in women with systemic lupus erythematosus. Arthritis Rheum. 1999; 42(1): 51-60.
- ↑Roman MJ, Crow MK, Lockshin MD et al. Rate and determinants of progression of atherosclerosis in systemic lupus erythematosus. Arthritis Rheum. 2007; 56(10): 3412-3419.
- ↑Asanuma Y, Oeser A, Shintani AK et al. Premature coronary-artery atherosclerosis in systemic lupus erythematosus. N Engl J Med. 2003; 349(25): 2407-2415.
- ↑Kiani AN, Magder L, Petri M. Coronary calcium in systemic lupus erythematosus is associated with traditional cardiovascular risk factors, but not with disease activity. J Rheumatol. 2008; 35(7): 1300-1306.
- ↑Yiu KH, Wang S, Mok MY et al. Pattern of arterial calcification in patients with systemic lupus erythematosus. J Rheumatol. 2009; 36(10): 2212-2227.
- ↑Bruce IN, Burns RJ, Gladman DD, Urowitz MB. Single photon emission computed tomography dual isotope myocardial perfusion imaging in women with systemic lupus erythematosus. I. Prevalence and distribution of abnormalities. J Rheumatol. 2000; 27(10): 2372- 2377.
- ↑Nikpour M, Gladman DD, Ibañez D, Bruce IN, Burns RJ, Urowitz MB. Myocardial perfusion imaging in assessing risk of coronary events in patients with systemic lupus erythematosus. J Rheumatol. 2009; 36(2): 288-294.
- ↑Sella EM, Sato EI, Leite WA, Oliveira JA, Barbieri A. Myocardial perfusion and coronary disease risk factors in systemic lupus erythematosus. Ann Rheum Dis. 2003; 62(11): 1066-1070.
- ↑Moschetti L, Piantoni S, Vizzardi E et al. Endothelial dysfunction in systemic lupus erythematosus and systemic sclerosis: a common trigger for different microvascular diseases. Front Med. 2022; 9: 849086.
- ↑Lima DS, Sato EI, Lima VC, Miranda F Jr, Hatta FH. Brachial endothelial function is impaired in patients with systemic lupus erythematosus. J Rheumatol. 2002; 29(2): 292-297.
- ↑El-Magadmi M, Bodill H, Ahmad Y et al. Systemic lupus erythematosus: an independent risk factor for endothelial dysfunction in women. Circulation. 2004; 110(4): 399-404.
- ↑Valdivielso P, Gómez-Doblas JJ, Macias M et al. Lupus-associated endotelial dysfunction, disease activity and arteriosclerosis. Cli Exp Rheumatol. 2008; 26(5): 827-833.
- ↑Poredos P. Intima-media thickness: indicator of cardiovascular risk and measure of the extent of atherosclerosis. Vasc Med. 2004; 9(1): 46-54.
- ↑O’Leary DH, Polak JF, Kronmal RA, Manolio TA, Burke GL, Wolfson SK Jr. Carotid-artery intima and media thickness as a risk factor for myocardial infarction and stroke in older adults. Cardiovascular Health Study Collaborative Research Group. N Engl J Med. 1999; 340(1): 14-22.
- ↑De Leeuw K, Smit AJ, De Groot E, Van Roon AM, Kallenberg CG, Bijl M. Longitudinal study on premature atherosclerosis in patients with systemic lupus erythematosus. Atherosclerosis. 2009; 206(2): 546-550.
- ↑Shang Q, Tam LS, Li EK, Yip GW, Yu CM. Increased arterial stiffness correlated with disease activity in systemic lupus erythematosus. Lupus. 2008; 17(12): 1096-1102.
- ↑Colombo BM, Murdaca G, Caiti M et al. Intima-media thickness: a marker of accelerated atherosclerosis in women with systemic lupus erythematosus. Ann N Y Acad Sci. 2007; 1108: 121-126.
- ↑Wu G-C, Liu H-R, Leng R-X et al. Subclinical atherosclerosis in patients with systemic lupus erythematosus: a systemic review and meta-analysis. Autoimmun Rev. 2016; 15(1): 22-37.
- ↑Vlachopoulos C, Aznaouridis K, Stefanadis C. Prediction of cardiovascular events and all-cause mortality with arterial stiffness: a systematic review and meta-analysis. J Am Coll Cardiol. 2010; 55(13): 1318-1327.
- ↑Selzer F, Sutton-Tyrrell K, Fitzgerald S, Tracy R, Kuller L, Manzi S. Vascular stiffness in women with systemic lupus erythematosus. Hypertension. 2001; 37(4): 1075-1082.
- ↑Selzer F, Sutton-Tyrrell K, Fitzgerald SG et al. Comparison of risk factors for vascular disease in the carotid artery and aorta in women with systemic lupus erythematosus. Arthritis Rheum. 2004; 50(1): 151-159.
- ↑Tso TK, Huang WN, Huang HY, Chang CK. Association of brachial-ankle pulse wave velocity with cardiovascular risk factors in systemic lupus erythematosus. Lupus. 2005; 14(11): 878-883.
- ↑Sabio JM, Vargas-Hitos J, Zamora-Pasadas M et al. Metabolic syndrome is associated with increased arterial stiffness and biomarkers of subclinical atherosclerosis in patients with systemic lupus erythematosus. J Rheumatology. 2009; 36(10): 2204-2211.
- ↑Maksimowicz-McKinnon K, Magder LS, Petri M. Predictors of carotid atherosclerosis in systemic lupus erythematosus. J Rheum. 2006; 33(12): 2458-2463.
- ↑Muscari A, Bozzoli C, Puddu GM et al. Association of serum C3 levels with the risk of myocardial infarction. Am J Med. 1995; 98(4): 357-364.
- ↑Manger K, Kusus M, Forster C et al. Factors associated with coronary artery calcification in young female patients with SLE. Ann Rheum Dis. 2003; 62(9): 846-850.
- ↑Thompson T, Sutton-Tyrrell K, Wildman RP et al. Progression of carotid intima-media thickness and plaque in women with systemic lupus erythematosus. Arthritis Rheum. 2008; 58(3): 835-842.
- ↑Bulkley BH, Roberts W. The heart in systemic lupus erythematosus and the changes induced in it by corticosteroid therapy: a study of 36 necropsy patients. Am J Med. 1975; 58(2): 243-264.
- ↑Karp I, Abrahamowicz M, Fortin PR et al. Recent corticosteroid use and recent disease activity: Independent determinants of coronary heart disease risk factors in systemic lupus erythematosus? Arthritis Rheum. 2008; 59(2): 169-175.
- ↑Werner N, Kosiol S, Schiegl T et al. Circulating endothelial progenitor cells and cardiovascular outcomes. N Engl J Med. 2005; 353(10): 999-1007.
- ↑Chironi G, Walch L, Pernollet MG et al. Decreased number of circulating CD34+KDR+ cells in asymptomatic subjects with preclinical atherosclerosis. Atherosclerosis. 2007; 191(1): 115-120.
- ↑Baker JF, Zhang L, Imadojemu S et al. Circulating endothelial progenitor cells are reduced in SLE in the absence of coronary artery calcification. Rheumatol Int. 2012; 32(4): 997-1002.
- ↑Robak E, Kierstan M, Cebula B et al. Circulating endothelial cells and angiogenic proteins in patients with systemic lupus erythematosus. Lupus. 2009; 18(4): 332-341.
- ↑Castejón R, Jiménez-Ortiz C, Rosado S, Tutor-Ureta P, Mellor-Pita S, Yebra-Bango M. Metabolic syndrome is associated with decreased circulating endothelial progenitor cells and increased arterial stiffness in systemic lupus erythematosus. Lupus. 2016; 25 (2): 129-136.
- ↑Castejón R, Jiménez-Ortiz C, Valero-González S, Rosado S, Mellor-Pita S, Yebra-Bango M. Decreased circulating endothelial progenitor cells as an early risk factor of subclinical atherosclerosis in systemic lupus erythematosus. Rheumatology. 2014; 53(4): 631-638.
ranm tv
Juan Antonio Vargas Núñez
Servicio de Medicina Interna. Hospital Puerta de Hierro Majadahonda
C/ Joaquín Rodrigo 1 · 28222 Majadahonda-Madrid
Tlf.: +34 661 786 885 | E-Mail: juanantonio.vargas@uam.es
An RANM. 2023;140(01):24-30
Enviado*: 08.11.22
Revisado: 28.11.22
Aceptado: 10.12.22
* Fecha de lectura en la RANM


