Resumen
La TC espectral ha supuesto una mejora diagnóstica reciente de esta modalidad de imagen. El objetivo de esta revisión crítica narrativa es analizar la variabilidad y utilidad clínica de las unidades Hounsfield en los estudios de TC espectral, dada su dependencia en función de la energía del haz de fotones empleado. Para la TC espectral definiremos las diferentes formas de reconstruir las imágenes y los mapas paramétricos que se pueden obtener para diagnosticar patologías tan prevalentes como la esteatosis hepática, caracterizar la composición de la litiasis, diferenciar la naturaleza de las complicaciones tras procedimientos y determinar la agresividad de lesiones tumorales. La capacidad de resolver diversas composiciones tisulares de la TC espectral hace que sea un método fiable para caracterizar lesiones al establecer su composición tisular por la información espectral. Las imágenes monoenergéticas a bajas energías permiten aumentar el contraste de tejidos blandos y fácilmente identificar tejidos con alta captación de contraste yodado. Las reconstrucciones a energías altas son útiles para reducir el artefacto metálico de las prótesis e implantes y diferenciar captación de contraste de depósitos de calcio que presentan una alta atenuación. Usando los datos espectrales además podemos obtener mapas paramétricos de contraste yodado, mapas de ácido úrico en las litiasis renoureterales y las artropatías por depósito y otros materiales en enfermedades tumorales y metabólicas.
Abstract
Dual energy CT is a recent upgrade to this diagnostic imaging technique. The purpose of this critical narrative review is to lay out the clinical applications of Hounsfield Units and their variation across the x-ray energy spectrum using DECT. We explore new reconstruction methods and parametric maps helpful for the diagnosis of prevalent pathologies such as fatty liver disease, urolithiasis, and to identify complications after interventions or determine the aggressiveness of tumoral lesions. The energy-resolving capabilities of DECT make it a reliable method for the characterisation of tissue and lesion composition. Lower energy monoenergetic images allow us to increase soft tissue contrast and easily identify tissues with higher contrast uptake. Higher energy monoenergetic images are useful to distinguish between contrast uptake and high attenuation calcium deposits and for metal artifact reduction. Parametric images showing uric acid, iodine, calcium, and other material decompositions can be obtained from spectral data for the diagnosis of tumoral or metabolic diseases, vascular lesions and characterisation of deposition arthritis and urolithiasis.
Palabras clave: Unidades Hounsfield; Tomografía computarizada; Yodo; Espectral.
Keywords: Hounsfield Units; Computed Tomography; Lodine; DECT.
INTRODUCCIÓN
Las unidades Hounsfield (UH) se emplean en los estudios de tomografía computarizada (TC) para medir de forma cuantitativa la atenuación de las estructuras y órganos en el sujeto de estudio. Aunque es una unidad estandarizada, para su evaluación deben considerarse los diversos factores que influyen en su valor cuando se obtienen con diferentes protocolos, parámetros y equipos de TC. El principal factor que afecta al valor de esta medida es la energía del haz de rayos X empleado en la adquisición de las imágenes. La incorporación de la TC espectral, con su capacidad para analizar la composición tisular de forma cuantitativa en función de la energía del haz de rayos X, hace relevante la revisión de esta información y la dependencia las UH obtenidas de los tejidos con la variación de la energía empleada para reconstruir las imágenes.
Nuestro objetivo principal en este trabajo es estudiar pues la variabilidad asociada a la cuantificación de las UH en las imágenes de TC y, en particular, el caso de uso de la TC espectral y sus reconstrucciones convencionales y monoenergéticas. Como objetivos secundarios se ilustrará como se obtienen las UH en entornos clínicos habituales y los factores que modifican su valor a diferentes energías. Se describirán también los criterios que permiten la caracterización de los diferentes tejidos biológicos en función de sus UH, las reconstrucciones que pueden obtenerse con las diferentes energías del TC espectral, y diferentes casos de uso de estas variaciones en las UH para diversas entidades patológicas.
Coeficiente de atenuación y unidades Hounsfield
Las imágenes de TC representan la reconstrucción del coeficiente de atenuación de los tejidos al paso de los rayos X. Este valor se obtiene a partir de la medida de la radiación emitida que logra atravesar los tejidos y llegar a los detectores. La diferencia entre la intensidad de la radiación emitida y la que llega al detector depende del coeficiente de atenuación y del grosor del material interpuesto en el trayecto del haz. Esta dependencia sigue una función exponencial (Ley de Lambert-Beer), donde se relaciona la intensidad transmitida (I) para un haz monoenergético de intensidad incidente (I0) al atravesar un material de coeficiente de atenuación (μ) y grosor conocido (x).
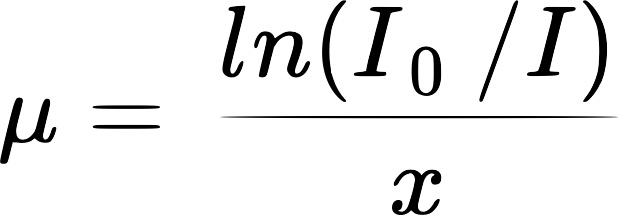
Por su parte, el coeficiente de atenuación depende del número atómico y la densidad del material interpuesto, estando determinado por la energía incidente. Por ejemplo, el coeficiente de atenuación para el agua tiene un valor de 1,84·102 cm-1 para 80 keV, mientras que para 120 keV su valor es 1,22·102 cm-1.
La atenuación del haz de rayos X se produce por la interacción de una parte de los fotones emitidos con el material que atraviesan, pudiendo ser dispersados o absorbidos, sin lograr alcanzar el detector. En el rango de las energías empleadas en radiología (20-200 keV) ocurren principalmente dos tipos de interacciones responsables de esta atenuación: el efecto fotoeléctrico y el efecto Compton.
El efecto fotoeléctrico se observa principalmente a energías bajas cuando un fotón experimenta una colisión con un electrón y lo desplaza de su orbital, quedando el fotón absorbido y liberándose el electrón. Cuando mayor es el número atómico del material, mayor es la energía necesaria para desplazar los electrones de sus orbitales y mayor la probabilidad de efecto fotoeléctrico. Por su lado, el efecto Compton ocurre cuando un fotón interacciona con un electrón de las capas más externas, transfiriendo parte de su energía cinética al dispersarse. Ambas interacciones son responsables de la atenuación del haz y su probabilidad de ocurrencia aumenta con la densidad del material. Gracias a esta dependencia podemos distinguir entre los distintos materiales atravesados por el haz de rayos X (1).
En los inicios de la TC se propuso una escala representativa de los posibles valores de atenuación, desde el aire (-1000) cuya atenuación es despreciable, con el agua como línea de base (Valor 0) y extendiéndose hasta infinito. Las unidades de cuantificación de los coeficientes de atenuación se conocen como unidades Hounsfield (UH). Estas UH son pues una transformación del coeficiente de atenuación del tejido estudiado, normalizado al coeficiente de atenuación del agua (2).
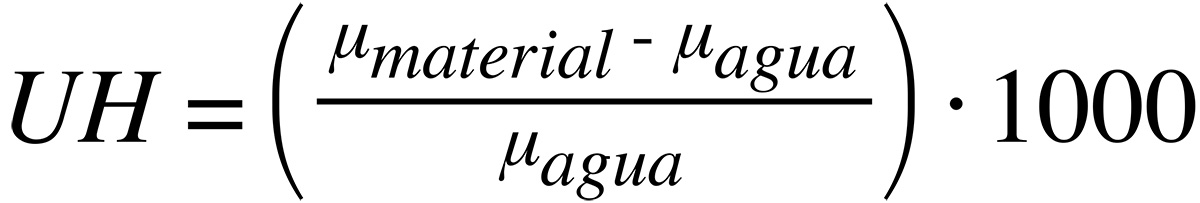
De esta expresión se deduce que las UH dependen de la energía del haz de rayos X. Por ello, y como ejemplo, dado un coeficiente de atenuación para el tejido adiposo (1,80·102 cm-1 para 80 keV y 1,61·102 cm-1 para 120 keV), sus UH varían entre -69 y -58 para 80 keV y 120 keV, respectivamente (3). Es decir, las UH no son medidas absolutas sino relativas.
La ley de Lambert-Beer es válida para un haz de rayos X monoenergético. Sin embargo, el tubo de rayos X de un equipo de TC emite haces multienergéticos, cuya energía máxima se corresponde con el kilovoltaje aplicado al tubo. Dado que en los escáneres TC convencionales no se puede discernir la energía del haz, su capacidad de caracterización tisular está limitada pues diferentes tejidos pueden presentar coeficientes de atenuación similares. La TC espectral es una tecnología capaz de extraer esta información para mejorar la caracterización de los tejidos (4).
Caracterización de tejidos mediante UH en el TC convencional
En TC convencional la caracterización de componentes tisulares está estandarizada a una adquisición de 120 kVp de energía. Estas UH han sido de gran utilidad para caracterizar diversas patologías como las litiasis renales (5), facilitando la elección del tratamiento óptimo (6), detectar la esteatosis hepática (7), establecer el diagnóstico de adenoma suprarrenal (8), y evaluar el riesgo coronario en función de la cantidad de grasa epicárdica y pericoronaria (9). En los accidentes cerebrovasculares se pueden utilizar para estimar el riesgo de vasoespasmo en la hemorragia subaracnoidea (10), el diagnóstico de la oclusión vascular (11) y el pronóstico de la hemorragia intraparenquimatosa (12). Ayudan a la distinción entre líquidos serosos y de contenido hemático o purulento, apoyando la diferenciación de pionefrosis frente a hidronefrosis (13), siendo de utilidad para caracterizar nódulos pulmonares y tiroideos (14)(15). La cuantificación de calcio coronario, la caracterización de placas ateroscleróticas, y objetivar el atrapamiento aéreo y el enfisema pulmonar son otras capacidades (16)(17). Permiten también cuantificar la densidad mineral ósea (18) y determinar la calidad ósea previa la instrumentación para predecir déficits de unión del material de osteosíntesis en cirugías ortopédicas (19) además de caracterizar la sarcopenia y mioesteatosis (20). Es decir, han tenido tradicionalmente una gran importancia en muchas aplicaciones clínicas pese a la incertidumbre conocida de que dos materiales de distinta composición puedan mostrar UH similares, incluso con densidad y número atómico distintos.
Caracterización de tejidos mediante UH en el TC espectral
La resolución energética es la capacidad de diferenciar atenuaciones diferentes a distintas energías. La TC espectral mejora este aspecto, aportando más información diagnóstica sobre el coeficiente de atenuación de cada material frente a la TC convencional (21). Existen diferentes modelos de adquirir TC espectral, en función de si existen dos fuentes independientes, cada una disparando un espectro de energía, si la fuente posee un filtro dividido que permite generar dos espectros energéticos distintos simultáneamente, si una sola fuente dispara dos espectros de energía diferentes de forma alternante, o si hay una única fuente, pero el detector es capaz de detectar un espectro energético de alta o baja energía (Figura 1) (1). En un generador de rayos X, el voltaje pico hace referencia al potencial máximo del tubo de rayos X, y se corresponde con la energía de los fotones más energéticos del haz. Al modificar la energía, por ejemplo, pasando de 120 kVp a 80 kVp, el espectro energético es distinto, modificando los valores de UH obtenidos en la imagen.
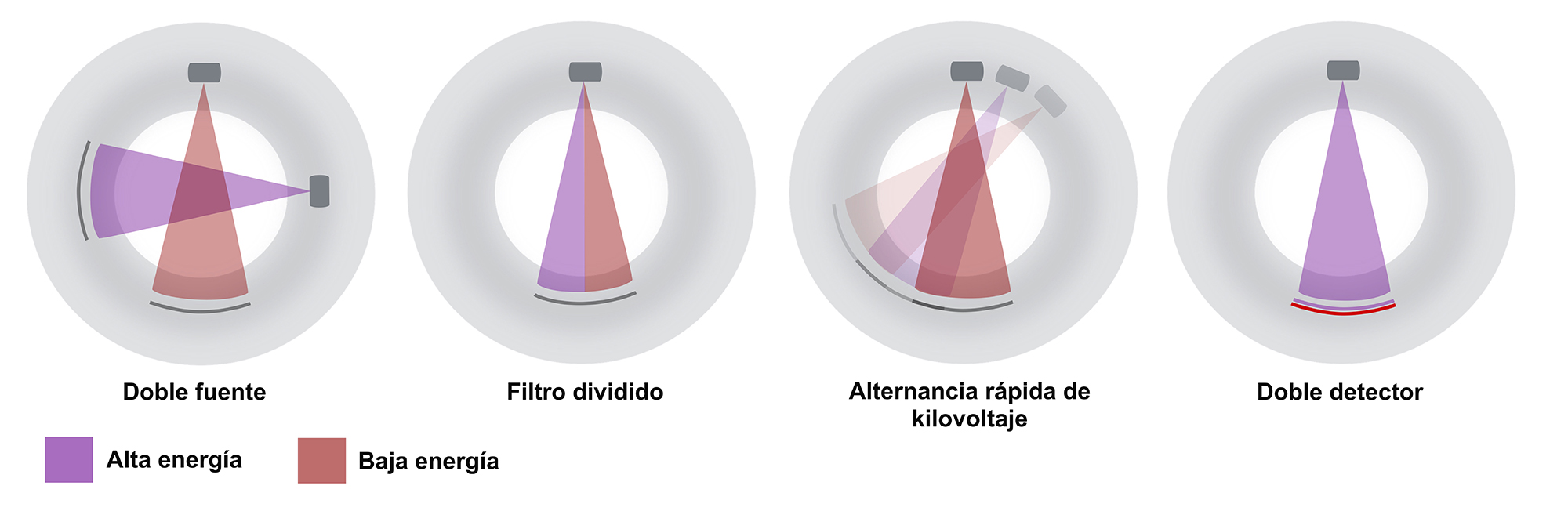
La TC espectral puede reconstruir imágenes convencionales polienergéticas, pero también imágenes monoenergéticas, que le confieren nuevas funcionalidades. Así, permite la obtención de imágenes virtuales sin contraste (23), aumenta la visualización del contraste en las imágenes de baja energía, y minimiza el artefacto del endurecimiento del haz causado por el material metálico con las reconstrucciones de alta energía (22). La mayor resolución energética también mejora la caracterización de materiales, posibilitando la cuantificación de yodo, calcio, grasa, hierro, de relevancia para el diagnóstico de enfermedades metabólicas, lesiones vasculares, caracterización de tumores y predicción de complicaciones hemorrágicas tras revascularizaciones (24)(25)(26). También ha demostrado su superioridad en la cuantificación de la grasa hepática en la esteatosis, en la sarcopenia (20)(25), y en la caracterización de la composición de litiasis (27)(28), además de la cuantificación más precisa del contenido de hierro hepático (29). Por su naturaleza análoga a la absorciometría de rayos X de doble energía (DEXA), permite la cuantificación de la densidad mineral ósea y permite mejorar el despistaje oportunista de osteoporosis, la caracterización de depósitos minerales en artropatías por depósito, y detectar el edema óseo con imágenes de sustracción de calcio (25).
MATERIALES Y MÉTODOS
Se procedió con una revisión bibliográfica mediante una búsqueda semiestructurada a través de las bibliotecas PubMed, Google Scholar y Cochrane Library, utilizando los términos “Hounsfield Units”, “CT Number”, “Spectral CT” y “Dual-energy CT” de forma aislada y en combinación con “Abdominal imaging”, “Neuroradiology”, “Chest”, “Head and neck”, “MSK”. Se accedió a nuevos artículos y estudios a través de la bibliografía de los artículos seleccionados en un primer momento.
Los casos clínicos que se presentan como ejemplos se han obtenido en el Hospital Universitario y Politécnico La Fe en un equipo Spectral CT 7500 (Philips Iberia) (Tabla 1). Las pruebas de aceptación del equipo se realizaron siguiendo el Protocolo Español de Control de Calidad en Radiodiagnóstico (SEFM, SPR, SERAM 2011). Se obtuvo la aprobación del comité de ética del centro para la obtención de forma retrospectiva de los casos mostrados.
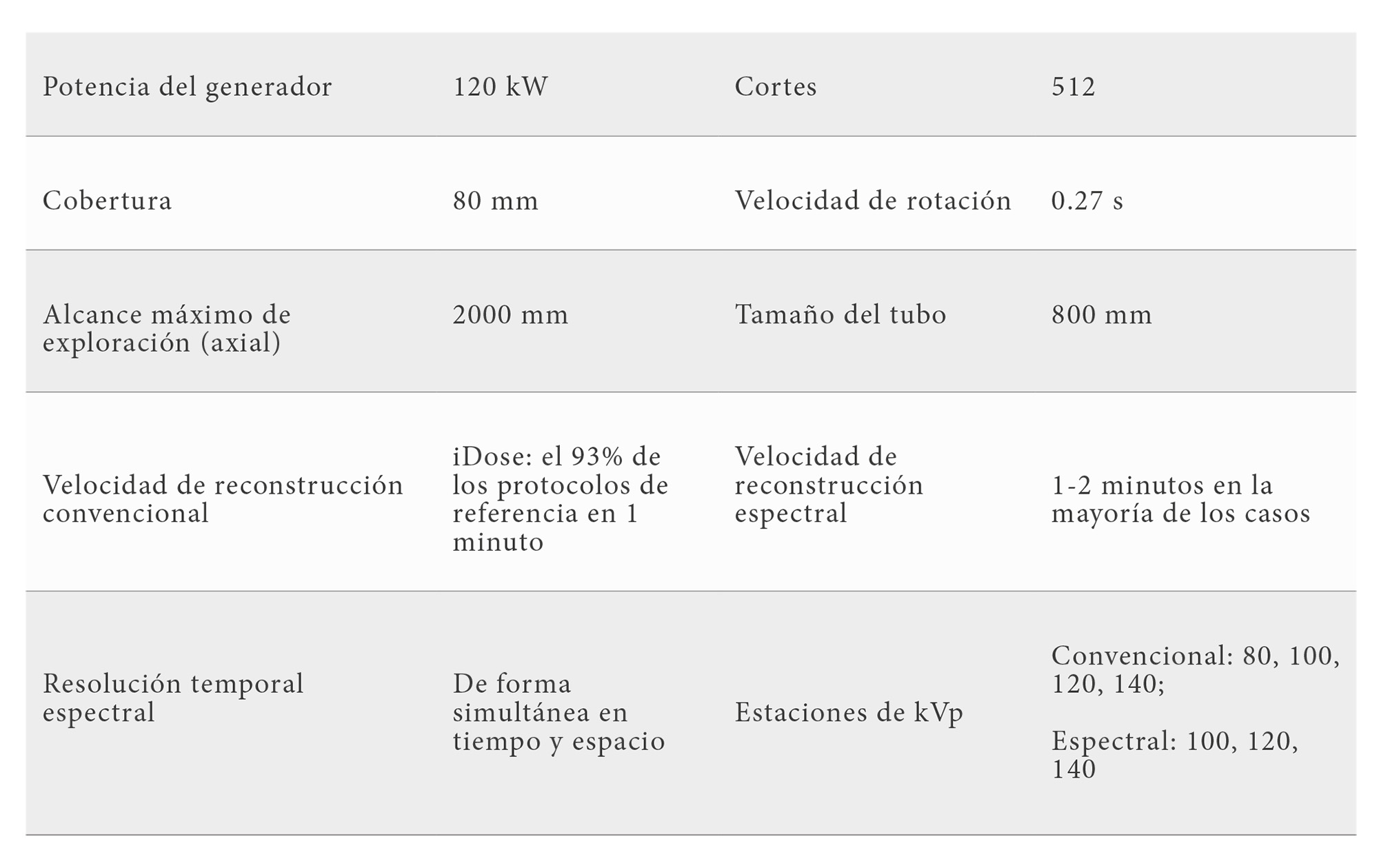
Para establecer las habilidades espectrales del equipo y establecer valores de referencia para la incertidumbre asociada a la estimación de las HU, se realizaron diversas adquisiciones a 100, 120 y 140 kVp con el maniquí “Electron Density Phantom Model 062M”. Este dispositivo contiene 16 tubos representativos de 8 tejidos biológicos (pulmón en inhalación y en exhalación, hígado, hueso trabecular, hueso cortical, grasa, mama y agua), distribuyéndose de forma que existe un tubo de cada tejido en la zona externa del maniquí y otro en la interna para conocer el error por endurecimiento del haz en el cálculo de las UH en las distintas regiones de interés (internas respecto a externas).
Los estudios se procesaron y visualizaron mediante el portal de software Philips IntelliSpace, obteniendo imágenes convencionales, monoenergéticas, sin contraste virtual (VNC) y mapas paramétricos de número atómico efectivo y densidad de yodo/urato. Para producir los gráficos de energía-atenuación mostrados se exportaron los datos de UH en intervalos de 10keV de las regiones de interés como archivo CSV anonimizado. Todas las imágenes y figuras son originales.
RESULTADOS
Maniquí
Las imágenes de los maniquíes se obtuvieron en condiciones clínicas habituales y se reconstruyeron a energía monoenergética de 40 keV con las curvas de atenuación para todo el espectro (40 – 200 keV) (Figura 2). El componente agua, al emplearse como referencia para estandarizar las UH del resto de tejidos, presenta una atenuación plana en 0 UH.
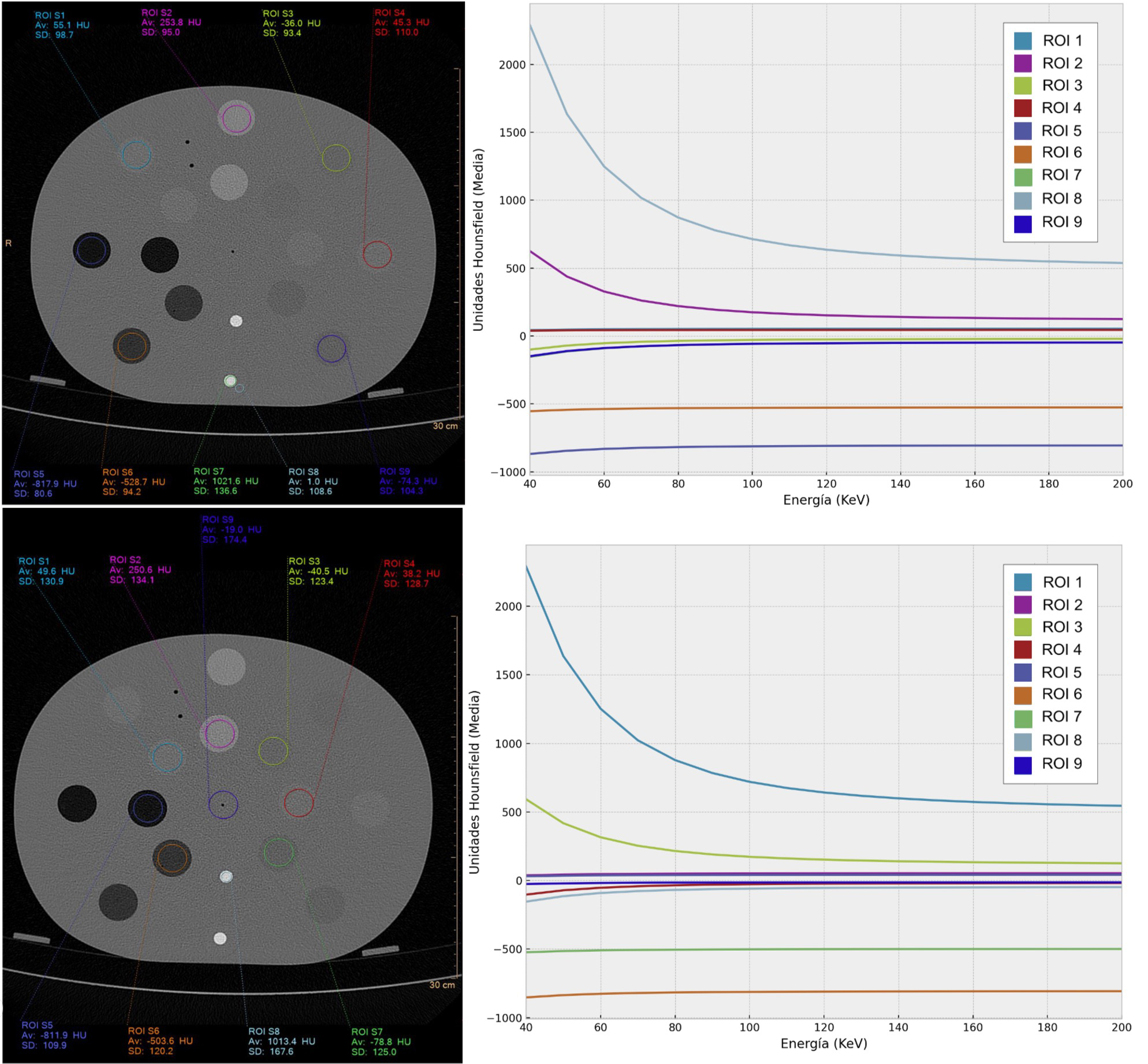
Las curvas de energía atenuación muestran el comportamiento de tejidos conocidos y nos permiten conocer el impacto del artefacto de atenuación del haz.
La grasa presenta una bajada de la atenuación a bajas energías en contraposición a las estructuras con alto contenido en calcio, como el hueso cortical y el esponjoso, para los que aumenta.
Para comprobar la precisión de estos datos los contrastamos con las curvas de la base de referencia estándar (3). En general se observa buena concordancia entre los valores suministrados por las distintas adquisiciones (a 100, 120 y 140 kVp) y los valores teóricos según el National Institute of Standards and Technology (NIST) (3).
Cabe destacar que cuando comparamos los insertos internos de los externos de un mismo material las diferencias son pequeñas, por tanto, con los equipos espectrales se consigue reducir el efecto de endurecimiento con el espectro energético.
Casos de Uso
Se exponen diferentes patologías representativas en las que los datos espectrales contribuyen a la caracterización de tejidos y componentes.
Adenoma adrenal
Se expone un hallazgo incidental en un estudio de TC sin contraste intravenoso donde se observó una lesión hipodensa en glándula suprarrenal derecha. La lesión muestra una densidad <10 HU, lo que orienta a adenoma con contenido lipídico. La curva espectral muestra una caída en la atenuación a energías bajas, característica de su contenido graso (Figura 3). Esta evaluación es independiente de la administración de contraste yodado, ya que la TC espectral puede diferenciar la captación del contraste yodado del componente lipídico mediante la reconstrucción virtual sin contraste.
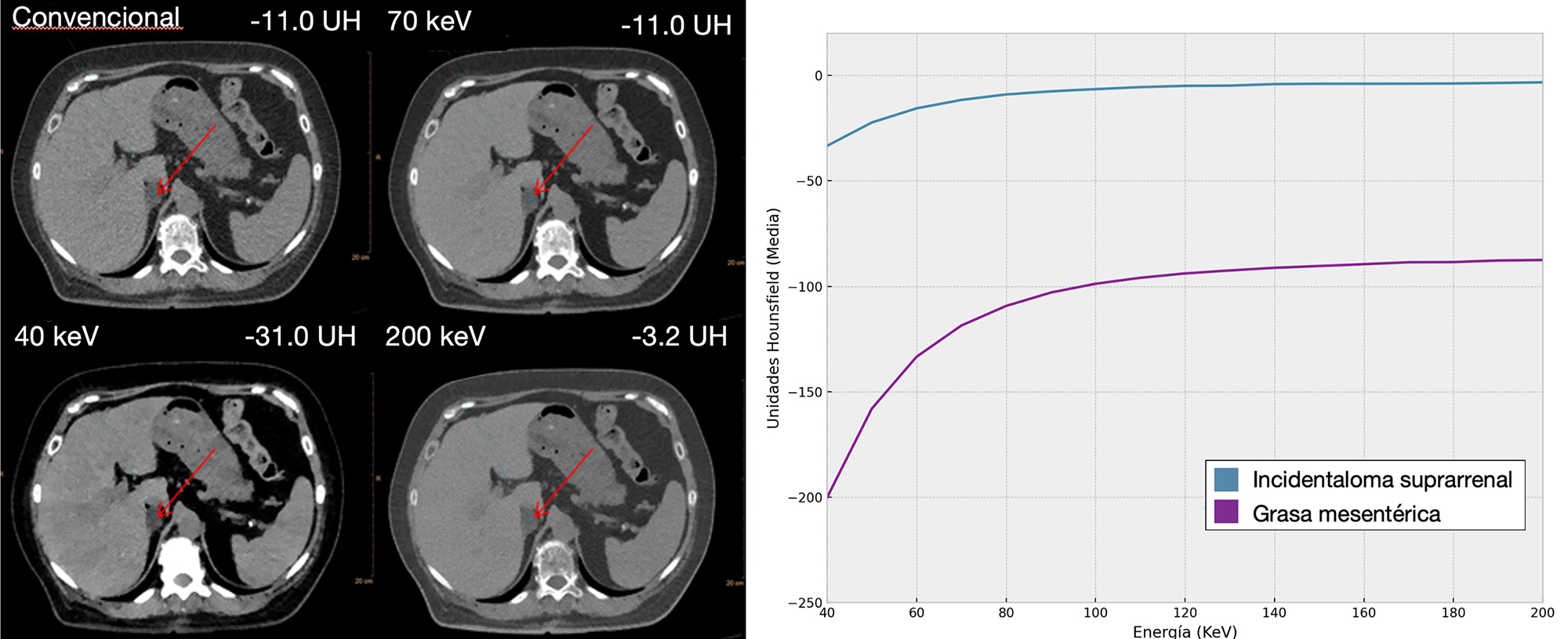
Comparamos las unidades Hounsfield de un incidentaloma suprarrenal con la grasa mesentérica. Ambos muestran un aumento de UH a mayor energía, morfología que describen los materiales con contenido lipídico.
Esteatosis hepática
En estudio con TC convencional sin contraste, una atenuación del parénquima hepático menor de 50 UH es específica para la esteatosis. La TC espectral permite obtener curvas de energía-atenuación e imágenes sin contraste virtual. En las curvas obtenidas, la caída de UH a bajas energías caracteriza al elevado contenido lipídico en la región de interés (Figura 4) frente a un hígado control normal sin esteatosis. Existen métodos de postproceso que aprovechan este efecto para estimar la fracción grasa empleando algoritmos de descomposición empleando la atenuación de materiales de composición conocida (agua, grasa, parénquima hepático sano) para estimar la proporción grasa (20).
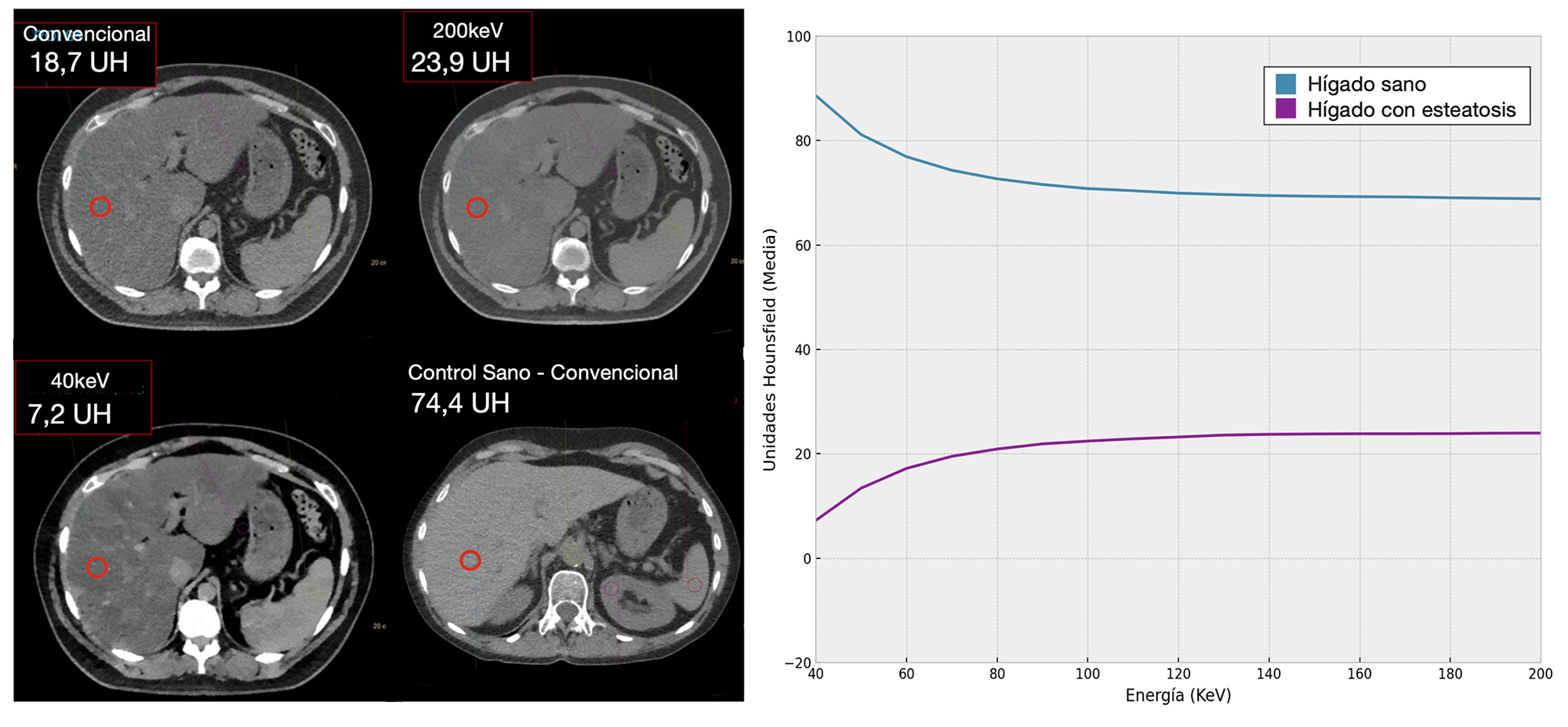
Si comparamos la curva descrita por el hígado sano y el que tiene esteatosis observamos que muestra una atenuación disminuida y una curva ascendente, que nos permite estimar la porción grasa.
Hemorragia intracraneal vs. extravasación de contraste
Una paciente sometida a embolización programada por aneurisma de arteria cerebral posterior con Cianoacrilato y Lipiodol presentó en los controles de TC sin contraste áreas hiperdensas que pueden corresponderse a hemorragia o a contraste extravasado. Las imágenes monoenergéticas a energías más altas reducen el artefacto de endurecimiento del haz causado por el material de embolización. Las imágenes virtuales sin contraste y los mapas de yodo confirman la presencia y estiman la concentración de yodo en el área de atenuación incrementada del lóbulo occipital (Figura 5). El mapa virtual sin contraste muestra la supresión de esta zona. En la imagen de densidad de yodo se evidencia la extravasación del contraste y permite caracterizar el hematoma. Nótese la falta de supresión del material de contraste en el mapa de densidad de yodo debido a la naturaleza yodada del Lipiodol. La imagen del número atómico muestra un valor más elevado, aportando seguridad en el diagnóstico. Si analizamos las curvas de energía atenuación para las cuatro regiones de interés encontramos una disminución acentuada de UH a energías más altas de las regiones con material de embolización (ROI 1) y extravasación de contraste (ROI 4) en comparación a al hueso (ROI 2) y al hematoma (ROI 3).
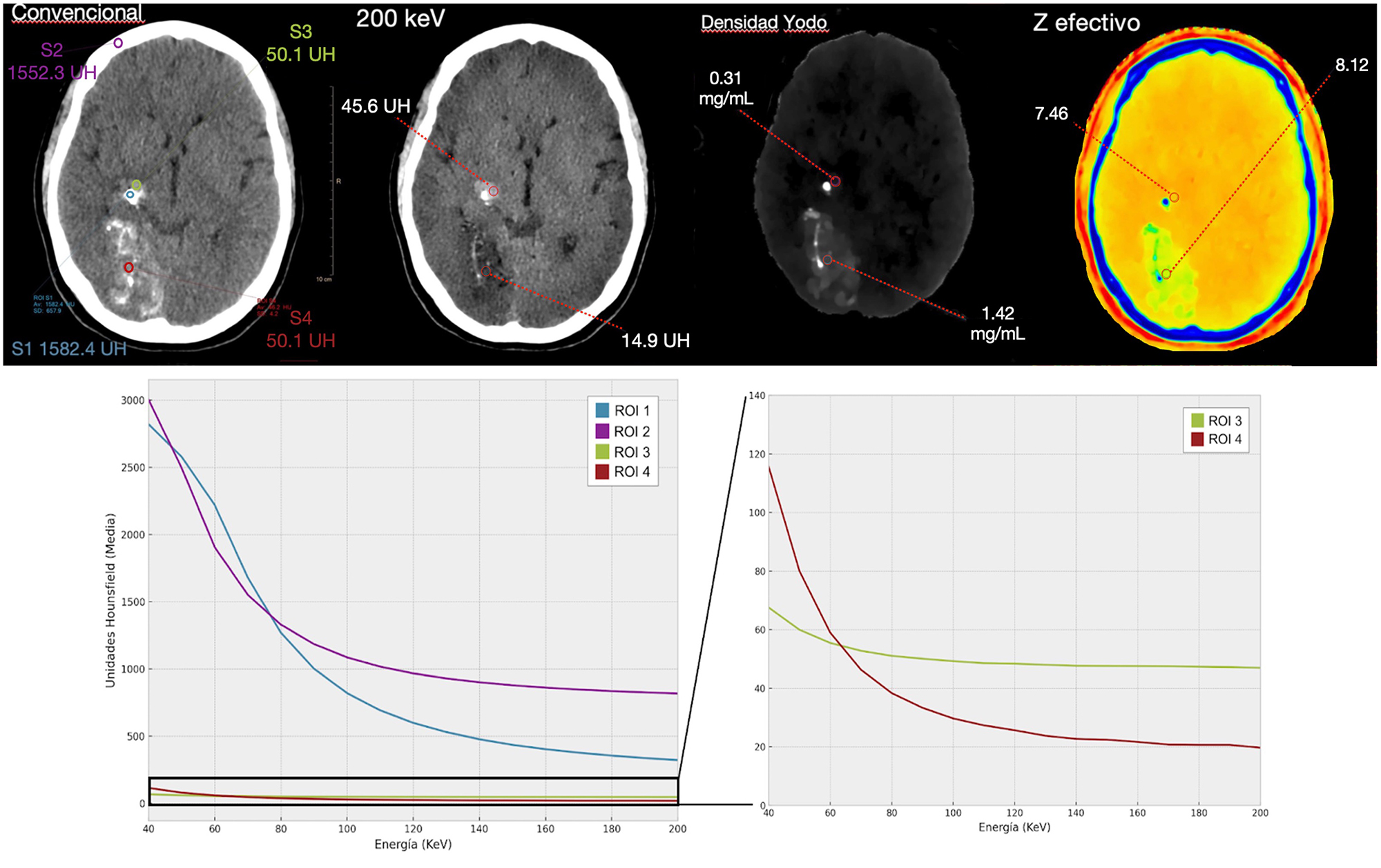
Comparando las imágenes obtenidas y curvas de HU-keV para las regiones de interés (ROI 1: material de embolización, ROI 2: hueso frontal, ROI 3: hematoma, ROI 4: extravasación de contraste) podemos distinguir la composición de cada una de ellas a pesar de su similar atenuación en la reconstrucción convencional.
Artropatía por gota
Obtenemos un estudio sin contraste de rodilla de un paciente con gonalgia y masa palpable en la rodilla que imposibilita la punción. Realizamos un estudio con TC en el que observamos numerosas imágenes hiperdensas intraarticulares planteando principalmente el diagnóstico diferencial entre artropatía gotosa y osteocondromatosis sinovial. Los mapas de ácido úrico permiten confirmar con seguridad la naturaleza de lesiones como el tofo gotoso. La curva que describe el urato hace que en estos estudios la atenuacióna distintas energías difiera significativamente de tejidos blandos y calcio (Figura 6). Estos mapas confirmaron la composición de ácido úrico, permitiendo diferenciar esta entidad de la osteocondromatosis sinovial otras artropatías por depósito.
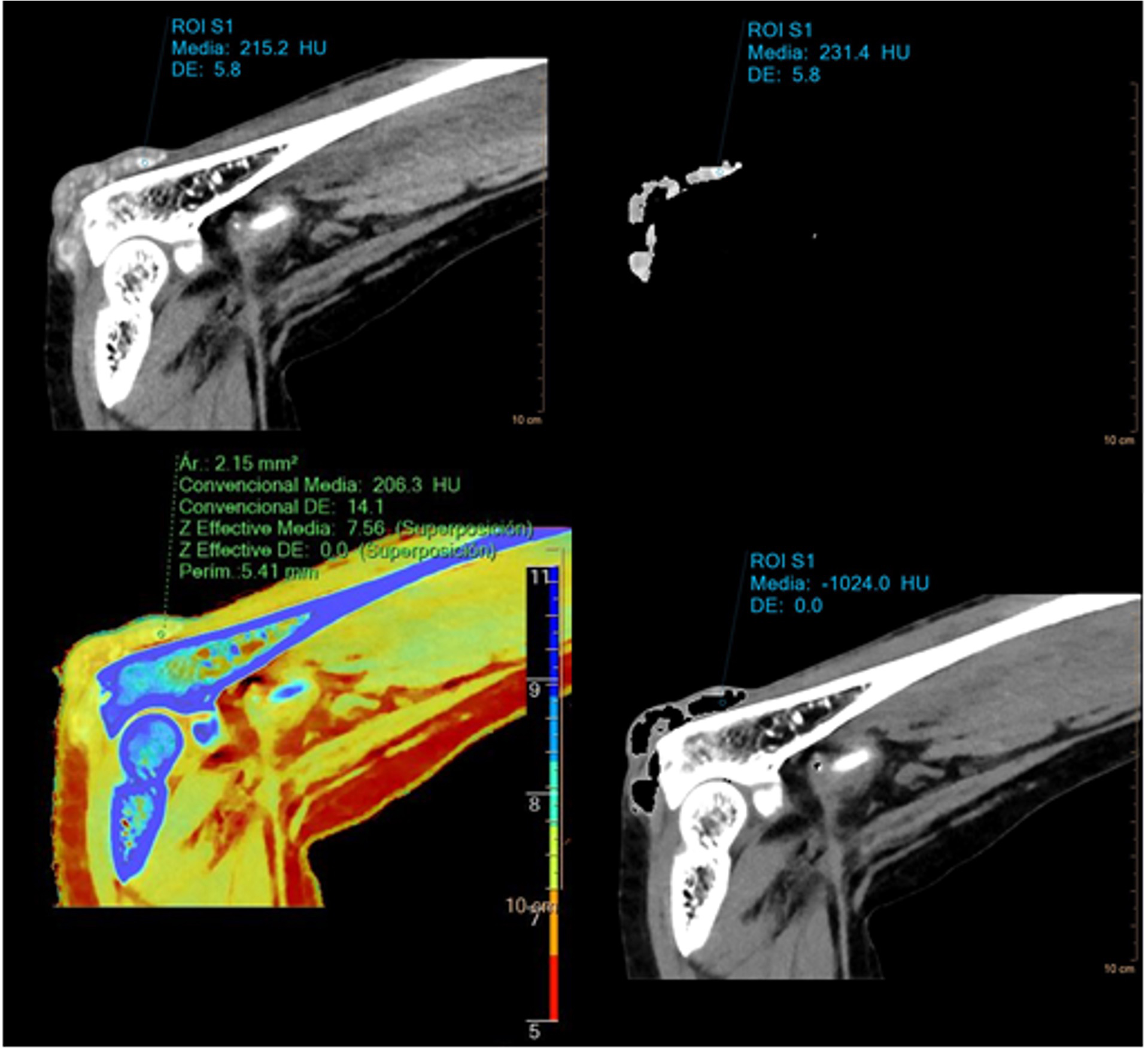
Es importante conocer que existen materiales inorgánicos (como endoprótesis y catéteres) que pueden ser incorrectamente identificados en los mapas como calcio o urato (28).
Metástasis pulmonares
En un estudio programado de Tórax con contraste de extensión por un adenocarcinoma de páncreas, se observan dos nódulos, uno pleural y otro pulmonar. En los estudios de TC con contraste puede ser difícil caracterizar la naturaleza de los nódulos usando solo sus características morfológicas.
Los mapas de yodo del TC espectral (Figura 7) permiten confirmar la avidez por el contraste de los nódulos y la captación de contraste en anillo del nódulo pulmonar. Estas características son típicas de una etiología tumoral metastásica (30).
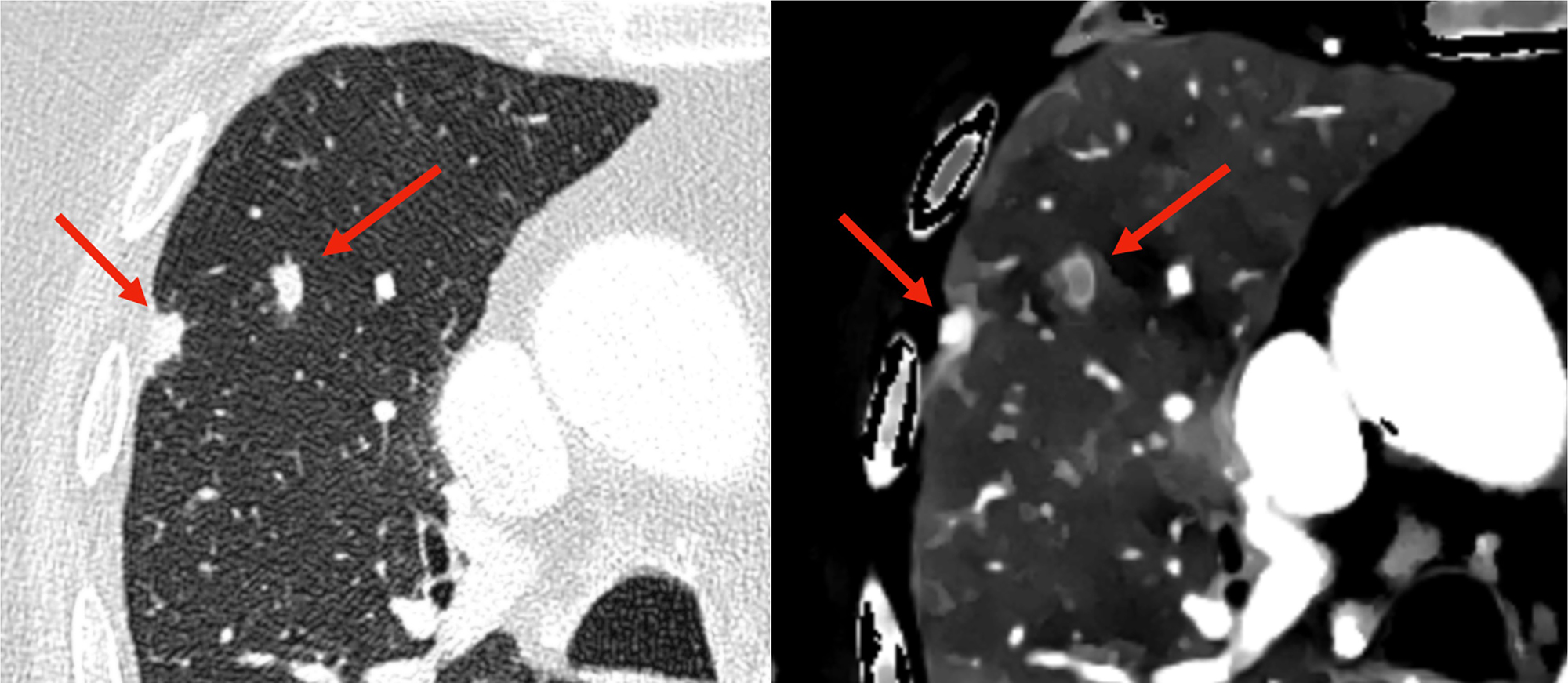
Dos nódulos de pequeño tamaño difíciles de caracterizar en los que en la imagen de densidad de Yodo observamos una imagen en anillo del nódulo pulmonar y una alta captación de yodo del nódulo pleural. Esto nos orienta a la naturaleza agresiva de la lesión pleural y metastásica de la lesión pulmonar.
Defectos de perfusión
El mapa de densidad de yodo permite evaluar defectos de perfusión con fiabilidad. Como ejemplo, en un control con TC espectral tras embolización de una comunicación arteriovenosa se detecta un área en forma de cuña, no visible en la imagen convencional, que representa un segmento hipoperfundido por la rama arterial embolizada (Figura 8). Los mapas paramétricos de yodo guardan relación con la perfusión y se correlacionan muy bien con los estudios de perfusión que emplean radionúclidos (31).
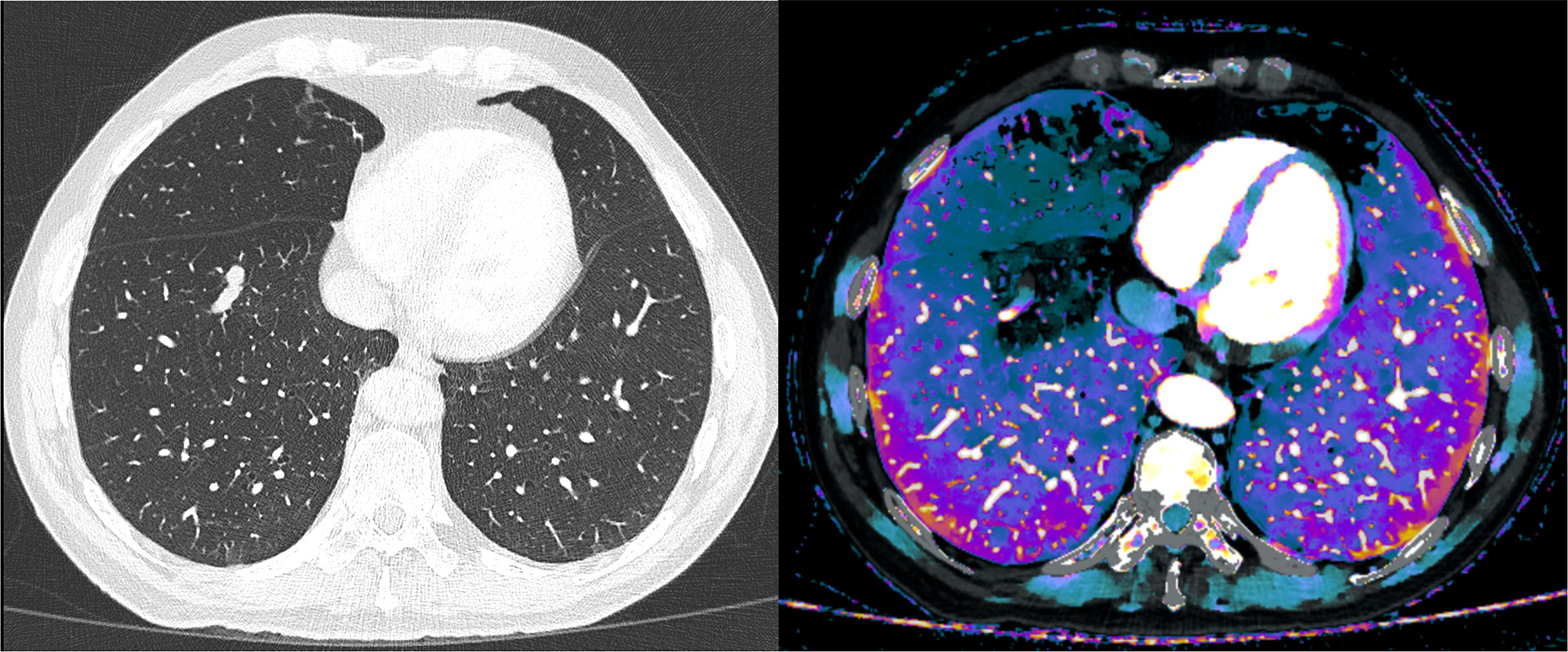
La imagen de superposición permitió observar un defecto de perfusión del segmento pulmonar dependiente de la arteria embolizada. También observamos un gradiente de densidad de yodo por flujo retrógrado de contraste desde la vena pulmonar aumentada de tamaño.
DISCUSIÓN
Esta revisión narrativa aborda de manera pictórica los factores que afectan a la cuantificación de la atenuación con UH en los estudios con TC convencional y espectral en la práctica clínica habitual. Gracias a la resolución energética y su capacidad de caracterizar la atenuación a distintas energías se pueden discriminar ciertos materiales por su comportamiento energético. Los materiales con un número atómico elevado, como el yodo, presentan una mayor atenuación a energías bajas, donde predomina el efecto fotoeléctrico.
A energías más altas, sin embargo, la interacción fotón-electrón depende principalmente del efecto Compton, determinado casi exclusivamente por la densidad del material.
La medida puntual de UH tiene demasiadas incertidumbres y es de mayor utilidad diagnóstica representar el comportamiento con las distintas energías. El comportamiento dinámico de los valores de UH a las diferentes energías, representados en las curvas de atenuación, es específico de ciertos materiales en función de su composición elemental. Cuando una estructura está compuesta por diferentes elementos, la curva que se genera es la combinación proporcional de las de los elementos que la componen.
En los tejidos corporales encontramos principalmente una mezcla de carbono, hidrógeno, oxígeno, nitrógeno y fósforo en proporciones variables. Estos elementos tienen una absorción en el borde K (K edge) a energías muy por debajo del rango de la TC. Sin embargo, el calcio y el yodo tienen un borde K de 4 y 33,2 keV respectivamente, más próximo a las energías mínimas utilizadas por la TC espectral (40 keV). Es por ello por lo que pueden caracterizarse con el TC espectral. Basándonos en esta característica, puede identificarse con fiabilidad el medio de contraste yodado en aquellas estructuras con captación intensa (como los tumores) o sin captación (como los defectos de perfusión) (Figuras 7 y 8). También pueden obtenerse imágenes virtuales sin contraste de estudios obtenidos directamente tras la administración de un medio de contraste aprovechando la baja atenuación del yodo a altas energías. Conociendo el comportamiento de las UH a bajas y altas energías, se puede cuantificar la concentración de yodo, que es proporcional a la pendiente de la curva que describe.
El uso de imágenes monoenergéticas y la obtención de curvas de energía-atenuación también permite la identificación de anormalidades o lesiones con contenido lipídico, como la esteatosis y los adenomas adrenales. La morfología típica de la curva con caída de la atenuación a bajas energías permite esta caracterización.
El número atómico efectivo se puede estimar utilizando estos trazados y nomogramas obtenidos de la base de datos de referencia estándar (3). Nos permite detectar la presencia de elementos de diferente número atómico en zonas de similar atenuación, para las que asumimos una misma densidad. Sirve también para estimar la densidad electrónica, que se utiliza para calcular y optimizar la dosis efectiva en distintos tejidos en radioterapia.
Tradicionalmente, la escala estandarizada de UH que se utiliza es unidimensional para una energía de referencia de 120 kVp, generando que muchos tejidos que comparten una atenuación similar no puedan diferenciarse. El empleo de una escala con representación multienergética permite diferenciar componentes y materiales. Los datos espectrales permiten, mediante algoritmos de descomposición multimaterial, obtener mapas paramétricos que estimen la concentración de los distintos materiales (yodo, ácido úrico y calcio, entre los más extendidos), número atómico efectivo y densidad electrónica a nivel de vóxel. A partir de estos datos pueden crearse imágenes derivadas o virtuales sin contraste, así como imágenes de los distintos componentes como los mapas de yodo que representan perfusión. También permite la cuantificación de lípidos y hierro, de utilidad por ejemplo en la cuantificación de la esteatosis hepática y de la sobrecarga férrica, incluso cuando coinciden en un mismo hígado.
CONCLUSIÓN
Las UH son el patrón de referencia en la representación de la atenuación en los estudios de TC, ya que ofrecen una base cuantitativa del valor del vóxel de la imagen. Su valor no es absoluto y está intrínsecamente ligado al voltaje empleado y la energía detectada. Es importante tener en cuenta los factores que las influencian y como se obtienen diversos los mapas paramétricos para poder realizar una adecuada interpretación de su significado.
DECLARACIÓN DE TRANSPARENCIA
Los autores/as de este artículo declaran no tener ningún tipo de conflicto de intereses respecto a lo expuesto en el presente trabajo.
BIBLIOGRAFÍA
- ↑So A, Nicolaou S. Spectral computed tomography: Fundamental principles and recent developments. Korea J Radiol. 2021; 22(1): 86-96. https://doi.org/10.3348/kjr.2020.0144
- ↑Hounsfield GN. Computed medical imaging: Nobel lecture, December 8, 1979. J Comput Assist Tomo. 1980; 4(5): 665-674. https://doi.org/10.1097/00004728-198010000-00017.
- ↑Hubbell J, Seltzer S. Substances of dosimetric interest. Tables of X-Ray mass attenuation coefficients and mass energy-absorption coefficients 1 keV to 20 MeV for elements Z = 1 to 92 and 48 additional. 1995 http://physics.nist.gov/PhysRefData/XrayMassCoef/cover.html, [online], http://physics.nist.gov/PhysRefData/XrayMassCoef/cover.html (Accessed July 5, 2023)
- ↑McCollough CH, Boedeker K, Cody D et al. Principles and applications of multienergy CT: Report of AAPM Task Group 291. Med Phys. 2020; 47(7): e881-e912. https://doi.org/10.1002/mp.14157
- ↑Rodríguez-Plata IT, Medina-Escobedo M, Basulto-Martínez M et al. Implementation of a technique based on Hounsfield units and Hounsfield density to determine kidney stone composition. Tomography. 2021; 7(4): 606-613. https://doi.org/10.3390/tomography7040051
- ↑Nakasato T, Morita J, Ogawa Y. Evaluation of Hounsfield units as a predictive factor for the outcome of extracorporeal shock wave lithotripsy and stone composition. Urolithiasis. 2015; 43(1): 69-75. https://doi.org/10.1007/s00240-014-0712-x
- ↑Jawahar A, González,B, Balasubramanian N, Adams W, Goldberg A. Comparison of computed tomography hepatic steatosis criteria for identification of abnormal liver function and clinical risk factors, in incidentally noted fatty liver. Eur J Gastroen Hepat. 2020; 32(2): 216–221. https://doi.org/10.1097/MEG.0000000000001502
- ↑Viëtor CL, Creemers SG, van Kemenade FJ, van Ginhoven TM, Hofland LJ, Feelders RA. How to differentiate benign from malignant adrenocortical tumors? Cancers. 2021; 13(17): 4383. https://doi.org/10.3390/cancers13174383
- ↑Ichikawa K, Miyoshi T, Osawa K et al. High pericoronary adipose tissue attenuation on computed tomography angiography predicts cardiovascular events in patients with type 2 diabetes mellitus: post-hoc analysis from a prospective cohort study. Cardiovasc diabetol. 2022; 21(1): 44. https://doi.org/10.1186/s12933-022-01478-9
- ↑Hu P, Yang X, Li Y et al. Predictive effects of admission white blood cell counts and Hounsfield unit values on delayed cerebral ischemia after aneurysmal subarachnoid hemorrhage. Clin Neurol Neurosur. 2022; 212: 107087. https://doi.org/10.1016/j.clineuro.2021.107087
- ↑Mühl-Benninghaus R, Dressler J, Haußmann A, Simgen A, Reith W, Yilmaz U. Utility of Hounsfield unit in the diagnosis of tandem occlusion in acute ischemic stroke. Neurol Sci. 2021; 42(6): 2391-2396. https://doi.org/10.1007/s10072-020-04798-4
- ↑Jeong H G, Bang J S, Kim B J, Bae H J, Han M K. Hematoma Hounsfield units and expansion of intracerebral hemorrhage: a potential marker of hemostatic clot contraction. Int J Stroke. 2021; 16(2): 163-171. https://doi.org/10.1177/1747493019895703
- ↑Erdogan A, Sambel M, Caglayan V, Avci, S. Importance of the Hounsfield unit value measured by computed tomography in the differentiation of hydronephrosis and pyonephrosis. Cureus. 2020; 12(11): e11675. https://doi.org/10.7759/cureus.11675
- ↑Zhang LX, Xiang JJ, Wei PY, Ding JW, Luo DC, Peng ZY, Han ZJ. Diagnostic value of computed tomography (CT) histogram analysis in thyroid benign solitary coarse calcification nodules. J Zhejiang Univ Sci B. 2018; 19(3): 211-217. https://doi.org/10.1631/jzus.B1700119
- ↑Yang HH, Lv YL, Fan XH, Ai ZY, Xu XC, Ye B, Hu DZ. Factors distinguishing invasive from pre-invasive adenocarcinoma presenting as pure ground glass pulmonary nodules. Radiat Oncol. 2020; 15(1): 186. https://doi.org/10.1186/s13014-020-01628-x
- ↑Banchhor SK, Londhe ND, Araki T, Saba L, Radeva P, Khanna NN, Suri JS. Calcium detection, its quantification, and grayscale morphology-based risk stratification using machine learning in multimodality big data coronary and carotid scans: a review. Comput Biol Med. 2018; 101: 184-198. https://doi.org/10.1016/j.compbiomed.2018.08.017
- ↑Mascalchi M, Camiciottoli G, Diciotti S. Lung densitometry: Why, how and when. J Thorac Dis. 2017; 9(9): 3319-3345. https://doi.org/10.21037/jtd.2017.08.17
- ↑Buenger F, Sakr Y, Eckardt N, Senft C, Schwarz F. Correlation of quantitative computed tomography derived bone density values with Hounsfield units of a contrast medium computed tomography in 98 thoraco-lumbar vertebral bodies. Arch Orthop Trauma Surg. 2022; 142(11): 3335-3340. https://doi.org/10.1007/s00402-021-04184-5
- ↑Lund EA, Samtani R, Winston M et al. Association of Perioperative Computed Tomography Hounsfield Units and Failure of Femoral Neck Fracture Fixation. J Orthop Trauma. 2020; 34(12): 632-638. https://doi.org/10.1097/BOT.0000000000001843
- ↑Molwitz I, Campbell GM, Yamamura J et al. Fat quantification in dual-layer detector spectral computed tomography: Experimental development and first in-patient validation. Invest Radiol. 2022; 57(7): 463-469. https://doi.org/10.1097/RLI.0000000000000858
- ↑Bolus D, Morgan D, Berland L. Effective use of the Hounsfield unit in the age of variable energy CT. Abdom Radiol. 2017; 42(3): 766-771. https://doi.org/10.1007/s00261-017-1052-4
- ↑Grajo JR, Sahani DV. Dual-energy CT of the abdomen and pelvis: Radiation dose considerations. J Am Coll Radiol. 2018; 15(8) :1128-1132. https://doi.org/10.1016/j.jacr.2017.08.012
- ↑Takane Y, Sato K, Kageyama R, Takano H, Kayano S. Accuracy of virtual non-contrast images with different algorithms in dual-energy computed tomography. Radiol Phys Technol. 2022; 15(3): 234-244. https://doi.org/10.1007/s12194-022-00668-0
- ↑Mahmoudi S, Bernatz S, Althoff FC et al. Dual-energy CT based material decomposition to differentiate intrahepatic cholangiocarcinoma from hepatocellular carcinoma. Eur J Radiol. 2022; 156: 110556.
- ↑Rajiah P, Sundaram M, Subhas N. Dual-Energy CT in musculoskeletal imaging: ¿What is the role beyond gout? AJR Am J Roentgenol. 2019; 213(3): 493-505. https://doi.org/10.2214/AJR.19.21095
- ↑Gibney B, Redmond CE, Byrne D, Mathur S, Murray N. A review of the applications of dual-energy CT in acute neuroimaging. Can Assoc Radiol J. 2020; 71(3): 253-265. https://doi.org/10.1177/0846537120904347
- ↑Lombardo F, Bonatti M, Zamboni GA et al. Uric acid versus non-uric acid renal stones: In vivo differentiation with spectral CT. Clin Radiol. 2017; 72(6): 490-496. doi: 10.1016/j.crad.2017.01.018.
- ↑Nourian A, Ghiraldi E, Friedlander JI. Dual-energy CT for urinary stone evaluation. Curr Urol Rep. 2020; 22: 1. https://doi.org/10.1007/s11934-020-01019-5
- ↑Basso L, Baldi D, Mannelli L, Cavaliere C, Salvatore M, Brancato V. Investigating dual-energy CT post-contrast phases for liver iron quantification: a preliminary study. Dose Response. 2021; 19(2): 15593258211011359. doi: 10.1177/15593258211011359
- ↑Sato Y, Ishiyama M, Nakano S, Nakao M, Mun M, Ninomiya H, Terauchi T, Oikado K. Ringlike peripheral increased iodine concentration for the differentiation of primary lung cancer and pulmonary metastases on contrast-enhanced dual-energy CT. AJR Am J Roentgenol. 2023; 220(6): 828-837. doi: 10.2214/AJR.22.28654.
- ↑Kikano EG, Rajdev M, Salem KZ, Laukamp K, Felice CD, Gilkeson RC, Gupta A. Utility of iodine density perfusion maps from dual-energy spectral detector CT in evaluating cardiothoracic conditions: a primer for the radiologist. AJR Am J Roentgenol. 2020; 214(4): 775-785. https://doi.org/10.2214/AJR.19.21818
Arturo Armiñana González
Hospital Universitario y Politécnico La Fe
Avda Fernando Abril Martorell 106 · 46026 Valencia.
E-Mail: arminana_art@gva.es
Año 2023 · número 140 (02) · páginas 101 a 113
Enviado: 12.01.23
Revisado: 25.01.23
Aceptado: 10.02.23


