Resumen
La psoriasis es una enfermedad cutánea crónica inmunomediada asociada frecuentemente a diferentes comorbilidades, entre las que destaca la artritis psoriásica, con un elevado impacto en la calidad de vida de los pacientes. Disponemos para su tratamiento de un importante arsenal terapéutico que incluye agentes tópicos, fototerapia y fármacos sistémicos. En los últimos años, la terapia biológica ha supuesto una auténtica revolución en el tratamiento de la psoriasis moderada a grave, por su gran eficacia y seguridad. Sin embargo, presenta algunas limitaciones como su administración exclusivamente parenteral, su elevado coste y la falta de eficacia y tolerancia en algunos casos. Por ello, recientemente, a partir de un mejor conocimiento de la fisiopatología de la psoriasis, han emergido nuevas opciones terapéuticas, algunas con la indicación aprobada y otros en investigación, que suponen un enriquecimiento para el clínico en el manejo terapéutico de la psoriasis: las pequeñas moléculas.
El objetivo de esta revisión es analizar los datos de eficacia y seguridad de estas moléculas que incluyen los inhibidores de la fosfodiesterasa (apremilast), inhibidores de las Janus quinasas (tofacitinib, baricitinib), inhibidores selectivos de la tirosina quinasa 2 (deucravacitinib), agonistas del receptor de adenosina A3 asociado a la proteína G (piclidenoson), agonistas inversos del receptor huérfano gamma T (vimirogant) y antagonistas del receptor de esfingosina-1-fosfato (ponesimod). Además, se comentan nuevas dianas moleculares. En definitiva, la vanguardia del tratamiento sistémico oral y tópico de la psoriasis.Abstract
Psoriasis is a chronic immune-mediated skin disease frequently associated with different comorbidities, among which psoriatic arthritis stands out, with a high impact on the quality of life of patients. We have an important therapeutic arsenal that includes topical agents, phototherapy and systemic drugs. In recent years, biological therapy has brought about a true revolution in the treatment of moderate to severe psoriasis, due to its great efficacy and safety. However, it has some limitations such as its exclusively parenteral administration, its high cost and the lack of efficacy and tolerance in some cases. Therefore, based on a better knowledge of the pathophysiology of psoriasis, new therapeutic options have emerged: the small molecules. They represent an enrichment for the clinician in the therapeutic management of psoriasis. Some of those have approved indication and others under investigation.
The objective of this review is to analyze the efficacy and safety data of these molecules that include phosphodiesterase inhibitors (apremilast), Janus kinase inhibitors (tofacitinib, baricitinib), selective tyrosine kinase 2 inhibitors (deucravacitinib), agonists G protein-associated A3 adenosine receptor (piclidenoson), orphan T-gamma receptor inverse agonists (vimirogant), and sphingosine-1-phosphate receptor antagonists (ponesimod). In addition, new molecular targets are discussed. In short, the frontline of new systemic treatment for psoriasis.Palabras clave: Psoriasis; Pequeñas moléculas; Inhibidores de la fosfodiesterasa; Inhibidores de la Janus kinasa; Dianas moleculares; Revisión.
Keywords: Psoriasis; Small molecules; Phosphodiesterase inhibitors; Janus kinase inhibitors; Molecular targets; review.
INTRODUCCIÓN
La psoriasis es una enfermedad crónica de la piel mediada por el sistema inmune, con una prevalencia del 2-3% e importante repercusión en la calidad de vida de los pacientes (1,2,3). Existen diferentes formas clínicas, siendo la forma más común la psoriasis en placas (que afecta al 85-90% de los pacientes). El Índice de Área y Severidad de la Psoriasis (Psoriasis Area and Severity Index, PASI, de 0 a 72) es la herramienta más empleada para evaluar la gravedad de la psoriasis. Para determinar la efectividad de un tratamiento se puede utilizar el PASI absoluto o el relativo (porcentaje de mejoría con respecto al valor basal, por ejemplo, un PASI 75, supone una mejoría del 75% con respecto a la cifra inicial) (4,5,6).
Un mejor conocimiento de la fisiopatología de la psoriasis ha permitido el desarrollo de agentes antiinflamatorios e inmunomoduladores cada vez más precisos, efectivos y selectivos, la llamada terapia dirigida (8). Se puede clasificar en dos grupos: agentes biológicos e inhibidores de moléculas pequeñas (8). Los fármacos biológicos son anticuerpos monoclonales o proteínas de fusión que bloquean las citoquinas proinflamatorias o sus receptores (9,10,11). La terapia biológica ha supuesto una auténtica revolución en el tratamiento de la psoriasis moderada a grave, por su gran eficacia y seguridad. Sin embargo, presenta algunas limitaciones como su administración exclusivamente parenteral, su elevado coste, inmunogenicidad y la falta de eficacia y tolerancia en algunos casos. Por ello, existe la necesidad del desarrollo continuo de nuevas terapias que permitan guiar las decisiones terapéuticas personalizadas, basadas en el conocimiento de nuevas dianas moleculares (9,12,13). En esta dirección, se han desarrollo nuevos fármacos como las denominadas pequeñas moléculas.
Las pequeñas moléculas se definen como aquellas moléculas que modulan el sistema inmunitario actuando a nivel de diversos receptores y vías moleculares celulares, resultando por tanto en el bloqueo de varias citoquinas y que, característicamente, poseen un peso molecular menor de un kilodalton (kDa) (8, 14,15). Comparadas con las terapias biológicas, presentan las ventajas de una mayor simplicidad y ausencia de inmunogenicidad (ya que se sintetizan químicamente). Además, algunas moléculas podrían atravesar la membrana celular, lo que las convierte en una opción terapéutica alternativa adecuada para los pacientes que no responden lo suficiente a las terapias con anticuerpos dirigidos (que actúan sobre la superficie celular o fuera de las células) (8, 16,17,18). Por otra parte, estas características permiten su administración por vía oral o tópica, siendo útiles en aquellos pacientes que, por preferencias personales, prefieren evitar las vías de administración más invasivas. Al mismo tiempo, suponen una opción más rentable comparado con los grandes y complejos agentes biológicos inyectables (8, 14, 16). Sin embargo, la mayoría de estas moléculas se encuentran en fase de desarrollo, persiguen mejorías relativas del 75% del PASI basal y carecen de evaluaciones de eficacia y seguridad a largo plazo (8,12). Por ello, el objetivo de esta revisión es recoger los datos disponibles de eficacia y seguridad de estos nuevos tratamientos. Entre ellos, incluimos aquellas moléculas con un desarrollo cínico más amplio como: los inhibidores de la fosfodiesterasa 4, los inhibidores de JAK/STAT y los inhibidores selectivos de la tirosina quinasa 2; y por otra parte, aquellas moléculas en desarrollo como: los agonistas del receptor de adenosina A3 asociado a la proteína Gi, los agonistas inversos del receptor huérfano gamma T (RORγ T) y los antagonistas del receptor de esfingosina-1-fosfato (S1PR1). Por otra parte, también se señalan nuevas dianas moleculares, susceptibles del desarrollo de nuevos agentes terapéuticos como los inhibidores de la catepsina S, los inhibidores de los canales de calcio activado por liberación de calcio (CRAC) y los inhibidores de purina nucleósido fosforilasa (PNPi).
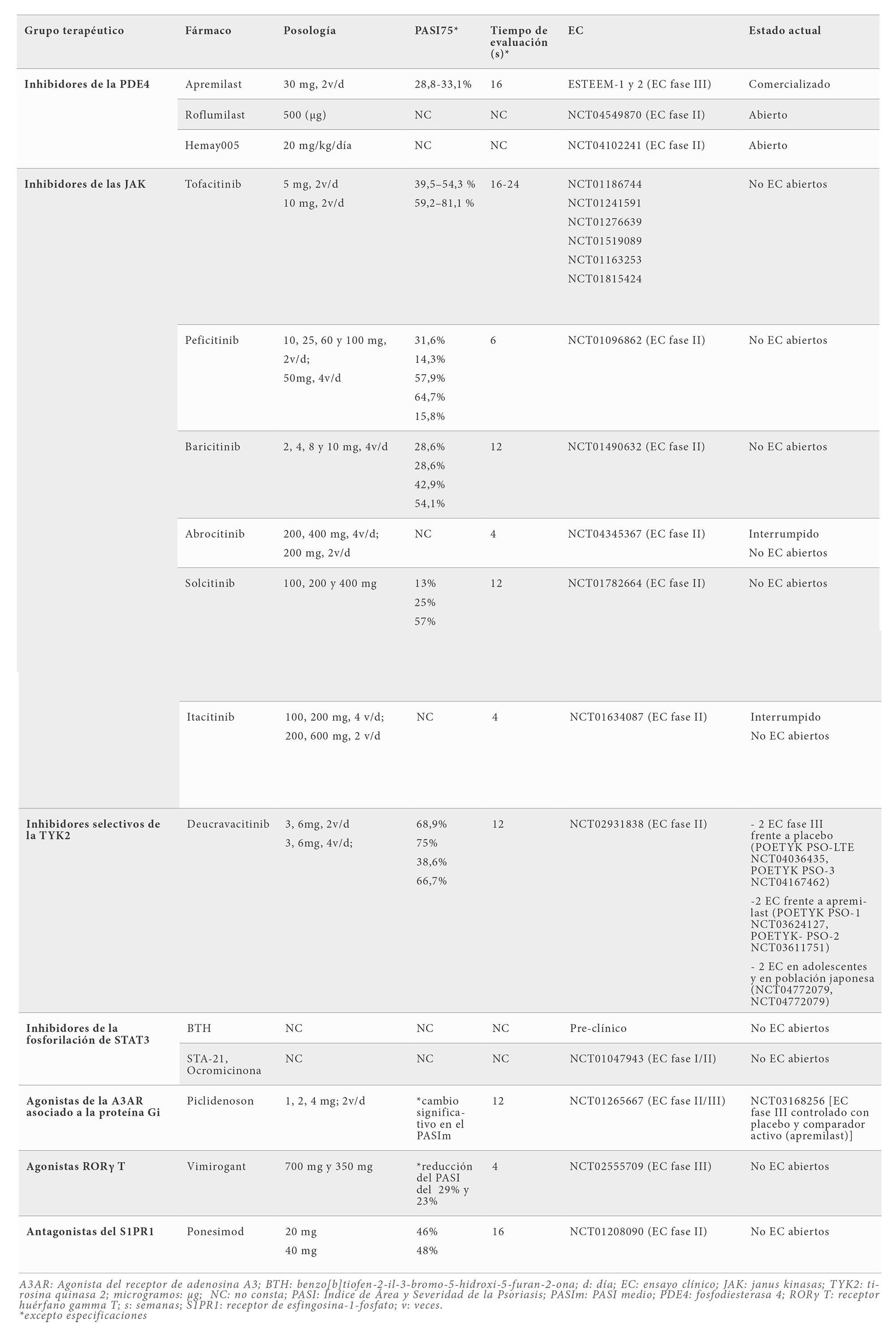
PEQUEÑAS MOLÉCULAS EN EL TRATAMIENTO DE LA PSORIASIS (Tabla 1)
Inhibidores de la Fosfodiesterasa 4 (PDE4)
La PDE4 es una enzima intracelular responsable de la hidrólisis de monofosfato de adenosina cíclico (cAMP), un segundo mensajero que juega un papel fundamental en la regulación de la respuesta inmune (19). La actividad reducida de PDE4 aumenta el nivel de cAMP citosólico, disminuyendo los mediadores proinflamatorios y elevando la producción de factores antiinflamatorios. Por ello, los inhibidores de la PDE4 se han empleado para el tratamiento de varios trastornos autoinmunes, incluida la psoriasis (19,20,21) (Fig. 1). Varios estudios han objetivado una disminución significativa de los niveles plasmáticos de Interleucina (IL)-17A, IL-17F e IL-22 durante el tratamiento de la psoriasis con apremilast, un inhibidor de PDE4 (22,23)
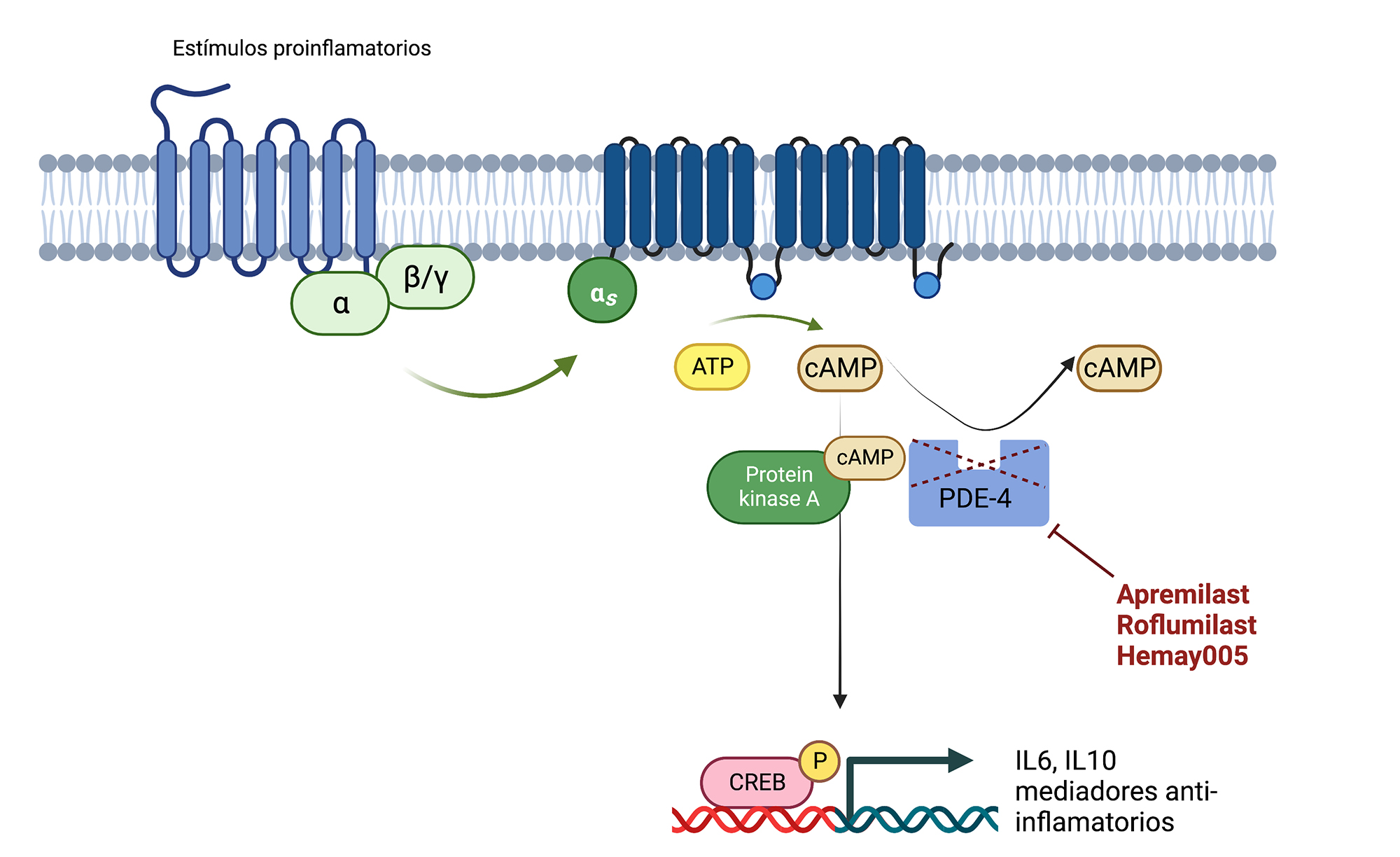
Apremilast (Otezla®, Amgen Europa).
Apremilast es un inhibidor de la PDE4 aprobado por la agencia americana del medicamento (Food and Drug Administration, FDA) para el tratamiento de la psoriasis en placas en 2014 (19). Se administra por vía oral a la dosis de 30 mg dos veces al día. En los ensayos clínicos de fase III, aleatorizados, doble ciego y controlados con placebo ESTEEM-1 y 2, se alcanzó una respuesta PASI 75 a las 16 semanas con apremilast en el 33,1 % y 28,8% respectivamente, frente al 5,3 % y 5,8% en la rama de placebo; y del 9,8% y 8,8% para un PASI 90, frente al 0,4 % y 1,5% de los pacientes que recibieron placebo (24, 25). En el estudio LIBERATE, que compara apremilast (30 mg dos veces al día) frente a placebo y frente a etanercept, no se encontraron diferencias significativas en los porcentajes del PASI75 alcanzados por ambos fármacos activos (26). En cuando a datos en práctica clínica real, en el estudio APPRECIATE, realizado en España, se objetiva la obtención de una respuesta rápida y mantenida. Hasta el 36,7% de los pacientes mantienen una respuesta PASI 75 a los 6 meses de tratamiento (27). Además, en este estudio se recogen datos de satisfacción de los pacientes, demostrando una rápida y marcada reducción del prurito, una mejoría del estado de ánimo y de la sensación de bienestar general (27). También ha demostrado una marcada eficacia, especialmente en ciertos fenotipos de la enfermedad, como la psoriasis en pequeñas placas (27).
En relación con otras variantes clínicas, apremilast, es una opción adecuada en localizaciones especiales (uñas, cuero cabelludo y palmoplantar). Así lo demuestra, por un lado, el estudio en práctica clínica real LAPIS-PSO, donde se observa que a los 4 meses de tratamiento con apremilast, un 62% de los pacientes había alcanzado una respuesta Nail Psoriasis Severity Index (NAPSI)-50 (28). Por otro lado, hasta el 43,4% de los pacientes con psoriasis del cuero cabelludo moderada-grave tratados con apremilast alcanzaron el objetivo primario (definido como la reducción de al menos 2 puntos en la Scalp Physician Global Assessment) a las 16 semanas frente al 13,8% de los pacientes tratados con placebo (29).
Apremilast también ha demostrado ser eficaz en el control de la artritis psoriásica. La respuesta, medida como American College of Rheumatology (ACR)20, ACR50 y ACR70, a la semana 16 en pacientes tratados con apremilast (30 mg dos veces al día) frente a placebo, en dos estudios retrospectivos observacionales, fueron del 32,1 % (placebo 18,9 %), 10,5 % (placebo 5 %) y 1,2 % (placebo 0,6 %) en el estudio PALACE-2 y 41 % (placebo 18 %), 15 % (placebo 8 %) y 4 % (placebo 2 %) en el estudio PALACE-3 respectivamente (30).
Finalmente, bajo la hipótesis de que la inhibición de la PDE4 pudiera mejorar el estado metabólico y normalizar la inmunidad disregulada, se está desarrollando el estudio IMAPA para evaluar los efectos de apremilast sobre el estado metabólico, vascular e inmunológico (27).
Apremilast presenta un buen perfil de seguridad. En su mayoría, las reacciones adversas notificadas son de leves a moderadas en gravedad (25-28). Los efectos adversos más frecuentes son la diarrea, náuseas, cefalea, nasofaringitis, infecciones del tracto respiratorio superior, vómitos y anorexia. La cefalea y la diarrea secretora son los efectos adversos que más frecuentemente conducen a la interrupción del tratamiento (20%) (27). Por ello, se debe monitorizar el peso en los pacientes, especialmente en aquellos que presenten un peso inferior al normal. Se recomienda, además, monitorizar periódicamente posibles alteraciones del estado de ánimo (27). Sin embargo, no es necesario llevar a cabo exámenes de detección de infecciones latentes como la tuberculosis o la infección por el virus de la hepatitis B (25-28). Es un fármaco contraindicado en el embarazo (25-29).
Apremilast, por su diana terapéutica, puede ser una opción adecuada en aquellos pacientes con infecciones recurrentes, crónicas o activas, con historia reciente de neoplasias (menos de 5 años), neoplasias activas u otros estados de inmunosupresión.
Roflumilast (Daxas ®, AstraZeneca).
Roflumilast es un inhibidor de acción prolongada de la enzima PDE4, comercializado para la enfermedad pulmonar obstructiva crónica grave. No obstante, nuevas investigaciones sugieren un papel relevante en el tratamiento tópico de la psoriasis (8,31). En un ensayo clínico en fase IIb, roflumilast en crema (0,3 % y 0,15%) mostró reducciones significativas en el PASI en comparación con la crema vehiculizada con placebo a las 6 semanas (32). Actualmente, está en curso un ensayo clínico de fase II (NCT04549870) (33). Roflumilast tópico al 0,3% ha sido aprobado por la FDA para la psoriasis en mayores de 12 años.
Hemay005 (S)-N-[5-[1-(3- etoxi-4-metoxifenil)-2-(metilsulfonil)etil]-4,6-dioxo-5,6-dihidro-4Htiofeno [3,4-c] pirrol-1-il] acetamida.
Hemay005 es un nuevo inhibidor de la PDE4. Datos preliminares muestran una actividad inhibidora similar a la de apremilast. En estudios preclínicos de modelos de ratón, demuestra una mayor eficacia para el tratamiento de la psoriasis en comparación con apremilast a dosis de 20 mg/kg/día, con un buen perfil de seguridad (34). Actualmente se encuentra abierto un ensayo clínico en fase II (NCT04102241) patrocinado por Tianjin Hemay Bio-Tech. Co (33,34).
Inhibidores de las Janus Kinases (JAK).
La familia de las JAK humanas es un grupo de tirosina quinasas, entre las que se incluyen JAK1, JAK2, JAK3 y tirosina quinasa 2 (TYK2) (14). Estas quinasas transmiten señales activadoras desde la membrana celular a las proteínas Signal Transducer and Activator of Transcription (STAT) (factores de transcripción intracelular) (14). Posteriormente, las STAT activadas se translocan al núcleo y regulan al alza la transcripción de los genes responsables de la producción de citoquinas (35). Existen siete transductores diferentes de señal que activan la translocación para la expresión génica: STAT1, STAT2, STAT3, STAT4, STAT5a, STAT 5b y STAT6. Entre ellos, STAT3 ha emergido como un actor clave en el desarrollo y la patogenia de la psoriasis (36, 37). Entre diferentes dianas moleculares, el receptor de IL-23 (involucrado en la patogenia de la psoriasis) es un heterodímero de JAK2 y TYK2, por lo que su inhibición constituye una potencial diana terapéutica. Sin embargo, diferentes receptores se asocian con diferentes JAK, de modo que el bloqueo selectivo de una JAK puede inhibir otra función biológica específica. Se han identificado nueve moléculas que inhiben la vía JAK/STAT (Fig. 2).
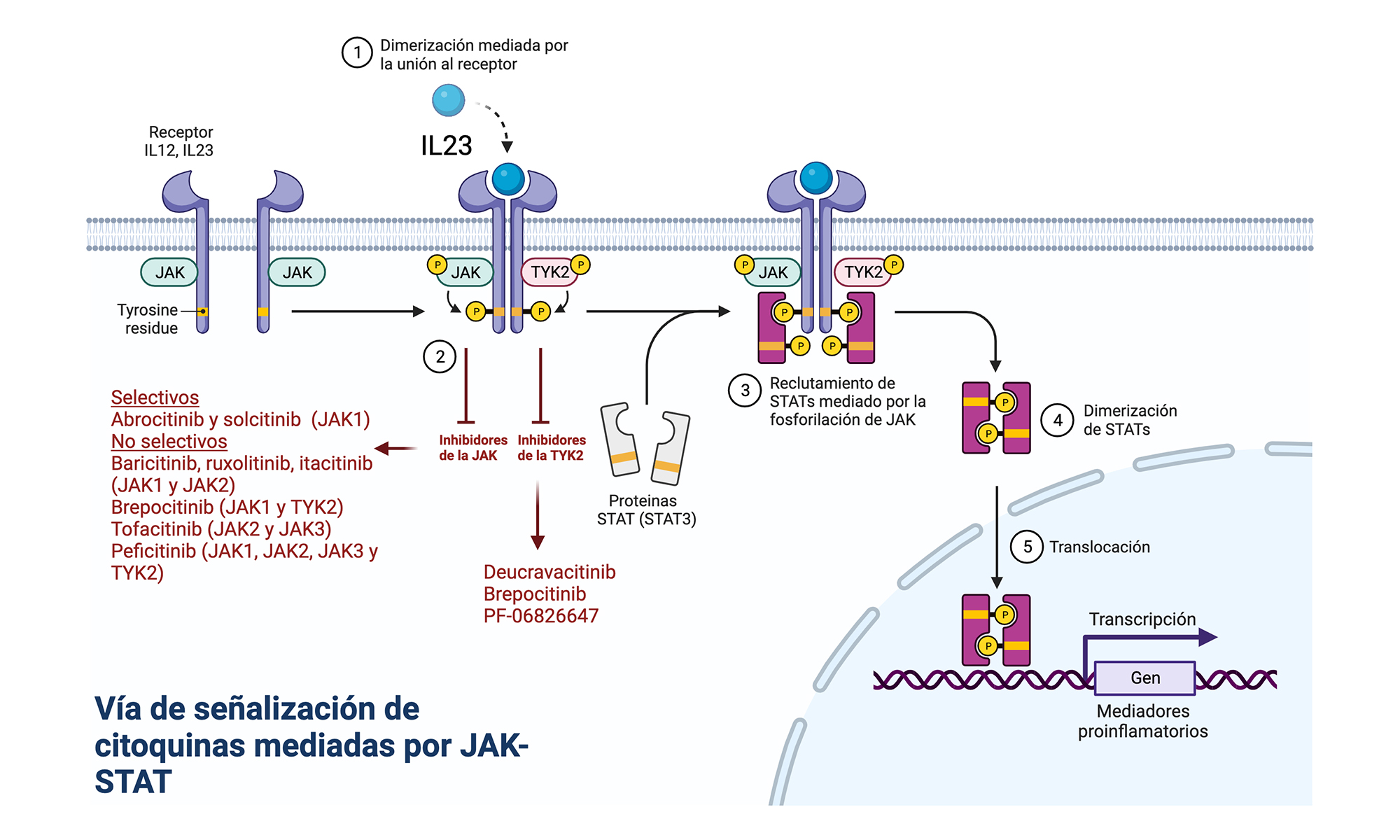
Algunos de estos fármacos actúan sobre un único componente específico de esta vía, como abrocitinib (anti JAK1), solcitinib (anti JAK1) y deucravacitinib (anti TYK2), mientras que otros lo hacen inhibiendo varios componentes, como baricitinib, ruxolitinib, itacitinib (anti JAK1 y JAK2), brepocitinib (anti JAK1 y TYK2), tofacitinib (anti JAK2 y JAK3) y peficitinib (anti JAK1, JAK2, JAK3 y TYK2). Todos ellos, excepto ruxolitinib, de aplicación tópica, se han empleado por vía oral para la psoriasis (14, 35).
Tofacitinib (Xeljanz®, Pfizer).
Tofacitinib es un potente inhibidor no selectivo de JAK1 y JAK3, con menor actividad contra JAK2 y TYK2. Actúa previniendo la activación de STAT y disminuyendo la producción de los mediadores proinflamatorios generados por IL-6, IL-15, interferón (IFN) ɑ y ɣ a través de la inhibición de JAK1 (35).
Tofacitinib es el más inhibidor de JAK más estudiado para el tratamiento de la psoriasis en placas (36). Sin embargo, pese a su aprobación en artritis psoriásica y en artritis reumatoide, no fue aprobado para la indicación de psoriasis y no hay ensayos abiertos para esta indicación. En estudios de fase III, aleatorizados, doble ciego y controlados con placebo, se encontraron tasas de respuesta (medidas como porcentaje de pacientes que alcanzan una respuesta PASI 75) entre las semanas 16-24 del 39,5–54,3 % (a dosis de 5 mg dos veces al día) y del 59,2–81,1 % (a dosis de 10 mg dos veces al día (35, 36). Sin embargo, actualmente no hay ensayos clínicos abiertos para esta indicación (33).
En cuanto al perfil de seguridad, un elevado número de pacientes muestra una alteración analítica del perfil lipídico, con aumento del colesterol circulante total y lipoproteínas de baja densidad, aumento de los niveles de creatinina y disminución de la hemoglobina y linfocitos en sangre, aunque tofacitinib es generalmente bien tolerado (36). Los acontecimientos adversos (AA) más frecuentemente notificados son: nasofaringitis, cefalea, diarrea, náuseas e infecciones de tracto respiratorio superior. En los ensayos clínicos de tofacitinib para la artritis reumatoide, se objetivó una mayor incidencia de infecciones oportunistas (incluida tuberculosis) a dosis de 10 mg/12h en comparación con 5 mg /12h (14, 36). Además, en las evaluaciones a largo plazo, se observó un aumento significativo de acontecimientos cardiacos, infecciones graves, neoplasias y exitus en pacientes con artritis y colitis ulcerosa. Recientemente, la FDA y la agencia europea del medicamento (EMA) han publicado advertencias sobre la seguridad de estos fármacos.
Peficitinib (ASP015K) (Smyraf®, Astellas Pharma).
El peficitinib muestra una mayor selectividad para JAK3 sobre JAK1, JAK2 y TYK2. La seguridad y eficacia terapéuticas de peficitinib se investigaron en un ensayo clínico de fase IIa, multicéntrico, doble ciego, aleatorizado, controlado con placebo durante 6 semanas en pacientes con psoriasis en placas (NCT01096862) (33). Se incluyeron un total de 124 pacientes con cinco ramas de tratamiento a diferentes dosis orales del fármaco (10, 25, 50 mg, 60 y 100 mg) y una con placebo. Como resultado, se observó que la gravedad general de la enfermedad se redujo significativamente después del tratamiento con peficitinib. Las mejoras fueron en gran medida dependientes de la dosis. También se informó que peficitinib tenía la capacidad de reducir el espesor epidérmico y la proliferación de los queratinocitos en las biopsias de piel. Los resultados fueron prometedores, si bien se trataba de un estudio a corto plazo (6 semanas), por lo que no es posible anticipar la efectividad a largo plazo o la seguridad de peficitinib en práctica clínica real. Por otra parte, peficitinib fue bien tolerado en la mayoría de los casos y no se registraron AA significativos (38). Este estudio se llevó a cabo en 2010 y actualmente no hay nuevos ensayos clínicos abiertos (33).
Baricitinib (Olumiant ®, Eli Lilly).
Baricitinib es un inhibidor selectivo de JAK1 y JAK2, aprobado por la FDA para el tratamiento de pacientes adultos con artritis reumatoide (2018) y dermatitis atópica (2022). En cuanto al tratamiento de la psoriasis moderada a grave, encontramos datos preliminares de un ensayo de fase IIb (NCT01490632) a 12 semanas, aleatorizado, doble ciego, controlado con placebo, a dosis de 2, 4, 8 y 10 mg una vez al día (39). Se incluyeron un total de 271 pacientes. A la semana 12, los grupos tratados con baricitinib presentaron mejoras significativas del PASI en comparación con el basal y alcanzaron mayores tasas respuesta para PASI 50 (excepto para la dosis de 2mg). Los mejores resultados se obtuvieron a mayores dosis. El porcentaje de pacientes que alcanzaron una respuesta PASI 75 fue del 43% a dosis de 8mg. El 81% de estos respondedores mantuvieron su respuesta a lo largo de 24 semanas (39). Su desarrollo clínico en la psoriasis se encuentra actualmente detenido.
Abrocitinib (Cibinqo ®, Pfizer).
Aprobado para la dermatitis atópica, abrocitinib es un inhibidor selectivo de JAK1. En 2015 se realizó un estudio de fase II con este fármaco para el tratamiento sistémico de la psoriasis (36). Se incluyeron un total de 59 pacientes tratados a diferentes dosis orales (200 mg al día, 400 mg cuatro veces al día y 200 mg dos veces al día). El objetivo primario consistía en medir el cambio en el PASI comparado con placebo a las 4 semanas. Sin embargo, se interrumpió su investigación (14,33).
Solcitinib (GlaxoSmithKline).
Solcitinib es un inhibidor selectivo de JAK1. En cuanto a su uso en psoriasis, se llevó a cabo un estudio aleatorizado de fase IIb con tres ramas de tratamiento (a dosis de 100, 200 y 400 mg) comparado con placebo (14). A las 12 semanas de tratamiento, el 57% de los pacientes tratados a dosis de 400 mg alcanzaron un PASI 75. Sin embargo, solo el 13% de los pacientes tratados con 100 mg alcanzaron el objetivo primario, encontrando 3 AA graves (trombocitopenia grave) en dicho grupo, por lo que el estudio fue cancelado (33).
Itacitinib.
Itacitinib es un inhibidor no selectivo de JAK2. En un estudio de fase II controlado con placebo, se investigó su eficacia incluyendo un total de 50 pacientes en cuatro ramas de tratamiento. La eficacia fue evaluada como cambios en el PASI a los 28 días. No se recogieron los EA de manera sistemática y los datos del estudio no han sido publicados (31, 33).
Inhibidores selectivos de la tirosina quinasa 2 (TYK2). Deucravacitinib (Sotyktu®, Bristol Myers Squibb).
Los inhibidores selectivos de la TYK2 proporcionan una mayor selectividad que el resto de los inhibidores de la JAK, lo cual sugería que la inhibición de la TYK2 podría lograr un perfil de eficacia y seguridad más equilibrado que el obtenido con los otros inhibidores de JAK. Entre ellos destaca deucravacitinib (BMS-986165). Deucravacitinib es un inhibidor selectivo oral de la TYK2 que actúa sobre las vías de IL-12, IL-23 e interferón tipo 1 (40). Los resultados publicados de un estudio de fase II, aleatorizado, doble ciego, controlado con placebo, han sido muy prometedores (41). En la semana 12, el 75% de los pacientes con deucravacitinib (12 mg al día) alcanzaron un PASI 75 frente al 7 % de los pacientes en la rama placebo. Se describieron AA en el 55-80 % de los pacientes en los grupos de intervención, porcentaje similar al grupo placebo (51%). Entre los AA más comunes se incluyeron: nasofaringitis, cefalea, diarrea, náuseas e infecciones del tracto urinario inferior. También se encontró un aumento de lesiones acneiformes en pacientes tratados con el fármaco. (40) Actualmente se encuentran abiertos varios ensayos clínicos en fase III (Tabla 1). Deucravacitinib ha sido recientemente aprobado por FDA con la indicación de psoriasis.
Inhibidores de la fosforilación de STAT3.
BTH (benzo[b]tiofen-2-il-3-bromo-5-hidroxi-5-furan-2-ona) se ha sugerido como un nuevo inhibidor de JAK/STAT. Es un análogo sintético de un compuesto natural derivado de una esponja marina (42). BTH inhibe la fosforilación de STAT3, evitando su translocación en el núcleo y reduciendo la proliferación de queratinocitos (42).
STA-21 (Ocromicinona) se ha empleado por vía tópica para el tratamiento de la psoriasis en un modelo de ratón y en un ensayo clínico de fase I/II (NCT01047943) en humanos. El tratamiento in vitro con STA-21 disminuye significativamente la translocación nuclear dependiente de citoquinas de STAT3 en queratinocitos humanos normales (43).
Agonistas del receptor de adenosina A3 asociado a la proteína Gi.
Los receptores de adenosina A3 son receptores acoplados a proteínas G involucrados en varias vías de señalización intracelulares. Regulan a la baja la vía de señalización NF-kB, disminuyendo la producción de citocinas proinflamatorias como TNF-a, IL-6 e IL-12, e inhibiendo la proliferación de linfocitos T (8). Piclidenoson (Can-Fite BioPharma) se encuentra en este grupo de fármacos. La eficacia de piclidenoson se ha demostrado en estudios clínicos de fase II. Los resultados de un ensayo de fase II controlado con placebo, multicéntrico, doble ciego, en el que participaron 75 pacientes a los que se administró piclidenoson a dosis de 1, 2 o 4 mg dos veces al día, mostraron que sólo el grupo de 2 mg logró una mejoría frente al placebo en el cambio medio del PASI en las semanas 8 y 12; en particular, el PASI 50 fue alcanzado por el 35,3% de los 17 pacientes tratados con dosis de 2 mg (44). La incidencia de AA en el brazo de 1, 2 y 4 mg fue del 58,3 %, 17,6 % y 13,3 % respectivamente, en comparación con el 21,1% en el brazo placebo. Todos ellos fueron leves/moderados, excepto una exacerbación grave de la psoriasis (14, 44). El fármaco se encuentra en investigación en un ensayo de fase III controlado con placebo y comparador activo (apremilast) (NCT03168256) (33).
Agonistas inversos del receptor huérfano gamma T (RORγ T).
RORgT es un factor de transcripción necesario para la diferenciación de células Th17, regulando la expresión de IL-17A, IL-17F, IL-22 y del receptor de IL-23 (45). La mayoría de los fármacos agonistas inversos de RORgT se encuentran en un periodo muy precoz de investigación. Vimirogant (VTP-43742), en un estudio de fase IIa, demostró una reducción del PASI del 29% y 23% a las 4 semanas en pacientes que recibieron 700 mg y 350 mg respectivamente (18). Los AA incluyeron cefalea, flushing, elevación de las enzimas hepáticas elevadas y náuseas (18). El resto de fármacos se encuentran en fase precoz de investigación (fase II y fase I) (33).
Antagonistas del receptor de esfingosina-1-fosfato (S1PR1).
La esfingosina-1-fosfato (S1P) participa en la proliferación y supervivencia celular, migración, inflamación y angiogénesis. La regulación negativa del receptor S1P inhibe la proliferación de queratinocitos y previene migración de linfocitos de los ganglios linfáticos a la piel en la psoriasis (14). Ponesimod es un antagonista del S1PR1. En un estudio en fase II, el PASI75 se alcanzó a las 16 semanas en el 46% y 48% de pacientes que recibieron ponesimod a dosis de 20 mg y 40 mg respectivamente (14). Los AA incluyeron elevación de transaminasas, disnea, mareos y alteraciones en la conducción cardiaca, por lo que está contraindicado en cardiópatas (14).
Nuevas dianas moleculares.
Inhibidores de la catepsina S.
La catepsina S tiene un papel importante en la presentación de antígenos por el complejo mayor de histocompatibilidad (MHC) de clase II y en la degradación de la matriz extracelular. Además, es responsable de la activación de la IL-36γ (46). Ausente en la piel humana normal, se ha encontrado expresión de catepsina S en los queratinocitos psoriásicos. Se están desarrollando inhibidores de las catepsinas (19).
Inhibidores de los canales de calcio activado por liberación de calcio (CRAC)
Las señales de calcio (Ca2+) juegan un papel fundamental en la función de las células inmunitarias: activación de los mastocitos, quimiotaxis de neutrófilos y pproliferación de los queratinocitos psoriásicos (14, 48). Aunque se han propuesto como tratamiento, varios aspectos de seguridad limitan su uso: la expresión ubicua, la potencial disfunción del músculo esquelético y la posible inmunosupresión crónica (48). Se ha propuesto que CM2489 (CalciMedica) sea utilizado en el tratamiento de la psoriasis. Ha completado la fase I de un ensayo clínico para la psoriasis de moderada a grave (48). A pesar de que es el único inhibidor del canal CRAC testado en humanos, no se pueden extraer conclusiones sobre su utilidad por la falta de información pública (48).
Inhibidores de purina nucleósido fosforilasa (PNP).
La PNP es una enzima responsable de la fosforólisis de inosina, deoxinosina, guanosina y desoxiguanosina (dGuo). Su inactivación conduce a la elevación de los niveles de dGuo lo que provoca la apoptosis de células T en división (19). Los únicos PNPi que han demostrado actividad clínica son los análogos del estado de transición (TSA), entre los que destacamos la ulodesina (DADMe–inmucilina- H, BCX-4208, Roche). Actualmente no existen datos publicados sobre este agente (33).
CONCLUSIONES
Avances recientes en la comprensión de la patogenia de la psoriasis ha llevado al desarrollo de nuevas terapias que actúan sobre varias vías de señalización (8, 15, 19). Algunos de los fármacos descritos en esta revisión muestran un prometedor perfil de eficacia y seguridad, suponiendo una opción para expandir el arsenal terapéutico. A pesar de mostrar una menor eficacia que los fármacos biológicos, irrumpen como opción terapéutica para los pacientes no respondedores, parcialmente respondedores a otras terapias, y/o aquellos con determinadas preferencias personales, pudiendo ser empleados en monoterapia o en terapia combinada (tópicos y otros orales o biológicos). Asimismo, al poseer una estructura simple, permiten su administración por vía oral/tópica y ofrecen una excelente relación costo-efectividad. En general, son fármacos bien tolerados, siendo la nasofaringitis y las infecciones del tracto respiratorio superior, los AA más prevalentes.
A excepción de Apremilast, que se viene empleando para el tratamiento de la psoriasis desde hace unos años, y deucravacitinib, aprobado en septiembre de 2022 por la FDA con esta indicación, el resto o han sido descartados para su uso en la psoriasis o se encuentran en diferentes estadios de investigación.
En definitiva, continúan emergiendo terapias sistémicas y tópicas novedosas para el tratamiento de la psoriasis. Sin embargo, el éxito de estos agentes depende de un buen perfil de eficacia y de seguridad que deberá determinarse en estudios futuros. Finalmente, el mejor entendimiento de las vías inflamatorias involucradas en la patogénesis de la psoriasis, pueden conducir a las estrategias terapéuticas eficaces en el manejo de esta enfermedad inflamatoria.
CONTRIBUCIONES DE LOS AUTORES
L.M-C (Conceptualización, Investigación, Metodología, Redacción-borrador original), R. S-R (Conceptualización, Validación, Redacción-revisión y edición), M. L-V, H. F (Conceptualización, Validación, Redacción- revisión), E.D. (Conceptualización, Metodología, Supervisión, Validación, Redacción-revisión y edición). Todos los autores han leído y están de acuerdo con la versión publicada del manuscrito.
DECLARACIÓN DE TRANSPARENCIA
Los autores no refieren ningún conflicto en relación con el artículo de interés.
- Luisa Martos-Cabrera: no refiere ningún conflicto en relación con el artículo de interés.
- Raquel Sampedro-Ruiz: no refiere ningún conflicto en relación con el artículo de interés.
- Mar Llamas-Velasco realiza o ha realizado las siguientes actividades: miembro de Advisory Board, consultor, recepción de becas, apoyo a la investigación, participación en ensayos clínicos, honorarios por impartir ponencias, con las siguientes compañías farmacéuticas: Abbvie, Almirall, Amgen, Biogen, Celgene, Janssen-Cilag, Leo Pharma, Lilly, MSD, Novartis, Pfizer, UCB, Kyowa Kirin, Brystol-Myers y Boehringer-Ingelheim.
- Hortensia de la Fuente: no refiere ningún conflicto en relación con el artículo de interés.
- Esteban Daudén realiza o ha realizado las siguientes actividades: miembro de Advisory Board, consultor, recepción de becas, apoyo a la investigación, participación en ensayos clínicos, honorarios por impartir ponencias, con las siguientes compañías farmacéuticas: Abbott/Abbvie, Almirall, Amgen, Biogen, Celgene, Janssen-Cilag, Leo Pharma, Lilly, MSD, Novartis, Pfizer, UCB, Brystol-Myers y Boehringer-Ingelheim.
FINANCIACIÓN
No.
BIBLIOGRAFÍA
- ↑Boehncke WH, Schön MP. Psoriasis. Lancet. 2015; 386(97): 983-994.
- ↑Parisi R, Symmons DPM, Griffiths CEM, Ashcroft DM. Global epidemiology of psoriasis: a systematic review of incidence and prevalence. J Invest Dermatol. 2013; 133(2): 377-385.
- ↑Llamas-Velasco M, de la Cueva P, Notario J, Martínez-Pilar L, Martorell A, Moreno-Ramírez D. Psoriasis moderada: Propuesta de definición. Actas Dermosifiliogr. 2017; 108(10): 911-917.
- ↑Takeshita J, Grewal S, Langan SM et al. Psoriasis and comorbid diseases. J Am Acad Dermatol. 2017; 76(3): 377-390.
- ↑Griffiths CEM, Armstrong AW, Gudjonsson JE, Barker JN. Psoriasis Lancet. 2021; 397(10281): 1301-1315.
- ↑Dand N, Mahil S, Capon F, Smith C, Simpson M, Barker J. Psoriasis and genetics. Acta Derm Venerol. 2020; 100(3): 55-65.
- Shobeiri SS, Khorrami M, Sankian M. Plaque-type psoriasis inhibitors. Int Immunopharmacol. 2021; 101(1): 108326.
- ↑Talamonti M, D’Adamio S, Bianchi L, Galluzzo M. The role of pharmacogenetics in chronic plaque psoriasis: Update of the literature. Mol Diagn Ther. 2017; 21(5): 467-480.
- ↑van Vugt LJ, van den Reek JMPA, Coenen MJH, de Jong EMGJ. A systematic review of pharmacogenetic studies on the response to biologics in patients with psoriasis. Br J Dermatol. 2018; 178(1): 86-94.
- ↑Linares-Pineda TM, Cañadas-Garre M, Sánchez-Pozo A, Calleja-Hernández MÁ. Gene polymorphisms as predictors of response to biological therapies in psoriasis patients. Pharmacol Res. 2016; 113(1): 71-80.
- ↑Ovejero-Benito MC, Prieto-Pérez R, Llamas-Velasco M et al. Polymorphisms associated with etanercept response in moderate-to-severe plaque psoriasis. Pharmacogenomics. 2017; 18(7): 631-638.
- ↑Reid C, Griffiths C. Psoriasis and treatment: past, present and future aspects. Acta Derm Venerol. 2020;100(3):70-80.
- ↑Tang H, Jin X, Li Y et al. A large-scale screen for coding variants predisposing to psoriasis. Nat Genet. 2014; 46(1): 45-50.
- ↑Gómez-García F, Gómez-Arias PJ, Montilla-López A et al. A scoping review on use of drugs targeting the JAK/STAT pathway in psoriasis. Front Med. 2022;(1)754116.
- ↑Gooderham M. Small molecules: an overview of emerging therapeutic options in the treatment of psoriasis. Skin Therapy Lett. 2013; 18(7): 1-4.
- ↑Thakur V, Mahajan R. Novel therapeutic target(s) for psoriatic disease. Front Med. 2022;9(1):712313.
- ↑Honma M, Hayashi K. Psoriasis: Recent progress in molecular‐targeted therapies. J Dermatol. 2021; 48(6): 761-777.
- ↑Balogh EA, Bashyam AM, Ghamrawi RI, Feldman SR. Emerging systemic drugs in the treatment of plaque psoriasis. Expert Opin Emerg Drugs. 2020; 25(2): 89-100.
- ↑Cervantes-Durán C, Velázquez-Hernández ME, Valentín-Escalera J, Bartolomé-Camacho MC, Rodríguez-Orozco AR, García-Pérez ME. Small molecules under development for psoriasis: on the road to the individualized therapies. Arch Dermatol Res. 2020; 312(9): 611-627.
- ↑Hansen RB, Kavanaugh A. Novel treatments with small molecules in psoriatic arthritis. Curr Rheumatol Rep. 2014; 16(9):443.
- ↑Milakovic M, Gooderham MJ. Phosphodiesterase-4 inhibition in psoriasis. Psoriasis. 2021; 11(1): 21-29.
- ↑Garcet S, Nograles K, Correa da Rosa J, Schafer PH, Krueger JG. Synergistic cytokine effects as apremilast response predictors in patients with psoriasis. J Allergy Clin Immunol. 2018; 142(3): 1010-1013.
- ↑Strober B, Alikhan A, Lockshin B, Shi R, Cirulli J, Schafer P. Apremilast mechanism of efficacy in systemic-naive patients with moderate plaque psoriasis: Pharmacodynamic results from the UNVEIL study. J Dermatol Sci. 2019; 96(3): 126-133.
- ↑Papp K, Reich K, Leonardi CL et al. Apremilast, an oral phosphodiesterase 4 (PDE4) inhibitor, in patients with moderate to severe plaque psoriasis: Results of a phase III, randomized, controlled trial (Efficacy and Safety Trial Evaluating the Effects of Apremilast in Psoriasis [ESTEEM 1]). J Am Acad Dermatol. 2015; 73(1): 37-49.
- ↑Paul C, Cather J, Gooderham M et al. Efficacy and safety of apremilast, an oral phosphodiesterase 4 inhibitor, in patients with moderate‐to‐severe plaque psoriasis over 52 weeks: a phase III, randomized controlled trial (ESTEEM 2). Br J Dermatol. 2015; 173(6): 1387-1399.
- ↑Aljefri YE, Ghaddaf AA, Alkhunani TA et al. Efficacy and safety of apremilast monotherapy in moderate-to-severe plaque psoriasis: a systematic review and meta-analysis. Dermatol Ther. 2022; 35(7): e15544.
- ↑Herranz P, Trasobares L, Mateu A et al. Caracterización y resultados de pacientes tratados con apremilast en la práctica clínica habitual española: Resultados del estudio APPRECIATE. Actas Dermosifiliogr. 2021; 112(9): 817-827.
- ↑Reich K, Korge B, Magnolo N et al. Quality-of-life outcomes, effectiveness and tolerability of apremilast in patients with plaque psoriasis and routine German dermatology care: Results from LAPIS-PSO. Dermatol Ther. 2022; 12(1): 203-221.
- ↑Van Voorhees AS, Stein Gold L, Lebwohl M et al. Efficacy and safety of apremilast in patients with moderate to severe plaque psoriasis of the scalp: Results of a phase 3b, multicenter, randomized, placebo-controlled, double-blind study. J Am Acad Dermatol. 2020; 83(1): 96-103.
- ↑Kavanaugh A, Gladman DD, Edwards CJ et al. Long-term experience with apremilast in patients with psoriatic arthritis: 5-year results from a PALACE 1-3 pooled analysis. Arthritis Res Ther. 2019; 21(1): 118.
- ↑Bellinato F, Gisondi P, Girolomoni G. Latest advances for the treatment of chronic plaque psoriasis with biologics and oral small molecules. BTT. 2021; 15(1): 247-253.
- ↑Lebwohl MG, Papp KA, Stein Gold L et al. Trial of roflumilast cream for chronic plaque psoriasis. N Engl J Med. 2020; 383(3): 229-239.
- ↑ClinicalTrials.gov [Internet]. National Library of Medicine (US). 2000 Feb 29. Acceso el 3 de enero 2023. http://clinicaltrials.gov/.
- ↑Liu X, Chen R, Zeng G et al. Determination of a PDE4 inhibitor Hemay005 in human plasma and urine by UPLC-MS/MS and its application to a PK study. Bioanalysis. 2018; 10(11): 863-875.
- ↑Azevedo A, Torres T. Tofacitinib: a new oral therapy for psoriasis. Clin Drug Investig. 2018; 38(2): 101-112.
- ↑Kvist-Hansen A, Hansen PR, Skov L. Systemic treatment of psoriasis with JAK inhibitors: a review. Dermatol Ther. 2020; 10(1): 29-42.
- ↑Calautti E, Avalle L, Poli V. Psoriasis: a STAT3-centric view. Int J Mol Sci. 2018; 19(1): 171.
- ↑Papp K, Pariser D, Catlin M et al. A phase 2a randomized, double-blind, placebo-controlled, sequential dose-escalation study to evaluate the efficacy and safety of ASP015K, a novel Janus kinase inhibitor, in patients with moderate-to-severe psoriasis. Br J Dermatol. 2015; 173(3): 767-776.
- ↑Papp KA, Menter MA, Raman M et al. A randomized phase 2b trial of baricitinib, an oral Janus kinase (JAK) 1/JAK2 inhibitor, in patients with moderate‐to‐severe psoriasis. Br J Dermatol. 2016; 174(6): 1266-1276.
- ↑Lé AM, Puig L, Torres T. Deucravacitinib for the treatment of psoriatic disease. Am J Clin Dermatol. 2022; 23(6): 813-822.
- ↑Papp K, Gordon K, Thaçi D et al. Phase 2 trial of selective tyrosine kinase 2 inhibition in psoriasis. N Engl J Med. 2018; 379(14): 1313-1321.
- ↑Xu X, Zhang HY. The immunogenetics of psoriasis and implications for drug repositioning. Int J Mol Sci. 2017; 18(12): 2650.
- ↑Miyoshi K, Takaishi M, Nakajima K, Ikeda M, Kanda T, Tarutani M et al. Stat3 as a therapeutic target for the treatment of psoriasis: a clinical feasibility study with STA-21, a Stat3 inhibitor. J Invest Dermatol. 2011; 131(1): 108-117.
- ↑Cohen S, Fishman P. Targeting the A3 adenosine receptor to treat cytokine release syndrome in cancer immunotherapy. Drug Des Devel Ther. 2019; 13(1): 491-497.
- ↑Tang L, Yang X, Liang Y, Xie H, Dai Z, Zheng G. Transcription factor retinoid-related orphan receptor γt: a promising target for the treatment of psoriasis. Front Immunol. 2018; 9(1): 1210.
- ↑Cervantes-Durán C, Avalos-Viveros M, Torner L et al. The 5-HT1A receptor agonist, 8-OH-DPAT, attenuates long-lasting pain in imiquimod-induced psoriasis in mice. Exp Dermatol. 2022; 31(4): 600-607.
- Yiu ZZ, Warren RB. Novel oral therapies for psoriasis and psoriatic arthritis. Am J Clin Dermatol. 2016; 17(3): 191-200.
- ↑Steinckwich N, Myers P, Janardhan KS et al. Role of the store-operated calcium entry protein, STIM1, in neutrophil chemotaxis and infiltration into a murine model of psoriasis-in flamed skin. FASEB J. 2015: 29(7): 3003-3013.
Luisa Martos Cabrera
Servicio de Dermatología del Hospital Universitario de La Princesa
C/ Diego de León, 62 · 28006 Madrid
Tlf.: +34 91 520 24 33 | E-Mail: luisa.martoscabrera@gmail.com
Año 2023 · número 140 (02) · páginas 142 a 152
Enviado: 03.06.23
Revisado: 09.06.23
Aceptado: 24.06.23


