Resumen
Este trabajo pretende profundizar en los mecanismos moleculares involucrados en los daños tisulares secundarios al envejecimiento y el posible efecto protector del cannabidiol (CBD) frente a estas lesiones en músculo, hígado, pulmón y sistema inmunitario. Se administró CBD durante 2,5 meses a la dosis diaria de 10 mg / Kg de peso en la comida preparada especialmente para este fin en ratas macho viejas Long Evans de 15 meses. La mitad de ellas (n = 14) se alimentaron durante 2,5 meses con el CBD y la otra mitad (n=15) con comida standard. Se utilizan además machos jóvenes de 2 meses (n=10) y de 5 meses (n= 8) como controles. Tras el sacrificio se obtiene el tejido muscular, hepático y el pulmonar para investigar por PCR la expresión génica y por Western Blot la cantidad de proteína de los parámetros de estrés oxidativo, inflamación y apoptosis más comunes. Los antioxidantes se midieron por ELISA. También se estudia en la sangre y en el bazo la función inmunitaria a través de la medida de la actividad Natural killer(NK), de la linfoproliferación y del estado redox de la misma. Se puede observar que el envejecimiento supone un incremento significativo de todos los parámetros de daño tisular en todos los tejidos estudiados con el consiguiente incremento de estrés oxidativo, inflamación y apoptosis y que la administración crónica de CBD es capaz de disminuir significativamente estos parámetros tanto en músculo, hígado como en pulmón, así como de potenciar la función inmunitaria con lo que podemos deducir que el CBD es un excelente protector frente al daño tisular inducido por el envejecimiento.
Abstract
This paper intents to investigate in depth on the molecular mechanisms involved in the aging dependent tissular damage and the possible protective effect of cannabidiol CBD on these lesions in the muscle, liver, lungs and the immune system. CBD was administered for 10 weeks at the daily dosage of 10 mg/ Kg body weight / day in a special rat chow prepared for that purpose to 15 months old male Long Evans rats. Half of the animals (n=14) were given CBD during 2,5 months whereas the other half (n= 15) were given standard rat chow for the same time. Additional male rats of 2 (n=10) and 5 (n= 8) months of age fed with standard rat chow were used as young controls. Muscle, liver and lung tissues were obtained after sacrifice to investigate the gene expression by PCR and the protein expression by Western blotting of the main oxidative stress, inflammation and apoptosis markers. Antioxidants were measured by ELISA. In the blood and spleen several markers for immune function like NK activity, lymphoproliferation and oxidative situation were also measured. Aging is associated with the increase of markers for tissular damage that involve the enhancement of nearly all oxidative stress, inflammation and apoptosis parameters Chronic administration of CBD reduces significantly all these parameters in muscle, liver and lungs and potentiates the immune system increasing NK activity and lymphoproliferation and reducing also oxidative stress. CBD has demonstrated to be a very good protective substance against age generated tissular damage in muscle, liver and lungs and an immune system enhancer.
Palabras clave: Inflamación; Estres oxidativo; Apoptosis; Cannabidiol; Envejecimiento; Higado; Pulmones; Músculo sistema inmunitario.
Keywords: Inflammation; Oxidative stress; Apoptosis; Cannabidiol; Aging; Liver; Lung; Muscle; Immune system.
INTRODUCCIÓN
El envejecimiento aparece porque las reacciones metabólicas que ocurren en las mitocondrias de nuestro cuerpo además de generar energía producen radicales libres que son los responsables del deterioro tisular. Precisamente entre los factores que juegan un papel importante en el envejecimiento [1], está la disfunción mitocondrial, que se caracteriza por un incremento del estrés oxidativo con aumento de la inflamación y consiguientemente, aumento también de la apoptosis lo que lleva al deterioro tisular y disminución de la funcionalidad de los órganos. Por todo ello, se acepta que son estos procesos los que contribuyen de manera evidente al deterioro tisular secundario al envejecimiento. Al comienzo de la vida, la producción de radicales libres es muy reducida, pero con los años se va incrementando de forma exponencial a la vez que disminuye la producción de antioxidantes, lo que supone un incremento del estrés oxidativo [2] y de la inflamación [3] que lleva también al aumento de la apoptosis.
El incremento del estrés oxidativo puede resultar tanto de un aumento en la producción de precursores de radicales de oxígeno reactivos, o de las propias especies reactivas del oxígeno (ROS), como de una reducción de los sistemas antioxidantes o de una combinación de todos ellos [4]. Con el avance del envejecimiento, las acciones de las ROS y de otros radicales son mucho más perjudiciales [5] porque los sistemas antioxidantes se ven disminuidos y por tanto existe una mayor probabilidad de que los ROS ejerzan su acción sobre sus moléculas diana que pueden ser proteínas, ácidos nucleicos y lípidos [6]. Con el envejecimiento, los niveles tisulares de antioxidantes que se producen de forma natural como el glutatión (GSH), la enzima superóxido dismutasa (SOD) y la catalasa (CAT) se reducen y por lo tanto, el estado antioxidante total está disminuido. Durante el proceso de envejecimiento se va a producir un deterioro progresivo de los diferentes órganos lo que va a conducir a la pérdida de sus funciones fisiológicas.
El proceso de deterioro no es igual en los diferentes individuos ni tampoco en los diferentes órganos y ello ha motivado la búsqueda de las causas de dichas diferencias con la intención de tratar de conseguir un enlentecimiento del proceso [7]. Aunque una parte de esta variabilidad pueda tener un origen genético, la verdad que es un proceso multifactorial en donde juegan un papel los estilos de vida y también otros factores externos [8], lo que ha conducido a la búsqueda de sustancias que puedan reducir las lesiones asociadas al envejecimiento y pudiesen conducir a una terapia antienvejecimiento [9].
Es imposible evitar el envejecimiento de nuestro organismo, pero es posible retardarlo. Muchos estudios han demostrado que un aporte suplementario de antioxidantes reduce la incidencia de ciertas enfermedades y mejora el estado de salud de los ancianos. La terapia con antioxidantes como la melatonina o el resveratrol [10,11,12] han demostrado ser capaces de reducir el estrés oxidativo, la inflamación y la apoptosis en diversos tejidos en animales viejos. También los cannabinoides parece que actúan de manera similar [5,13] incluso protegiendo algunos tejidos de la acción tóxica de sustancias que fomentan estrés oxidativo, inflamación y apoptosis [14].
CBD
El CBD es un cannabinoide presente en el cáñamo indio (Cannabis indica) y uno de los ingredientes fundamentales de la marihuana. Al revés de lo que ocurre con el Tetrahidrocannabinol (THC) carece de efectos psicotrópicos y su uso es legal en la mayoría de los países del mundo occidental [15].
Se ha sugerido que este compuesto podría participar activamente en la reducción de los fenómenos oxidativos responsables del envejecimiento impidiendo el efecto negativo de los radicales libres [14,16]. Aunque el CBD se aisló ya en los años 40 del pasado siglo y su estructura molecular se pudo establecer en los años 60, solo muy recientemente se ha incrementado de forma importante el interés en dicha sustancia [17,18]. Su mecanismo de acción no está todavía completamente claro hoy, aunque se conocen muchos receptores a través de los que ejerce su acción.
Los receptores de los cannabinoides propiamente tales según se fueron descubriendo se les fue nominando como CB1 o CB2 y finalmente CB3 [19]. Así como los receptores CB1 están fundamentalmente localizados en el sistema nervioso central (SNC) donde desempeñan acciones en los procesos de memoria, cognición, actividad motora y también están presentes en los nervios periféricos donde contribuyen a la percepción del dolor [20]. Los receptores CB2 están localizados en el sistema inmunitario donde juegan un papel importante en la regulación de las citoquinas proinflamatorias. Sin embargo, el grado de afinidad del CBD por estos receptores es baja ya que su interacción más importante es con el THC y también con los endocannabinoides.
Por el contrario, la acción ansiolítica, relajante, antidepresiva e inductora de sueño parece que tiene lugar a través de la interacción del CBD sobre receptores de 5HT1(serotonina) [21,22] aumentando la disponibilidad de este neurotransmisor cerebral.
En el caso de los efectos antiálgicos y especialmente del dolor neuropático parece ocurrir a través de su interacción con receptores de potencial transitorio (TRP) de tipo vanilloide, que es el mismo tipo de receptor que utiliza la capsaicina para actuar favorablemente sobre el dolor neuropático [23].
Además de los mecanismos mencionados, el CBD parece actuar también inhibiendo la recaptación de endocannabinoides como la anandamida y además también como modulador alostérico del receptor de GABA (tipo Valium) [24].
Los cannabinoides endógenos (endocannabinoides) [25] intervienen en numerosas funciones fisiológicas lo que incluye la modulación del dolor, las respuestas al estrés, el aprendizaje y la memoria y tienen también efectos ansiolíticos, pero además, facilitan la curación acelerada de las heridas [26]. Tienen estructura lipídica como la anandamida (AEA) y el 2-araquidonoilglicerol (2-AG) y comparten sus receptores (CB1 and CB2) y también otros unidos a proteínas G con otros cannabinoides como el THC. Se sintetizan a partir de fosfolípidos de membrana por acción de la acil fosfatidiletanolamina fosfolipasa D (NAPE-PLD) y se metabolizan por la hidrolasa de las amidas de ácidos grasos (en inglés, fatty acid amide hydrolase FAAH) y también por la monoacilglicerol lipasa (MAGL) [27]. Otros componentes de los cannabinoides, además de los anteriores, son la oleoiletanolamida (OEA) y la palmitoiletanolamida (PEA). Además de los receptores mencionados, los endocannabinoides utilizan también otros como el TRPV1 y el PPARα. Precisamente estos receptores son potenciales dianas terapéuticas para un amplio grupo de enfermedades que incluyen enfermedades degenerativas neurológicas como el Alzheimer o el Parkinson, pero también la depresión, la ansiedad y el dolor crónico [26].
Un elemento muy importante en la regulación de los endocannabinoides es precisamente la FAAH que cataboliza no solo anandamida sino también AEA, OEA, PEA y otros lípidos [28,29]. La FAAH es muy abundante en el hígado, en el cerebro [30,31] y también en las raíces nerviosas de los ganglios dorsales o lo que es igual en aquellas regiones relacionadas con la transmisión del dolor que incluyen la amígdala, el tálamo y la sustancia gris periacueductal [32].
En los últimos 20 años se han desarrollado muchas sustancias inhibidoras de la FAAH para intentar aumentar la acción de los endocannabinoides aunque ninguna ha podido llegar a alcanzar el ámbito de la clínica [33,34] por sus efectos secundarios. Sin embargo, muy recientemente se ha descrito una paciente en el Reino Unido que presentaba una ausencia total de percepción dolorosa desde el nacimiento que resultó carecer de FAAH por lo que sus niveles de endocannabinoides eran muy elevados y eso suponía la incapacidad de percibir ningún tipo de dolor [35].
Todos estos datos proporcionan precisamente la posibilidad de actuación del CBD como elemento protector tisular en base a sus efectos antioxidantes y antiinflamatorios y por ello, se decidió realizar este estudio para comprobar los posibles efectos beneficiosos del CBD tanto en tejidos como en el sistema inmunitario.
La investigación se ha llevado a cabo en ratas Long Evans (Janvier Labs, Le Genest Saint Isle, France) de dos y cinco meses de edad que han servido como jóvenes controles y otras de 15 meses de edad que se han usado como ratas viejas para investigar las alteraciones debidas a la edad y el efecto que sobre dichas alteraciones tiene la administración oral de CBD. Esta se llevó a cabo mediante la adición de CBD (CBD full spectrum Phexia, Madrid, España) durante 10 semanas a la comida de los animales.
Tras el período de tratamiento los animales fueron sacrificados por decapitación con guillotina. Tras el sacrificio se disecaron los órganos de interés, en este caso, sangre, bazo, músculo, hígado y pulmones, se congelaron en nitrógeno líquido y se mantuvieron a -80ºC hasta su análisis.
La realización de los análisis bioquímicos en hígado y pulmón han tenido lugar en los departamentos de Fisiología y de Bioquímica y Biología molecular de la Facultad de Medicina de la Universidad Complutense de Madrid. El estudio de la función inmunitaria y en músculo se ha llevado a cabo en el departamento de Genética, Fisiología y Microbiología (Unidad de Fisiología Animal) de la Facultad de Biología de la Universidad Complutense de Madrid.
RESULTADOS Y DISCUSION
Estudio inmunitario
Se obtuvieron durante el sacrificio de los animales tanto jóvenes como viejos a las 10 semanas de tratamiento con CBD muestras de bazo, timo y fracción celular de células blancas de la sangre que fueron procesadas inmediatamente tras someter a las muestras a un proceso de cultivo ex vivo para determinar actividad NK , la linfoproliferación y el estrés oxidativo. Lo mismo se llevó a cabo en los dos grupos de animales jóvenes sin tratamiento [36].
A nivel del sistema inmunitario se ha podido observar una disminución de la actividad NK (asesinas por naturaleza) en las ratas viejas en comparación con los jóvenes controles y una disminución además de la linfoproliferación, tanto la inducida por concavalina A como la inducida por lipopolisacárido (LPS) La administración de CBD produjo efectos muy beneficiosos ya que se ha visto una potenciación significativa (p<0,001) de la actividad de las células NK que juegan un papel muy importante en la defensa frente a las células tumorales y una recuperación de las dos respuestas linfoproliferativas (p<0,05). Además, se ha podido constatar también un incremento del estrés oxidativo a nivel de las células sanguíneas con aumento de malondialdehído (MDA) (p<0,001) y de glutatión oxidado (GSSG) (p<0,05) con disminución de glutatión reducido (GSH) (p<0,05). El tratamiento con CBD presenta un efecto antioxidante muy potente en el sistema inmunitario, con disminución de MDA (p<0,05) y GSSG (p<0,01) e incremento del GSH (p<0,05) lo que lleva en términos prácticos a un incremento de su capacidad de defensa del organismo.
Esto significa que el CBD sería capaz de potenciar el sistema inmunitario en los pacientes que lo reciban mejorando por lo tanto su capacidad de respuesta a infecciones de todo tipo.
Efecto sobre el músculo
En el sacrificio de los animales se obtienen muestras de los músculos digástrico y gastrocnemio que se congelan en el momento en nitrógeno líquido y luego se mantiene a -80ºC hasta su procesamiento.
Puede observarse que los animales viejos presentan un aumento de MDA (p<0,05) muscular tanto absoluto como cuando se establece una relación con los mg de proteína. Este efecto es neutralizado por el tratamiento con CBD con lo que consigue mejorar de forma evidente la capacidad funcional del musculo.
Efecto sobre el hígado
Se comprobó utilizando una tinción con hematoxilina-eosina si el envejecimiento era capaz de generar lesiones evidenciables a nivel del tejido hepático de los animales viejos y no se pudo detectar ninguna alteración significativa, ni tampoco en los animales tratados con CBD. Sin embargo, al analizar la concentración de mieloperoxidasa (MPO) en el parénquima hepático se detectó un aumento significativo en los animales viejos que se reducía significativamente hasta alcanzar los valores de los jóvenes al tratarlos con CBD. Esto supone la constatación en las ratas de 15 meses de edad de que el hígado presenta ya una infiltración de macrófagos y neutrófilos activados como primer paso de las lesiones que aparecerán algo más adelante [36,37]. Se han determinado parámetros relacionados con el estrés oxidativo como son la glutatión peroxidasa (GPx) y la glutatión S transferasa (GST), con la inflamación como el factor de necrosis tumoral alfa (TNF-α), y la interleucina 1 beta (IL-1β) y con la apoptosis como es la proteína X asociada a Bcl-2 (BAX) y el factor inductor de apoptosis (AIF).
Puede verse como los niveles de MDA, marcador de estrés oxidativo, están significativamente incrementados en los animales viejos (p<0,05) y como el tratamiento con CBD los retorna a los valores de las ratas jóvenes.
Puede observarse también que los niveles de interleucina IL-1β, marcador de inflamación, en el hígado se incrementan mucho con el envejecimiento (p<0,001) y como el tratamiento con CBD es capaz de evitar dicho incremento. De la misma forma ocurre con el tumor necrosis factor (TNF-α) que es otro marcador de inflamación, se incrementa mucho con el envejecimiento (p<0,001) y el tratamiento con CBD lo impide.
El factor nuclear kappa B (NF-κB) que es otro marcador muy importante de inflamación experimenta también un incremento significativo con el envejecimiento en todos sus heterodímeros (NFκB-p65, NFκB-p52, NFκB-p50), que sin embargo, se restablecen totalmente al tratar a las ratas con CBD (p<0,001).
Como parámetros relacionados con el estrés oxidativo tenemos también la GST, la GPx y la glutatión reductasa (GR). La primera sufre una reducción marcada con el envejecimiento (p<0,01) que es bloqueada por el tratamiento con CBD. La GPx y la GR disminuyen también significativamente (p<0,01) con la edad y de igual forma el tratamiento con CBD es capaz de evitarlo.
Finalmente, si estudiamos la apoptosis, vemos como los niveles de BAX que es una proteína proapoptótica se incrementan mucho con el envejecimiento y el CBD lo impide de manera muy evidente (p<0,0001).
Otro elemento que juega un papel importante en la apoptosis y también en la inflamación son las caspasas. Así podemos ver como la caspasa 1 (CASP-1) se incrementa con el envejecimiento (p<0,0001) en la rata Long Evans y el tratamiento con CBD la reduce. Puede observarse el aumento significativo del AIF con la edad y como el tratamiento crónico con CBD disminuye los valores hasta el nivel presente en los animales jóvenes (p<0,0001).
Todos los cambios inducidos por el tratamiento con CBD son altamente significativos como puede verse en los valores de p. Los valores pueden verse en la tabla 1.
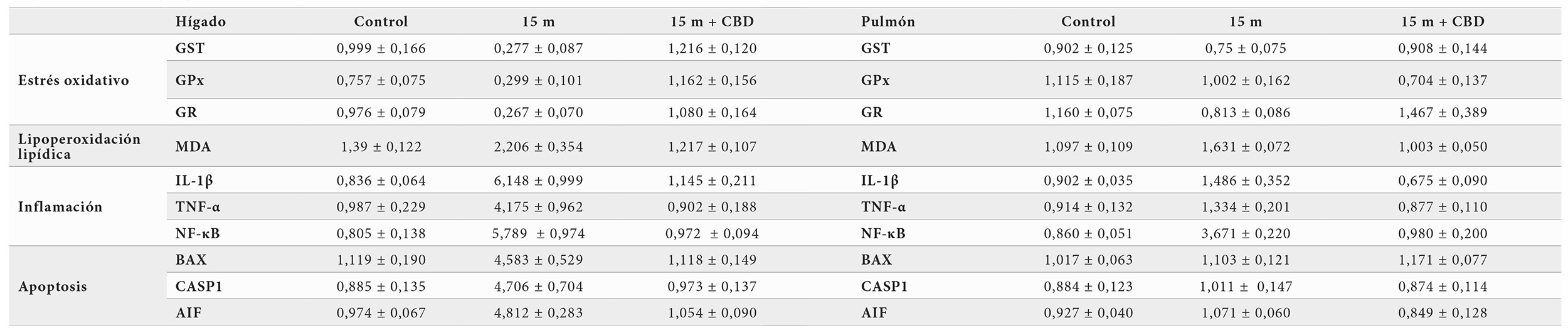
De todos estos datos puede deducirse que el CBD es capaz de reducir el estrés oxidativo, la inflamación y la apoptosis en el hígado. También reduce el estrés oxidativo en el músculo y finalmente estimula al sistema inmunitario que está reducido en su función también con la edad.
Lo mismo que hemos visto antes en cuanto a la expresión de los genes de las distintos productos se ha observado también en la expresión de las proteínas correspondientes, aunque existen diferencias. NFκB aumenta con el envejecimiento (p<0,01) y el tratamiento con CBD lo disminuye (p<0,05). También aumenta AIF (p<0,05) y el tratamiento con CBD lo evita (p<0,01).
De todo lo mencionado hasta ahora se deduce que en el hígado de las ratas macho Long Evans viejas existe un aumento del estrés oxidativo asociado al envejecimiento con incrementos de MDA y de hemo-oxigenasa 1 (HO-1) a la vez que disminuye la actividad de los enzimas antioxidantes GR, GPx, y GST al compararlos con los jóvenes controles. La administración crónica de CBD ha sido capaz de revertir la situación reduciendo los niveles de radicales libres de oxígeno y restaurando lo niveles de actividad enzimática como se había demostrado ya con anterioridad en otros estudios [38], con lo que se consigue una efectiva protección celular [39].
GR y GPx son enzimas responsables de la reducción y oxidación del GSH. También se protege a las células del daño oxidativo al restaurar los niveles de expresión de GST que se expresa de manera elevada en el hígado [38,40].
El CBD, es capaz de bloquear las reacciones oxidativas de los radicales libres, bien sea quelando éstos directamente o bien metabolizándolos en otras sustancias menos reactivas [39]. Esto ha podido verse anteriormente en modelos experimentales en ratones [14] y también en cultivos celulares in vitro [41]. Concretamente el CBD impide la formación de radicales superóxido. También ha demostrado ser capaz de reducir los niveles de óxido nítrico (NO) en el hígado tras la administración de un citostático a ratones [42].
El CBD reduce además la producción de especies reactivas de oxígeno (ROS) mediante el bloqueo de la reacción de Fenton mediada por metales [43].
La actividad antioxidante del CBD se inicia mediante la activación del factor Nrf2 (Nrf2 es un factor de transcripcion derivado del eritroide 2 que regula la defensa frente al estres oxidativo) [44] que es responsable de la transcripción de algunos antioxidantes potentes y de genes citoprotectores [6]. También es capaz de aumentar los diversos heterodímeros de la SOD que son responsables de su acción antiinflamatoria [45].
La interacción de los ROS con los ácidos grasos insaturados da lugar a la aparición de hidroperóxidos lipídicos y aldehídos, como el 4-hidroxinonenal (4-HNE), o el MDA [46]. También pueden formarse incluso isoprostanos [47]. Estos procesos activan el factor nuclear Nrf2 y además modifica el funcionamiento de las membranas celulares y potencia a algunos prooxidantes mediados por la vía del NFκB a la vez que inhibe los enzimas antioxidantes (ej, tiorredoxina reductasa y CAT) [48].
Todo ello conduce a la alteración de los procesos metabólicos que conduce a la disfunción celular e incluso a su muerte por apoptosis [49]. Además, el estrés oxidativo favorece la lipoperoxidación y la oxidación de proteínas lo que también contribuye a alterar la función celular a través de su influencia sobre el metabolismo [4,50].
En situaciones de inflamación el CBD es capaz de aumentar la actividad tanto de la GPx como de la GR, lo que conduce a una reducción importante de los marcadores de estrés oxidativo como el MDA [20], mientras que incrementa los valores de GSH.
En el estudio también pudimos constatar el incremento de los marcadores hepáticos de inflamación como NFκB-p65, NFκB-p52, NFκB-p50, IL-1β y TNF-α en el grupo de animales viejos, al compararlos con los jóvenes lo que confirma la presencia con la edad de un aumento de la inflamación además del incremento del ya mencionado estrés oxidativo. El tratamiento con CBD fue también capaz de reducir los niveles de estos parámetros hasta volver a alcanzar los niveles de expresión de las ratas jóvenes.
El CBD ha demostrado además ser capaz de modular al sistema endocannabinoide aumentando los niveles de anandamida, lo que modifica la interacción de los cannabinoides con sus receptores [51]; por lo que la acción antioxidante más importante del CBD ocurre precisamente por su interacción con dichos receptores. De hecho, los receptores activados por peroxisomas alfa (PPAR-α), estimulan la producción de antioxidantes como la SOD [5]. Además dependiendo de su concentración el CBD, puede activar o inhibir distintos tipos de receptores cannabinoides (CB1 y CB2), o también otros tipos como los (TRP) o los nucleares como los (PPAR).
En el tejido hepático de los animales viejos también se incrementan los marcadores de apoptosis AIF, BAX, and CASP-1 tanto en su expresión génica como en la proteica medida por Western blot y el tratamiento con CBD es capaz de revertir sobre todo la expresión génica significativamente, con lo que se justifica suficientemente la disminución de las lesiones tisulares.
Los niveles del marcador antiapoptótico Bcl-2 no se modifican por el envejecimiento ni tampoco por el tratamiento con CBD como ya se había observado previamente. Por ello es más correcto utilizar la relación entre Bcl-2 y BAX que ésta sí que disminuye siempre durante los procesos apoptóticos [52] como ocurre también en nuestro estudio. El tratamiento con CBD es capaz de restaurar los niveles de dicha relación con lo que disminuye la muerte celular.
En nuestro modelo de rata macho Long Evans de 15 meses no se detecta a nivel histológico básico ninguna alteración tisular probablemente porque estamos todavía en una situación inicial de vejez. Sin embargo, sí se detecta un aumento de la MPO que es sinónimo de infiltración inmunitaria como primer paso para una eventual alteración histológica tanto sea con infiltración de macrófagos como de neutrófilos activados. Este incremento de MPO no aparece en el grupo de animales viejos tratados con CBD con lo que se confirma su efecto beneficioso.
Efectos a nivel del pulmón
A nivel del pulmón se han investigado los mismos parámetros relacionados con la edad que en el hígado y se ha podido evidenciar un aumento del estrés oxidativo por el aumento del MDA (p<0,01) que fue revertido de forma eficaz por el tratamiento con CBD. Aunque se vio también una disminución en los niveles de enzimas antioxidantes GST y GPx, sin embargo, no fue significativo. Por el contrario, la expresión génica de NFκB (p<0,001), TNF-α (p<0,05) y de IL-1β (p<0,05) están muy incrementadas en los animales de 15 meses con respecto a los jóvenes; lo que significa que el pulmón está muy inflamado como habíamos visto anteriormente en el pulmón de ratas viejas Wistar [53]. El tratamiento con CBD es capaz de disminuir significativamente dichos valores hasta recuperar los niveles de los jóvenes con lo que disminuyen los niveles de la inflamación. (Ver los valores en la tabla 1).
En cuanto al comportamiento de los marcadores de apoptosis AIF y CASP-1 estos también sufren un aumento significativo con la edad en el tejido pulmonar (p<0,001), que asimismo se reduce significativamente por la administración de CBD.
Sin embargo, los resultados de BAX no se modifican con la edad lo que haría pensar que el pulmón está algo menos afectado por el envejecimiento en virtud de su permanente situación prooxidante frente a la que tiene que defenderse, como habíamos observado anteriormente en ratas Wistar [53].
Todos estos datos indican que los pulmones que son órganos especialmente expuestos a la acción oxidante del aire atmosférico y de los elementos polucionantes que lleva en suspensión, presentan también con el envejecimiento toda una serie de alteraciones oxidativas inflamatorias y apoptóticas ya detectadas anteriormente [54]. El tratamiento con CBD es capaz de neutralizar al menos en parte dichas alteraciones alcanzando de nuevo los valores de los animales jóvenes.
Podemos concluir que el tratamiento crónico con CBD en ratas Long Evans de 15 meses tiene un efecto muy positivo a nivel del músculo, del pulmón y más significativamente en el hígado y en el sistema inmunitario disminuyendo las lesiones tisulares inducidas por el estrés oxidativo, la inflamación y la apoptosis asociadas a la edad.
DECLARACIÓN DE TRANSPARENCIA
Los autores/as de este artículo declaran no tener ningún tipo de conflicto de intereses respecto a lo expuesto en el presente trabajo.
BIBIOGRAFÍA
- ↑López-Otín C, Blasco MA, Partridge L, Serrano M, Kroemer G. The hallmarks of aging. Cell. 2013; 153: 1194-1217. doi:10.1016/j.cell.2013.05.039.
- ↑Kireev R, Bitoun S, Cuesta S et al. Treatment protects liver of zucker rats after ischemia/reperfusion by diminishing oxidative stress and apoptosis. Eur J Pharmacol. 2013; 701: 185-193. doi:10.1016/j.ejphar.2012.11.038.
- ↑Kireev RA, Vara E, Viña J, Tresguerres JAF. Melatonin and oestrogen treatments were able to improve neuroinflammation and apoptotic processes in dentate gyrus of old ovariectomized female rats. Age (Dordr). 2014; 36: 9707. doi:10.1007/s11357-014-9707-3.
- ↑Dalleau S, Baradat M, Guéraud F, Huc L. Cell death and diseases related to oxidative stress: 4-Hydroxynonenal (HNE) in the balance. Cell Death Differ. 2013; 20: 1615-1630. doi:10.1038/cdd.2013.138.
- ↑Gallelli CA, Calcagnini S, Romano A et al. Modulation of the oxidative stress and lipid peroxidation by endocannabinoids and their lipid analogues. Antioxidants (Basel). 2018; 7: 93. doi:10.3390/antiox7070093.
- ↑Vomund S, Schäfer A, Parnham MJ, Brüne B, von Knethen A. Nrf2, the master regulator of anti-oxidative responses. Int J Mol Sci. 2017; 18: 2772. doi:10.3390/ijms18122772.
- ↑Partridge L, Deelen J, Slagboom PE. Facing up to the global challenges of ageing. Nature. 2018; 56: 45-56. doi:10.1038/s41586-018-0457-8.
- ↑Steves CJ, Spector TD, Jackson SHD. Ageing, genes, environment and epigenetics: What twin studies tell us now, and in the future. Age Ageing. 2012; 41: 581-586. doi:10.1093/ageing/afs097.
- ↑Di Micco R, Krizhanovsky V, Baker D, d’Adda di Fagagna, F. Cellular senescence in ageing: From mechanisms to therapeutic opportunities. Nat Rev Mol Cell Biol. 202; 22: 75-95. doi:10.1038/s41580-020-00314-w.
- ↑Tresguerres JAF, Kireev R, Forman K, Cuesta S, Tresguerres AF, Vara E. Effect of chronic melatonin administration on several physiological parameters from old wistar rats and SAMP8 mice. Curr Aging Sci. 2012; 5: 242-253. doi:10.2174/1874609811205030012.
- ↑Paredes SD, Rancan L, Kireev R et al. Melatonin counteracts at a transcriptional level the inflammatory and apoptotic response secondary to ischemic brain injury induced by middle cerebral artery blockade in aging rats. Biores Open Access. 2015; 4(1): 407-416. doi:10.1089/biores.2015.0032.
- ↑Paredes SD, Rancan L, Cruz García M, Vara E, Tresguerres JAF. Resveratrol and aging. En: Joseph M Wu and Tze-chen Hsieh, editors. Resveratrol: State-of-the-art science and health applications. Singapore: World Scientific; 2018; p. 257-273.
- ↑Oh YT, Lee JY, Lee J, Lee JH, Kim J-E, Ha J, Kang I. Oleamide suppresses lipopolysaccharide-induced expression of iNOS and COX-2 through Inhibition of NF-kappaB activation in BV2 murine microglial cells. Neurosci Lett. 2010; 474: 148-153. doi:10.1016/j.neulet.2010.03.026.
- ↑Pan H, Mukhopadhyay P, Rajesh M. Cannabidiol attenuates cisplatin-induced nephrotoxicity by decreasing oxidative/nitrosative stress, inflammation, and cell death. J Pharmacol Exp Ther. 2009; 328: 708-714. doi:10.1124/jpet.108.147181.
- ↑Zuardi AW. History of cannabis as a medicine: a review. Braz J Psychiatry. 2006; 28: 153-157. doi:10.1590/s1516-44462006000200015.
- ↑Atalay S, Jarocka-Karpowicz I, Skrzydlewska E. Antioxidative and anti-inflammatory properties of cannabidiol. Antioxidants (Basel). 2019; 9: 21. doi:10.3390/antiox9010021.
- ↑Bonini SA, Premoli M, Tambaro S et al. Cannabis sativa: a comprehensive ethnopharmacological review of a medicinal plant with a long history. J Ethnopharmacol. 2018; 227: 300-315. doi:10.1016/j.jep.2018.09.004.
- ↑Lintzeris N, Driels J, Elias N, Arnold JC, McGregor IS, Allsop DJ. Medicinal cannabis in Australia, 2016: the cannabis as medicine survey (CAMS-16). Med J Aust. 2018; 20: 211-216. doi:10.5694/mja17.01247.
- ↑Tham M, Yilmaz O, Alaverdashvili M, Kelly MEM, Denovan-Wright EM, Laprairie RB. Allosteric and orthosteric pharmacology of cannabidiol and cannabidiol-dimethylheptyl at the type 1 and type 2 cannabinoid receptors. Br J Pharmacol. 2019; 176: 1455-1469. doi:10.1111/bph.14440.
- ↑Costa B, Trovato AE, Comelli F, Giagnoni G, Colleoni M. The non-psychoactive cannabis constituent cannabidiol is an orally effective therapeutic agent in rat chronic inflammatory and neuropathic pain. Eur J Pharmacol. 2007; 556: 75-83. doi:10.1016/j.ejphar.2006.11.006.
- ↑Zuardi AW, Cosme RA, Graeff FG, Guimarães FS. Effects of ipsapirone and cannabidiol on human experimental anxiety. J Psychopharmacol. 1993; 7: 82-88. doi:10.1177/026988119300700112.
- ↑Linge R, Jiménez-Sánchez L, Campa L et al. Cannabidiol induces rapid-acting antidepressant-like effects and enhances cortical 5-HT/glutamate neurotransmission: Role of 5-HT1A Receptors. Neuropharmacology. 2016; 103: 16-26. doi:10.1016/j.neuropharm.2015.12.017.
- ↑Sagredo O, Ramos JA, Decio A, Mechoulam R, Fernández-Ruiz J. Cannabidiol reduced the striatal atrophy caused 3-nitropropionic acid in vivo by mechanisms independent of the activation of cannabinoid, vanilloid TRPV1 and adenosine A2A receptors. Eur J Neurosci. 2007; 26: 843-851. doi:10.1111/j.1460-9568.2007.05717.x.
- ↑Leweke FM, Piomelli D, Pahlisch F. Cannabidiol enhances anandamide signaling and alleviates psychotic symptoms of schizophrenia. Transl Psychiatry. 2012; 2: e94. doi:10.1038/tp.2012.15.
- ↑Di Marzo V, Bifulco M, De Petrocellis L. The Endocannabinoid system and its therapeutic exploitation. Nat Rev Drug Discov. 2004; 3: 771-784. doi:10.1038/nrd1495.
- ↑Lowe H, Toyang N, Steele B, Bryant J, Ngwa W. The endocannabinoid system: a potential target for the treatment of various diseases. Int J Mol Sci. 2021; 22: 9472. doi:10.3390/ijms22179472.
- ↑Cristino L, Bisogno T, Di Marzo V. Cannabinoids and the expanded endocannabinoid system in neurological disorders. Nat Rev Neurol. 2020; 16: 9-29. doi:10.1038/s41582-019-0284-z.
- ↑Deutsch DG, Chin SA. Enzymatic synthesis and degradation of anandamide, a cannabinoid receptor agonist. Biochem Pharmacol. 1993; 46: 791-796. doi:10.1016/0006-2952(93)90486-g.
- ↑Cravatt BF, Giang DK, Mayfield SP, Boger DL, Lerner RA, Gilula NB. Molecular characterization of an enzyme that degrades neuromodulatory fatty-acid amides. Nature. 1996; 384: 83-87. doi:10.1038/384083a0.
- ↑Tsou K, Nogueron MI, Muthian S. Fatty Acid Amide Hydrolase is located preferentially in large neurons in the rat central nervous system as revealed by immunohistochemistry. Neurosci Lett. 1998; 254: 137-140. doi:10.1016/s0304-3940(98)00700-9.
- ↑Egertová M, Cravatt BF, Elphick MR. Comparative analysis of Fatty Acid Amide Hydrolase and Cb(1) Cannabinoid receptor expression in the mouse brain: Evidence of a widespread role for Fatty Acid Amide Hydrolase in regulation of endocannabinoid signaling. Neuroscience. 2003; 11: 481-496. doi:10.1016/s0306-4522(03)00145-3.
- ↑Lau BK, Drew GM, Mitchell VA, Vaughan CW. Endocannabinoid modulation by FAAH and monoacylglycerol lipase within the analgesic circuitry of the periaqueductal grey. Br J Pharmacol. 2014; 171: 5225-5236. doi:10.1111/bph.12839.
- ↑Bisogno T, Maccarrone M. Latest advances in the discovery of Fatty Acid Amide Hydrolase inhibitors. Expert Opin Drug Discov. 2013; 8: 509-522. doi:10.1517/17460441.2013.780021.
- ↑Tripathi RKP. A perspective review on Fatty Acid Amide Hydrolase (FAAH) inhibitors as potential therapeutic agents. Eur J Med Chem. 2020; 188: 111953. doi:10.1016/j.ejmech.2019.111953.
- ↑Mikaeili H, Habib AM, Yeung CWL et al. Molecular basis of FAAH-OUT-Associated human pain insensitivity. Brain. 2023; 146: 3851-3865. doi:10.1093/brain/awad098.
- ↑Díaz-Del Cerro, Félix J, Joyera N, Tresguerres JAF, De la Fuente M. El Cannabidiol: Posible estrategia para mejorar la inmunosenescencia y el estrés oxidativo del envejecimiento en ratas macho : 63º Congreso de la Sociedad Española de Geriatría y Gerontología (SEGG), Junio 2023, Pamplona, España.
- ↑Mazzoli A, Crescenzo R, Cigliano L et al. Early hepatic oxidative stress and mitochondrial changes following western diet in middle aged rats. Nutrients. 2019; 11: 2670. doi:10.3390/nu11112670.
- ↑Park JH, Ha H. Short-term treatment of Daumone improves hepatic inflammation in aged mice. Korean J Physiol Pharmacol. 2015; 19. 269-274. doi:10.4196/kjpp.2015.19.3.269.
- ↑Yang W, Burkhardt B, Fischer L et al. Age-dependent changes of the antioxidant system in rat livers are accompanied by altered MAPK activation and a decline in motor signaling. EXCLI J. 2015; 14: 1273-1290. doi:10.17179/excli2015-734.
- ↑Rancan L, Linillos-Pradillo B, Centeno J, Paredes SD, Vara E, Tresguerres JAF. Protective actions of cannabidiol on aging-related inflammation, oxidative stress and apoptosis alterations in liver and lung of long evans rats. Antioxidants (Basel). 2023; 12: 1837. doi:10.3390/antiox12101837.
- ↑Salminen LE, Paul RH. Oxidative stress and genetic markers of suboptimal antioxidant defense in the aging brain: a theoretical review. Rev Neurosci. 2014; 25: 805-819. doi:10.1515/revneuro-2014-0046.
- ↑Rajesh M, Mukhopadhyay P, Bátkai S et al. Cannabidiol attenuates high glucose-induced endothelial cell inflammatory response and barrier disruption. Am J Physiol Heart Circ Physiol. 2007; 293: H610-619. doi:10.1152/ajpheart.00236.2007.
- ↑Fouad AA, Albuali WH, Al-Mulhim AS, Jresat I. Cardioprotective effect of cannabidiol in rats exposed to doxorubicin toxicity. Environ Toxicol Pharmacol. 2013; 36: 347-357. doi:10.1016/j.etap.2013.04.018.
- ↑Hamelink C, Hampson A, Wink DA, Eiden LE, Eskay RL. Comparison of cannabidiol, antioxidants, and diuretics in reversing binge ethanol-induced neurotoxicity. J Pharmacol Exp Ther. 2005; 314: 780-788. doi:10.1124/jpet.105.085779.
- ↑Juknat A, Pietr M, Kozela E et al. Microarray and pathway analysis reveal distinct mechanisms underlying cannabinoid-mediated modulation of lps-induced activation of BV-2 microglial cells. PLoS One. 2013; 8: e61462. doi:10.1371/journal.pone.0061462.
- ↑Rajesh M, Mukhopadhyay P, Bátkai S et al. Cannabidiol attenuates cardiac dysfunction, oxidative stress, fibrosis, and inflammatory and cell death signaling pathways in diabetic cardiomyopathy. J Am Coll Cardiol. 2010; 56: 2115-2125. doi:10.1016/j.jacc.2010.07.033.
- ↑Ayala A, Muñoz MF, Argüelles S. Lipid peroxidation: Production, metabolism, and signaling mechanisms of malondialdehyde and 4-Hydroxy-2-Nonenal. Oxid Med Cell Longev. 2014; 2014: 360438. doi:10.1155/2014/360438.
- ↑Milne GL, Yin H, Hardy KD, Davies SS, Roberts LJ. Isoprostane generation and function. Chem Rev. 2011; 111: 5973-5996. doi:10.1021/cr200160h.
- ↑Łuczaj W, Gęgotek A, Skrzydlewska E. Antioxidants and HNE in redox homeostasis. Free Radic Biol Med. 2017; 111: 87-101. doi:10.1016/j.freeradbiomed.2016.11.033.
- ↑Środa-Pomianek K, Michalak K, Świątek P, Poła A, Palko-Łabuz A, Wesołowska O. Increased lipid peroxidation, apoptosis and selective cytotoxicity in colon cancer cell line lovo and its doxorubicin-resistant subline lovo/dx in the presence of newly synthesized phenothiazine derivatives. Biomed Pharmacother. 2018; 106: 624-636. doi:10.1016/j.biopha.2018.06.170.
- ↑Sottero B, Rossin D, Poli G, Biasi F. Lipid oxidation products in the pathogenesis of inflammation-related gut diseases. Curr Med Chem. 2018; 25: 1311-1326. doi:10.2174/0929867324666170619104105.
- ↑Ibeas Bih C, Chen T, Nunn AV, Bazelot M, Dallas M, Whalley BJ. Molecular targets of cannabidiol in neurological disorders. Neurotherapeutics. 2015; 12(4): 699-730. doi:10.1007/s13311-015-0377-3.
- ↑Pollack M, Phaneuf S, Dirks A, Leeuwenburgh C. The role of apoptosis in the normal aging brain, skeletal muscle, and heart. Ann N Y Acad Sci. 2002; 959: 93-107. doi:10.1111/j.1749-6632.2002.tb02086.x.
- ↑Puig Á, Rancan L, Paredes SD et al. Melatonin decreases the expression of inflammation and apoptosis markers in the lung of a senescence-accelerated mice model. Exp Gerontol. 2016; 75: 1-7. doi:10.1016/j.exger.2015.11.021.
- Acuña-Castroviejo D, Carretero M, Doerrier C et al. Melatonin protects lung mitochondria from aging. Age (Dordr). 2012; 34: 681-692. doi:10.1007/s11357-011-9267-8.
ranm tv
Jesús Á. Fernández-Tresguerres Hernández
Real Academia Nacional de Medicina de España
C/ Arrieta, 12 · 28013 Madrid
Tlf.: +34 91 159 47 34 | E-Mail: guerres@med.ucm.es
Año 2024 · número 141 (01) · páginas 10-18
Enviado*: 21.11.23
Revisado: 26.11.23
Aceptado: 20.12.23
* Fecha de lectura en la RANM


