Resumen
La iniciativa EUCAIM (Cancer Image Europe) es una Infraestructura Digital Europea para la investigación con imágenes médicas en cáncer que surge en el contexto de una transformación radical de la medicina, orientada hacia la precisión, la prevención y la personalización. Este artículo presenta la visión estratégica, los objetivos científicos y técnicos, así como el impacto potencial de EUCAIM como infraestructura digital federada europea para la investigación en oncología basada en imágenes médicas. A través de la integración de datos clínicos y de imagen, el uso de la inteligencia artificial y la estandarización de los procesos de anotación y curación de datos, EUCAIM pretende acelerar la innovación, mejorar la reproducibilidad y facilitar a los investigadores el acceso a datos de alta calidad. Se analiza además su estructura organizativa, el papel de los nodos federados, la interoperabilidad técnica y semántica, y los marcos regulatorios asociados. Finalmente, se discute su papel dentro del Espacio Europeo de Datos de Salud y su sostenibilidad a largo plazo como motor para la investigación clínica avanzada.
Abstract
The EUCAIM (Cancer Image Europe) initiative emerges within the transformation of modern medicine towards precision, prevention, and personalization. This review presents the strategic vision, scientific and technical objectives, and the potential impact of EUCAIM as a federated European digital infrastructure for cancer research based on medical imaging. By integrating clinical and imaging data, leveraging artificial intelligence, and standardizing data annotation and curation processes, EUCAIM aims to accelerate innovation, improve reproducibility, and facilitate researchers access to high-quality datasets. The article explores its organizational structure, the role of federated nodes, technical and semantic interoperability, and associated legal frameworks. Finally, its alignment with the European Health Data Space and its long-term sustainability as an engine for clinical research are discussed.
Palabras clave: Imagen médica; Inteligencia artificial; Infraestructura federada; Reproducibilidad.
Keywords: Medical imaging; Artificial intelligence; Federated infrastructure; Reproducibility.
INTRODUCCIÓN
En la última década, la medicina ha experimentado una transformación profunda. Desde un conocimiento de base poblacional y epidemiológico, ha evolucionado hacia un modelo más centrado en cada paciente individual con sus singularidades y expresiones, basado en una medicina de precisión con el empleo de biomarcadores, y guiado por una multitud de datos de calidad que representan el propio ecosistema del paciente (1). Todo ello además validado en una evidencia científica constatada.
Por su parte, la imagen médica desempeña un papel esencial en numerosas enfermedades, permitiendo con todas sus modalidades y técnicas de imagen la detección y tipificación de lesiones, la definición de su extensión y la valoración de su respuesta al tratamiento (2). Así, por ejemplo, la mamografía es fundamental para detectar y caracterizar el cáncer de mama mujeres dentro de los programas de cribado poblacional, mientras que la ecografía es imprescindible para detectar y caracterizar el cáncer primario de hígado en la población diana con cirrosis hepática. Numerosas técnicas de imagen se emplean continuamente para definir la extensión de la enfermedad, como la Tomografía Computarizada (TC) en los pacientes con cáncer de colon, y la planificación y evaluación de la respuesta al tratamiento como la Resonancia Magnética (RM) en pacientes con glioblastoma cerebral. Vemos pues que la imagen médica está muy implantada en el diagnóstico y seguimiento de muchos pacientes con muy diversos tipos de cáncer.
Más allá de su valor clínico inmediato, la imagen médica es en una fuerza transformadora en el viaje sanitario del paciente durante el trascurso de su enfermedad y también durante toda su existencia, ya que respalda muchas de las decisiones clínicas, mejora la respuesta en las situaciones de urgencia, acelera la investigación farmacológica, e impulsa la innovación y transferencia de los nuevos conocimientos a la práctica clínica (2). Su papel va mucho más allá de las exploraciones que se realizan en las salas de radiología de cualquier centro hospitalario. La imagen médica es hoy central en la configuración de la salud global del futuro ya que genera una información clínicamente pertinente que favorece una mayor calidad de vida de muchos pacientes y ciudadanos.
Así, y de una forma general, hoy en día se considera que la imagen médica es clave para prevenir, diagnosticar y tratar adecuadamente más del 80% de las enfermedades. En el caso concreto de Europa se realizan muchas exploraciones con imagen médica con muy diversos equipamientos e intenciones, incluyendo la detección precoz de lesiones y enfermedades; el conocimiento de su extensión y características principales; y para controlar el efecto de un tratamiento para cada paciente, siempre que su enfermedad sea observable con alguna de las diversas modalidades de imagen actualmente existentes. Garantizar un acceso equitativo a la tecnología de la imagen médica y reutilizar las imágenes médicas en la investigación empleando la Inteligencia Artificial (IA) para mejorarlas y extraer más información subrogada de ellas es un imperativo de las sociedades desarrolladas (2, 3).
Pese a todo este arsenal de modalidades y técnicas, y pese a su amplia utilización clínica en muchos pacientes con cáncer, existen áreas de mejora en el papel de la imagen médica en la medicina de precisión. En este aspecto, la imagen colabora con el descubrimiento y la validación de diversas métricas objetivas, conocidas como biomarcadores de imagen. Estos biomarcadores son características que se extraen de las imágenes mediante múltiples procesos computacionales y que proporcionan una información subrogada cuantificable que es además accesible y reproducible cuando se adquieren con la metodología adecuada (4). Estos biomarcadores dan información repetible en el tiempo sobre el estado de los órganos, los tejidos, las lesiones y los procesos fisiopatológicos que subyacen en cada persona y paciente (Figura 1). Es muy de destacar que los biomarcadores de imagen pueden obtenerse como valor añadido en todas las exploraciones radiológicas y de medicina nuclear que se realizan a cualquier paciente, por lo que proveen de una información relevante y actualizada del estado de muchos órganos y lesiones, repetida además en el tiempo cada vez que se repite una prueba al paciente (5, 6).
La amplia utilización de tecnologías como la TC, la RM, la tomografía por emisión de positrones (PET) y la ecografía (US) de alta resolución, combinadas con la obtención de sus biomarcadores de imagen mediante algoritmos de procesado de imágenes avanzados, están revolucionando el diagnóstico y el seguimiento de numerosas enfermedades, muy especialmente en pacientes con cáncer. En este contexto, podemos identificar el desarrollo de los biomarcadores de imagen como un paso importante en la investigación médica de precisión. Como se ha comentado, un biomarcador es un valor cuantitativo que proporciona una información precisa sobre la distribución y magnitud de un estado biológico, un proceso patológico o un desenlace o evento clínico desconocido que se desarrollará durante la historia natural de la enfermedad o tras la instauración de un tratamiento específico. Un biomarcador de imagen se empleará, tanto en la asistencia práctica como en ensayos clínicos, sólo si la información subrogada que genera es fiable, precisa, reproducible, accesible, sensible a pequeños cambios, y segura para el paciente (6).
Además, dada la multicausalidad y las comorbilidades, se reconoce como muy necesario vincular los datos que provienen de múltiples entornos clínicos y analíticos, incluida la radiómica con los biomarcadores de imagen, en modelos predictores que permitan estimar con una mayor precisión los cambios relevantes de la enfermedad en un paciente determinado y los desenlaces-eventos futuros relevantes para así alcanzar el mayor beneficio terapéutico posible para cada paciente (7, 9) (Figura 1).
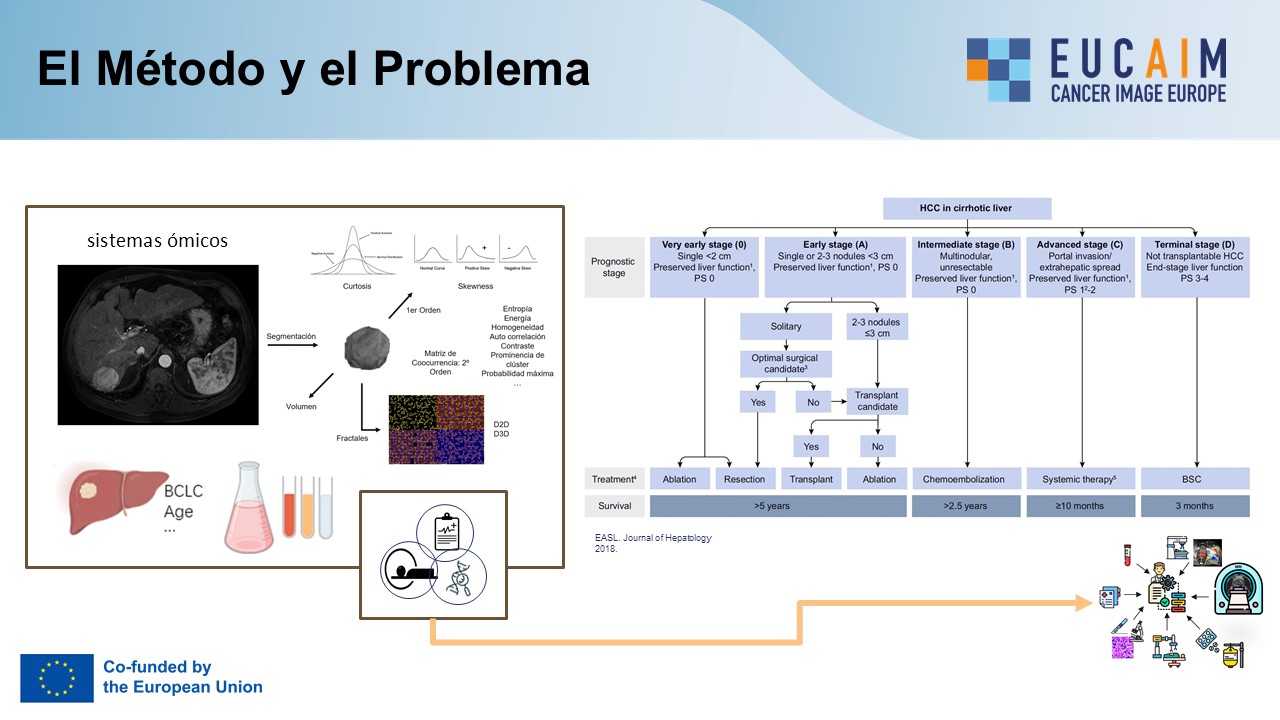
Aunque ya se emplean biomarcadores de imagen validados en diferentes entornos clínicos, como en pacientes con daño oclusivo vascular cerebral y cardíaco, su uso en pacientes con cáncer todavía no se ha implementado pese a la gran cantidad de publicaciones existentes sobre su impacto y sobre mejoras en su implementación metodológica (1, 4, 5, 7, 10). Entre las múltiples barreras para la traslación clínica de los biomarcadores de imagen destacan la alta complejidad biológica y heterogeneidad de los tumores, que dificultan la estandarización de los biomarcadores, y la imposibilidad de estandarizar protocolos técnicos dado en continuo desarrollo y mejoras en las imágenes obtenidas en el práctica asistencial. Para solventar esta crisis de reproducibilidad se están desarrollando líneas de investigación muy potentes, especialmente las basadas en soluciones con IA, donde se requiere una gran cantidad de imágenes anotadas de calidad y un entorno de procesamiento seguro para estos el entrenamiento y validación de estos programas computacionales. Así, se reconoce que la IA puede solventar el problema de la falta de reproducibilidad en la extracción de características radiómicos que se comporten como biomarcadores de imagen y se integren en modelos predictores robustos y armonizados (8, 11). Pero para ello se necesitan grandes repositorios de imágenes médicas donde estos algoritmos puedan entrenarse y ajustarse de forma fiable.
Cada año se generan en Europa más de 1.000 millones de estudios de imagen médica, aunque menos del 0,01% de ellos se reutilizan para la investigación o la innovación, limitando la implementación de biomarcadores de imagen robustos en la medicina de precisión. Para revertir esta situación, se creó en 2023 EUCAIM (Cancer Image Europe) como un amplio consorcio que reúne a varios Estados miembros de la UE con el objetivo de crear un Atlas federado de Imágenes Oncológicas que reúna más de 60 millones de imágenes anonimizadas para 2027 (Figura 2). La transformación digital de la salud y el uso de la IA aplicada a datos, incluyendo los biomarcadores de imagen, ayudará a afrontar los retos actuales con más eficiencia (3).
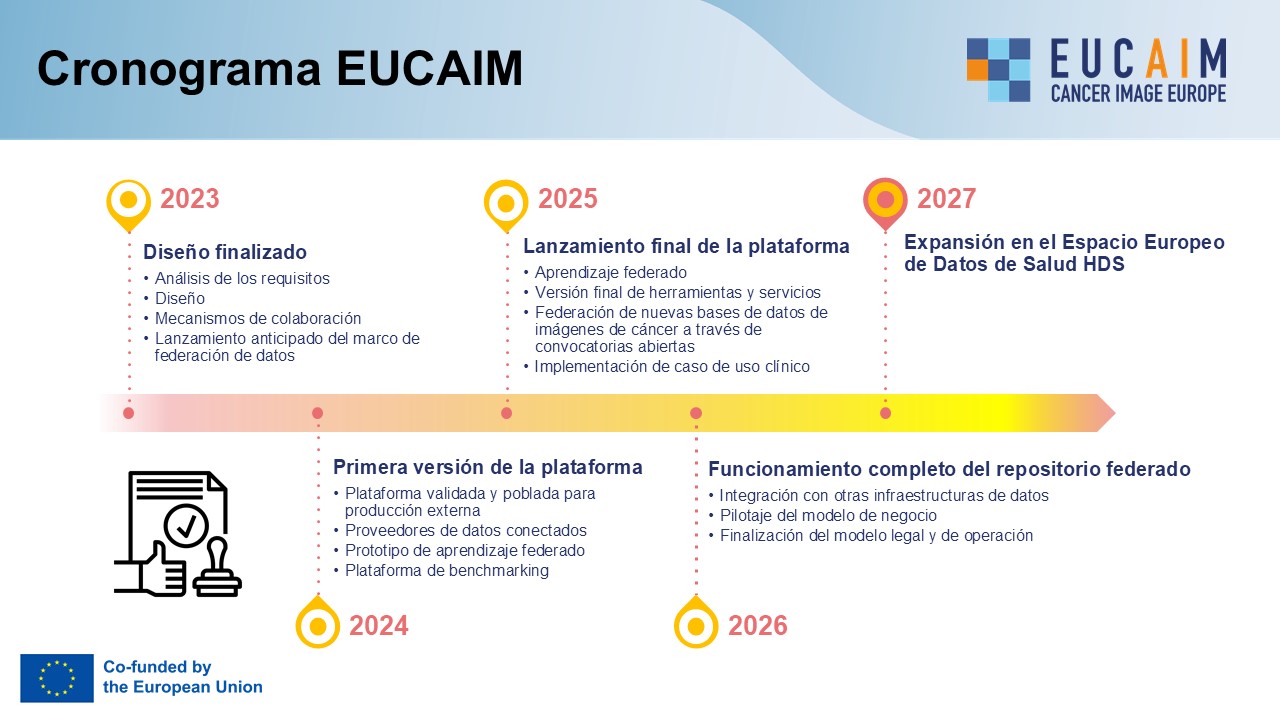
Sin embargo, el aprovechamiento completo de estas tecnologías requiere superar desafíos como la heterogeneidad de datos, la falta de interoperabilidad y su escasa reutilización para nuevos proyectos. EUCAIM nace como una infraestructura digital Europea para la investigación con imágenes médicas en cáncer para responder a estos retos mediante la creación de una infraestructura híbrida, tanto centralizada como federada, que promueve la reutilización responsable, segura y eficiente de imágenes médicas a escala europea. EUCAIM es una iniciativa emblemática del Plan Europeo de Lucha contra el Cáncer (EBCP, del inglés Europe Beating Cancer Plan) para aprovechar al máximo el potencial de los datos y las tecnologías digitales basadas en la IA y computación de altas prestaciones (HPC, del inglés High Performance Computing) para combatir el cáncer acelerando los desarrollos en IA y la innovación empresarial. Su objetivo final es promover la utilización de soluciones de IA como dispositivos médicos (AIaMDs, del inglés Artificial Intelligence as Medical Devices) centrados en la imagen médica para avanzar en la medicina de precisión (3) y facilitando el desarrollo y validación de dichas soluciones (Figura 3).
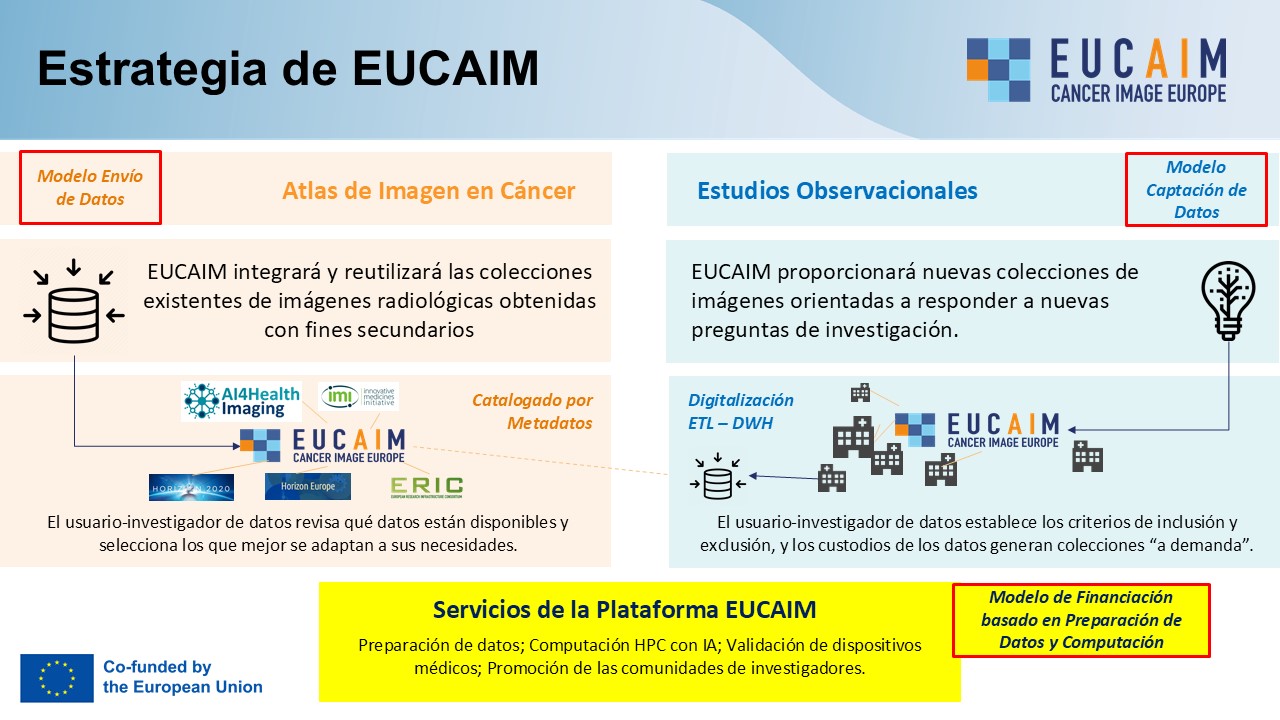
La Infraestructura
EUCAIM reúne una red paneuropea de instituciones médicas, centros de investigación y socios tecnológicos con el objetivo de construir un repositorio federado y seguro de datos e imágenes oncológicas. Este ecosistema apoya el desarrollo de modelos de IA capaces de aportar valor clínico, acelerar ensayos y mejorar la toma de decisiones. La infraestructura se articula en torno a nodos de referencia (como Health-RI en Países Bajos y la Universitat Politècnica de València en España), donde se centralizan los flujos de procesamiento, análisis y validación de datos. A través del uso de estándares como DICOM, NIfTI y mCODE, junto con metadatos armonizados y codificados de acuerdo con la especificación HealthDCAT-AP (estándar propuesto para el Espacio Europeo de Datos de Salud), EUCAIM garantiza una semántica interoperable y una trazabilidad completa (12). (Figura 4) El objetivo principal de esta infraestructura es evitar la fragmentación de los repositorios de imagen de pacientes con cáncer para su uso secundario continuado y mejorar el acceso a las imágenes anotadas y datos asociados almacenados en los hospitales mediante procesos digitales avanzados de ETL (del inglés, Extract, Transform, Load) (13).
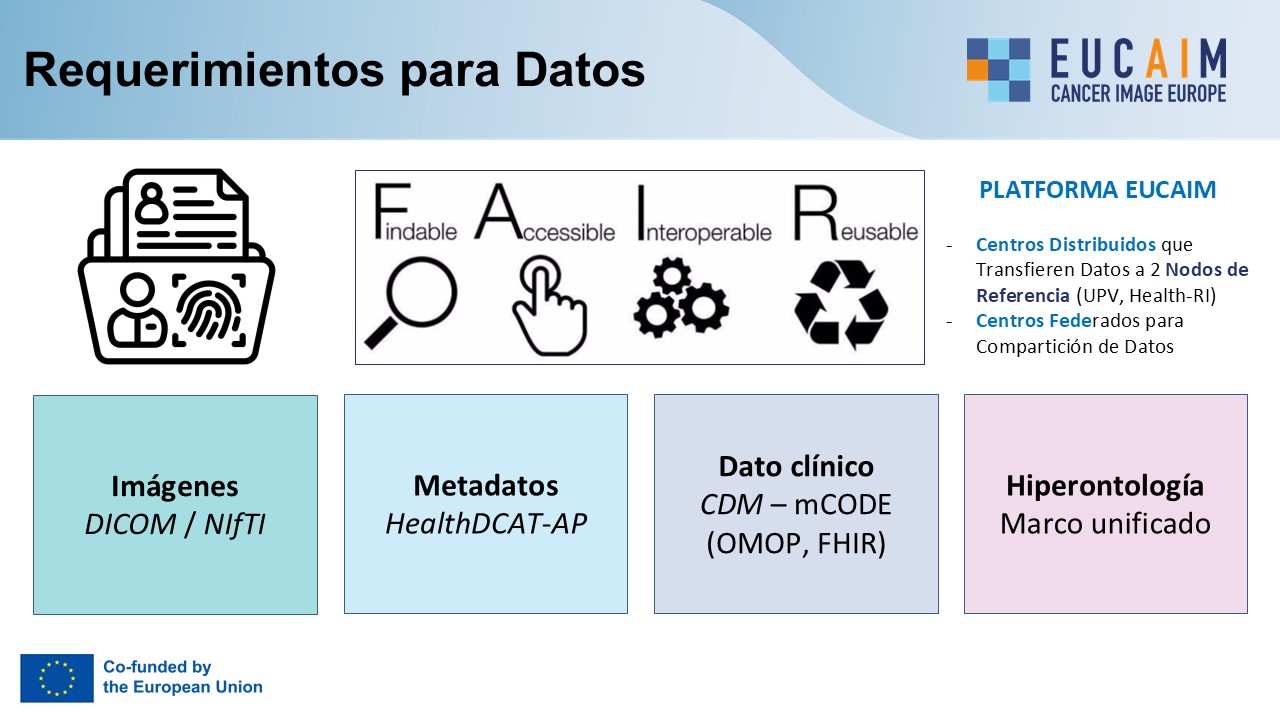
En sus primero años de implementación, EUCAIM ha puesto en marcha una Plataforma (DIGITAL-2022-CLOUD-AI-02) de almacenamiento y acceso a datos y soluciones computaciones para investigadores y empresas innovadoras. Este entorno está validado y accesible, contando con 94 socios, más de 180 asociados, numerosos proveedores de datos conectados, prototipos de aprendizaje federado, catálogos de datos y programas computacionales, catálogo de servicios y estándares, y propuestas de interoperabilidad para el espacio europeo de datos de salud (EHDS, del inglés European Health Data Space) (13, 14) (Figura 4).
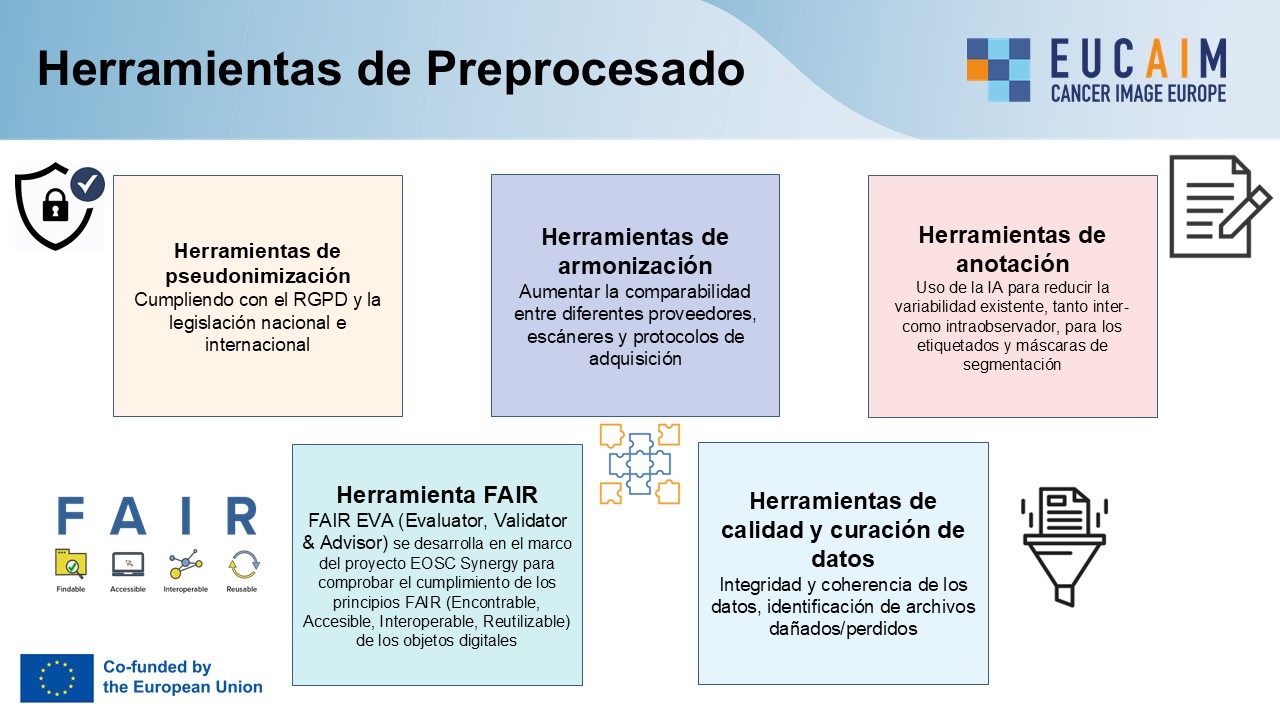
En esta plataforma se han implementado herramientas avanzadas de pseudonimización, curación de datos, anotación automática con IA y evaluación FAIR (del inglés Findable, Accessible, Interoperable, Reusable) para asegurar la calidad, privacidad y utilidad de los conjuntos de datos (Figura 5).
Uno de los pilares del proyecto es su estrategia legal y ética centrada en un MoU (del inglés, Memorandum of Understanding), que junto con los acuerdos de DTA (del inglés, Data Transfer Agreement), y DSA (del inglés, Data Sharing Agreement), que regulan la gobernanza del acceso a datos. Además, se promueve una capa de servicios de analítica avanzada que permita a startups, hospitales y universidades construir, probar y validar soluciones sobre colecciones de datos reales. La plataforma EUCAIM permite descubrir, visualizar y solicitar acceso a estas colecciones a través de una interfaz sencilla y eficiente (13).
Entre los logros principales que esta infraestructura Europea se ha propuesto caben destacar el desarrollo, catalogación y comparación de soluciones de IA para implementar una medicina de precisión; la mejorar en las estimaciones diagnósticas, predictivas y pronósticas mediante los biomarcadores de imagen y la IA; y la promoción de un Espacio Federado Seguro (SPE, del inglés Secure Processing Environment) de base hospitalaria para dinamizar los Estudios Observacionales con datos del mundo real (RWD, del inglés Real World Data). Es decir, EUCAIM integrará y reutilizará las colecciones existentes de imágenes radiológicas obtenidas con fines secundarios y, de forma simultánea, proporcionará nuevas colecciones de imágenes extraídas de los hospitales orientadas a responder a las nuevas preguntas de investigación con una capa de servicios de validación de dispositivos médicos, preparación de datos, computación HPC con IA, y promoción de las comunidades de investigadores. Desde su diseño, la Plataforma cuenta además con un sistema de gestión y asesoramiento legal, con normativas de uso adecuado y ético de las colecciones de datos, catálogos de metadatos e interoperabilidad entre repositorios, y con responsables en la formación, difusión y comunicación de sus logros y prestaciones (Figura 5).
El proyecto de construcción y validación de la Plataforma finalizará en Diciembre del 2026 (Figura 2). Es por ello por lo que el Consorcio ha decidido solicitar su constitución como persona jurídica mediante el instrumento EDIC (del inglés, European Digital Infrastructure Consortium) para la ejecución de proyectos plurinacionales. En este sentido, ya se ha constituido un grupo de trabajo coordinado por España y se ha pre-notificado a la Unión Europea la solicitud EDIC (Misión, Visión, Objetivos y Estrategia de implementación). Esta EDIC facilitará el acceso a conjuntos de datos de alta calidad, impulsará la capacidad de investigación e innovación de empresas emergentes y PYMES para su recorrido regulatorio y su salida al mercado. Será también un marco de apoyo funcional, operativo y legal para un acceso seguro mediante la puesta en marcha de un Entorno Seguro de Proceso (SPE, del inglés Secure Processing Environment), controlado y conforme a la normativa vigente, en línea con la legislación de la UE sobre gobernanza de datos y el espacio y del EHDS (15).
La plataforma permite la conexión con ensayos clínicos en curso, proyectos previos como AI4HI, así como nuevos estudios observacionales. Esta dinámica se potencia con la inclusión del nodo central en el futuro EDIC (Consorcio Europeo de Infraestructuras Digitales), asegurando su sostenibilidad operativa, tecnológica y jurídica más allá de los años de financiación inicial. Finalmente, EUCAIM se posiciona como una infraestructura clave para la creación del EHDS, promoviendo el uso secundario del dato médico, acelerando la innovación y democratizando el acceso a recursos de alto valor.
EUCAIM representa pues una apuesta estratégica sin precedentes por parte de la Unión Europea para transformar la investigación médica y clínica mediante la integración masiva de datos de imagen oncológica e incluso como repositorio de imágenes de los artículos de autores europeos publicados en revistas de la Sociedad Europea de Radiología (16). Al fomentar la estandarización, la interoperabilidad y el acceso seguro, EUCAIM no solo mejora la reproducibilidad de los estudios científicos, sino que también abre nuevas oportunidades para la inteligencia artificial aplicada a la salud. Su estructura distribuida, su arquitectura técnica federada y su alineamiento con marcos legales garantizan una evolución sostenible. Además, su orientación práctica hacia la generación de valor clínico y su enfoque abierto a la colaboración con empresas, universidades y hospitales, hacen de esta plataforma un ejemplo modélico de infraestructura digital avanzada y anonimizada para datos y soluciones computacionales (17, 18). A medida que el proyecto madura, su impacto se ampliará a otras áreas de la medicina de precisión, sirviendo como catalizador de una nueva era de investigación médica transfronteriza, ética y basada en datos (19).
Conclusiones
EUCAIM proporciona una plataforma sólida y confiable para que los investigadores, médicos e innovadores puedan dotar al repositorio y acceder a las imágenes radiológicas y de medicina nuclear de pacientes con enfermedades oncológicas diversas, lo que permite la evaluación comparativa, testar y validar tecnologías impulsadas por IA. Al conectar datos de imágenes oncológicas de alta calidad con expertos en inteligencia artificial, EUCAIM facilita la colaboración y acelera el desarrollo de soluciones innovadoras para el diagnóstico y tratamiento del cáncer. Esta infraestructura beneficia a los investigadores al proporcionarles soluciones para acceder, compartir y procesar datos paneuropeos de imágenes del cáncer; a los innovadores al proveerles de un marco de referencia con un catálogo bien definido y estandarizado de datos y herramientas para facilitar la certificación de dispositivos; a los médicos para dotarles de un espacio donde experimentar y validar clínicamente nuevas herramientas para el diagnóstico, pronóstico y tratamiento del cáncer; y al ciudadano al mejorar su calidad de vida con un diagnóstico precoz, tratamiento personalizado y mejor evaluación pronóstica empleando biomarcadores de imagen y modelos integrados con IA para ayudar a la toma de decisiones en salud.
DECLARACIÓN DE TRANSPARENCIA
Los autores/as de este artículo declaran no tener ningún tipo de conflicto de intereses respecto a lo expuesto en el presente trabajo.
BIBLIOGRAFÍA
- ↑Veiga-Canuto D, Cerdá Alberich L, Fernández-Patón M, et al. Imaging biomarkers and radiomics in pediatric oncology: a view from the PRIMAGE (PRedictive In silico Multiscale Analytics to support cancer personalized diaGnosis and prognosis, Empowered by imaging biomarkers) project. Pediatr Radiol. 2024;54(4):562-570.
- ↑World Health Organization. Strengthening medical imaging. https://www.who.int/activities/strengthening-medical-imaging. Acceso 10-julio-2025.
- ↑Martí-Bonmatí L, Blanquer I, Tsiknakis M, et al. Empowering cancer research in Europe: the EUCAIM cancer imaging infrastructure. Insights Imaging. 2025;16(1):47.
- ↑Kocak B, Akinci D’Antonoli T, Mercaldo N, ey al. METhodological RadiomICs Score (METRICS): a quality scoring tool for radiomics research endorsed by EuSoMII. Insights Imaging. 2024;15(1):8.
- ↑Marti-Bonmati L, Cerdá-Alberich L, Pérez-Girbés A, et al. Pancreatic cancer, radiomics and artificial intelligence. Br J Radiol. 2022;95(1137):20220072.
- ↑Martí Bonmatí L, Alberich-Bayarri A, García-Martí G, et al. Biomarcadores de imagen, imagen cuantitativa y bioingeniería [Imaging biomarkers, quantitative imaging, and bioengineering]. Radiologia. 2012;54(3):269-278.
- ↑Rodríguez-Ortega A, Alegre A, Lago V, et al. Machine Learning-Based Integration of Prognostic Magnetic Resonance Imaging Biomarkers for Myometrial Invasion Stratification in Endometrial Cancer. J Magn Reson Imaging. 2021;54(3):987-995.
- ↑Mali SA, Ibrahim A, Woodruff HC, et al. Making Radiomics More Reproducible across Scanner and Imaging Protocol Variations: A Review of Harmonization Methods. J Pers Med. 2021;11(9):842.
- ↑Martí-Bonmatí L. Estimaciones de Causalidad con Imagen Médica en Oncología. An RANM. 2021;138(01): 16–23.
- ↑Martí-Bonmatí L. La Radiómica y los Biomarcadores de Imagen. ANALES RANM [Internet]. Real Academia Nacional de Medicina de España; An RANM · Año 2019 ; 136(01):34-42.
- ↑Martí-Bonmatí L. Inteligencia artificial en imagen médica. An RANM. 2024;141(02): 111–118.
- ↑Hussein R, Gyrard A, Abedian S, Gribbon P, Martínez SA. Interoperability framework of the european health data space for the secondary use of data: interactive European Interoperability Framework-Based Standards compliance toolkit for AI-Driven projects. J Med Internet Res. 2025;27:e69813.
- ↑Cancer Image Europe. Available via https://cancerimage.eu/. Accessed July 2025
- ↑Gyrard A, Abedian S, Gribbon P, et al. Lessons learned from European Health Data Projects with cancer use cases: implementation of health standards and internet of things semantic interoperability. J Med Internet Res. 2025;27:e66273.
- ↑European Digital Infrastructure Consortium (EDIC). https://digital-strategy.ec.europa.eu/en/policies/edic. Acceso 10/julio/2025.
- ↑Martí-Bonmatí L, Blanquer I, Hamm B, et al. Empowering imaging research through the EUCAIM repository: a new opportunity for ESR journals’ authors. Eur Radiol. 2025 May 23.
- ↑Gabelloni M, Faggioni L, Borgheresi R, et al. Bridging gaps between images and data: a systematic update on imaging biobanks. Eur Radiol. 2022;32(5):3173-3186.
- ↑Kondylakis H, Catalan R, Alabart SM, et al.. Documenting the de-identification process of clinical and imaging data for AI for health imaging projects. Insights Imaging. 2024;15(1):130.
- ↑Martí-Bonmatí L, Veiga-Canuto D, Cerdá Alberich L. Modelo predictivo de la agresividad biológica de tumores de estirpe neuroblástica en edad pediátrica incorporando la radiómica. An RANM. 2024;141(03): 209–220.
ranm tv
Luis Martí-Bonmatí
Real Academia Nacional de Medicina de España
C/ Arrieta, 12 · 28013 Madrid
Tlf.: +34 91 159 47 34 | E-Mail: luis_marti@iislafe.es
Año 2025 · número 142 (02) · páginas 124 a 131
Enviado*: 01.07.25
Revisado: 09.07.25
Aceptado: 21.07.25
* Fecha de lectura en la RANM


