Resumen
El cáncer colorrectal (CCR) es una de las principales causas de morbilidad y mortalidad a nivel mundial, y constituye el tumor de mayor incidencia en España. A pesar de los avances en cribado y tratamiento, una proporción significativa de pacientes con enfermedad localizada recae tras la cirugía, lo que refleja la persistencia de enfermedad mínima residual (MRD). En este contexto, el ADN tumoral circulante (ctDNA) ha emergido como un biomarcador revolucionario capaz de detectar MRD con una sensibilidad y especificidad muy superiores a las herramientas convencionales como el antígeno carcinoembrionario (CEA) y las técnicas de imagen.
El ctDNA permite identificar clones tumorales residuales, estratificar el riesgo de recaída y anticipar recurrencias clínicas hasta un año antes que la radiología. Existen dos enfoques tecnológicos principales: los ensayos Tumor Informed, que se basan en mutaciones específicas del tumor y ofrecen una elevada sensibilidad, y los Tumor Agnostic, que utilizan paneles predeterminados o firmas epigenéticas, con mayor rapidez y aplicabilidad universal. Numerosos estudios prospectivos y ensayos clínicos —entre ellos DYNAMIC, CIRCULATE-JAPAN y BESPOKE— han demostrado el valor pronóstico del ctDNA, consolidándolo como el marcador más robusto en CCR localizado. Además, su monitorización seriada abre la posibilidad de guiar decisiones terapéuticas, permitiendo reducir tratamientos innecesarios en pacientes con ctDNA negativo y plantear estrategias de intensificación en ctDNA positivo.
Sin embargo, persisten retos relevantes: la baja liberación tumoral en ciertos casos (low shedders), los falsos positivos derivados de hematopoyesis clonal (CHIP), la ausencia de estandarización entre plataformas y el elevado coste. A pesar de ello, el futuro apunta a una integración creciente del ctDNA en la práctica clínica, tanto en la individualización del tratamiento adyuvante como en la detección precoz de recaídas y, potencialmente, en el cribado poblacional.
En conclusión, el ctDNA constituye un cambio de paradigma en la oncología de precisión del CCR, ofreciendo la oportunidad de personalizar el manejo terapéutico y mejorar los resultados clínicos mediante una aproximación más temprana y biológicamente fundamentada.Abstract
Colorectal cancer (CRC) remains one of the leading causes of cancer-related morbidity and mortality worldwide and represents the most frequently diagnosed tumor in Spain. Despite advances in screening and treatment, a substantial proportion of patients with localized disease experience relapse after surgery, reflecting the persistence of minimal residual disease (MRD). In this context, circulating tumor DNA (ctDNA) has emerged as a revolutionary biomarker capable of detecting MRD with sensitivity and specificity far superior to conventional tools such as carcinoembryonic antigen (CEA) and imaging techniques.
CtDNA enables the identification of residual tumor clones, stratification of recurrence risk, and early detection of relapse up to one year before clinical or radiological evidence. Two main technological approaches are currently available: Tumor-Informed assays, which rely on patient-specific tumor mutations and offer high sensitivity but require tumor tissue and longer turnaround times; and Tumor-Agnostic assays, based on predefined panels or epigenetic signatures, which are faster and universally applicable but generally less sensitive. Numerous prospective studies and clinical trials —including DYNAMIC, CIRCULATE-JAPAN, and BESPOKE— have consistently demonstrated the strong prognostic value of ctDNA, consolidating it as the most robust biomarker in localized CRC. Moreover, longitudinal ctDNA monitoring provides an opportunity to guide therapeutic decisions: reducing unnecessary chemotherapy in ctDNA-negative patients while considering treatment intensification in ctDNA-positive cases.
Nevertheless, significant challenges remain, including low shedding tumors, false positives derived from clonal hematopoiesis (CHIP), lack of standardization across platforms, and high costs. Despite these limitations, the future of ctDNA in clinical practice is highly promising, with potential applications not only in tailoring adjuvant therapy and enabling earlier detection of relapse but also in population-based CRC screening.
In conclusion, ctDNA represents a paradigm shift in precision oncology for CRC, offering the opportunity to personalize therapeutic management and improve patient outcomes through earlier, biology-driven interventions.Palabras clave: Cáncer colorrectal; ADN tumoral circulante (ctDNA); Enfermedad mínima residual (MRD); Biomarcadores; Terapia adyuvante; Oncología de precisión; Detección precoz de recaida.
Keywords: Colorectal cancer; Circulating tumor DNA (ctDNA); Minimal residual disease (MRD); Biomarkers; Adjuvant therapy; Precision oncology; Early recurrence detection.
INTRODUCCIÓN
El cáncer colorrectal (CCR) constituye en la actualidad uno de los principales retos de la oncología moderna, tanto por su elevada incidencia como por el notable impacto clínico, social y económico que conlleva. Según los datos más recientes de la Sociedad Española de Oncología Médica (SEOM 2025) (1), elaborados a partir de los registros nacionales (REDECAN) (2) y de la Agencia Internacional para la Investigación del Cáncer (IARC) de la Organización Mundial de la Salud (3), el CCR se sitúa como la neoplasia maligna más frecuente en España, con 44.573 nuevos diagnósticos anuales, lo que representa aproximadamente el 15% de todos los tumores malignos. La prevalencia a cinco años se estima en 84.763 casos y la mortalidad anual alcanza los 15.114 fallecimientos, lo que convierte al CCR en la segunda causa de muerte por cáncer en nuestro país.
El pronóstico del CCR depende de forma crítica del estadio tumoral en el momento del diagnóstico. La supervivencia global a cinco años supera el 90% en el estadio I (T1–2, N0), se sitúa entre el 60% y el 80% en el estadio II (T3–4, N0), desciende al 30–60% en el estadio III (N+) y cae por debajo del 5% en el estadio IV, correspondiente a enfermedad metastásica. Desde el punto de vista epidemiológico, aproximadamente el 10–15% de los pacientes se diagnostican en estadio I, el 30% en estadio II, el 35% en estadio III y entre el 20% y el 25% en estadio IV. En conjunto, los estadios I y II representan más de 28.000 nuevos casos anuales en España, constituyendo el núcleo principal de pacientes con CCR potencialmente curable mediante cirugía, con o sin tratamiento adyuvante (Figura 1).

Los programas de cribado poblacional, basados fundamentalmente en la detección de sangre oculta en heces y la colonoscopia, han contribuido de forma significativa al incremento del diagnóstico precoz. Sin embargo, un número relevante de pacientes continúa presentándose en estadios avanzados. Además, las herramientas actualmente empleadas para la monitorización postquirúrgica —principalmente el antígeno carcinoembrionario (CEA) y las técnicas de imagen, como la tomografía computarizada— presentan limitaciones importantes en la detección de la enfermedad mínima residual (EMR; minimal residual disease, MRD), ya que identifican la recaída cuando la carga tumoral es ya elevada, del orden de ≥10⁹ células.
En este contexto, el concepto de enfermedad mínima residual adquiere una relevancia central. La EMR se define como la persistencia de células tumorales viables tras un tratamiento con intención curativa que no son detectables mediante los métodos diagnósticos convencionales. La identificación de la EMR a través del ADN tumoral circulante (ADNtc; circulating tumor DNA, ctDNA) representa un auténtico cambio de paradigma en el manejo del CCR localizado. Este biomarcador permite detectar la recurrencia tumoral en fases mucho más precoces, cuando la carga celular se sitúa en torno a 10⁵–10⁶ células. Este intervalo temporal, denominado “periodo ventana”, abre la posibilidad de intervenir de forma anticipada, antes de que la enfermedad sea clínicamente manifiesta, ofreciendo así una oportunidad única para optimizar el tratamiento adyuvante y mejorar los resultados oncológicos.
Tratamiento adyuvante en los estadios II y III
La cirugía constituye la base del tratamiento del cáncer colorrectal (CCR) localizado. Sin embargo, incluso tras una resección completa con intención curativa, un porcentaje significativo de pacientes presenta recaída, fundamentalmente como consecuencia de la persistencia de enfermedad mínima residual (EMR). Con el objetivo de reducir este riesgo, se emplea la quimioterapia adyuvante, cuya indicación y magnitud del beneficio varían en función del estadio tumoral. De acuerdo con las guías de la European Society for Medical Oncology (ESMO), los esquemas de tratamiento adyuvante se basan en fluoropirimidinas (5-fluorouracilo o capecitabina), asociadas a ácido folínico y oxaliplatino, fundamentalmente mediante los regímenes FOLFOX o CAPOX (4,5).
En el estadio II, aproximadamente el 80% de los pacientes se curan exclusivamente con cirugía. En este contexto, la quimioterapia adyuvante aporta un beneficio adicional modesto en términos de supervivencia global, estimado en torno al 3–5%. Dicho beneficio se concentra principalmente en los pacientes considerados de alto riesgo, definidos por la presencia de factores adversos como tumores T4, perforación u obstrucción intestinal, invasión linfática o perineural, un número insuficiente de ganglios linfáticos resecados y la ausencia de inestabilidad de microsatélites (fenotipo MSS). En consecuencia, se distinguen estadios II de bajo riesgo, en los que la cirugía suele ser suficiente, y estadios II de alto riesgo, en los que se recomienda la administración de quimioterapia adyuvante (Figura 2).
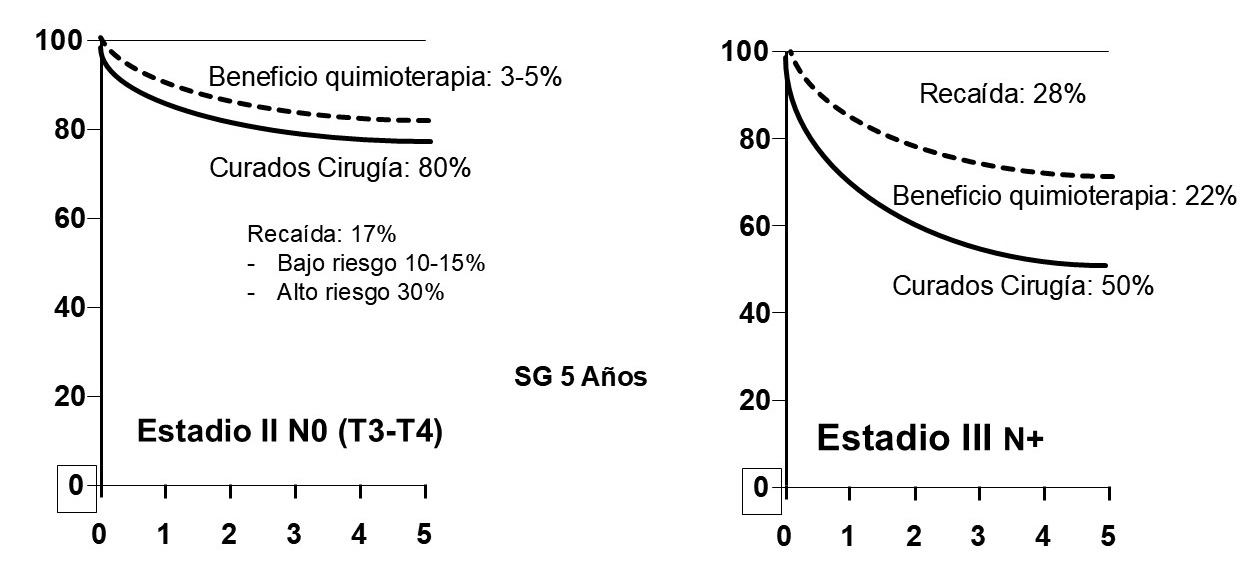
En el estadio III, la cirugía por sí sola permite la curación de aproximadamente el 50% de los pacientes, mientras que la adición de quimioterapia adyuvante basada en oxaliplatino incrementa la supervivencia global en torno a un 20–22%. El estudio IDEA (6), publicado en 2017, supuso un cambio relevante en el abordaje terapéutico al proponer una adaptación de la duración del tratamiento en función del riesgo. Así, los pacientes con tumores T1–3 N1 obtienen un beneficio adecuado con tres meses de quimioterapia adyuvante, mientras que aquellos con tumores T4 y/o afectación ganglionar N2 se benefician más claramente de seis meses de tratamiento (Figura 2).
No obstante, la toxicidad asociada a estos tratamientos constituye un problema clínico de primera magnitud. El oxaliplatino puede inducir neuropatía periférica acumulativa, en ocasiones irreversible, además de toxicidad hematológica, gastrointestinal (diarrea, mucositis) y sistémica (astenia, deterioro de la calidad de vida). Esta realidad genera una doble problemática: por un lado, el sobretratamiento de pacientes que no habrían recaído tras la cirugía; por otro, el subtratamiento de pacientes que, a pesar de recibir quimioterapia estándar, presentan recurrencia tumoral debido a la persistencia de EMR. A ello se suman las posibles hospitalizaciones, las bajas laborales y el impacto psicológico asociado al tratamiento citotóxico.
Biología del ADN tumoral circulante y fundamentos de la enfermedad mínima residual
El ADN tumoral circulante (ADNtc) constituye una fracción del ADN libre circulante (cell-free DNA, cfDNA), detectable en plasma y en otros fluidos biológicos. El ADN libre procede de múltiples procesos fisiológicos y patológicos, entre los que se incluyen la apoptosis de células normales, la necrosis, la secreción activa a través de vesículas extracelulares y la liberación asociada a inflamación o daño tisular. Sus concentraciones pueden aumentar tras el ejercicio físico, en procesos inflamatorios o enfermedades autoinmunes y, de forma especialmente relevante, como consecuencia de la hematopoyesis clonal asociada a la edad, conocida como clonal hematopoiesis of indeterminate potential (CHIP), fenómeno frecuente en individuos mayores de 60 años .
No obstante, el ADNtc presenta una serie de características biológicas específicas que permiten diferenciarlo del ADN libre de origen no tumoral y que sustentan su utilidad clínica como biomarcador.
Diversos trabajos y revisiones han analizado de forma extensa el papel del ADNtc en el CCR localizado, poniendo de manifiesto su valor pronóstico y predictivo en este contexto clínico (7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18).
Origen y características del ADNtc
El ADNtc se libera al torrente sanguíneo fundamentalmente como consecuencia de la muerte celular tumoral, a través de procesos de apoptosis y necrosis, aunque también puede ser secretado activamente por las células malignas mediante exosomas y microvesículas. Desde el punto de vista estructural, se presenta altamente fragmentado, con una longitud media de 90–150 pares de bases, inferior a la de los fragmentos derivados de células normales, que suelen medir entre 160 y 170 pares de bases. Esta diferencia en los patrones de fragmentación constituye una de las bases biofísicas que facilitan su identificación y enriquecimiento analítico (Figura 3).
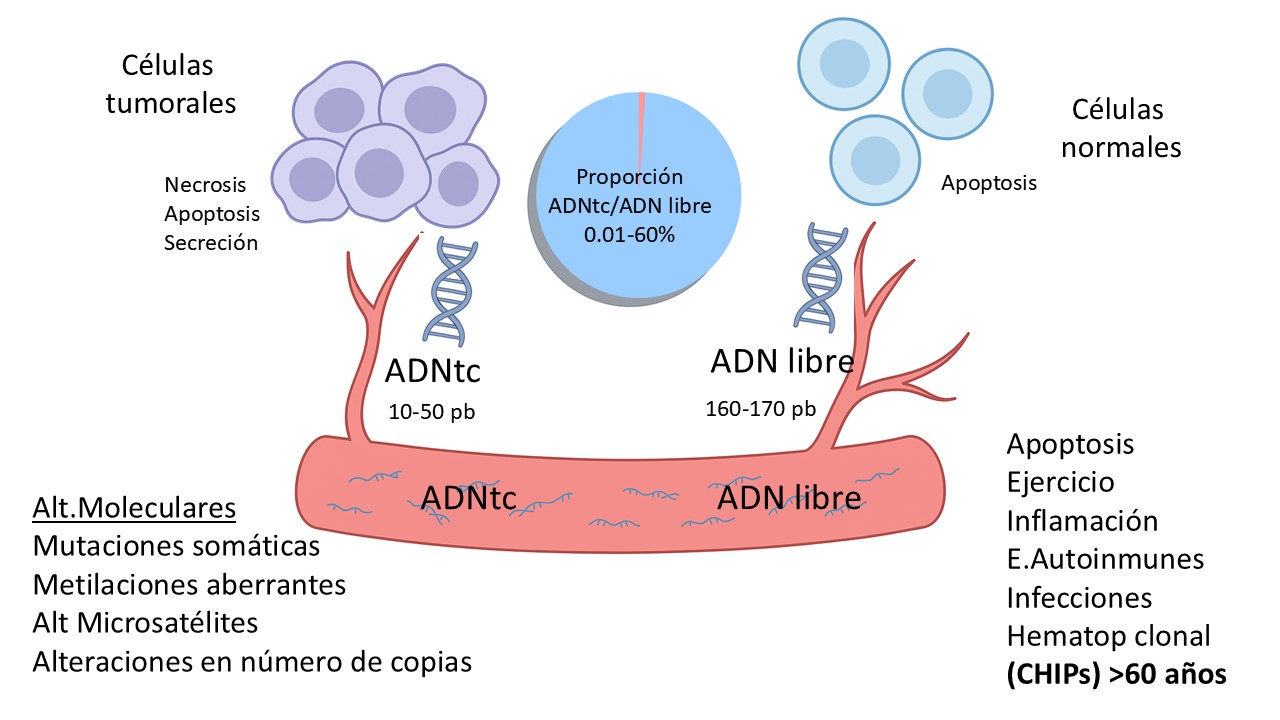
El ADNtc incorpora, además, las alteraciones moleculares características del tumor de origen, entre las que destacan: a) mutaciones somáticas puntuales, como las que afectan a genes clave en el CCR (TP53, KRAS, NRAS, BRAF o PIK3CA); b) alteraciones estructurales, incluyendo inestabilidad de microsatélites, reordenamientos cromosómicos y variaciones en el número de copias; c) cambios epigenéticos, en particular patrones aberrantes de metilación del ADN, que constituyen marcadores altamente específicos, estables y reproducibles.
Otra propiedad esencial del ADNtc es su corta vida media, estimada entre 16 minutos y 2,5 horas, consecuencia de su rápida depuración por el hígado, los riñones y la acción de nucleasas plasmáticas. Esta cinética confiere al ADNtc la capacidad de reflejar en tiempo casi real la dinámica tumoral: una desaparición rápida tras la cirugía sugiere una resección completa, mientras que su persistencia o reaparición indica la presencia de enfermedad mínima residual o una recurrencia incipiente.
El ADNtc como marcador de enfermedad mínima residual
La EMR se define como la persistencia de células tumorales viables tras la resección del tumor primario, que no son detectables mediante los métodos clínicos convencionales. La detección de EMR mediante ADNtc se fundamenta en su capacidad para identificar alteraciones moleculares tumorales con una sensibilidad muy superior a la de los marcadores clásicos y las técnicas de imagen (8–18).
Se estima que las modalidades radiológicas convencionales requieren una masa tumoral aproximada de 10⁹ células para identificar una lesión, mientras que la detección de ADNtc es posible con cargas tumorales del orden de 10⁵–10⁶ células. Este notable diferencial de sensibilidad explica por qué el ADNtc puede anticipar la recaída clínica entre 6 y 12 meses antes de que sea evidente desde el punto de vista radiológico. (Figura 4).
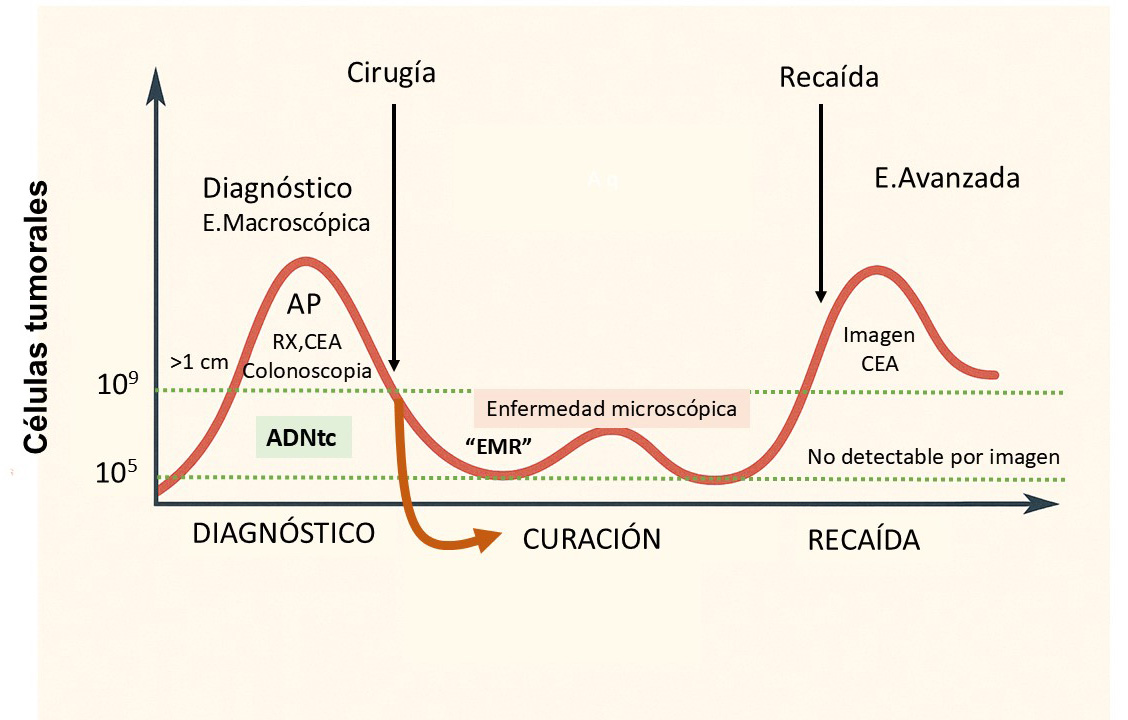
La presencia de ADNtc tras la cirugía o al finalizar la quimioterapia adyuvante constituye un indicador robusto de enfermedad persistente y, en la mayoría de los estudios publicados, se asocia a un riesgo de recaída cercano al 100% en ausencia de tratamiento adicional. Por el contrario, la negatividad persistente del ADNtc tras la resección se correlaciona con una elevada probabilidad de curación.
Limitaciones biológicas
Pese a su extraordinario potencial, la biología del ADNtc presenta limitaciones intrínsecas que deben ser consideradas. Algunos tumores, en función de su localización anatómica (como las metástasis peritoneales o pulmonares) o de determinadas características biológicas, liberan cantidades menores de ADN tumoral al torrente sanguíneo, lo que puede reducir la sensibilidad de la técnica. Asimismo, la presencia de alteraciones clonales derivadas de la hematopoyesis asociada a la edad (CHIP), especialmente frecuentes en personas de edad avanzada, puede dar lugar a falsos positivos si no se descartan mediante el análisis paralelo del ADN de leucocitos periféricos.
Implicaciones clínicas
El ADNtc no solo constituye un biomarcador pronóstico de enorme potencia, sino que se está consolidando progresivamente como una herramienta predictiva de respuesta a los tratamientos adyuvantes y como un elemento clave en la toma de decisiones terapéuticas. Su capacidad para detectar la EMR con meses de antelación respecto a los métodos convencionales abre una auténtica ventana de oportunidad para intervenir de forma precoz, ya sea intensificando el tratamiento en pacientes de alto riesgo o evitando terapias innecesarias en aquellos con bajo riesgo de recaída.
Tecnologías de detección del ADN tumoral circulante
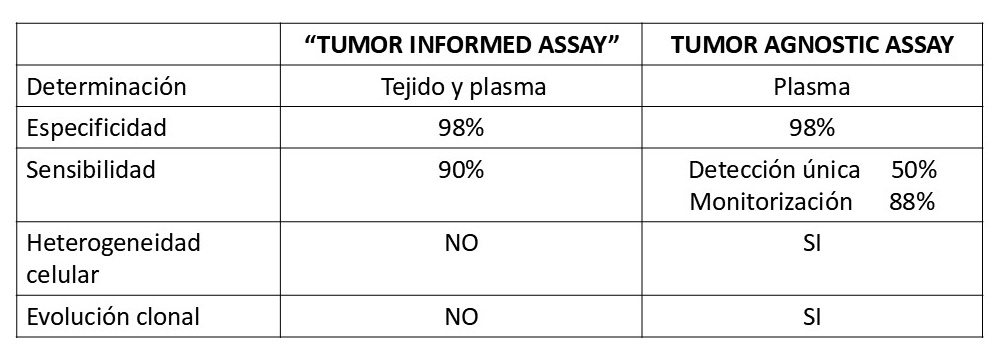
El desarrollo de las plataformas de secuenciación de nueva generación (next-generation sequencing, NGS) y de técnicas ultrasensibles de PCR digital ha permitido trasladar el análisis del ADN tumoral circulante (ADNtc) desde el ámbito experimental a la práctica clínica. En la actualidad existen dos enfoques tecnológicos principales para la detección de enfermedad mínima residual (EMR): los denominados “tumor-informed assays” y los “tumor-agnostic assays”. Ambos comparten una elevada especificidad, aunque difieren de forma relevante en sensibilidad, rapidez, costes y aplicabilidad clínica (19, 20) (Figura 5).
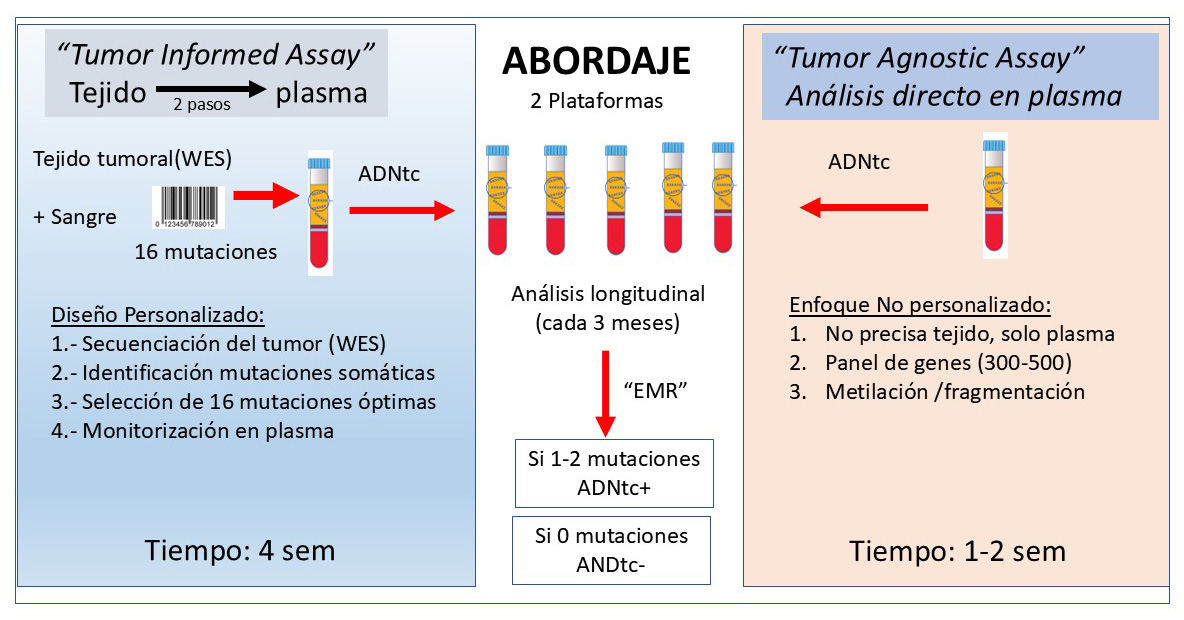
Enfoque “Tumor-informed”
El enfoque tumor-informed se basa en el diseño de una prueba personalizada a partir del análisis genómico del tumor primario. El proceso consta de dos etapas fundamentales:
- secuenciación del tumor primario —habitualmente del exoma completo, que abarca unos 20.000 genes— junto con el ADN germinal del paciente obtenido a partir de una muestra sanguínea, con el fin de identificar mutaciones somáticas exclusivas del tumor;
- monitorización posterior en plasma mediante PCR digital o NGS dirigida, focalizada en un conjunto seleccionado de mutaciones somáticas representativas del tumor (habitualmente entre 16 y 20).
Una ventaja adicional de este enfoque es la eliminación de las mutaciones derivadas de la hematopoyesis clonal (CHIP), ya que estas se identifican en la muestra sanguínea germinal y no en la secuenciación del tumor primario.
La principal fortaleza de los tumor-informed assays es su elevada sensibilidad, con tasas reportadas de hasta el 88% en estudios clínicos. Sin embargo, presentan limitaciones relevantes: requieren disponer de tejido tumoral, implican un tiempo de preparación de aproximadamente 4–6 semanas para el diseño del panel personalizado y suponen un coste elevado.
Enfoque “Tumor-agnostic”
El enfoque tumor-agnostic prescinde del análisis del tumor primario y se basa en la secuenciación directa del ADNtc en plasma. Habitualmente analiza paneles de 300–500 genes y busca mutaciones recurrentes, patrones específicos de fragmentación o alteraciones epigenéticas, particularmente de metilación, características del cáncer colorrectal. Entre los genes más representativos se incluyen KRAS, NRAS, TP53, APC, PIK3CA, BRAF, SMAD4 y CTNNB1. El procedimiento es idéntico para todos los pacientes y, por tanto, no está personalizado.
Su principal fortaleza reside en la rapidez y accesibilidad, ya que permiten obtener resultados en aproximadamente una semana y no requieren tejido tumoral, lo que los hace especialmente atractivos para la práctica clínica general. No obstante, su sensibilidad es inferior a la de los ensayos tumor-informed cuando se emplean determinaciones únicas (en torno al 50%), aunque se incrementa de forma sustancial mediante monitorización seriada, alcanzando cifras cercanas al 88%. En el contexto del CCR localizado, esta monitorización longitudinal resulta esencial y se recomienda realizar una determinación basal a las 2–3 semanas tras la cirugía, seguida de controles cada tres meses durante al menos dos o tres años (Figura 6).
Limitaciones técnicas comunes
Ambos enfoques comparten una serie de limitaciones técnicas, entre las que destacan los falsos negativos y los falsos positivos.
Los falsos negativos, estimados en torno al 5–10%, pueden deberse a una carga tumoral extremadamente baja, a la presencia de alteraciones genómicas no incluidas en el panel analizado, a la heterogeneidad tumoral con representación incompleta de los distintos clones (fenómeno de “ilusión clonal”) o a la localización del tumor en compartimentos con escasa liberación de ADNtc a la circulación sistémica, como el peritoneo o el pulmón.
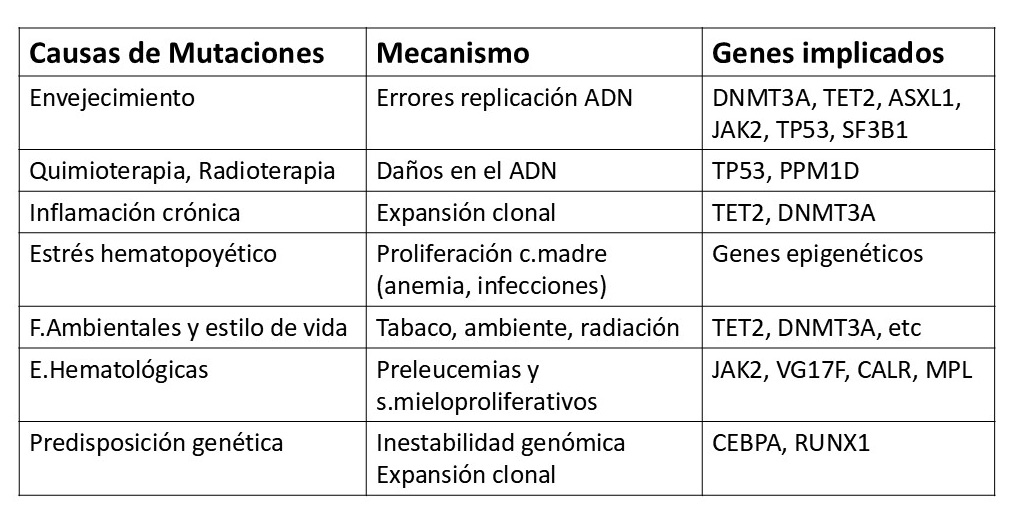
Los falsos positivos, que pueden alcanzar hasta un 5%, se asocian principalmente —además de al ejercicio, la inflamación o las enfermedades autoinmunes— a la presencia de hematopoyesis clonal (CHIP). Este fenómeno no neoplásico, caracterizado por la adquisición de mutaciones somáticas en células madre hematopoyéticas y la expansión clonal resultante, se detecta hasta en el 20% de las personas mayores de 60 años. Los genes más frecuentemente implicados, las causas de estas mutaciones y los mecanismos subyacentes se resumen en la figura 7. Este problema es especialmente relevante en las plataformas de un solo paso, en las que resulta recomendable incorporar análisis epigenéticos y filtros bioinformáticos avanzados, aunque persiste un riesgo moderado de confusión, particularmente en el caso de mutaciones en TP53.
Por último, cabe señalar que los genes alterados detectados por ambos enfoques son en gran medida coincidentes. Los más frecuentemente identificados en el CCR son TP53, APC y KRAS, seguidos, con menor frecuencia, por PIK3CA, SMAD4, BRCA2, POLE, PTEN, MET, ERBB2 y MLH1 (21).
En conjunto, tanto los enfoques tumor-informed como tumor-agnostic han demostrado un papel decisivo en la detección de la EMR. La elección entre uno u otro debe basarse en consideraciones clínicas, logísticas y económicas, así como en la disponibilidad de tejido tumoral y en el contexto asistencial en el que se aplique la técnica.
Evidencia clínica disponible en cáncer colorrectal localizado: los datos (versión revisada)
Estudios con plataformas de dos pasos (tumor-informed assays)
La validación clínica del ADN tumoral circulante (ADNtc) como biomarcador de enfermedad mínima residual (EMR) en el cáncer colorrectal (CCR) localizado ha experimentado un avance exponencial en la última década. Numerosos estudios prospectivos, ensayos clínicos aleatorizados y metaanálisis han demostrado de forma consistente su extraordinario valor pronóstico y su potencial para guiar decisiones terapéuticas en el contexto del tratamiento adyuvante.
Los primeros estudios
El trabajo pionero fue publicado en 2016 por Tie y colaboradores en Melbourne (22), estableciendo de manera inequívoca el valor pronóstico del ADNtc. En este estudio, que incluyó 230 pacientes con CCR en estadio II sometidos a resección quirúrgica, la ausencia de ADNtc tras la cirugía se asoció con tasas de supervivencia libre de recaída superiores al 85%, mientras que su presencia fue predictiva de recaída en prácticamente todos los casos. Los resultados estadísticos fueron particularmente llamativos, con una razón de riesgo (HR) para recaída de 18 (IC95%: 7,9–40), cifras hasta entonces inéditas en oncología.
Estos hallazgos fueron posteriormente confirmados por el mismo grupo en pacientes con estadio III (JAMA Oncol 2019) (23), en cáncer de recto localmente avanzado (Gut 2019) (24) y en un metaanálisis publicado en 2021 (International Journal of Cancer) (25). Resultados concordantes fueron descritos por un grupo danés (JAMA Oncology 2019) (26) y por un grupo español (Clinical Cancer Research 2022) (27), con HR de magnitud similar. En conjunto, estos estudios consolidaron al ADNtc como el biomarcador pronóstico más potente descrito hasta la fecha en el CCR localizado, superando claramente a las variables clínicas y patológicas tradicionales.
Ensayos clínicos aleatorizados
La verdadera prueba de concepto llegó con el ensayo fase II prospectivo y aleatorizado DYNAMIC II, publicado en The New England Journal of Medicine en 2022 (28). En este estudio multicéntrico, que incluyó 455 pacientes con CCR en estadio II, la indicación de quimioterapia adyuvante en el brazo experimental se basó exclusivamente en la positividad del ADNtc, mientras que en el brazo estándar se utilizó la estratificación clínica y patológica convencional.
Los resultados demostraron que la estrategia guiada por ADNtc permitió reducir en un 53% el uso de quimioterapia adyuvante sin detrimento en la supervivencia libre de recaída. A los dos años, las tasas de supervivencia fueron prácticamente idénticas en ambos grupos (93,5% en el brazo estándar frente a 92,4% en el brazo guiado por ADNtc). La actualización del estudio publicada en 2025 (Nature Medicine) (29) ha confirmado la estabilidad de estos resultados, estableciendo que los pacientes con ADNtc negativo pueden evitar de forma segura la quimioterapia adyuvante.
En el contexto del estadio III, el ensayo DYNAMIC III (presentado en ASCO 2025) (30) evaluó el papel del ADNtc como herramienta para intensificar el tratamiento adyuvante. Aunque confirmó de nuevo su extraordinario valor pronóstico, el estudio no logró demostrar un beneficio clínico de la intensificación terapéutica, probablemente reflejando la ausencia de fármacos eficaces capaces de modificar la historia natural de los pacientes con ADNtc positivo. En particular, la estrategia de intensificación con FOLFIRI no resultó efectiva.
El programa CIRCULATE-JAPAN
El programa CIRCULATE-JAPAN, y en especial el estudio observacional GALAXY, constituye una de las iniciativas más ambiciosas a nivel mundial en este campo. GALAXY incluyó a más de 2.000 pacientes con CCR en estadios II–IV tras resección completa (31, 32, 33, 34). Los resultados mostraron que los pacientes con ADNtc negativo tras la cirugía alcanzaban una supervivencia libre de enfermedad del 90,5%, mientras que en los pacientes ADNtc positivos esta descendía al 38,4%.
Un hallazgo particularmente relevante fue que los pacientes inicialmente ADNtc positivos que negativizaban el marcador tras la quimioterapia adyuvante alcanzaban supervivencias similares a las de aquellos que eran negativos desde el inicio, lo que sugiere un valor predictivo adicional del ADNtc. Por el contrario, la persistencia del ADNtc tras el tratamiento se asoció a un riesgo extremadamente elevado de recaída, abriendo la puerta a estrategias de escalada terapéutica con nuevos fármacos.
Dentro de este programa se desarrollan los ensayos VEGA y ALTAIR. VEGA, un estudio fase III de no inferioridad, evalúa la desescalada del tratamiento adyuvante (CAPOX frente a observación) en pacientes con estadio II de alto riesgo y estadio III ADNtc negativos. Los resultados preliminares presentados en AACR, ASCO y ESMO 2025 no han permitido aún confirmar la no inferioridad (35, 36).
El estudio ALTAIR, también fase III, analiza la escalada terapéutica en pacientes ADNtc positivos mediante trifluridina/tipiracilo frente a placebo. Los resultados presentados en ASCO y ESMO 2025 mostraron una mejora en la supervivencia libre de enfermedad a favor del tratamiento activo, aunque sin alcanzar significación estadística global (HR 0,79; IC95%: 0,60–1,05), salvo en el subgrupo de pacientes con estadio IV resecado (37, 38).
Estudios en práctica clínica real
El estudio BESPOKE CRC, desarrollado en Estados Unidos, incluyó a 1.792 pacientes en estadios I–III procedentes de 133 centros (39). Este estudio prospectivo y observacional confirmó que los pacientes con ADNtc negativo tras el tratamiento presentaban tasas de supervivencia libre de enfermedad superiores al 95% a largo plazo, mientras que en los ADNtc positivos estas descendían al 28%. La monitorización seriada permitió detectar recaídas con una anticipación de 8–12 meses respecto a la tomografía computarizada, y confirmó la ausencia de beneficio de la quimioterapia en los pacientes ADNtc negativos tras la cirugía.
En el cáncer de recto localmente avanzado, un ensayo aleatorizado dirigido por Tie (40) mostró que una estrategia guiada por ADNtc reducía de forma significativa la exposición a quimioterapia sin comprometer los resultados oncológicos.
Estudios con plataformas de un solo paso (tumor-agnostic assays)
Los primeros trabajos con plataformas tumor-agnostic demostraron una alta especificidad mediante la combinación de análisis genómicos y epigenéticos, en particular la evaluación de patrones de metilación aberrante para minimizar el impacto de la hematopoyesis clonal (41).
El ensayo COSMOS-CRC01 (42), realizado en Japón, confirmó que los pacientes con ADNtc negativo presentaban supervivencias libres de recaída cercanas al 90%, frente a aproximadamente el 30% en los pacientes ADNtc positivos, demostrando que el ADNtc era el factor pronóstico más potente, incluso por encima del estadio patológico.
El estudio PEGASUS (43), desarrollado en Italia y España, evaluó estrategias de escalada y desescalada terapéutica basadas en ADNtc, sugiriendo que los pacientes ADNtc negativos podrían evitar quimioterapia, mientras que los positivos podrían beneficiarse de tratamientos más intensivos. Por el contrario, el ensayo COBRA (44) no logró demostrar beneficio clínico, aunque fue interrumpido precozmente por futilidad tras un reclutamiento muy limitado.
Metaanálisis
Un metaanálisis reciente seleccionó seis estudios que cumplían criterios metodológicos estrictos, con un total de 1.190 pacientes (45). El análisis confirmó que la positividad del ADNtc tras la cirugía se asocia a un riesgo de recaída con HR superiores a 10, mientras que los pacientes ADNtc negativos presentan supervivencias a tres años superiores al 85%. Asimismo, se constató que la monitorización seriada incrementa la sensibilidad y permite anticipar la recaída hasta 12 meses antes de su detección radiológica o mediante CEA.
Conclusiones
La evidencia actualmente disponible permite afirmar que el ADN tumoral circulante (ADNtc) constituye el biomarcador pronóstico más potente descrito hasta la fecha en el cáncer colorrectal (CCR) localizado, claramente superior a los factores clínicos y patológicos clásicos. Su capacidad para detectar enfermedad mínima residual (EMR) con cargas tumorales del orden de 10⁵–10⁶ células, frente a las ≈10⁹ necesarias para las técnicas de imagen o el antígeno carcinoembrionario (CEA), explica su capacidad para anticipar la recaída clínica entre 6 y 12 meses.
El valor clínico del ADNtc como herramienta para desescalar la quimioterapia adyuvante en pacientes con ADNtc negativo, especialmente en el estadio II, ha sido ya validado en ensayos clínicos aleatorizados y estudios prospectivos, demostrando que estos pacientes pueden evitar de forma segura tratamientos innecesarios. Por el contrario, aunque el ADNtc identifica con gran precisión a los pacientes con alto riesgo de recaída, su papel como marcador predictivo del beneficio de la intensificación terapéutica en los casos ADNtc positivos requiere aún resultados más consistentes de los ensayos fase III en curso.
Desde el punto de vista práctico, la determinación del ADNtc debe realizarse al menos 2–3 semanas tras la cirugía y mantenerse de forma seriada cada tres meses durante los dos o tres primeros años. Existen, no obstante, limitaciones biológicas y técnicas, como la liberación variable de ADNtc según la localización tumoral, la heterogeneidad clonal o la hematopoyesis clonal asociada a la edad (CHIP), que pueden generar falsos resultados si no se aplican controles adecuados. Asimismo, la falta de estandarización entre plataformas y el acceso limitado a esta tecnología siguen siendo barreras relevantes para su implementación generalizada.
Pese a ello, el ADNtc representa un cambio de paradigma en la oncología de precisión. Su incorporación progresiva a la práctica clínica anticipa un escenario en el que las decisiones terapéuticas en el CCR localizado dejarán de basarse exclusivamente en parámetros clínico-patológicos para apoyarse en la biología molecular dinámica de cada paciente, optimizando resultados clínicos y favoreciendo un uso más eficiente de los recursos sanitarios.
DECLARACIÓN DE TRANSPARENCIA
El autor/a de este artículo declara no tener ningún tipo de conflicto de intereses respecto a lo expuesto en el presente trabajo.
BIBLIOGRAFÍA
- ↑Sociedad Española de Oncología Médica (SEOM). Las cifras del cáncer en España 2025 [Internet]. Madrid: SEOM; 2025 [citado 2025]. Disponible en: https://seom.org
- ↑Red Española de Registros de Cáncer (REDECAN) [Internet]. Madrid: REDECAN; 2025 [citado 2025]. Disponible en: https://www.redecan.org
- ↑International Agency for Research on Cancer (IARC). Global Cancer Observatory [Internet]. Lyon: IARC; 2025 [citado 2025]. Disponible en: https://gco.iarc.fr
- ↑Argilés G, Tabernero J, Labianca R, et al. Localised colon cancer: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2020;31(10):1291–1305.
- ↑Grothey A, Sobrero AF, Shields AF, et al. Duration of adjuvant chemotherapy for stage III colon cancer. N Engl J Med. 2018;378:1177–1188.
- ↑Taieb J, Souglakos J, Boukovinas I, et al. Combined analyses of circulating tumor DNA and Immunoscore in patients with stage III colon cancer: a post hoc analysis of the PRODIGE-GERCOR IDEA-France/HORG-IDEA-Greece trials. J Clin Oncol. 2025;43(13):1564–1577.
- ↑Krell M, Llera B, Brown Z. Circulating tumor DNA and management of colorectal cancer. Cancer. 2024;130:1–13.
- ↑Aredo JV, Jamali A, Zhu J, et al. Liquid biopsy approaches for cancer characterization and residual disease detection. ASCO Educ Book. 2025;45:e1–e23.
- ↑Pathak P, Chan G, Deming DA, Chee CE. State-of-the-art management of colorectal cancer. ASCO Educ Book. 2024;44:3–15.
- ↑Conca V, Ciraci O, Bocaccio C, et al. Waiting for the liquid revolution in adjuvant colon cancer. Cancer Treat Rev. 2024;126:102735.
- ↑Malla M, Loree JM, Kasi PM, Parikh AR. Using circulating tumor DNA in colorectal cancer. J Clin Oncol. 2022;40:2846–2857.
- ↑Shergill A, Parikh AR. Investigating ctDNA in early-stage colon cancer. Oncology (Williston Park). 2022;36(10):620–626.
- ↑Arisi M, Dotan E, Fernandez S. Circulating tumor DNA in precision oncology. Int J Mol Sci. 2022;23:444.
- ↑Dasari A, Morris VK, Allegra CJ, et al. ctDNA applications in colorectal cancer: NCI task force white paper. Nat Rev Clin Oncol. 2020;17:757–770.
- ↑Naidoo M, Gibbs P, Tie J. ctDNA and adjuvant therapy for colorectal cancer. Cancers (Basel). 2021;13:346.
- ↑Schraa SJ, van Rooijen KL, Koopman M, et al. Cell-free circulating tumor DNA before surgery as a prognostic factor. Cancers (Basel). 2022;14:2218.
- ↑Pascual J, Attard G, Bidard FC, et al. ESMO recommendations on the use of circulating tumour DNA assays for patients with cancer: a report from the ESMO Precision Medicine Working Group. Ann Oncol. 2022;33(8):750–768.
- ↑Alese OB, Cook N, et al. Circulating tumor DNA: an emerging tool in gastrointestinal cancers. ASCO Educ Book. 2022;42:279–298.
- ↑Abidoye O, Ahn DH, Borad MJ, et al. Circulating tumor DNA testing for minimal residual disease and its application in colorectal cancer. Cells. 2025;14(3):161.
- ↑Crisafulli G. Liquid biopsy and challenge of assay heterogeneity for minimal residual disease assessment in colon cancer treatment. Genes (Basel). 2025;16(1):71.
- ↑Yang J, Yu C, Li H, et al. Evaluation of molecular residual disease by a fixed gene panel in resectable colorectal cancer. Cancer Res Treat. 2024;56:1183–1196.
- ↑Tie J, Wang Y, Tomasetti C, et al. Circulating tumor DNA analysis detects minimal residual disease and predicts recurrence in patients with stage II colon cancer. Sci Transl Med. 2016;8(346):346ra92.
- ↑Tie J, Cohen JD, Wang Y, et al. Circulating tumor DNA analyses as markers of recurrence risk and benefit of adjuvant therapy for stage III colon cancer. JAMA Oncol. 2019;5(12):1710–1717.
- ↑Tie J, Cohen JD, Wang Y, et al. Serial circulating tumour DNA analysis during multimodality treatment of locally advanced rectal cancer. Gut. 2019; 68:663–671.
- ↑Tie J, Cohen JD, Lo SN, et al. Prognostic significance of postsurgery circulating tumor DNA in nonmetastatic colorectal cancer: an individual patient pooled analysis. Int J Cancer. 2021;148(4):1014–1026.
- ↑Reinert T, Henriksen TV, Christensen E, et al. Analysis of plasma cell-free DNA by ultradeep sequencing in patients with stages I–III colorectal cancer. JAMA Oncol. 2019;5(8):1124–1131.
- ↑Henriksen TV, Tarazona N, Frydendahl A, et al. Circulating tumor DNA in stage III colorectal cancer beyond minimal residual disease detection. Clin Cancer Res. 2022;28(3):507–517.
- ↑Tie J, Cohen JD, Lahouel K, et al. Circulating tumor DNA analysis guiding adjuvant therapy in stage II colon cancer. N Engl J Med. 2022; 386:2261–2272.
- ↑Tie J, Wang Y, Lo SN, et al. Circulating tumor DNA analysis guiding adjuvant therapy in stage II colon cancer: 5-year outcomes of the DYNAMIC trial. Nat Med. 2025;31(5):1509–1518.
- ↑Tie J, Wang Y, Loree JM, et al. ctDNA-guided adjuvant chemotherapy escalation in stage III colon cancer: primary analysis of the DYNAMIC-III trial. J Clin Oncol. 2025;43(16 Suppl):3503.
- ↑Kotani D, Oki E, Nakamura Y, et al. Molecular residual disease and efficacy of adjuvant chemotherapy in patients with colorectal cancer. Nat Med. 2023;29:127–134.
- ↑Yukami H, Nakamura Y, Mishima S, et al. Circulating tumor DNA dynamics in colorectal cancer with molecular residual disease: updated analysis of the GALAXY study. J Clin Oncol. 2024;42(Suppl 3):6.
- ↑Nakamura Y, Watanabe J, Akazawa N, et al. ctDNA-based molecular residual disease and survival in resectable colorectal cancer. Nat Med. 2024;30:3272–3283.
- ↑Kataoka K, Muro K, Nakamura Y, et al. Survival benefit of adjuvant chemotherapy based on molecular residual disease detection in resected colorectal liver metastases. Ann Oncol. 2024;35:1015–1025.
- ↑VEGA Trial Investigators. ctDNA-guided randomized non-inferiority trial (VEGA) comparing post-surgical observation vs standard chemotherapy in ctDNA-negative resected colorectal cancer (CIRCULATE-Japan). Presented at: AACR/ASCO 2025. (Abstract).
- ↑VEGA Trial Investigators. A randomized, ctDNA-guided de-escalation study for post-surgical management of ctDNA-negative resected colorectal cancer (CIRCULATE-Japan platform). Presented at: ESMO Gastrointestinal Cancers Congress 2025; 2–5 Jul 2025; Barcelona, Spain. Abstract 20.
- ↑Bando H, Watanabe J, Kotaka M, et al. A randomized, double-blind, phase III study comparing trifluridine/tipiracil (FTD/TPI) versus placebo in patients with molecular residual disease following curative resection of colorectal cancer (ALTAIR). J Clin Oncol. 2025;43(suppl 4):LBA22.
- ↑Bando H, Watanabe J, Kotaka M et al. Phase III randomized study of trifluridine/tipiracil (FTD/TPI) versus placebo in patients with molecular residual disease following curative resection of colorectal cancer (ALTAIR; NCT04457297). Presented at: ESMO Gastrointestinal Cancers Congress 2025; 2–5 Jul 2025; Barcelona, Spain. Ann Oncol 2025;36 (supp S1) Abstract 30.
- ↑Kasi PM, Aushev VN, Langer N, et al. Circulating tumor DNA for informing adjuvant chemotherapy in stage II/III colorectal cancer: interim analysis of the BESPOKE CRC study. J Clin Oncol. 2024;42(Suppl 3):9.
- ↑Tie J, Cohen JD, Wang Y, et al. ctDNA-informed adjuvant chemotherapy in locally advanced rectal cancer: DYNAMIC-Rectal. J Clin Oncol. 2024;42(Suppl 3):12.
- ↑Parikh AR, Van Seventer EE, Siravegna G, et al. Minimal residual disease detection using a plasma-only circulating tumor DNA assay in colorectal cancer. Clin Cancer Res. 2021;27(20):5586–5594.
- ↑Nakamura Y, Tsukada Y, Matsuhashi N, et al. Colorectal cancer recurrence prediction using a tissue-free epigenomic minimal residual disease assay. Clin Cancer Res. 2024;30(19):4377–4387.
- ↑Lonardi S, Pietrantonio F, Tarazona N, et al. The PEGASUS trial: post-surgical liquid biopsy–guided treatment of stage III and high-risk stage II colon cancer. Ann Oncol. 2023;34(Suppl):S1268–S1269.
- ↑Morris VK, Yothers G, Kopetz S, et al. Circulating tumor DNA as a predictive biomarker in adjuvant chemotherapy for stage II colon cancer: COBRA trial. J Clin Oncol. 2024;42(Suppl):5.
- ↑Negro S, Pulvirenti A, Trento C, et al. Circulating tumor DNA as a real-time biomarker for minimal residual disease and recurrence prediction in stage II colorectal cancer. Int J Mol Sci. 2025;26(6):2486.
ranm tv
Eduardo Díaz-Rubio
Real Academia Nacional de Medicina de España
C/ Arrieta, 12 · 28013 Madrid
Tlf.: +34 91 159 47 34 | E-Mail: ediazrubio@gmail.com
Enviado*: 09.12.25
Revisado: 12.12.25
Aceptado: 28.12.25
* Fecha de lectura en la RANM


