Resumen
El cáncer de vejiga constituye un importante problema de salud pública debido a su elevada incidencia, recurrencia y mortalidad. La distinción entre el tumor vesical no músculo-invasivo (TVNMI) y el tumor vesical músculo-invasivo (TVMI) es fundamental, ya que representa el principal punto de inflexión pronóstico y terapéutico de la enfermedad.
La RM vesical, aplicada conforme al sistema VI-RADS (Vesical Imaging-Reporting and Data System), proporciona un marco estandarizado para la adquisición e interpretación de las imágenes, con el objetivo de estimar la probabilidad de invasión del músculo detrusor. Este sistema clasifica los hallazgos en una escala de 1 a 5 según el riesgo creciente de infiltración muscular, mejorando la reproducibilidad diagnóstica, la comunicación multidisciplinar y la toma de decisiones clínicas.
El protocolo de RM combina secuencias anatómicas potenciadas en T2 con secuencias funcionales de difusión (DWI) y contraste (DCE), otorgando mayor peso a las secuencias funcionales. Una interpretación adecuada requiere estudios de alta calidad, lo que implica una correcta preparación del paciente y un protocolo técnicamente optimizado.
Las categorías VI-RADS 1–2 presentan un alto VPN, lo que puede evitar la re-RTU en casos con histología concordante. La categoría VI-RADS 5 se asocia a un alto riesgo de invasión del músculo detrusor y de extensión extravesical, mientras que las categorías VI-RADS 3–4 muestran diferentes equilibrios entre sensibilidad y especificidad.
La RM vesical realizada tras la cistoscopia o la identificación tumoral por otra técnica de imagen, y antes de la RTU diagnóstica, permite en algunos casos (VI-RADS 1,2 y 5) acortar los tiempos diagnósticos y la reducción de procedimientos innecesarios (Re-RTU).
Existen limitaciones en localizaciones anatómicas complejas, divertículos, lesiones planas, variantes histológicas y en la evaluación tras RTU o instilaciones con BCG. Para alcanzar una precisión diagnóstica comparable a la de un lector experto, el radiólogo requiere una curva de aprendizaje.Abstract
Bladder cancer represents a major public health problem due to its high incidence, recurrence rate, and associated mortality. Distinguishing between non–muscle-invasive bladder cancer (NMIBC) and muscle-invasive bladder cancer (MIBC) is essential, as it constitutes the main prognostic and therapeutic turning point of the disease.
Bladder MRI performed according to the VI-RADS (Vesical Imaging-Reporting and Data System), provides a standardized framework for image acquisition and interpretation aimed at estimating the likelihood of detrusor muscle invasion. The system categorizes imaging findings on a 1–5 scale based on increasing risk of muscular infiltration, thereby improving diagnostic reproducibility, multidisciplinary communication, and clinical decision-making.
The MRI protocol combines high-resolution T2-weighted anatomical sequences with functional diffusion-weighted imaging (DWI) and dynamic contrast-enhanced (DCE) sequences, with greater emphasis placed on functional imaging. Accurate interpretation requires high-quality examinations, including appropriate patient preparation and a technically optimized protocol.
VI-RADS categories 1–2 show a high negative predictive value, which may allow avoidance of repeat transurethral resection (re-TURB) in cases with concordant histology. VI-RADS category 5 is associated with a high risk of detrusor muscle invasion and extravesical extension, whereas categories 3–4 demonstrate different balances between sensitivity and specificity.
Bladder MRI performed after cystoscopy or tumor detection by another imaging modality and prior to diagnostic transurethral resection (TURB) may, in selected cases (VI-RADS 1, 2, and 5), shorten diagnostic pathways and reduce unnecessary procedures, including repeat TURB.
Limitations exist in anatomically complex locations, bladder diverticula, flat lesions, histological variants, and post-TURB or post-BCG settings. Achieving diagnostic accuracy comparable to that of expert readers requires a dedicated learning curve for radiologists.Palabras clave: VI-RADS; Diagnóstico por imagen; Estadificación tumoral; Resonancia Magnética; Neoplasias de vejiga urinaria.
Keywords: Urinary Bladder; Neoplasms; Magnetic Resonance imaging; Diffusion Magnetic; Resonance Imaging; Neoplasm Staging; Diagnostic Imaging; VI-RADS.
INTRODUCCIÓN
El cáncer de vejiga representa uno de los principales desafíos de la oncología urológica debido a su elevada incidencia, alta tasa de recurrencia y mortalidad asociada. Según el Observatorio Global del Cáncer (GLOBOCAN 2022), es el noveno tumor más frecuente y la decimotercera causa de muerte por cáncer a nivel mundial (1). En España, fue el quinto tumor más frecuente en incidencia en 2023 y ocupa el octavo lugar en mortalidad, siendo el segundo cáncer urológico en prevalencia tras el de próstata (2).
La elevada tasa de recurrencia obliga a múltiples procedimientos diagnósticos y terapéuticos —controles endoscópicos, resecciones transuretrales e instilaciones intravesicales—, lo que conlleva una considerable morbilidad para los pacientes y una sobrecarga asistencial y económica para los sistemas sanitarios.
Su elevada incidencia, prevalencia y mortalidad subrayan la necesidad de establecer estrategias eficaces para la prevención, el diagnóstico precoz y la optimización terapéutica, con el fin de mejorar los resultados clínicos y reducir la morbimortalidad asociada.
El abordaje del cáncer vesical requiere comprender sus factores de riesgo, histología, anatomía y la estadificación TNM, ya que la distinción entre no músculo-invasivo (TVNMI) y músculo-invasivo (TVMI) constituye el punto de inflexión pronóstico y terapéutico.
Epidemiología y factores de riesgo
El tabaquismo es el principal factor de riesgo, hasta el 65 % de los casos, debido a la excreción urinaria de carcinógenos como aminas aromáticas, hidrocarburos aromáticos policíclicos y nitrosaminas, con una clara relación dosis-respuesta (3,4). Aunque el riesgo disminuye tras el cese del hábito tabáquico, no se equipara al de los no fumadores. La exposición ocupacional a aminas aromáticas en industrias como el caucho, tintes, cuero, pintura o metalurgia explica aproximadamente el 10 % de los casos (4,5). Otros factores de riesgo incluyen anomalías congénitas (uraco persistente), tratamientos previos con ciclofosfamida o radioterapia pélvica, infecciones urinarias crónicas y el uso prolongado de catéteres permanentes. En regiones endémicas de África y Oriente Medio, la esquistosomiasis se asocia de forma característica al carcinoma escamoso de vejiga (5).
El cáncer de vejiga es más frecuente en varones, con una proporción aproximada de 4:1 respecto a las mujeres, y la mayoría de los diagnósticos se realizan a partir de los 65 años (1).
Anatomía vesical
La vejiga es un órgano hueco, muscular y extraperitoneal, cuya pared está formada por tres capas principales. La capa más interna corresponde a la mucosa, compuesta por el urotelio y la lámina propia; esta última puede contener una fina capa de músculo liso denominada muscularis mucosae. La capa intermedia es la muscularis propia o músculo detrusor, constituida por fibras musculares lisas entrelazadas, cuya invasión define el tumor vesical músculo-invasivo (TVMI). La capa más externa corresponde a la serosa únicamente en la cúpula vesical, estando el resto de la superficie recubierta por una adventicia de tejido conectivo y grasa perivesical. Desde el punto de vista oncológico, esta disposición anatómica es crítica, ya que la invasión tumoral modifica el estadio y el pronóstico de la enfermedad (6).
Histología tumoral
El carcinoma urotelial (antes conocido como “de células transicionales”) representa aproximadamente el 90 % en países occidentales (7), existen variantes con peor pronóstico: micropapilar (que se asocia a invasión linfovascular), plasmocitoide (con tendencia a diseminación peritoneal), sarcomatoide (comportamiento agresivo) (6). Otros subtipos histológicos son el escamoso (3–5 %, asociado a esquistosomiasis), adenocarcinoma (<2 %, relacionado con uraco persistente o metaplasia glandular), células pequeñas (<1 %, de origen neuroendocrino, muy agresivo) (6-8).
Sistema TNM
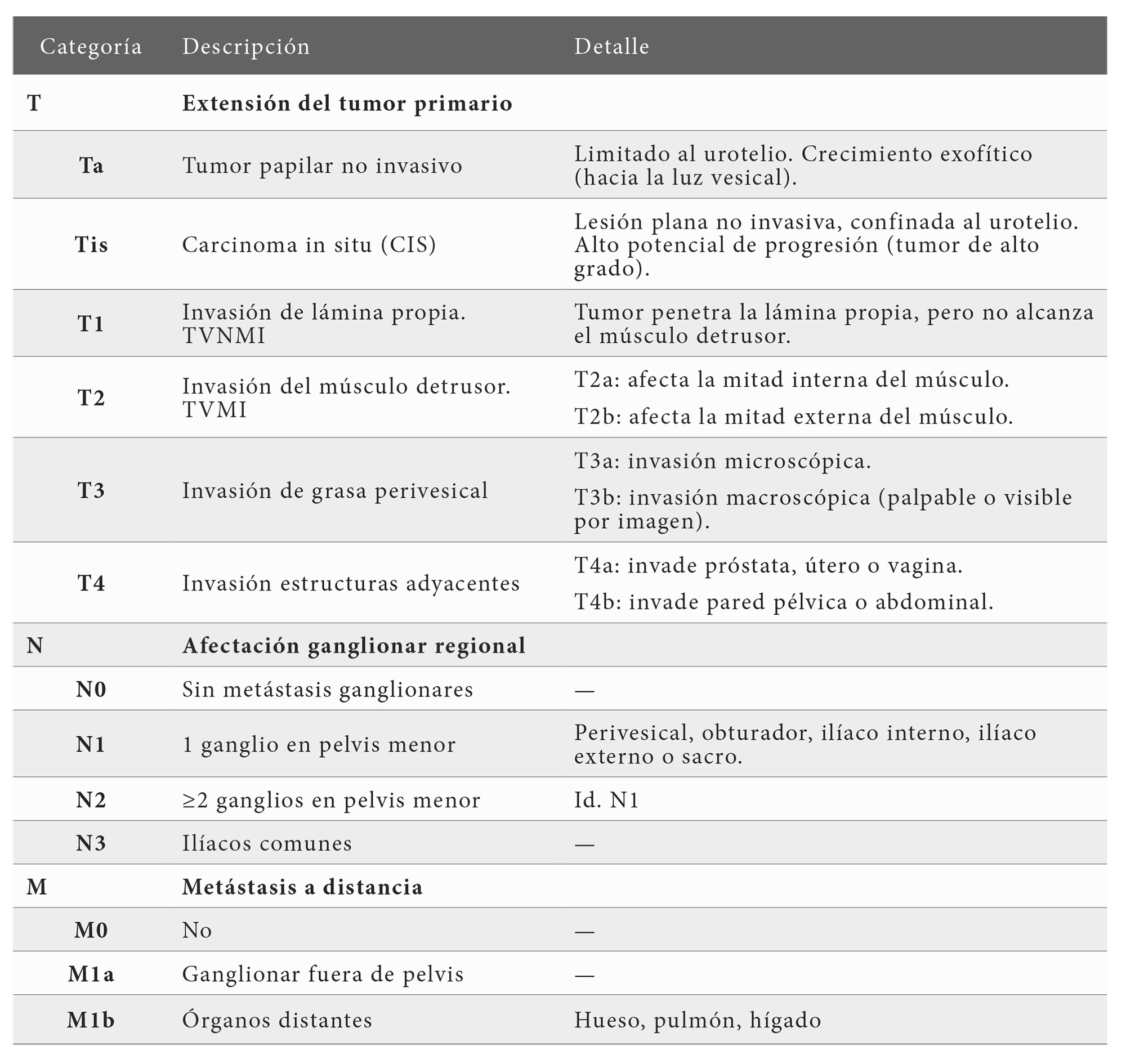
El sistema TNM, cuya versión vigente corresponde a la 8.ª edición (2017) es el estándar universal para la estadificación del cáncer vesical, permitiendo orientar el tratamiento y definir el pronóstico (9). La categoría T describe la extensión del tumor primario y tiene implicaciones críticas para el pronóstico y el tratamiento. El estadio T1 incluye tumores confinados a mucosa y lámina propia sin infiltración muscular, TVNMI. En cambio, el estadio T2 indica invasión del músculo detrusor, lo que se asocia con mayor agresividad biológica y peor pronóstico, TVMI (9-10). (Tabla 1)
Diagnóstico del Cáncer de Vejiga
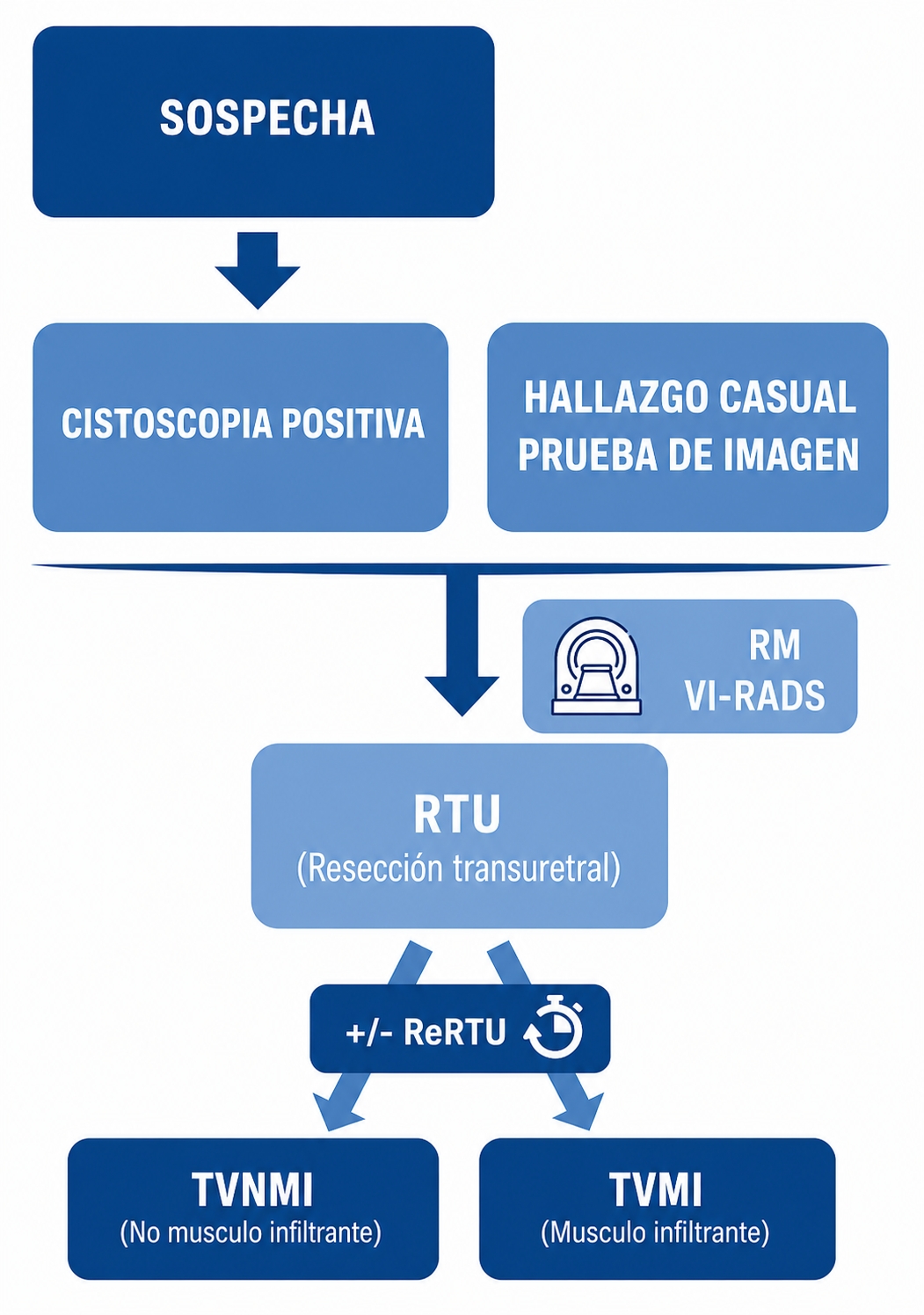
La hematuria macroscópica indolora constituye el principal signo de alarma (10). Actualmente, no se considera ninguna prueba de cribado poblacional para su detección precoz. Según las guías de la European Association of Urology (EAU), la evaluación inicial ante la sospecha clínica incluye anamnesis, citología urinaria, cistoscopia, resección transuretral de vejiga (RTU-V) y pruebas de imagen para la estadificación (11) (Figura 1).
La cistoscopia permite identificar lesiones vesicales sospechosas y, en un segundo tiempo bajo anestesia, se realiza la RTU-V, procedimiento de referencia para la obtención de diagnóstico histológico y la resección del tumor visible. Esta técnica conlleva posibles complicaciones como hematuria franca, perforación y, raramente, diseminación extravesical (sobre todo en TVMI). Es imprescindible que la muestra incluya músculo detrusor para una correcta estadificación. No obstante, la RTU-V presenta limitaciones, la infraestadificación tumoral y la posibilidad de enfermedad residual. Se ha descrito persistencia tumoral tras la primera RTU en hasta el 30 % de los casos, dependiendo de la experiencia del operador (11,12).
Por este motivo, las guías de la EAU recomiendan la realización de una segunda RTU (re-RTU-V) en casos de resección incompleta, ausencia de músculo en la muestra inicial y en la mayoría de los tumores T1, a excepción de tumores Ta de bajo grado o carcinoma in situ primario. La re-RTU-V debe realizarse idealmente entre las 2 y 6 semanas posteriores a la intervención inicial, lo que puede retrasar la estadificación definitiva y el inicio del tratamiento (13,14).
La radiología contribuye al diagnóstico, estadificación, planificación terapéutica y seguimiento del cáncer de vejiga (15,16).
La ecografía abdominal es útil como prueba inicial en estudio de hematuria y para la detección oportunista de lesiones vesicales. La sensibilidad es limitada en vejigas no distendidas, pacientes incontinentes y lesiones pequeñas, planas o localizadas en el cuello. Estudios recientes en distintos centros han explorado el uso de la ecografía con contraste (CEUS) en el cáncer vesical, mostrando que puede discriminar entre tumores Ta–T1/bajo grado y T2/alto grado con elevada sensibilidad y especificidad (17).
El TC con contraste tiene papel en la evaluación del tracto urinario superior y en la valoración de la extensión extravesical (estadificación T), el compromiso ganglionar (N) y la detección de metástasis a distancia (M) (15,18).
La RM permite una estadificación local más precisa gracias a su superior resolución de contraste tisular respecto a la TC, lo que facilita una mejor diferenciación de las capas de la pared vesical y una valoración más exacta de la invasión del músculo detrusor. Además, resulta útil en la reevaluación tras tratamientos sistémicos como la quimioterapia o inmunoterapia o durante la vigilancia activa de tumores T1 (10, 19, 20-23).
Es relevante considerar que, tras la RTU-V aparecen cambios inflamatorios que modifican la apariencia de la pared vesical y pueden simular o enmascarar una lesión. Por este motivo, se recomienda realizar la RM de diagnóstico previa a la RTU. Si el procedimiento ya se ha efectuado, la sensibilidad y especificidad del estudio disminuyen, y se aconseja esperar al menos 6–8 semanas antes de realizar la exploración, a fin de reducir los cambios inflamatorios (24). El creciente respaldo de las sociedades científicas refleja la sólida evidencia disponible sobre el rendimiento diagnóstico y el elevado valor predictivo negativo de la RM vesical (11).
VI-RADS
El sistema VI-RADS (Vesical Imaging-Reporting and Data System) proporciona directrices estandarizadas para la adquisición, interpretación y categorización de los hallazgos de la RM con el objetivo de mejorar la reproducibilidad diagnóstica, la comunicación interdisciplinar y la toma de decisiones clínicas (10).
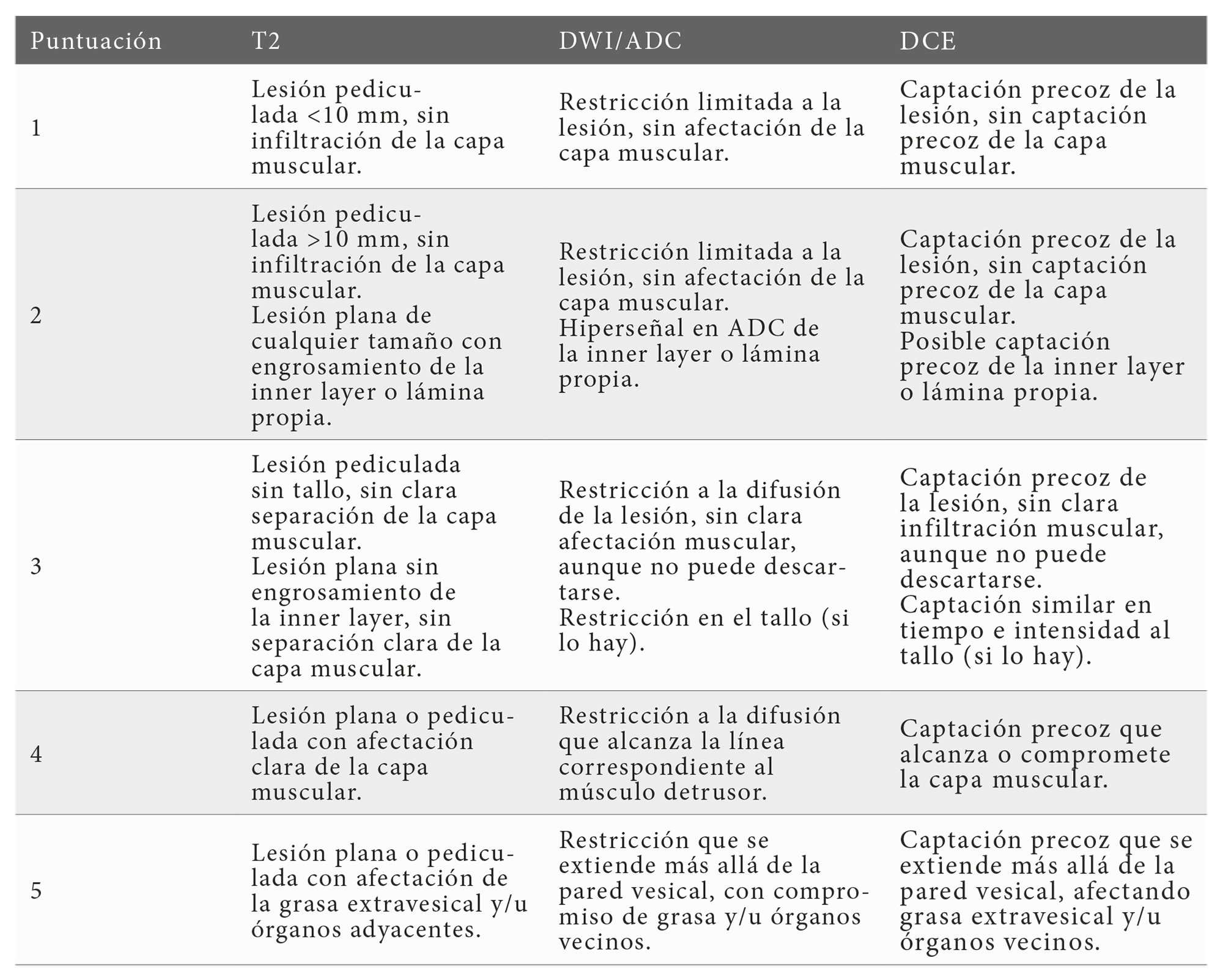
A diferencia de otros sistemas, VI-RADS no estima la probabilidad de malignidad, sino que estratifica el riesgo de invasión del músculo detrusor de los tumores vesicales. La puntuación se establece en una escala ordinal de 1 a 5, según la probabilidad creciente de afectación muscular (10), agrupándose en baja probabilidad (VI-RADS 1–2), probabilidad intermedia (VI-RADS 3) y alta probabilidad de invasión (VI-RADS 4–5). (Tabla 2). Además, evalúa toda la vejiga, permitiendo detectar tumores multifocales.
Desde el punto de vista morfológico, las neoplasias vesicales pueden clasificarse en polipoides, sésiles o planas, en función de su patrón de crecimiento y base de implantación sobre la pared (23). Las lesiones polipoides tienen un crecimiento exofítico intravesical, frecuentemente con un pedículo o tallo de anclaje que en RM suele mostrar una señal en T2, baja señal en valores b altos de DWI, señal elevada en ADC. Las lesiones sésiles presentan una base de implantación amplia, mientras que las lesiones planas se reconocen como un engrosamiento discreto y difuso de la mucosa.
El sistema VI-RADS se basa en la evaluación combinada de tres secuencias clave de RM (10, 24) (Figura 2):
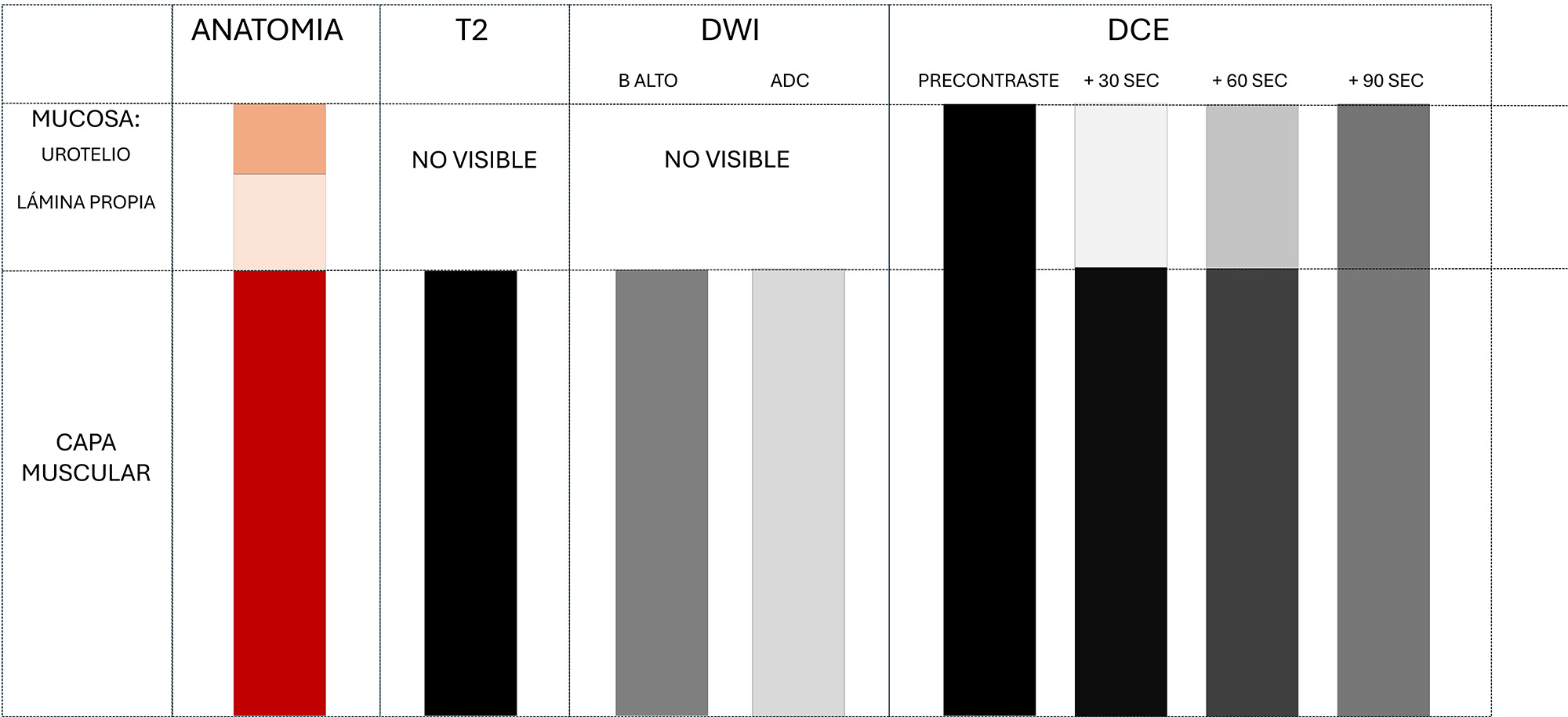
- Las secuencias potenciadas en T2: permiten evaluar la morfología tumoral, su tamaño y localización. En condiciones normales, el músculo detrusor se identifica como una banda hipointensa continua, mientras que el urotelio y la lámina propia no se identifican salvo en presencia de patología inflamatoria o tumoral. La interrupción o pérdida de continuidad de esta banda hipointensa es indicativa de invasión muscular.
- Las secuencias de difusión (DWI) y los mapas ADC son fundamentales para la detección de lesiones pequeñas y para la valoración de la invasión del músculo detrusor. En situaciones normales, el músculo detrusor muestra una señal intermedia en valores b altos y no presenta restricción en los mapas ADC, mientras que los tumores vesicales muestran restricción a la difusión, lo que permite una mejor delimitación de la lesión y su extensión.
- Las secuencias dinámicas con contraste (DCE) aportan información adicional sobre el patrón de realce. En condiciones normales, la mucosa y la lámina propia presentan un realce precoz e intenso, mientras que el músculo detrusor muestra un realce más tardío y progresivo. Aproximadamente a los 90 segundos tras la administración del contraste, el relace entre capas tiende a igualarse, puede originar errores diagnósticos si no se interpreta adecuadamente.
Para garantizar estudios de alta calidad, resulta esencial una adecuada preparación del paciente. Se recomienda vaciar la vejiga entre una y dos horas antes de la exploración y posteriormente ingerir de forma progresiva entre 0,5-1 litro de agua, con el objetivo de lograr una distensión vesical moderada. Una vejiga insuficientemente distendida dificulta la evaluación anatómica, mientras que una sobredistensión puede adelgazar excesivamente la pared (<3 mm), impidiendo distinguir las capas y generar artefactos por movimiento.
Deben evitarse sondajes vesicales recientes, ya que pueden inducir inflamación y artefactos por gas; en caso de haberse realizado, se aconseja esperar al menos 72 horas. Siempre que no existan contraindicaciones, es recomendable la administración de un antiespasmódico y un ayuno mínimo de 4 horas para reducir el peristaltismo intestinal. En presencia de gas rectal significativo, puede considerarse la colocación de una sonda rectal. La aplicación de bandas de saturación abdominal contribuye a minimizar los artefactos respiratorios (10,24).
Desde el punto de vista técnico, se recomienda realizar el estudio en equipos de 1,5 T o 3 T, utilizando bobinas multicanal (≥16 canales). Las secuencias T2 deben adquirirse en al menos dos planos, preferiblemente tres, con un grosor de corte de 3–4 mm y sin supresión grasa. Aunque no existe consenso sobre la orientación del plano axial, se aconseja orientarlo perpendicularmente a la base de la lesión; en ausencia de una lesión dominante, puede orientarse hacia el trígono vesical.
La secuencia de difusión debe incluir valores b altos (800–1000 s/mm², pudiendo alcanzar hasta 2000 s/mm² o valores sintéticos), con generación de mapas ADC y adquisición en preferiblemente dos planos. El estudio dinámico con contraste se realiza mediante secuencias T1 con supresión grasa tras la administración de gadolinio (0,1 mmol/kg), con adquisiciones cada 20–30 segundos durante un mínimo de 3 minutos. La utilización de técnicas de sustracción puede aumentar la precisión en la evaluación del realce tumoral (10,24).
Interpretación sistema VI-RADS
La categoría final VI-RADS se obtiene mediante la integración de los hallazgos en las secuencias T2, DWI y DCE (Tabla 2). Cuando dos o más secuencias coinciden en la puntuación, esa es la categoría asignada.
En caso de discrepancia, se priorizan las secuencias funcionales, otorgando mayor peso a la DWI sobre la DCE, siempre que no existan artefactos que limiten su interpretación (10,24) (Figura 3).
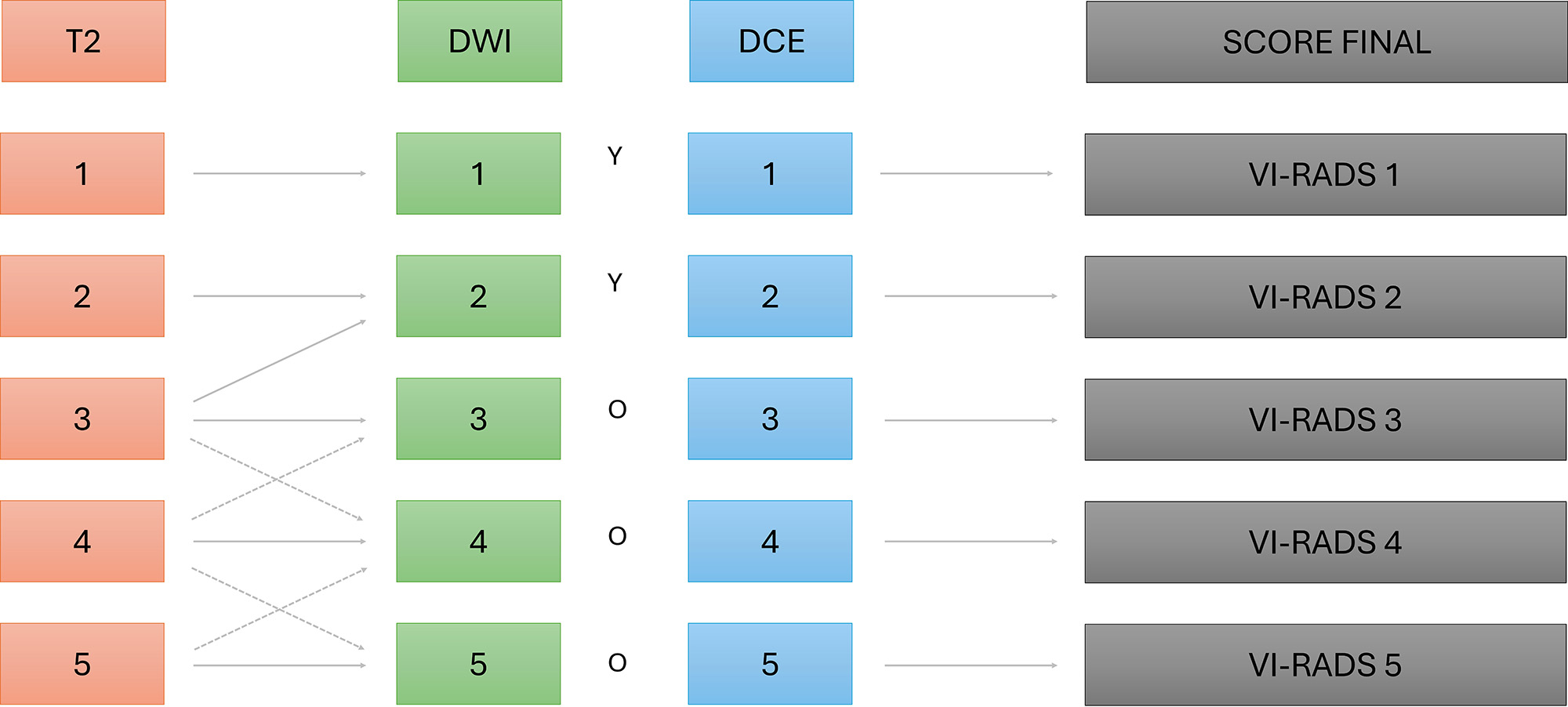
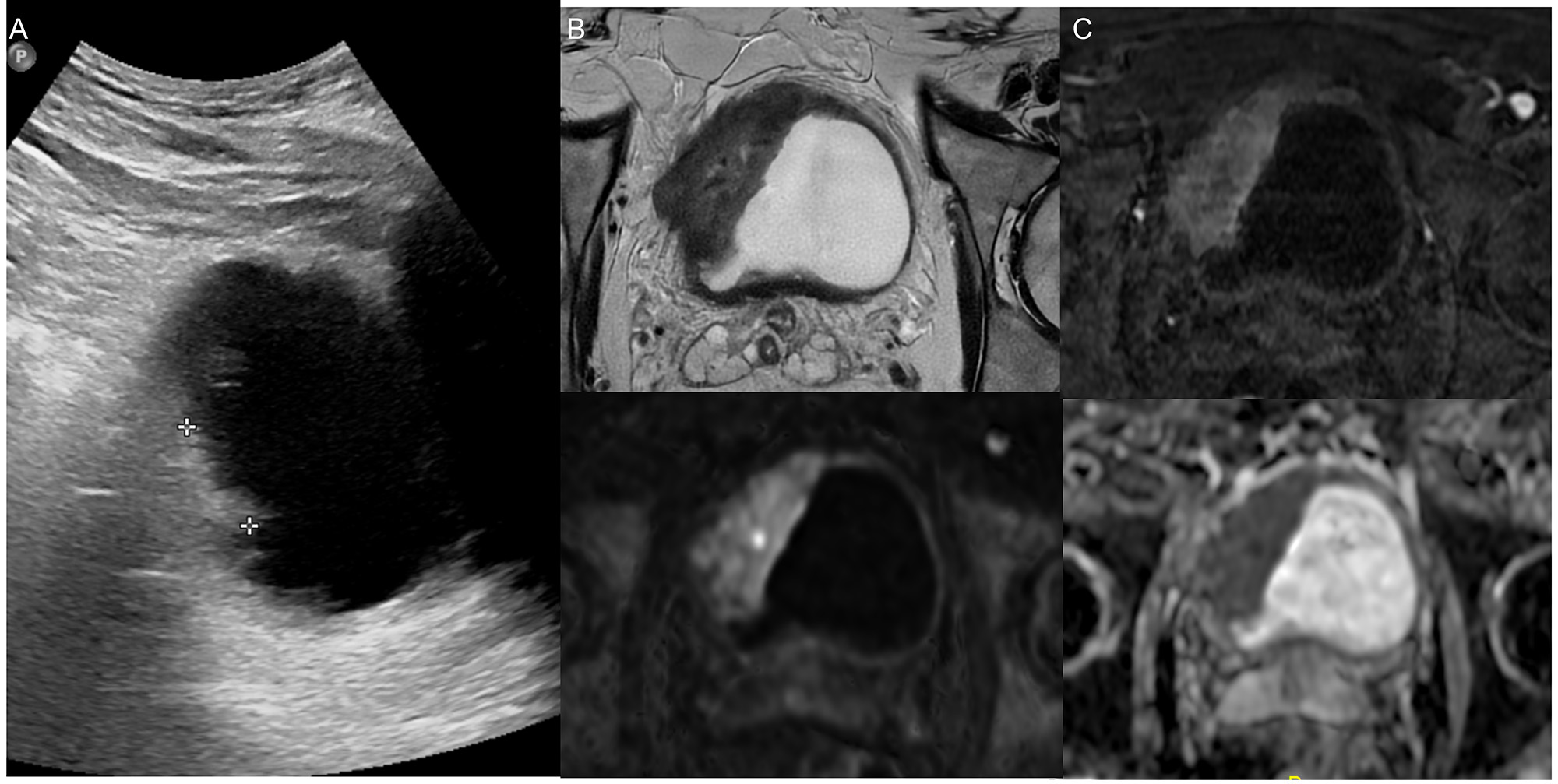
La evidencia disponible indica que la DWI de alta calidad es la secuencia más determinante para la detección y estadificación del cáncer de vejiga, mientras que la DCE incrementa la confianza diagnóstica, especialmente en lesiones pequeñas, en lectores menos experimentados o en estudios con artefactos (24) (Figuras 4–7).
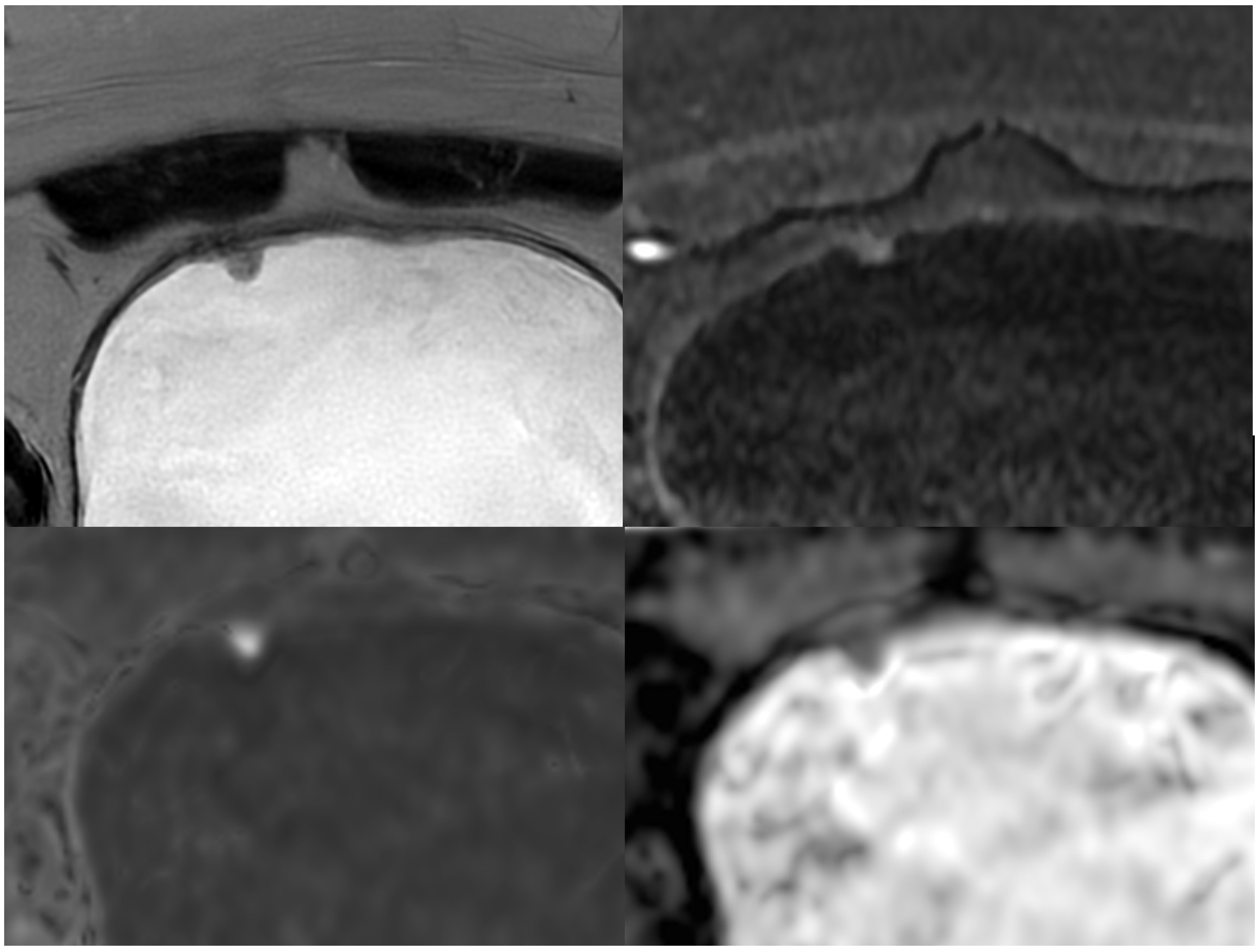
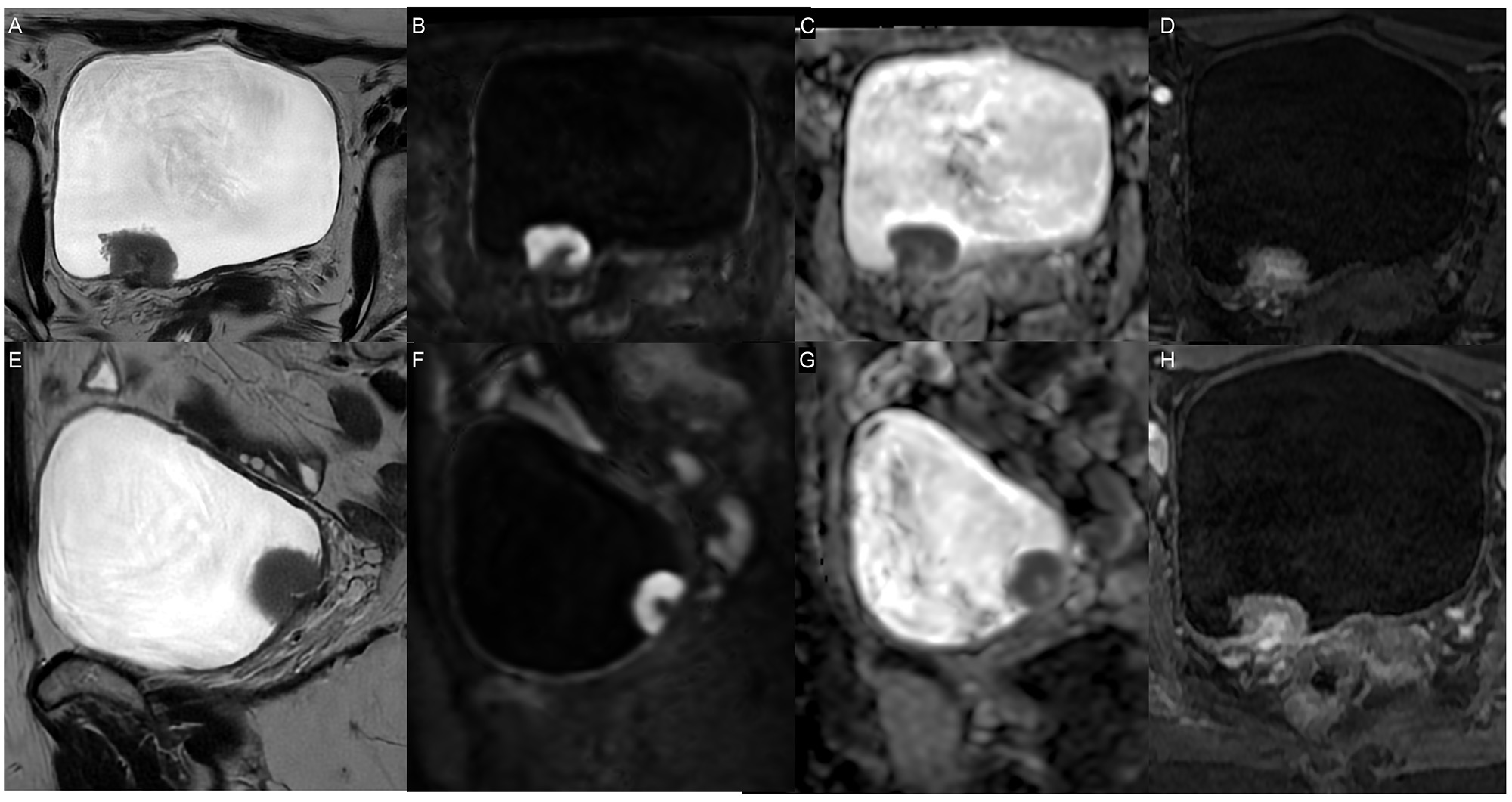
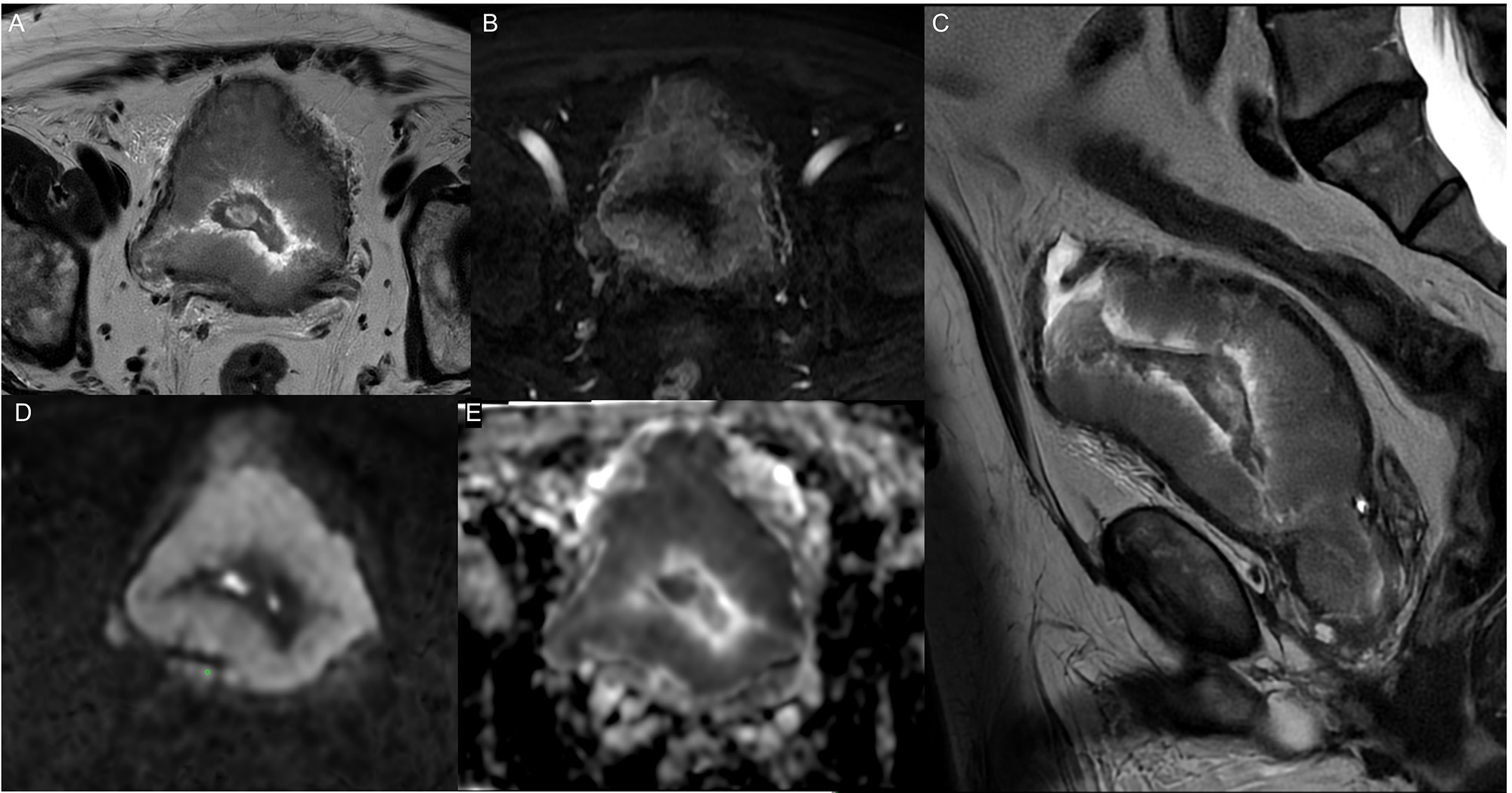
Limitaciones RM Vejiga
Determinadas localizaciones anatómicas, como los meatos ureterales, el cuello vesical y la cúpula, pueden dificultar la evaluación debido a la distorsión de las capas de la pared y a los movimientos (24).
Los divertículos vesicales constituyen un escenario particular, ya que carecen de capa muscular propia, lo que impide clasificarlos como VI-RADS 4, los tumores pueden limitarse a la mucosa o invadir la grasa perivesical. (24)
Las lesiones planas y determinadas variantes histológicas no uroteliales o atípicas pueden mostrar patrones de señal y realce menos característicos, reduciendo la fiabilidad del sistema. No obstante, estudios recientes han demostrado que VI-RADS mantiene un elevado rendimiento diagnóstico en tumores con variantes histológicas del carcinoma urotelial, con sensibilidades del 82–94 % y especificidades del 94–100 %. En estos casos, hallazgos como señal heterogénea en T2, necrosis intratumoral o valores ADC bajos pueden sugerir un comportamiento biológico más agresivo y alertar al radiólogo sobre la posible presencia de una variante histológica (25).
La evaluación tras la RTU o después del tratamiento intravesical con BCG supone otro desafío diagnóstico, debido a los cambios inflamatorios, hemorrágicos y fibróticos que pueden simular o enmascarar recidiva tumoral y alterar la interpretación de las secuencias funcionales. Por este motivo, siempre que sea posible, la RM debe planificarse antes de cualquier manipulación vesical; cuando esto no sea factible, es recomendable diferir el estudio al menos 6–8 semanas tras la RTU (24).
Finalmente, la correcta aplicación del sistema VI-RADS requiere experiencia. Diversos estudios coinciden en que es necesaria una curva de aprendizaje estimada de 100–150 casos para alcanzar una precisión diagnóstica comparable a la descrita en la literatura, incluso utilizando protocolos técnicamente optimizados (19).
Aplicabilidad clínica
En la práctica clínica, el uso de la RM vesical y del sistema VI-RADS puede adaptarse a los recursos disponibles y a los objetivos diagnósticos de cada centro (Figura 1). Con el fin de optimizar recursos, reducir procedimientos invasivos y acortar los tiempos diagnósticos, la RM podría reservarse preferentemente para lesiones con sospecha de invasión muscular, como lesiones pediculadas sospechosas, lesiones sésiles o planas, excluyendo aquellas claramente benignas o de muy bajo riesgo.
La RM vesical realizada tras la cistoscopia o la detección tumoral por otra técnica de imagen y antes de la RTU diagnóstica aporta un elevado VPN en lesiones de bajo riesgo (VI-RADS ≤2). En escenarios seleccionados, y siempre en concordancia con los hallazgos histopatológicos y el contexto clínico, permite seleccionar pacientes en los que podría evitarse la re-RTU-V, reduciendo procedimientos invasivos, morbilidad y tiempos diagnósticos.
En el extremo opuesto, ante una alta sospecha de invasión muscular y extensión extravesical (VI-RADS 5), la RM muestra una elevada concordancia con el diagnóstico de tumor vesical músculo-invasivo. En estos casos, la información aportada por la RM permite planificar una RTU más dirigida, orientada a la confirmación histológica y a la obtención de material tisular, minimizando el riesgo de complicaciones como la perforación vesical asociada a biopsias profundas.
El manejo de las lesiones VI-RADS 3 y 4 continúa siendo motivo de debate. Diversos estudios han confirmado el buen rendimiento diagnóstico del sistema, con sensibilidades cercanas al 87 % y especificidades del 86–94 %, además de una alta concordancia interobservador(26-30). VI-RADS 3 ofrece mayor sensibilidad, mientras que VI-RADS 4 es más específico; por ello, VI-RADS 3 se considera el punto de corte razonable para la sospecha de invasión muscular, guiando la indicación de re-RTU tras una RTU inicial negativa. (26-31)
El cáncer de vejiga constituye un problema de salud pública mundial, con alta incidencia, recurrencia y mortalidad. Su manejo depende de una estadificación precisa, que distinga entre TVNMI y TVMI.
La RM es una técnica no invasiva que permite una evaluación locorregional precisa del cáncer vesical. El sistema VI-RADS ha estandarizado la adquisición e interpretación de los estudios mejorando la comunicación entre especialidades. Se trata de una escala de riesgo de infiltración del músculo detrusor, en la que las categorías VI-RADS 1 y 2 presentan un alto valor predictivo negativo para descartar invasión muscular, mostrando además una buena correlación con el estadio histopatológico. La implementación de VI-RADS optimiza la estratificación del riesgo, reduce procedimientos invasivos innecesarios y contribuye a una planificación terapéutica más precisa y personalizada en el cáncer de vejiga.
DECLARACIÓN DE TRANSPARENCIA
Los autores/as de este artículo declaran no tener ningún tipo de conflicto de intereses respecto a lo expuesto en el presente trabajo.
BIBLIOGRAFÍA
- ↑International Agency for Research on Cancer. Bladder cancer fact sheet: GLOBOCAN 2022 [Internet]. Lyon: IARC; 2022 [cited 2026 Mar 12]. Available from: https://gco.iarc.who.int/today
- ↑Asociación Española Contra el Cáncer. Cáncer de vejiga [Internet]. Madrid: AECC; 2024 [cited 2026 Mar 12]. Available from: https://www.contraelcancer.es/es/todo-sobre-cancer/tipos-cancer/cancer-vejiga
- ↑Freedman ND, Silverman DT, Hollenbeck AR, Schatzkin A, Abnet CC. Association between smoking and risk of bladder cancer among men and women. JAMA. 2011;306(7):737-745.
- ↑Burger M, Catto JWF, Dalbagni G, et al. Epidemiology and risk factors of urothelial bladder cancer. Eur Urol. 2013;63(2):234-241.
- ↑Daneshmand S. Epidemiology and risk factors of urothelial carcinoma of the bladder [Internet]. In: UpToDate. Waltham (MA): UpToDate; 2025 [cited 2026 Mar 12]. Available from: https://www.uptodate.com
- ↑Netter FH. Atlas de anatomía humana. 7th ed. Barcelona: Elsevier; 2019.
- ↑WHO Classification of Tumours Editorial Board. Urinary and male genital tumours. 5th ed. Lyon: International Agency for Research on Cancer; 2022.
- ↑Bolla SR, Odeluga N, Amraei R. Histology, bladder. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2023 [cited 2026 Mar 12]. Available from: https://www.ncbi.nlm.nih.gov/books/
- ↑Amin MB, Edge SB, Greene FL, et al., editors. AJCC cancer staging manual. 8th ed. New York: Springer; 2017.
- ↑Panebianco V, Narumi Y, Altun E, et al. Multiparametric magnetic resonance imaging for bladder cancer: Development of VI-RADS (Vesical Imaging-Reporting and Data System). Eur Urol. 2018;74(3):294-306.
- ↑European Association of Urology. EAU guidelines on non-muscle-invasive bladder cancer (Ta, T1 and CIS) [Internet]. Arnhem: EAU; 2024 [cited 2026 Mar 12]. Available from: https://uroweb.org/guidelines/non-muscle-invasive-bladder-cancer
- ↑European Association of Urology. EAU guidelines on muscle-invasive and metastatic bladder cancer [Internet]. Arnhem: EAU; 2024 [cited 2026 Mar 12]. Available from: https://uroweb.org/guidelines/bladder-cancer-muscle-invasive-and-metastatic
- ↑Akand M, Muilwijk T, Raskin Y, de Vrieze M, Joniau S, van der Aa F. Quality control indicators for transurethral resection of non-muscle-invasive bladder cancer. Clin Genitourin Cancer. 2019;17(6):e784-e792.
- ↑Beijert IJ, Hentschel AE, Bründl J, et al. Second TURB, restaging TURB or repeat TURB in primary T1 non-muscle-invasive bladder cancer: Impact on prognosis? Int Urol Nephrol. 2024;56:1323-1333.
- ↑Lee CH, Tan CH, Faria SC, Kundra V. Role of imaging in the local staging of urothelial carcinoma of the bladder. AJR Am J Roentgenol. 2017;208(6):1193-1205.
- ↑Hoegger MJ, Strnad BS, Ballard DH, et al. Urinary bladder masses, rare subtypes, and masslike lesions: Radiologic-pathologic correlation. Radiographics. 2022;42(7):E233-E254.
- ↑Ge XY, Lan ZK, Chen J, Zhu SY. Effectiveness of contrast-enhanced ultrasound for detecting the staging and grading of bladder cancer: A systematic review and meta-analysis. Med Ultrason. 2021;23(1):29-35.
- ↑Alhammami QS, Alzahrani RMA, Alnasser HE, et al. CT versus MRI for staging bladder cancer: A systematic review. Int J Med Dev Ctries. 2025.
- ↑Del Giudice F, Flammia RS, Pecoraro M, et al. The accuracy of Vesical Imaging-Reporting and Data System (VI-RADS): An updated comprehensive multi-institutional systematic review and meta-analysis. World J Urol. 2022;40(7):1733-1742.
- ↑Pecoraro M, Cipollari S, Messina E, et al. Multiparametric MRI for bladder cancer: A practical approach to the clinical application of VI-RADS. Radiology. 2025;314:e233459.
- ↑Brembilla G, Basile G, Cosenza M, et al. Neoadjuvant chemotherapy VI-RADS scores for assessing muscle-invasive bladder cancer response with multiparametric MRI. Radiology. 2024;313(3):e233020.
- ↑Pecoraro M, Del Giudice F, Magliocca F, et al. Vesical Imaging-Reporting and Data System (VI-RADS) for assessment of response to systemic therapy for bladder cancer: Preliminary report. Abdom Radiol (NY). 2022;47:763-770.
- ↑Lai AL, Birkhäuser FD, Eberli D, Donati OF. VI-RADS in bladder cancer: Overview, pearls and pitfalls. Eur J Radiol. 2023;160:110666.
- ↑Prietto dos Santos JF, Ghezzi CLA, Pedrollo IM, et al. Practical guide to VI-RADS: MRI protocols, lesion characterization, and pitfalls. Radiographics. 2024;44(2):e230149.
- ↑Aslan S, Tasdemir MN, Cakir E, Oguz U, Tok B. Predicting variant histology in bladder cancer: the role of multiparametric MRI and VI-RADS. Eur Radiol. 2025.
- ↑Del Giudice F, Barchetti G, De Berardinis E, et al. Prospective assessment of VI-RADS score in predicting muscle-invasive bladder cancer. Eur Radiol. 2020;30(3):1846-1855.
- ↑Woo S, Panebianco V, Narumi Y, et al. Diagnostic performance of VI-RADS for prediction of muscle-invasive bladder cancer: Systematic review and meta-analysis. Eur Urol Oncol. 2021;4(3):306-315.
- ↑Barchetti G, Simone G, Ceravolo I, et al. Multiparametric MRI of the bladder: Interobserver agreement and accuracy with VI-RADS. Eur Radiol. 2019;29(10):5492-5499.
- ↑Etxano J, López-Maseda A. Aplicaciones clínicas de la resonancia magnética de vejiga: más allá de la clasificación VI-RADS®. Radiología. 2025.
- ↑Etxano J, Rodríguez-Vigil B, Pérez F, et al. Vesical Imaging-Reporting and Data System (VI-RADS®): experiencia inicial en la clasificación del cáncer de vejiga músculo-infiltrante. Actas Urol Esp. 2021;45(4):320-325.
- ↑Galgano SJ, Goyal N, Longo J, Chauhan R, Samanta S, Davenport MS. The role of imaging in bladder cancer diagnosis and staging. Diagnostics (Basel). 2020;10(9):703.
Claudia Fontenla-Martínez
Servicio de Radiología. Hospital Universitario y Politécnico La Fe. Valencia.
Avd. Fernando Abril Martorell,106 · 46026
Tlf.: +34 663 494 729 | E-Mail: claufontenla@gmail.com
Enviado: 14.12.25
Revisado: 22.12.25
Aceptado: 10.01.26


