Resumen
La ocronosis exógena representa una dermatosis pigmentaria poco frecuente. Históricamente vinculada al uso de hidroquinona y otros derivados fenólicos tópicos. Aunque fue descrita hace ya más de un siglo, su fisiopatología no ha sido correctamente descifrada hasta tiempos extremadamente recientes y supone un enorme reto, tanto para el clínico por lo difícil de su abordaje diagnóstico-terapeútico dada la escasa evidencia científica, como para las autoridades preventivas debido al uso indiscriminado de agentes despigmentantes a menudo de forma no regulada. No obstante, recientes avances en el conocimiento de los mecanismos fisiopatológicos subyacentes en esta enfermedad, en el papel de la dermatoscopia a la hora de realizar el diagnóstico y en la irrupción de las técnicas físicas con las terapias basadas en láser a la cabeza podrían abrir un nuevo horizonte en el manejo de esta entidad. La presente revisión tratará de aportar algo de luz en esta dermatosis que continua teniendo tantas sombras recogiendo y ordenando la evidencia científica disponible en la actualidad y proponiendo un algoritmo de manejo diagnóstico-terapeútico que trate de servir de apoyo al clínico que se enfrenta a esta patología.
Abstract
Exogenous ochronosis represents an uncommon pigmentary dermatosis. Historically linked to the use of hydroquinone and other topical phenolic derivatives. Although it was described more than a century ago, its pathophysiology has not been accurately elucidated until very recently. It poses a major challenge both for clinicians—due to the difficulty of its diagnostic and therapeutic approach given the scarce scientific evidence—and for regulatory authorities, owing to the indiscriminate use of depigmenting agents, often in unregulated settings. Nevertheless, recent advances in the understanding of the underlying pathophysiological mechanisms of this disease, in the role of dermoscopy in establishing the diagnosis, and in the emergence of physical techniques—led by laser-based therapies—may open a new horizon in the management of this entity. The present review aims to shed some light on this dermatosis, which continues to have many uncertainties, by compiling and organizing the scientific evidence currently available and proposing a diagnostic-therapeutic management algorithm intended to support clinicians facing this condition.
Palabras clave: Ocronosis exógena; Tirosinasa; Hidroquinona; Dermatoscopia; Láser.
Keywords: Exogenous ochronosis; Hydroquinone; Tyrosinase; Dermoscopy; Laser therapy.
INTRODUCCIÓN
El término ocronosis procede del vocablo latino ochre y fue introducido por el célebre patólogo prusiano Rudolph Virchow en 1865 para describir la tonalidad amarillento-parduzca observada en los depósitos pigmentarios hallados en un paciente afecto de ocronosis endógena, enfermedad también conocida como alcaptonuria (1). Esta enfermedad metabólica de origen hereditario, con un patrón de transmisión autosómico recesivo, se origina por la falta o disminución de la enzima ácido homogentísico oxidasa, encargada de degradar los aminoácidos tirosina y fenilalanina. Como consecuencia, se acumula ácido homogentísico en el organismo, lo que provoca la típica pigmentación azul oscura de los tejidos cartilaginosos y del tejido conjuntivo así como el resto de manifestaciones sistémicas (2).
Con posterioridad, y tomando como referencia la pigmentación anómala descrita por Virchow, se reconoció una forma adquirida u ocronosis exógena, consecuencia de la exposición prolongada a determinados compuestos fenólicos tópicos. Esta variante fue descrita por primera vez a comienzos del siglo XX por el patólogo alemán Ludwig Pick, quien observó un cuadro cutáneo similar tras la exposición a fenol. Décadas más tarde, otro hallazgo decisivo llegó con los trabajos de Findlay y De Beer (1975), que establecieron de manera inequívoca la relación entre el uso crónico de hidroquinona tópica y la aparición de esta patología (3,4).
Existen por tanto dos formas de ocronosis bien diferenciadas: 1) La endógena o alcaptonuria, de caracter genético y con afectación sistémica; 2) La exógena, de carácter adquirido y circunscrita a la piel, provocada por la acumulación dérmica de pigmentos ocronóticos tras el uso prolongado de derivados fenólicos —entre ellos la hidroquinona— como agentes despigmentantes.
Esta última constituye el objeto de la presente revisión. Aunque inicialmente considerada una curiosidad clínica limitada a pacientes de piel oscura en África y Sudamérica, en la actualidad se reconoce su aparición en individuos de distintos fototipos y procedencias, impulsada por el uso global de cosméticos blanqueadores. Su importancia radica no sólo en el impacto estético y psicológico que produce, sino también en las dificultades diagnósticas y terapéuticas que plantea, siendo con frecuencia confundida con el empeoramiento de la hiperpigmentación subyacente (3).
Dado el relativo desconocimiento de esta entidad y el aparente aumento de su incidencia, se realizó una revisión de la literatura utilizando como término principal de búsqueda exogenous ochronosis. La búsqueda se llevó a cabo en las bases de datos PubMed y Cochrane Library, incluyendo todos los estudios disponibles hasta la fecha.
ETIOLOGÍA Y PATOGÉNESIS
Aunque esta enfermedad se ha descrito con la exposición prolongada a multitud de compuestos fenólicos como el resorcinol o el ácido pícrico, siendo el más íntimamente relacionado por mucho la hidroquinona. La hipótesis vigente hasta este mismo año es la postulada por Penneys en 1985 que describía a la ocronosis exógena como una enfermedad causada por la inhibición de la ácido homogentísico oxidasa producida por la hidroquinona tras fotooxidarse, causando una acumulación de ácido homogentísico que posteriormente se polimeriza formando los acúmulos clásicos de pigmento ocronótico en la dermis (5).
Recientemente, Ito et al. han propuesto un auténtico cambio de paradigma a partir de un estudio traslacional. Demuestran que la homogentisato dioxigenasa (HGD) ni siquiera se expresa en la piel humana. Su expresión es fundamentalmente hepática, donde detoxifica el ácido homogentísico, por lo que es improbable que la hidroquinona tópica alcance el hígado en cantidades suficientes para inhibirla y, además, la afinidad de la hidroquinona por la HGD es baja. En conjunto, todo ello hace poco verosímil que la inhibición de HGD sea el mecanismo causal de la ocronosis exógena. En su lugar, plantean que la tirosinasa oxida la hidroquinona lo cual, tras distintas cascadas químicas, genera hidroquinona-eumelanina (HQ-EM) e hidroquinona-feomelanina (HQ-PM) entre otros productos. Al acumularse en los melanosomas, estos compuestos provocan una reducción tóxica de la actividad del melanocito (de ahí el efecto despigmentante de la hidroquinona), y no una inhibición directa de la tirosinasa, como se había postulado. Parte de los metabolitos de bajo peso molecular, sin embargo, escapan del melanosoma y, en lugar de migrar hacia las porciones superiores de epidermis, se filtran a la dermis, donde se unen a fibras de colágeno fotodañadas, formando las partículas ocronóticas características, lo cual explica que esta enfermedad se produzca casi exclusivamente en areas fotoexpuestas (6).
EPIDEMIOLOGÍA
La evidencia más reciente sintetizada por Ishack y Lipner sitúa a la ocronosis exógena asociada a hidroquinona como una entidad que predomina en la mediana edad y muestra una ligera preponderancia del sexo femenino. La susceptibilidad por fototipo es clara: la enfermedad aparece con mayor frecuencia en fototipos altos, resulta extraordinariamente infrecuente en pacientes de fototipo II y no se han publicado casos en fototipo I. En cuanto a la distribución étnica, la población negra es, con diferencia, la más afectada; le siguen las poblaciones asiáticas, mientras que en personas blancas los casos son excepcionales (3). Un segundo eje epidemiológico clave es la exposición acumulada a hidroquinona, tanto en concentración del producto como en duración del uso. La revisión de Ishack y Lipner identifica una correlación positiva entre concentraciones superiores al 4% y el desarrollo de la enfermedad, así como entre exposición prolongada y aparición de lesiones. De hecho, en la mayoría de los casos descritos la hidroquinona superaba el 4% y la duración de uso fue igual o superior a 4–5 años. No obstante, los autores señalan que existen casos con concentraciones ≤4% y exposiciones más breves, lo que sugiere que, aunque dosis y tiempo actúan como potentes moduladores del riesgo, no son los únicos determinantes (3).
En ausencia de estudios con inferencia estadística formal de la incidencia en la población, los datos históricos aportan aproximaciones poblacionales útiles. En una serie sudafricana de 5.128 usuarios de cremas con hidroquinona tópica no regulada durante un año, se observó que el 7,7% desarrolló ocronosis exógena, una cifra que ilustra la magnitud del problema cuando existe acceso y uso prolongado sin supervisión (7).
De forma concordante, el estudio clásico de Findlay et al. que sentó las bases de la asociación entre hidroquinona y ocronosis exógena documentó que el 11% de los pacientes desarrolló la enfermedad tras el uso de hidroquinona al 6–8% durante periodos de hasta ocho años (8).
Finalmente, conviene subrayar el posible subregistro en determinados entornos. Qorbani et al. destacan que, en Estados Unidos, solo se publicaron 39 casos de ocronosis exógena entre 1983 y 2020, pese a la amplia difusión de tratamientos despigmentantes (9).
CLÍNICA
La ocronosis exógena suele manifestarse como máculas o pápulas marrón-grisáceas o negro-azuladas en áreas fotoexpuestas, típicamente en personas con antecedente de uso prolongado de cosméticos despigmentantes para melasma. Esta hiperpigmentación, casi siempre asintomática, se localiza sobre prominencias óseas, con predilección por la cara, el cuello, la espalda y las superficies extensoras (4) (Figuras 1 y 2). El principal diagnóstico diferencial clínico de la ocronosis exógena es, paradójicamente, el propio melasma. No obstante, deben considerarse otras causas de hiperpigmentación facial, como el liquen plano pigmentoso, la hiperpigmentación postinflamatoria o la hiperpigmentación secundaria a fármacos como la amiodarona.
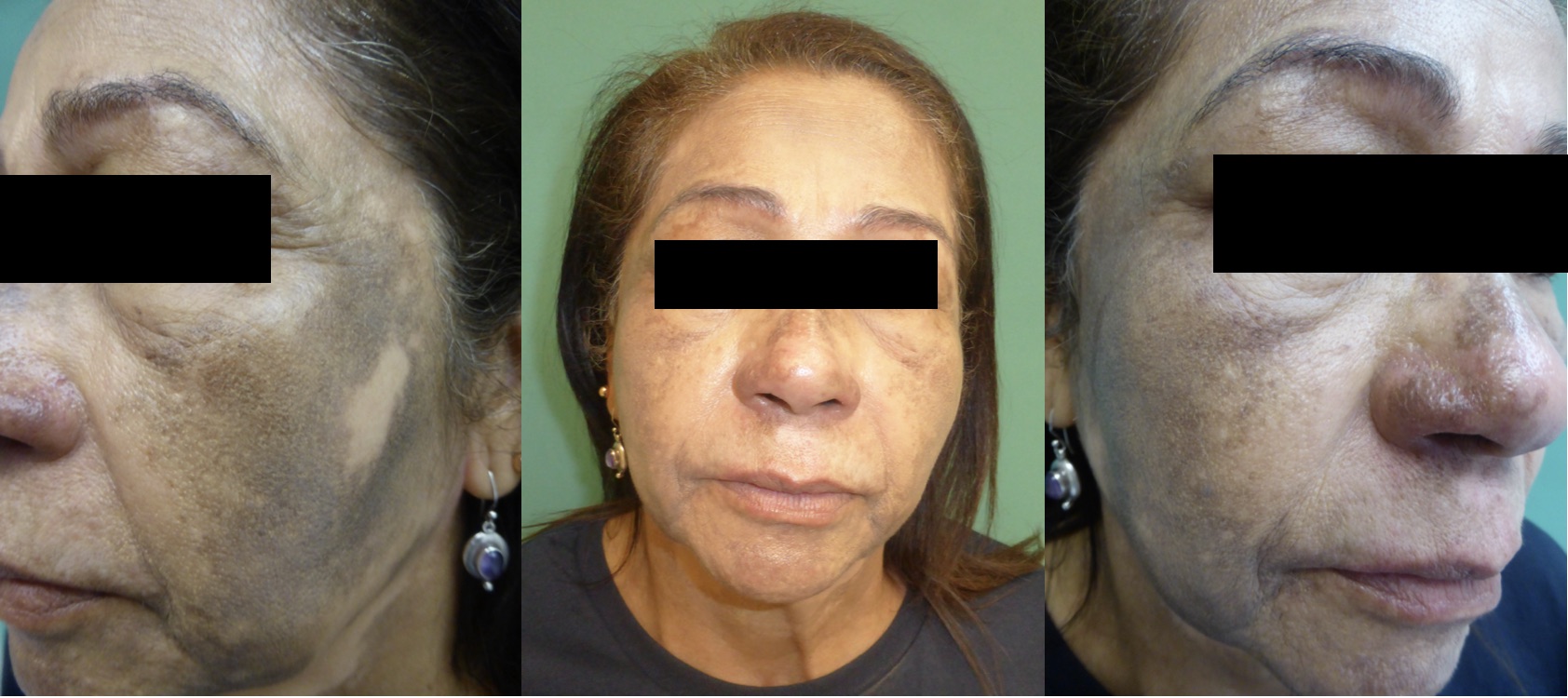
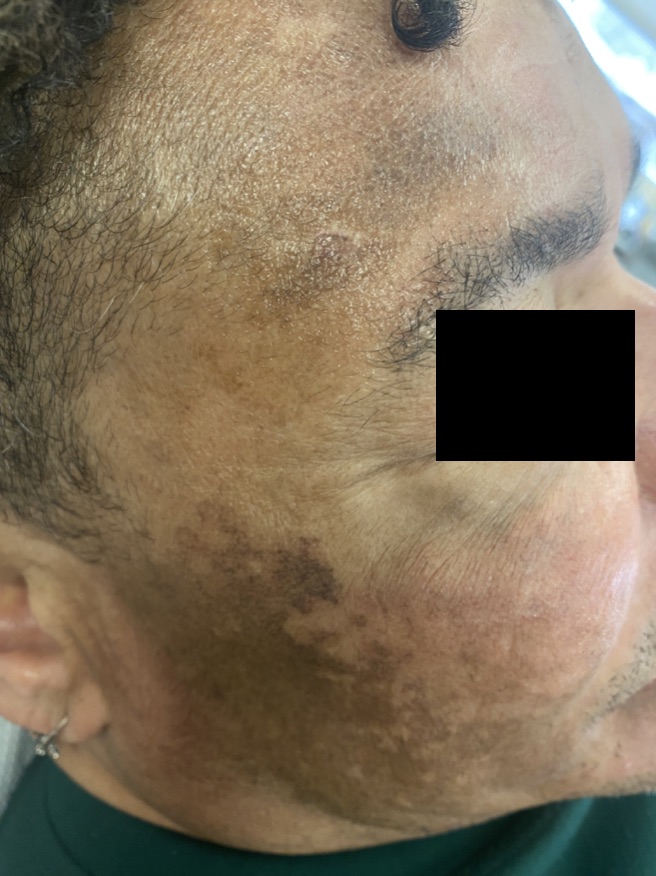
Las lesiones papulo-nodulares típicas fueron descritas por Findlay como “pápulas similares al caviar”. Estas lesiones representan los estadios más graves y avanzados de la enfermedad en los que su diferencia con el melasma es más evidente (8)
Se han propuesto diversas clasificaciones para esta enfermedad, la primera de ellas fue la propuesta en 1979 por Dogliotti y Leibowitz diferenciando tres estadios de la enfermedad (10):
- Estadio I: eritema e hiperpigmentación leve. Es el estadio que supone un mayor reto diagnóstico.
- Estadio II: hiperpigmentación progresiva, millium coloide hiperpigmentado y escasa atrofia.
- Estadio III: Lesiones papulo-nodulares con o sin inflamación circundante.
Destaca también la clasificación propuesta por Hardwick et al en 1989 tras la realización de un estudio epidemiológico con una muestra de 68 pacientes, estableciendo 5 grados consistentes en:
- Grado I: Pigmentación macular tenue con aspecto ahumado.
- Grado II: Moteado macular evidente o presencia de pequeñas pápulas.
- Grado III: Depósitos pigmentarios oscuros y pápulas.
- Grado IV: Millium coloide ( de 1 mm o mayor).
- Grado V: Nódulos o quistes de aspecto queloideo.
En este estudio el grado más frecuente fue el primero, seguido del segundo (11).
DIAGNÓSTICO
En el diagnóstico de esta enfermedad la dermatoscopia ha resultado ser un arma fundamental desde que se publicara el primer estudio al respecto en 2008 (12), permitiendo realizar el diagnóstico de sospecha desde etapas tempranas, lo cual es de capital importancia ya que es fundamental diferenciar precozmente la ocronosis exógena del melasma para evitar el uso de posibles cremas despigmentantes que puedan agravar el cuadro clínico.
Mientras que el melasma presenta un patrón reticulado marrón claro sobre un fondo claro marrón más tenue, la ocronosis exógena presenta un patrón consistente en glóbulos oscuros sobre un fondo marronaceo, que a menudo obliteran los orificios foliculares (4).
Un reciente estudio multicéntrico realizado por Vinay et al mostró que las características dematoscópicas más relevantes por orden de frecuencia eran los siguientes: la obliteración de los orificios foliculares, el punteado pigmentado y las áreas marronaceas amorfas. Los autores recalcan también como hallazgos relevantes las telangiectasias y las estructuras en forma de coma (13) (Figura 3).
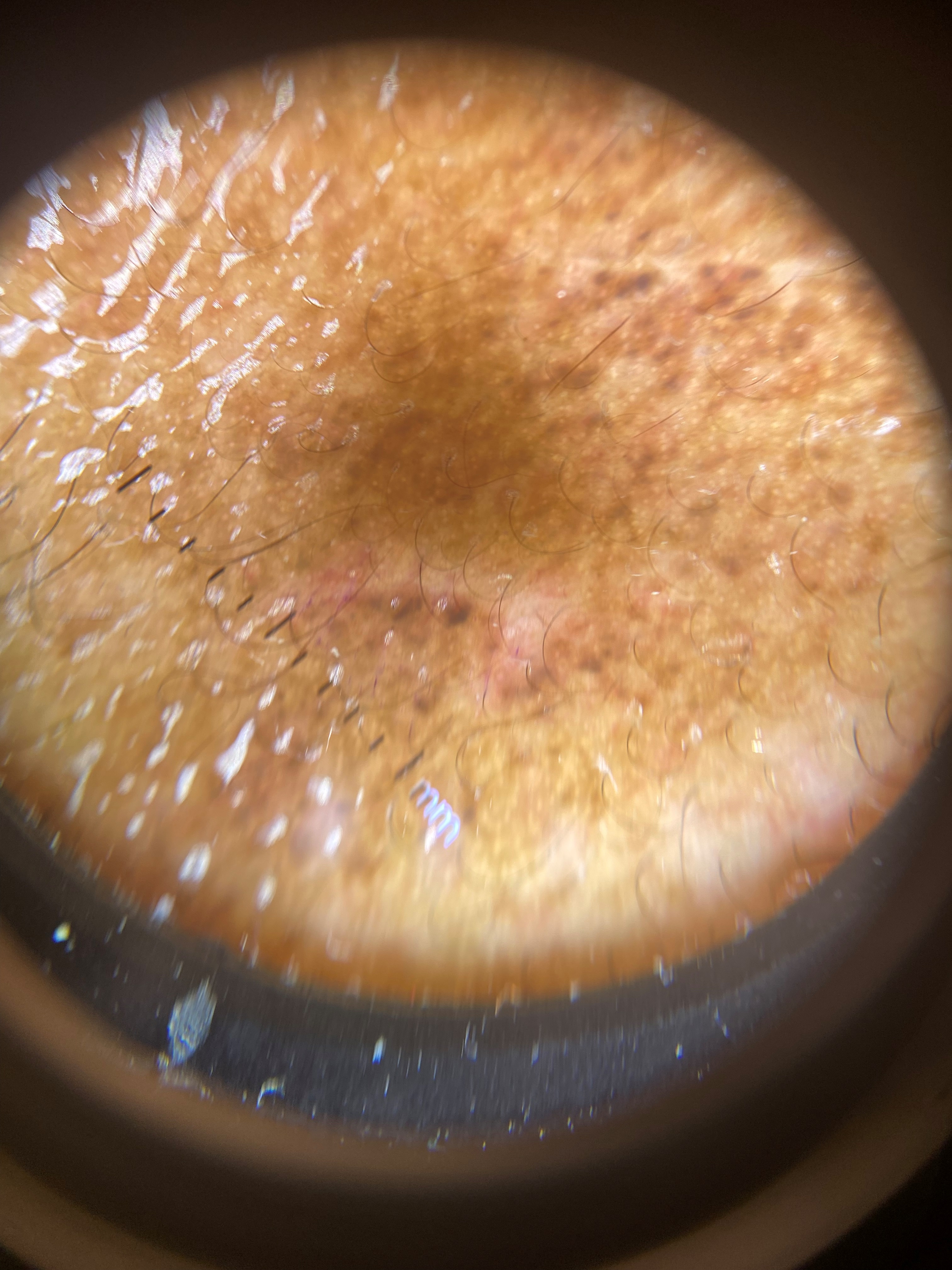
Entre otras técnicas diagnósticas potencialmente útiles podemos encontrar la microcopia confocal de reflectancia, en la cual se pueden observar espacios hiporrefrectivos de forma ovalada o “de plátano” en la dermis, sirviendo así como un reflejo no invasivo de los característicos hallazgos de esta entidad en la histopatología (14).
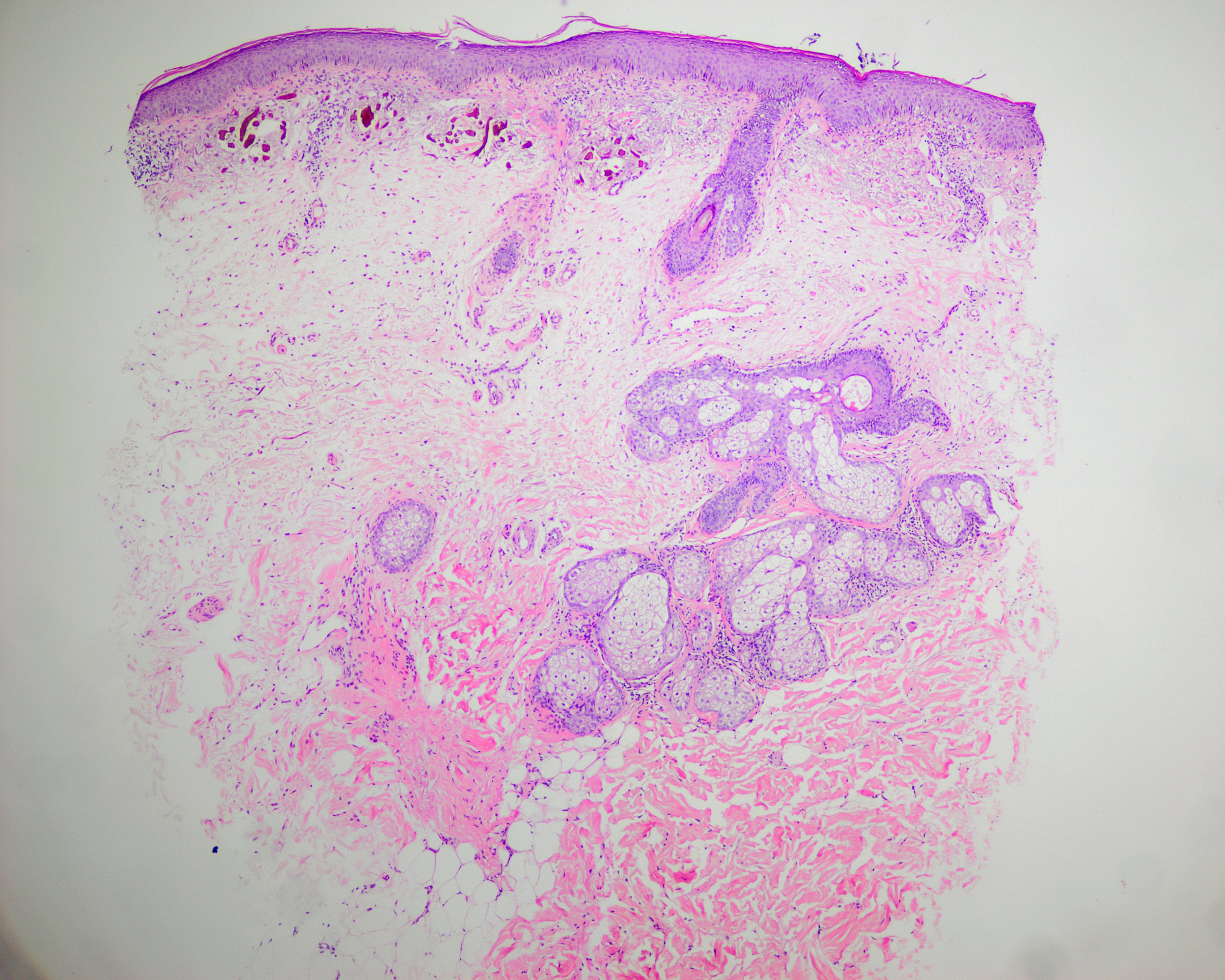
No obstante a pesar de todos estos avances diagnósticos, el gold standard continua siendo la histopatología, con unos hallazgos realmente característicos, que de hecho dieron nombre a la enfermedad, pues lo que se puede observar son fibras de coloración amarillento-marronacea (ocre) con forma de “plátano” en la dermis (Figuras 4 y 5). En estadios más avanzados de la enfermedad estas fibras se degradan y se genera millium coloide, surgiendo a su vez un significativo infiltrado inflamatorio formado por histiocitos, células plasmáticas y células gigantes multinucleadas (4).
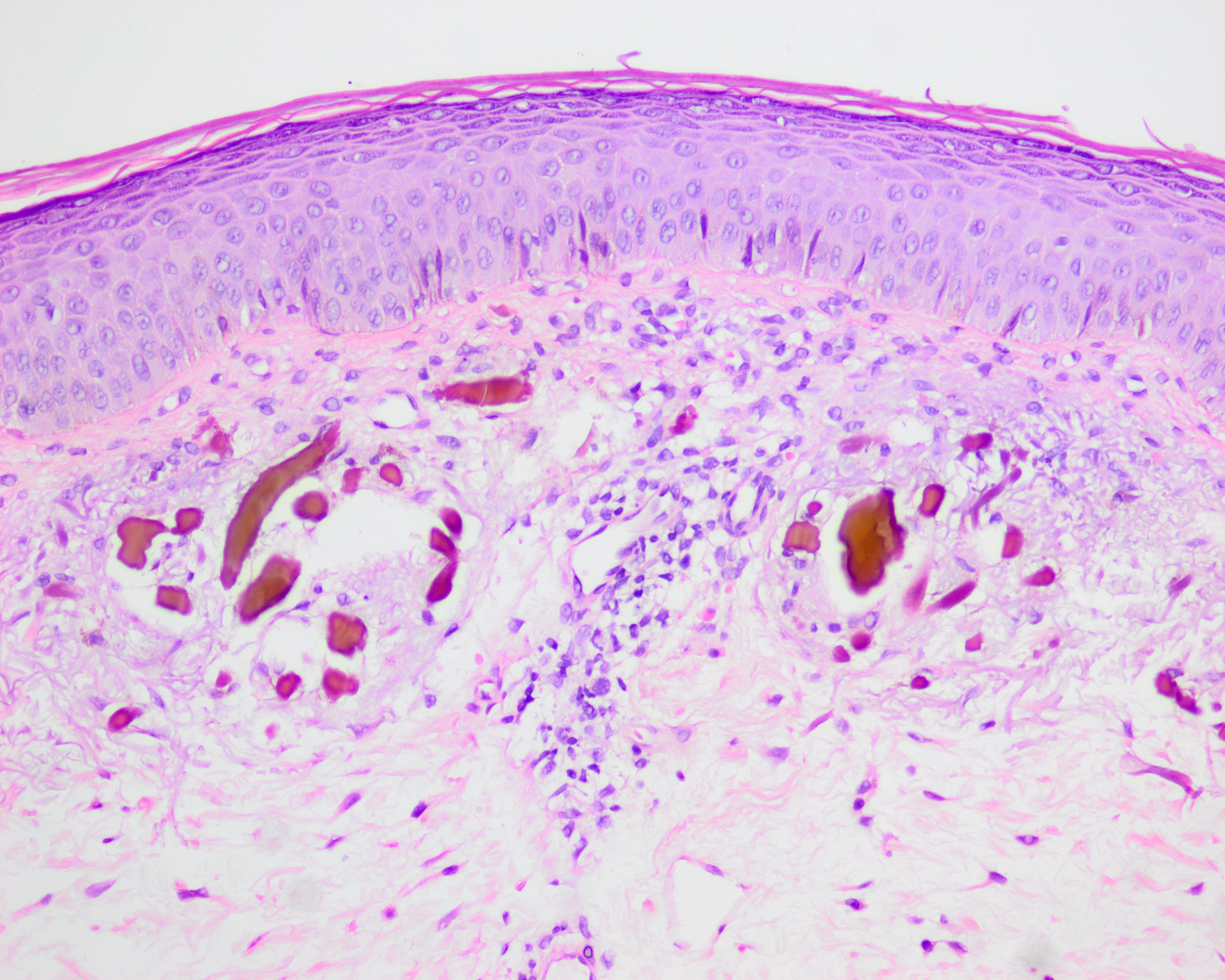
eosina x 4).gena; nótese el punteado pigmentado.
TRATAMIENTO
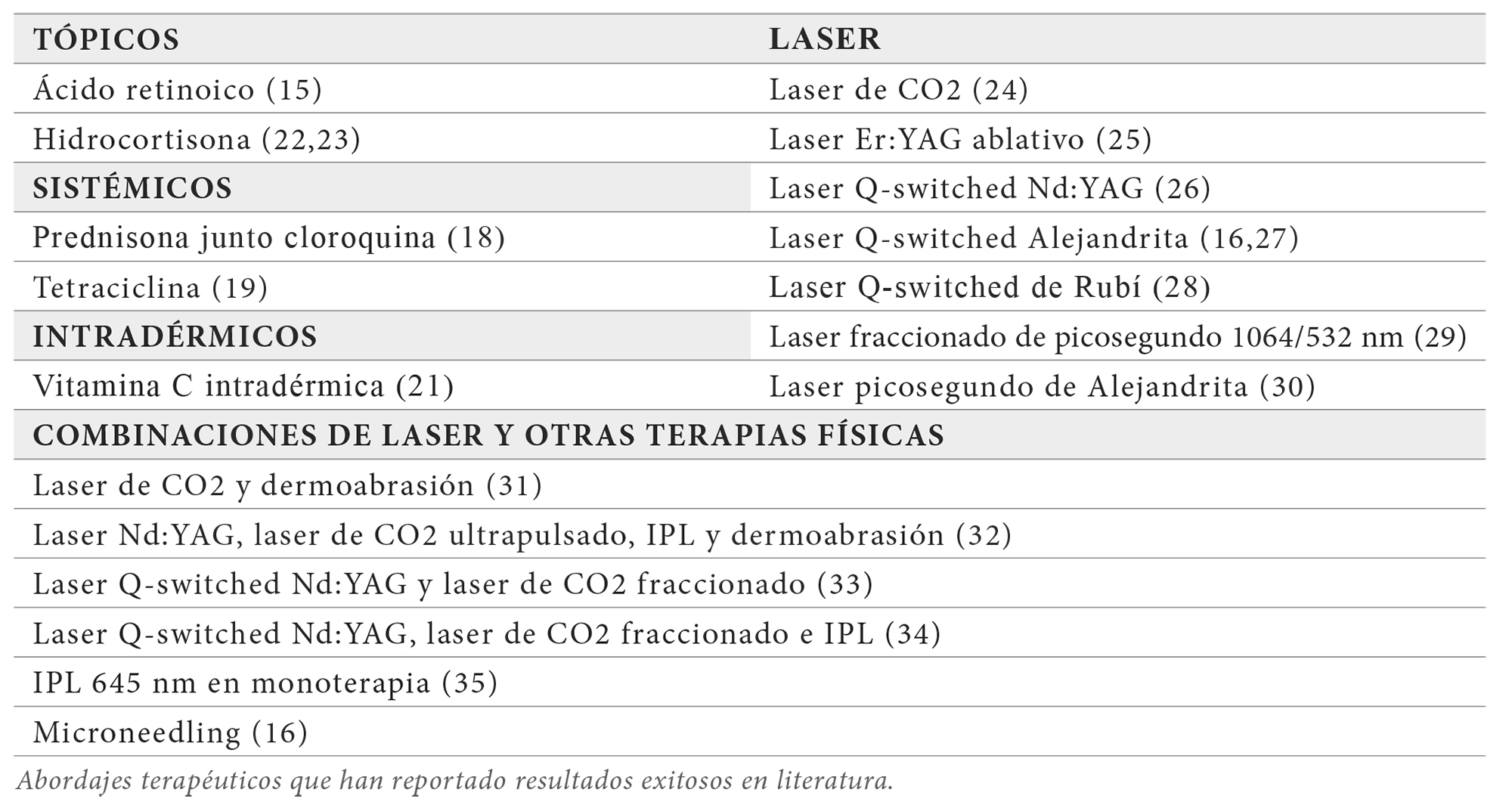
El abordaje terapéutico de la ocronosis exógena continúa siendo un reto clínico significativo. A diferencia de otras discromías, esta entidad presenta a menudo una respuesta pobre e impredecible a los tratamientos convencionales para la hiperpigmentación, lo que obliga a considerar estrategias combinadas, tratamientos físicos avanzados y la prevención como un pilar esencial. La literatura coincide en que ningún tratamiento ofrece resultados universales, pero los avances recientes han ampliado el abanico terapéutico, especialmente en láseres y técnicas mínimamente invasivas. En la tabla 1 se incluyen las opciones terapéuticas empleadas hasta la actualidad.
El primer paso es siempre eliminar el agente causal a la mayor brevedad posible e instaurar medidas de fotoprotección, Esta actuación terapéutica es la única que cuenta con un amplio consenso en la literatura.
Respecto a las terapias tópicas, algunos pequeños estudios publicados en el siglo pasado reportaron mejoría con la aplicación de retinoides tópicos en monoterapia (15). No obstante, la evidencia actual nos lleva a pensar que estos compuestos utilizados de manera tópica constituyen una alternativa poco eficaz en el tratamiento de la ocronosis exógena (16). Los corticoides tópicos han generado resultados controvertidos. Existen estudios que muestran resultados positivos con concentraciones de hidrocortisona al 2,5% (17,18). No obstante, en una de las más grandes y recientes revisiones no se encontró mejoría alguna al aplicar estos compuestos (16). A su vez el ácido tricloroacético tampoco parece tener un papel relevante en la terapéutica de esta enfermedad (19).
Tanto los corticoides como las tetraciclinas por vía sistémica han demostrado beneficios en esta enfermedad. Sin embargo, los estudios publicados son siempre en el contexto de comorbilidad con sarcoidosis sistémica (recordemos que ambas enfermedades pueden asociarse a pacientes de raza negra) lo cual justifica el empleo de actuaciones terapéuticas con mayor perfil de toxicidad como ciclos largos de 30 mg de prednisona que de otro modo no se hubieran planteado como alternativa en la ocronosis exógena (20,21).
Las terapias que sin duda más efectos beneficiosos han demostrado son las físicas y dentro de estas tiene un papel capital el tratamiento con láser. La base de estos tratamientos se debe a que cuando la energía es emitida por el equipo y se genera el pulso, los cuerpos ocronóticos actúan como cromóforos, absorbiendo esta energía lo que lleva a su destrucción y posterior eliminación por parte de las células partícipes de la cascada inflamatoria que se genera inmediatamente después (16, 22-33).
En la tabla 1 podemos observar todos los regímenes de laserterapia que han demostrado efectos beneficiosos incluyendo el láser de CO2, el láser Q-switched de Erb:YAG ( laser de granate de itrio-aluminio dopado con erbio), el láser Q-switched Nd:YAG (laser de granate de itrio-aluminio dopado con neodimio), el láser Q-switched de Alejandrita (es el que con más frecuencia y más amplios estudios tiene publicados), el láser Q-switched de Rubí, el laserterapia fraccionado de picosegundo 1064/532 nm, el láser picosegundo de Alejandrita y combinaciones de los anteriores entre ellos o con otras terapias físicas como la dermoabrasión o la IPL (intense pulse light, luz intensa pulsada). Destacar que esta última ha demostrado también beneficios en solitario.
Cabe mencionar que en 2023 se publicó por primera vez un estudio en el que 3 de 5 pacientes respondían de manera exitosa al tratamiento con Microneedling (16). Esta técnica, surgida en el mundo de la dermocosmética, consiste en crear microlesiones a través de la epidermis hasta llegar a la dermis superficial con pequeñas agujas, lo cual estimula la liberación de factores de crecimiento e induce la producción de colágeno, pudiendo constituir una alternativa barata y con un muy buen perfil de seguridad para el tratamiento de esta enfermedad (34).
Por último, en un estudio reciente, se informa de resultados exitosos empleando como tratamiento vitamina C intradérmica cada 4 semanas consiguiendo a los 3 meses un aclaramiento del 80% de la hiperpigmentación. (35). Sin duda, hacen falta más estudios que validen esta opción terapéutica.
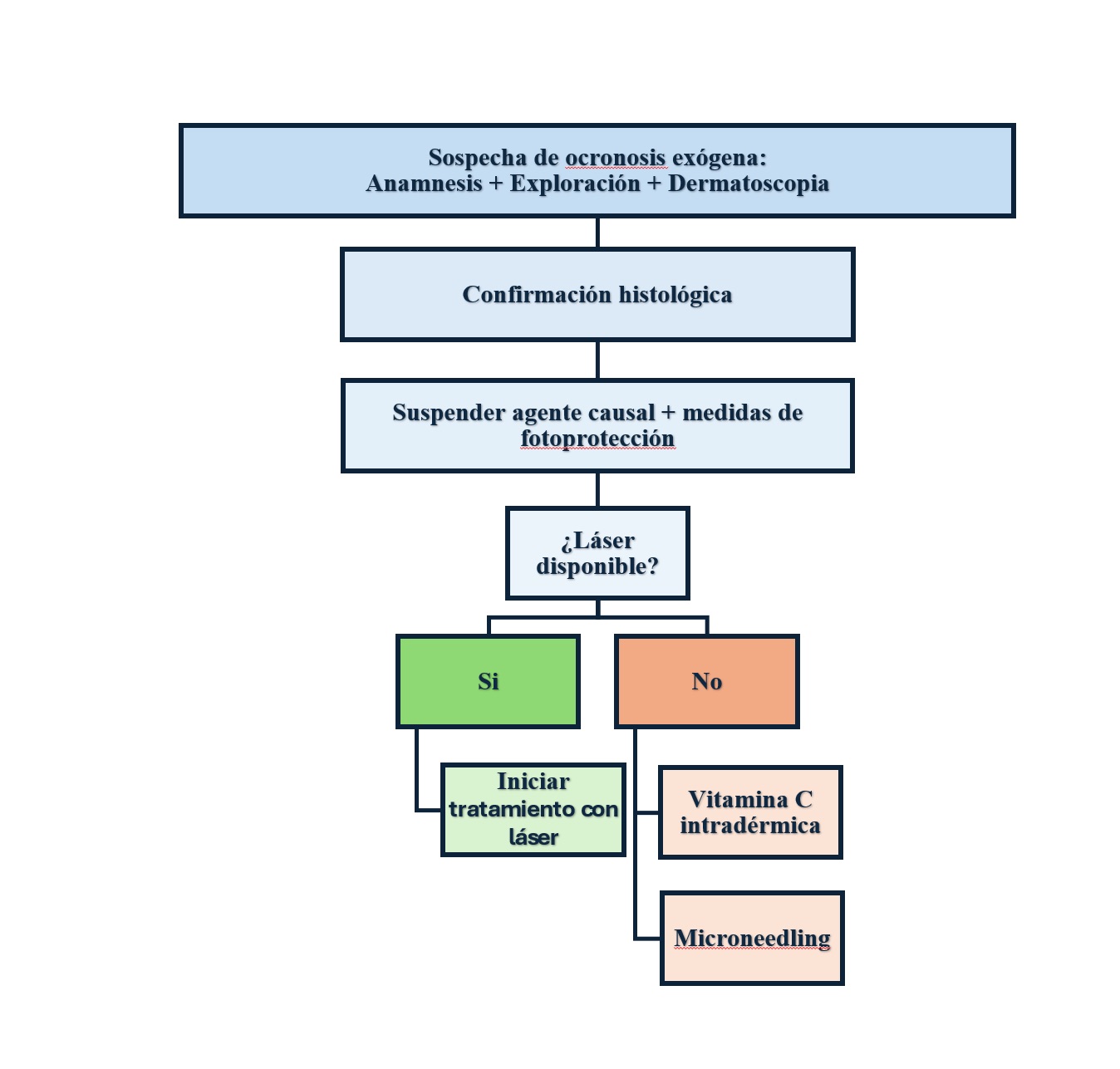
En base a la evidencia actualmente disponible, en la Figura 4 proponemos un algoritmo de manejo para los clínicos que se enfrentan a esta patología (Figura 4).
CONCLUSIÓN
La ocronosis exógena, durante mucho tiempo considerada una rareza clínica, se ha consolidado como un problema emergente en paralelo a la expansión global del uso de agentes despigmentantes tópicos. Su reconocimiento precoz es fundamental, dado que con frecuencia se interpreta erróneamente como una exacerbación del melasma, lo que conduce a intensificar el uso de hidroquinona y, en consecuencia, a precipitar una progresión acelerada de la enfermedad.
En los últimos años, los avances en fisiopatología han permitido reformular por completo el modelo etiopatogénico clásico. La hipótesis tradicional basada en la inhibición cutánea de la homogentisato oxidasa, una enzima cuya expresión está prácticamente restringida al hígado, ha sido desplazada por un paradigma más sólido: la hidroquinona es metabolizada por la tirosinasa generando compuestos que se acumulan en los melanosomas y, posteriormente, difunden hacia la dermis, donde se forman complejos con fibras colágenas fotoalteradas. Este mecanismo explica la pigmentación ocronótica característica y su predilección casi exclusiva por áreas crónicamente fotoexpuestas.
Desde el punto de vista clínico, la enfermedad se manifiesta con un espectro amplio que abarca desde discretas máculas grisáceas hasta pápulas y nódulos hiperpigmentados de mayor entidad. El desarrollo de la dermatoscopia ha supuesto un hito diagnóstico al permitir la identificación de patrones específicos como los glóbulos marrón-negruzcos y la obliteración de orificios foliculares incluso en estadios iniciales. No obstante, la histopatología continúa siendo el patrón de oro, aportando la visualización inequívoca de las clásicas fibras ocronóticas en forma de “cuerpos de banana”.
El abordaje terapéutico sigue siendo especialmente complejo. La suspensión inmediata de la hidroquinona y la instauración de fotoprotección estricta constituyen la base del manejo, si bien rara vez logran una reversión significativa. Las terapias tópicas ofrecen beneficios limitados y los tratamientos sistémicos se reservan para contextos excepcionales. Las modalidades físicas representan el área de mayor progreso: con la terapéutica láser constituyendo el pilar fundamental de los recientes avances y el microneedling y la administración intradérmica de vitamina C constituyendo posibles alternativas de indudable atractivo, aunque la calidad de la evidencia continúa siendo pobre.
En definitiva, la ocronosis exógena constituye una entidad prevenible pero de difícil manejo una vez instaurada. El fortalecimiento de la regulación sobre agentes despigmentantes y la optimización de técnicas diagnósticas y terapéuticas emergentes serán pilares esenciales para mitigar su impacto en los próximos años.
DECLARACIÓN DE TRANSPARENCIA
Los autores/as de este artículo declaran no tener ningún tipo de conflicto de intereses respecto a lo expuesto en el presente trabajo.
BIBLIOGRAFÍA
- ↑Findlay GH. Ochronosis. Clin Dermatol. 1989;7(2):28–35.
- ↑Beddard AP, Plumtre CM. A further note on ochronosis associated with carboluria. Q S Med. 1912;5:505–507.
- ↑Ishack S, Lipner SR. Exogenous ochronosis associated with hydroquinone: a systematic review. Int J Dermatol. 2022;61(6):675-684. doi: 10.1111/ijd.15878.
- ↑Simmons BJ, Griffith RD, Bray FN, Falto-Aizpurua LA, Nouri K. Exogenous ochronosis: a comprehensive review of the diagnosis,epidemiology, causes, and treatments. Am J Clin Dermatol. 2015;16(3):205-212. doi: 10.1007/s40257-015-0126-8.
- ↑Penneys NS. Ochronosislike pigmentation from hydroquinone bleaching creams. Arch Dermatol. 1985;121(10):1239–1240.
- ↑Ito S, Kolbe L, Weets G, Rogers T, et al. Exogenous ochronosis by hydroquinone is not caused by inhibition of homogentisate dioxygenase but potentially by tyrosinase-catalysed metabolism of hydroquinone. Br J Dermatol. 2025;193(5):959-967. doi: 10.1093/bjd/ljaf273.
- ↑Phillips JI, Isaacson C, Carman H. Ochronosis in black South Africans who used skin lighteners. Am J Dermatopathol 1986; 8(1): 14–21.
- ↑Findlay GH, Morrison JGL, Simson LW. Exogenous ochronosisand pigmented colloid milium from hydroquinone bleaching creams. Br J Dermatol 1975; 93(6): 613–622. https://doi.org/10.1111/j.1365-2133.1975.tb05110.x.
- ↑Qorbani A, Mubasher A, Sarantopoulos GP, Nelson S, Fung MA. Exogenous Ochronosis (EO): Skin lightening cream causing rare caviar-like lesion with banana-like pigments; review of literature and histological comparison with endogenous counterpart. Autops Case Rep. 2020;10(4):197. doi:10.4322/acr.2020.197.
- ↑Dogliotti M, Leibowitz M. Granulomatous ochronosis – A cosmetic-induced skin disorder in blacks. S Afr Med J. 1979;56(3):757–760.
- ↑Hardwick N, Van Gelder LW, Van der Merwe CA, Van der Merwe MP. Exogenous ochronosis: An epidemiological study. Br J Dermatol. 1989;120(2):229–238. doi: 10.1111/j.1365-2133.1989.tb07787.x.
- ↑Charlin R, Barcaui CB, Kac BK, Soares DB, Rabello-Fonseca R,Azulay-Abulafia L. Hydroquinone-induced exogenous ochrono-sis: a report of four cases and usefulness of dermoscopy. Int J Dermatol. 2008;47(1):19–23.
- ↑Vinay K, Mehta H, Bhat YJ, et al. Clinical and dermoscopic characteristics of exogenous ochronosis: results of a multicentre study by the International Dermoscopy Society Dermoscopy in Skin of Color Task Force. Clin Exp Dermatol. 2025;50(9):1777-1785. doi: 10.1093/ced/llaf159.
- ↑Gil I, Segura S, Martínez-Escala E, Lloreta J, Puig S, Vélez M, et al. Dermoscopic and reflectance confocal microscopic features of exogenous ochronosis. Arch Dermatol. 2010;146(9):1021–1025. doi: 10.1001 archdermatol.2010.205.
- ↑Camarasa JG, Serra-Baldrich E. Exogenous ochronosis with allergic contact dermatitis from hydroquinone. Contact Dermatitis. 1994;31(1):57-58.
- ↑Lazar M, De La Garza H, Vashi NA. Exogenous Ochronosis: Characterizing a Rare Disorder in Skin of Color. J Clin Med. 2023;12(13):4341. doi: 10.3390/jcm12134341.
- ↑Cullison D, Abele DC, O’Quinn JL. Localized exogenous ochronosis. J Am Acad Dermatol. 1983;8(6):882–889.
- ↑Lawrence N, Bligard CA, Reed R, Perret WJ. Exogenous ochronosis in the United States. J Am Acad Dermatol. 1988;18(5):1207–1211.
- ↑Diven DG, Smith EB, Pupo RA, Lee M. Hydroquinone-induced localized exogenous ochronosis treated with dermabrasion and CO2 laser. J Dermatol Surg Oncol. 1990;16(11):1018–1022.
- ↑Moche MJ, Glassman SJ, Modi D, Grayson W. Cutaneous an-nular sarcoidosis developing on a background of exogenous ochronosis: a report of two cases and review of the literature. Clin Exp Dermatol. 2010;35(4):399–402.
- ↑Fisher AA. Tetracycline treatment for sarcoid-like ochronosis due to hydroquinone. Cutis. 1988;42(1):19–20.
- ↑Carvalho CG, Vilela V, Rocha AE, Carvalho GD, França ER, Rodrigues AG. Exogenous ochronosis treated with CO2 Laser. Surg Cosmet Dermatol. 2016;8 (4):370–372. doi:10.5935/scd1984-8773.201684863.
- ↑Chaptini C, Huilgol SC. Erbium-doped yttrium aluminium garnet ablative laser treatment for endogenous ochronosis. Australas J Dermatol. 2015;56(3):212–214. doi:10.1111/ajd.12199.
- ↑Tan SK. Exogenous ochronosis – successful outcome after treatment with Q-switched Nd:YAG laser. J Cosmet Laser Ther. 2013;15(5):274–278. doi:10.3109/14764172.2012.758379.
- ↑Bellew SG, Alster TS. Treatment of exogenous ochronosis with a Q-switched alexandrite (755 nm) laser. Dermatol Surg. 2004;30(4):555–558. doi:10.1111/j.1524-4725.2004.30177.x.
- ↑Kramer KE, Lopez A, Stefanato CM, Phillips TJ. Exogenous ochronosis. J Am Acad Dermatol. 2000;42(5):869–871. doi:10.1016/s0190-9622(00)90257-3.
- ↑Méndez Baca I, Al-Niaimi F, Colina C, Anuzita A. A case of ochronosis successfully treated with the picosecond laser. J Cosmet Dermatol. 2019;18(5):1322–1325. doi:10.1111/jocd.12834.
- ↑Almutairi R, Usmani S, Mubarak S, Aldaraji W. Novel picosecond 755 nm alexandrite laser for treating exogenous ochronosis. Int J Dermatol. 2024;63(12):455–456. doi:10.1111/ijd.17290.
- ↑Diven DG, Smith EB, Pupo RA, Lee M. Hydroquinone-induced localized exogenous ochronosis treated with dermabrasion and CO2 laser.J Dermatol Surg Oncol. 1990;16(11):1018–1022. doi:10.1111/j.1524-4725.1990.tb00326.x.
- ↑França ER, Paiva V, Toscano LPN, Nunes GJB, Rodrigues TFA. Exogenous ochronosis: a case report. Surg Cosmet Dermatol. 2010;2 (4):319–321.
- ↑Kanechorn-Na-Ayuthaya P, Niumphradit N, Aunhachoke K, Nakakes A, Sittiwangkul R, Srisuttiyakorn C. Effect of combination of 1064 nmQ-switched Nd:YAG and fractional carbon dioxide lasers for treating exogenous ochronosis. J Cosmet Laser Ther. 2013;15(1):42–45. doi:10.3109/ 14764172.2012.748198.
- ↑Ceglio WW, Careta MF, Patriota R, Torezan LA. Exogenous ochronosis successfully treated with the combination of intense pulsed light and fractional CO(2) laser. An Bras Dermatol. 2023;98(1):138–140. doi:10.1016/j.abd.2021.08.013.
- ↑Lee MD, Weiss E. Treatment of exogenous ochronosis with advanced fluorescence technology. Dermatol Surg. 2014;40(9):1046–1048. doi:10.1097/01.DSS.0000452636.14458.ed.
- ↑Hou A, Cohen B, Haimovic A, Elbuluk N. Microneedling: A Comprehensive Review. Dermatol Surg. 2017;43(3):321-339. doi: 10.1097/DSS.0000000000000924.
- ↑Rajesh Gulwani P, Parekh AR, Shah HA. Intradermal vitamin C: A new paradigm in the treatment of exogenous ochronosis. Indian J Dermatol Venereol Leprol. 2024 Mar 14:1-3. doi: 10.25259/IJDVL_890_2023.
Andrés Arteaga-Trincado
Servicio de Dermatología del Hospital Universitario de La Princesa
C/ Diego de León, 62 · 28006, Madrid, España.
Tlf.: +34 628 239 804 | E-Mail: a.arteaga.tr@gmail.com
Enviado: 22.12.25
Revisado: 28.12.25
Aceptado: 08.01.26


