Resumen
La evidencia científica acumulada en las últimas décadas ha mostrado el importante papel de la dieta en la prevención de diversas patologías de relevancia creciente, como son las enfermedades cardiovasculares y la diabetes tipo 2. Los polifenoles, una amplia familia de compuestos presentes en los alimentos de origen vegetal, han mostrado en estudios mecanísticos, preclínicos, clínicos y observacionales un gran potencial en la prevención y/o modulación de diversas alteraciones cardiometabólicas. No obstante, todavía quedan múltiples aspectos en este terreno por elucidar, como la explicación de variaciones interindividuales en la respuesta a estos compuestos. Igualmente, una fracción de polifenoles de la dieta, los denominados no extraíbles o antioxidantes macromoleculares (de alto peso molecular o asociados a macromoléculas como la fibra) ha sido hasta el momento mucho menos considerada en los estudios sobre el tema, a pesar de que han presentado resultados prometedores. Este artículo presenta diversos trabajos recientes en relación al efecto de los polifenoles en salud, abordando tres aspectos clave: a) la determinación de ingestas de los mismos, como paso necesario para poder establecer asociaciones con salud; b) el estudio del metabolismo de los polifenoles, ya que son los metabolitos derivados de la extensa transformación que sufren estos compuestos los que finalmente pueden ejercer actividades biológicas sistémicas; c) el potencial de estos compuestos en el manejo de distintos parámetros de riesgo cardiometabólico. Globalmente, el desarrollo de los estudios sobre los polifenoles de la dieta (a través de una aproximación integral que incluya las fracciones extraíble y no extraíble) debería permitir establecer, tras la superación de las limitaciones existentes, recomendaciones de salud pública sobre la ingesta recomendada de polifenoles, que puedan trasladarse al conjunto de la población o a grupos poblacionales específicos.
Abstract
Accumulated scientific evidence has shown the important role of diet in the prevention of various pathologies of increasing relevance, such as cardiovascular disease and type 2 diabetes. Polyphenols, a large family of compounds present in plant-based foods, have shown in mechanistic, preclinical, clinical and observational studies a relevant potential in the prevention and/or modulation of several cardiometabolic alterations. However, there are still multiple aspects in this area to be elucidated, such as the explanation of interindividual variations in the response to these compounds. Similarly, a fraction of polyphenols in the diet, the so-called non-extractable or macromolecular antioxidants (of high molecular weight or associated with macromolecules such as dietary fiber) has so far been much less considered in studies on the subject, despite they have produced promising results. This article presents several recent studies on the health effects of polyphenols, addressing three key aspects: (a) estimation of dietary intakes, as a previous step in order to establish potential associations with health outcomes; b) the study of the metabolic fate of polyphenols, since metabolites derived from extensive transformation after intake are the compounds that can ultimately exert systemic biological activities; c) the potential of these compounds in the management of different cardiometabolic risk parameters. Overall, the development of studies on dietary polyphenols (through a comprehensive approach including extractable and non-extractable fractions) should allow, after overcoming existing constraints, the establishment of dietary recommendations on polyphenol intake, either for general population or for specific population groups.
Palabras clave: Polifenoles; Dieta; Metabolismo; Microbiota; Enfermedades cardiometabolicas.
Keywords: Polyphenols; Diet; Metabolism; Microbiota; Cardiometabolic diseases.
INTRODUCCIÓN
En las sociedades actuales, con una alta prevalencia de enfermedades no transmisibles, resulta cada vez más relevante tener en cuenta la importancia de la nutrición para un estado óptimo de salud. Así, hoy se sabe que la alimentación, junto con otros aspectos del estilo de vida, son responsables de hasta el 90% de los casos de diabetes tipo 2, el 70% de los de enfermedades cardiovasculares y el 30% de los de cáncer (1-3). Por lo que se refiere específicamente a la dieta, un estudio reciente realizado con datos de casi doscientos países ha estimado en diez millones las muertes producidas en el año 2017 atribuibles a una alimentación inadecuada; por ejemplo, el bajo consumo de frutas era responsable de unos dos millones de muertes en ese año, mientras que el de cereales integrales dio lugar a tres millones de muertes (4). Por otro lado, en el contexto actual en el que la preocupación por la salud forma parte también de la preocupación más amplia por el medio ambiente, resulta relevante indicar que se ha observado que las dietas más saludables son además las dietas más sostenibles: un trabajo reciente evaluó, a través de distintos parámetros, el impacto ecológico del cultivo de diferentes categorías de alimentos, concluyendo que la producción de aquellos alimentos con mejores beneficios para la salud es además la que resulta menos dañina para el medio ambiente (5).
Respecto a los componentes de los alimentos responsables de estos efectos en salud, tradicionalmente se han estudiado los macro- y micronutrientes. No obstante, en las últimas décadas las investigaciones en nutrición se han volcado en los denominados compuestos bioactivos, esto es, compuestos que no son imprescindibles para la salud pero que presentan efectos beneficiosos cuando son consumidos como parte habitual de la dieta. A modo de ejemplo, algunos compuestos bioactivos son los los carotenoides, los fitoesteroles, los glucosinolatos (todos ellos en alimentos de origen vegetal) o los ácidos grasos omega-3 de origen marino.
POLIFENOLES DE LA DIETA
Sin duda, la categoría de compuestos bioactivos más estudiada es la de los polifenoles. Estos compuestos son un amplio grupo de sustancias que consumimos habitualmente e incluyen varios miles de estructuras en el reino vegetal. Se caracterizan por poseer al menos un anillo benzénico al que se encuentra asociado al menos un grupo hidroxilo. A partir de este esqueleto común se generan una gran cantidad de estructuras divididas principalmente en cuatro grandes familias: flavonoides (incluyen flavanoles, flavonas, flavonoles, antocianinas e isoflavonas), ácidos fenólicos (divididos en ácidos hidroxibenzoicos e hidroxicinámicos), estilbenos y lignanos. Adicionalmente, otros compuestos fenólicos no entran en ninguna de las categorías anteriores, como pueden ser los alcoholes fenólicos. La Tabla 1 muestra algunas estructuras representativas de las distintas clases de polifenoles. Cabe destacar que estos compuestos se encuentran ampliamente distribuidos entre todas las categorías de alimentos de origen vegetal (frutas, verduras, legumbres, frutos secos, cereales), en productos derivados (vino, cerveza) y en algunos alimentos específicos (cacao, café, té y la mayoría de las especias).

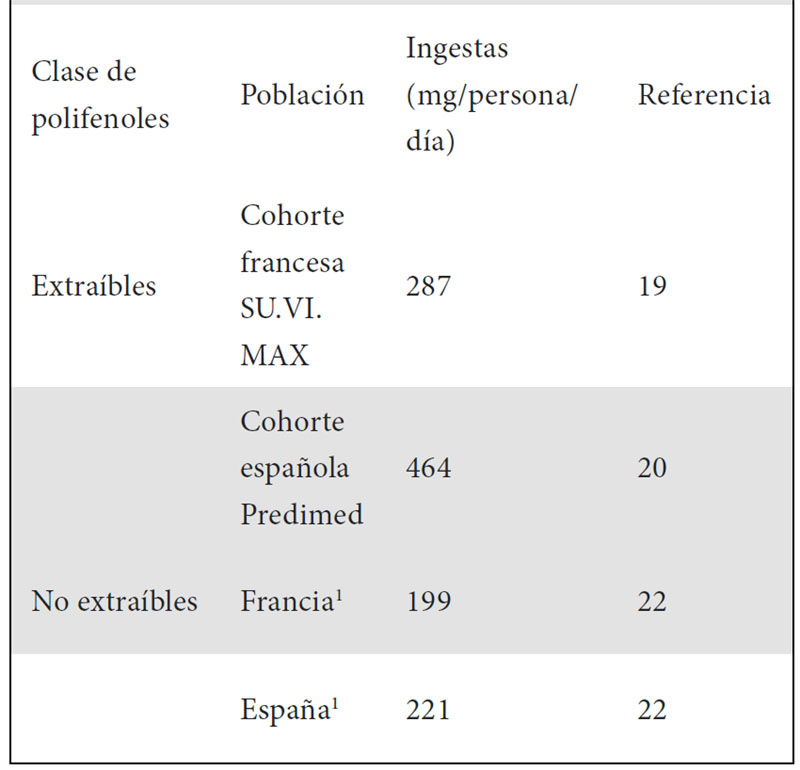
1 Datos de consumo de alimentos procedentes de encuestas nacionales
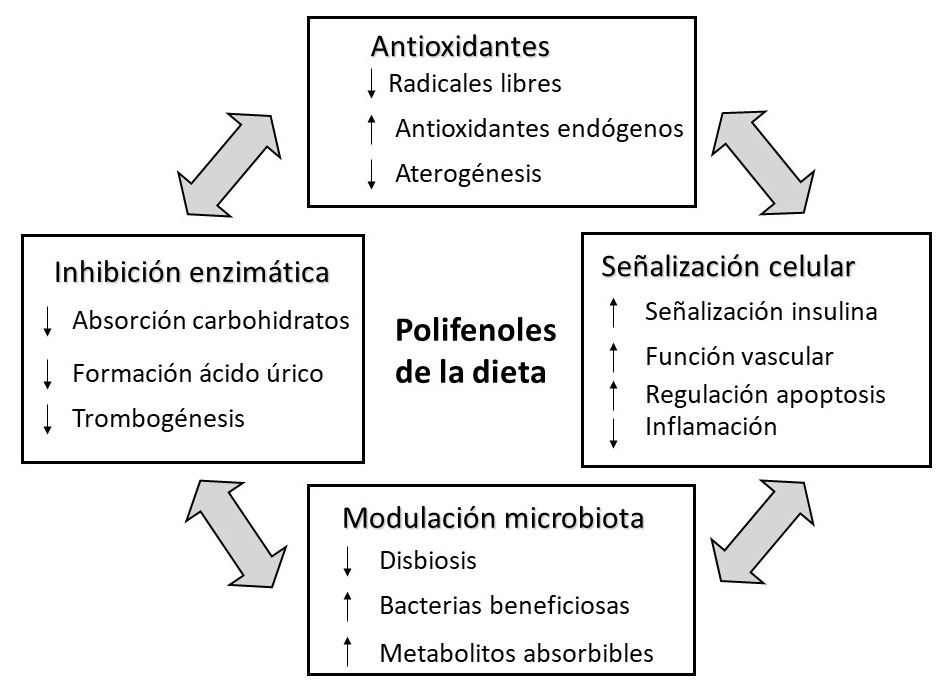
La investigación acumulada sobre los polifenoles ha permitido mostrar diversos mecanismos por los cuales estos compuestos pueden tener un efecto beneficioso en salud (Figura 2). Tradicionalmente estas sustancias se han estudiado por su carácter antioxidante. En este sentido, cabe destacar que son capaces tanto de rebajar los niveles de radicales libres, principalmente en el tubo digestivo a través de los compuestos intactos (posteriormente se abordará la extensa metabolización que sufren los polifenoles), como de estimular los sistemas endógenos de defensa antioxidante, y también de reducir los niveles de LDLs oxidadas, disminuyendo por tanto el riesgo de ateroma. No obstante, los polifenoles presentan también otros mecanismos de acción. Así, son capaces de modular a la microbiota colónica en distintos sentidos: reducen la disbiosis, aumentan la población de especies bacterianas beneficiosas, y la transformación de estos compuestos por la microbiota da lugar a metabolitos absorbibles y beneficiosos, como se discutirá más adelante. Un tercer mecanismo de acción de los polifenoles tiene que ver con su capacidad para inhibir distintas enzimas, lo que da lugar a efectos en la reducción de la absorción de carbohidratos (inhibiendo enzimas del tubo digestivo), en la formación de ácido úrico (a través de la inhibición de la xantina oxidorreductasa) y de la trombogéneis (mediante el bloqueo de enzimas como el tromboxano A2, TXA2, la ciclooxigenasa, COX y la lipooxigenasa, LPO). Finalmente, los polifenoles son capaces de actuar sobre distintas vías de señalización celular afectando a factores de transcripción. Así, se ha descrito que estos compuestos estimulan la vía de señalización de la insulina, mejoran la función vascular, tienen un efecto antiinflamatorio (a través del bloqueo de la vía NFκB), son capaces de modular la respuesta apoptótica (en unas circunstancias incrementándola y en otras disminuyéndola) y mejoran la función vascular (mediante un aumento en los niveles de óxido nítrico, derivado de un incremento en la transcripción de la óxido nítrico sintasa endotelial, eNOS, y de la inhibición de la óxido nítrico sintasa inducible, iNOS) (6-11). Cabe destacar que estos mecanismos de acción se han comprobado en ensayos preclínicos o clínicos según el caso, que han dado lugar a resultados acordes con los observado en estudios epidemiológicos. Por todo ello, en la actualidad existe una evidencia científica acumulada sobre el papel de estos compuestos en la reducción del riego de enfermedades cardiovasculares y diabetes tipo 2 (12-13) y, en menor medida, de ciertos tipos de cáncer y enfermedades neurodegenerativas (14-15).
No obstante, a pesar del conocimiento acumulado sobre los polifenoles, gran parte de los estudios realizados sobre los mismos han sido parciales, puesto que no ha considerado la totalidad de estos compuestos. En concreto, para realizar estudios con polifenoles se lleva a cabo una extracción acuoso-orgánica a partir de los alimentos, asumiéndose que, al igual que ocurre con otros componentes alimentarios, una vez optimizados los solventes necesarios para la extracción de los compuestos, todos ellos se encontrarán en el sobrenadante derivado de dicha extracción. Sin embargo, lo cierto es que en los residuos de estas extracciones permanecen una parte de polifenoles de la dieta, los denominados polifenoles no extraíbles o NEPP (mientras que en el sobrenadante se encontrarían los polifenoles extraíbles o EPP). Desde el punto de vista químico, los NEPP son, o bien estructuras poliméricas, o bien estructuras de bajo peso molecular que se encuentran asociadas a distintas macromoléculas de los alimentos, tales como la proteína y de la fibra (16). Los NEPP reciben también el nombre de polifenoles macromoleculares ya que son o estructuras poliméricas macromoleculares per se o estructuras que se encuentran asociadas a otros compuestos macromoleculares. Esta clasificación, que puede resultar excesivamente conceptual o química, tiene una elevada relevancia nutricional ya que al consumir un alimento se están incluyendo todas las fracciones de polifenoles (los EPP y los NEPP). De hecho, en alimentos comunes tales como el plátano o la judía pinta, el contenido en NEPP es muy superior al de EPP (17).
Por tanto, es necesaria una aproximación integral a los polifenoles de la dieta, considerando tanto los EPP como los NEPP. En los últimos años se han venido realizando un cierto número de investigaciones sobre los posibles efectos cardiometabólicos de los NEPP. No obstante, estos estudios deben completarse con trabajos sobre el metabolismo de los polifenoles como un aspecto imprescindible para que puedan ejercer sus efectos en salud. Así mismo, resulta relevante aumentar el conocimiento sobre las ingestas de polifenoles en distintas poblaciones, para poder establecer posibles asociaciones con el estado de salud. Estos aspectos serán abordados en los siguientes epígrafes.
INGESTAS DE POLIFENOLES
La evaluación de la ingesta de polifenoles en una dieta es una tarea ardua, debido a múltiples razones. En primer lugar, al construir las tablas de referencia de contenido en los alimentos, no se trata de determinar un único compuesto sino varios cientos de estructuras diferentes. Además, su contenido se puede evaluar empleando distintos métodos de análisis que dan lugar a diferentes resultados, sin que exista hasta el momento un método oficial para realizar esta determinación. Al mismo tiempo, se deben tener en cuenta las diferencias existentes entre las distintas variedades de un mismo alimento; el contenido de antocianinas (una clase de polifenoles) no es el mismo en la piel de una manzana roja que en la de una amarilla. Finalmente, nos encontramos con que las informaciones sobre el contenido de polifenoles en alimentos se encuentran distribuidas en centenares de artículos de la bibliografía científica.
Por esta razón, hace unos años se planteó desarrollar una base de datos de contenido de polifenoles en alimentos, Phenol-Explorer (www.phenol-explorer.eu), actualmente disponible como una herramienta abierta online (18). El disponer de esta base de datos -aunque centrada en EPP- ha permitido avanzar en gran medida en el conocimiento de la ingesta de estos compuestos en distintas poblaciones. Así, en el año 2011 fue posible determinar en la cohorte francesa SU.VI.MAX (Supplementation en vitamins et mineraux antioxydants), formada por varios miles de sujetos, la ingesta total de más de trescientos polifenoles individuales, mientras que estudios anteriores no habían incluido más de cincuenta polifenoles (19). Esta aproximación se ha empleado después en otras cohortes, siendo posible estimar las ingestas de polifenoles en el estudio español Predimed o en una cohorte brasileña de personas ancianas (20, 21). Resulta destacable que, si bien las ingestas totales de polifenoles en todas estas poblaciones han estado en un rango parecido (entre 800 a 1200 mg/persona/día como valor medio), las características dietéticas de cada lugar contribuyen con alimentos específicos a la ingesta de polifenoles. Así, en España destacan la contribución de la aceituna y el aceite de oliva, mientras que en Brasil lo hace el frijol y en Francia la endivia. De manera que se puede afirmar que existen múltiples combinaciones posibles de alimentos con las que se puede alcanzar una elevada ingesta de polifenoles. Estos resultados han permitido llevar a cabo asociaciones entre dieta y salud, determinando por ejemplo en la cohorte Predimed que una mayor ingesta de polifenoles se asociaba con un menor riesgo de mortalidad. En estudios posteriores en otras cohortes se han obtenido resultados especialmente relevantes. En concreto, recientemente se ha descrito en una amplia cohorte danesa (de más de 50.000 sujetos) que las ingestas totales de flavanoides se asociaban inversamente con el riesgo de mortalidad total, cardiovascular o por cáncer (14). Este estudio ha obtenido otra conclusión especialmente relevante, como es el hecho de que para ciertas clases de polifenoles (por ejemplo, las flavonas) superar determinados niveles de ingesta resulta negativo y conlleva un aumento en el riesgo de mortalidad. Esto es algo que se había descrito previamente para algunos antioxidantes, como el beta-caroteno, sabiéndose que a altas dosis se transforman en prooxidantes. Sin embargo, este hecho no se había observado para los polifenoles, resultando especialmente relevante en un contexto como el actual donde se tiende a consumir extractos o complementos alimenticios enriquecidos en estos compuestos, sin que el consumidor sea consciente de los riegos que esto puede implicar.
Igualmente se ha determinado la ingesta de NEPP en distintas poblaciones. Por ejemplo, un estudio comparó las ingestas de estos compuestos provenientes de frutas y verduras (al ser los alimentos que más contribuyen a la ingesta de estos) en cuatro países europeos. El resultado fue que las dietas actuales de Francia y Alemania presentan mayor ingesta de esta clase de compuestos frente a las de Holanda y España (22). Los estudios sobre ingesta de NEPP son todavía escasos, pero siguen obteniéndose nuevos resultados, como los descritos recientemente en una población anciana en España (23). A la vista de la importante contribución de los NEPP a la ingesta total de polifenoles (Tabla 1), es necesario continuar ampliando estos trabajos.
METABOLISMO DE POLIFENOLES
Los estudios sobre metabolismo de polifenoles se han centrado en los EPP, sobre los que existe ya un conocimiento muy importante. Brevemente, tras la ingesta de estos compuestos una parte es absorbida en el intestino delgado, pudiendo ser transformados en el enterocito a través de reacciones de fase 1 y fase 2. Posteriormente, los polifenoles pasan al hígado, donde sufren en mayor medida este tipo de reacciones y a continuación son vertidos a la circulación sistémica. Una vez allí, pueden distribuirse en tejidos y circular durante un tiempo hasta pasar finalmente al riñón y ser expulsados en la orina. No obstante, una parte de estos compuestos retorna a través de la circulación enterohepatica al intestino delgado, donde junto con aquellos compuestos que no habían sido absorbidos previamente en esta parte del tubo digestivo, pasarán al colon. Allí, los polifenoles son sujetos a extensas transformaciones por parte de la microbiota. Los metabolitos generados pueden ser absorbidos, siendo transformados minoritariamente en el propio colonocito y en mayor medida en el hígado donde van a pasar a experimentar todo el proceso anteriormente descrito para los polifenoles absorbidos en el intestino delgado. Finalmente, una parte de los polifenoles será sometida a excreción fecal (24).
Por el contrario, el metabolismo de los NEPP ha sido mucho menos estudiado que el de los EPP. En este sentido, cabe plantearse dos preguntas generales: ¿los NEPP generan en su transformación metabolitos diferentes químicamente a los derivados del metabolismo de los EPP? Y, ¿existen diferencias en el proceso general de metabolismo de los NEPP respecto a los EPP?
En relación con la primera pregunta, se ha podido establecer que existen dos vías para el metabolismo de estos compuestos, como refleja la Figura 3 (16). La primera de estas vías estaría relacionada con la liberación de partes de las estructuras de los NEPP sin que haya transformaciones químicas de las mismas. Así, las estructuras poliméricas del tipo proantocianidinas no extraíbles (NEPA) pueden depolimerizarse parcialmente, mientras que los compuestos fenólicos de bajo peso molecular asociados a la fibra pueden ser liberados de la matriz. Estos compuestos posteriormente son absorbidos y pueden sufrir conjugación hepática, dando lugar por ejemplo a formas metiladas de la epicatequina. Esta vía tiene lugar principalmente en el colon, que es el órgano al cual la mayoría de los NEPP llegan intactos, en menor medida en el intestino delgado y una parte muy pequeña en el estómago. Uno de los experimentos que permitió alcanzar estas conclusiones fue un ensayo preclínico con ratas suplementadas con agua, epicatequina libre o NEPA. La epicatequina libre no fue detectada en orina en el grupo control, pero sí en los otros dos grupos, como era esperable. Pero lo más destacable es que en el concentrado de NEPA el contenido en epicatequina libre era de un 0,01%, es decir, diez mil veces menos que en la epicatequina libre. Sin embargo, la señal detectada en el grupo NEPA fue cien veces inferior a la del grupo de epicatequina libre y, por tanto, cien veces superior a lo esperado. Esto indica la depolimerización parcial de los NEPA (25).
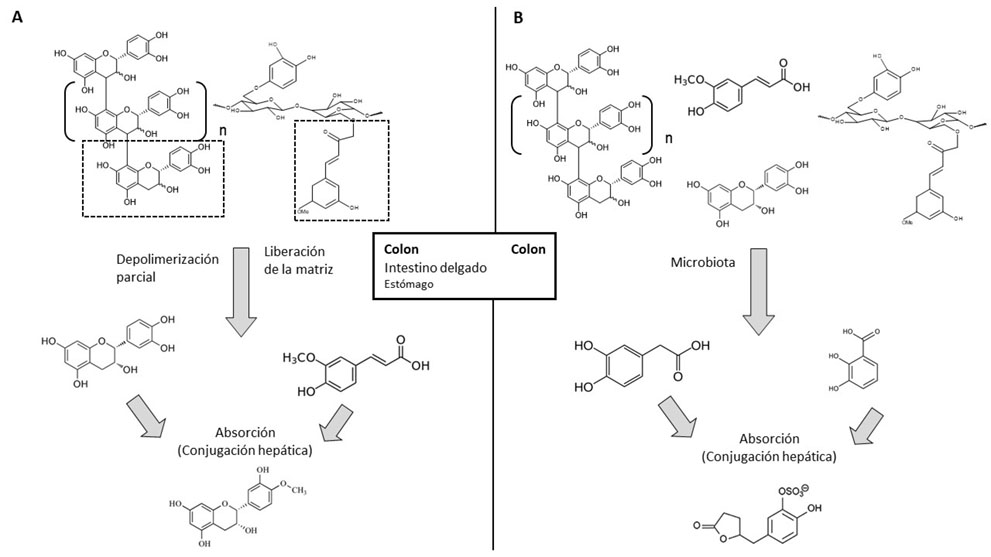
La segunda vía de transformación de los NEPP se produce cuando tanto los compuestos originales intactos como los fragmentos generados en la vía 1 llegan al colon y son sometidos a una extensa transformación por parte de la microbiota, dando lugar principalmente a ácidos fenólicos de bajo peso molecular. Estos metabolitos derivados pueden ser absorbidos y a continuación sufrir reacciones de conjugación hepática, como sería el caso de una forma sulfatada de la dihidroxifenilvalerolactona. Este proceso tiene lugar íntegramente en el colon. A modo de ejemplo, en un estudio preclínico donde las ratas fueron suplementadas con un concentrado de NEPA se detectaron una gran cantidad de metabolitos microbianos en orina en concentraciones al menos diez veces superiores a las del grupo control (26). Cabe destacar que muchos de estos metabolitos han mostrado actividades biológicas en estudios mecanísticos. Así, los ácidos 4- hidroxifenilpropiónico, 3-hidroxifenilacético y 4-hidroxifenilacético han mostrado actividad antiinflamatoria; los ácidos 3,4-dihidroxifenilpropiónico y 3,4-dihidroxibenzoico han dado lugar a efectos en el metabolismo de la insulina; los ácidos 3,4-dihidroxifenilacético y 4-hidroxibenzoico han mostrado capacidad antioxidante y para el ácido ferúlico se ha descrito capacidad para mejorar la función vascular (27-30).
Todos los compuestos detectados, tanto en la vía 1 como en la vía 2 de los NEPP son similares a los derivados de EPP; esto tiene sentido, ya que químicamente los NEPP no son estructuras independientes, sino con diferente tamaño molecular o asociación a la matriz alimentaria respecto a los EPP. Por tanto, respecto a la primera pregunta antes planteada sobre el metabolismo de los NEPP, se puede afirmar que da lugar a estructuras similares a las generadas tras la transformación metabólica de los EPP. Queda plantearse, sin embargo, si habrá diferencias en el proceso de metabolización (etapas, duración, enzimas implicados, etc.) de los NEPP respecto al de los EPP. En este sentido, se han detectado dos diferencias, que se describen a continuación.
La primera diferencia se refiere a que los metabolitos de los NEPP presentan tiempo de absorción retardados respecto al de los derivados de los EPP. Así, en un estudio clínico en adultos sanos se realizó una suplementación con quince gramos de fibra antioxidante de uva (producto derivado de la uva rico en NEPP), a la vez que en paralelo se seguía a un grupo control no suplementado. Entre el momento basal y las veinticuatro horas después de la ingesta (periodo en el que se fueron administrando comidas sin polifenoles) se fue evaluando la capacidad antioxidante plasmática por el método FRAP (ferric reducing/antioxidant power assay) como marcador indirecto de la biodisponibilidad de polifenoles. El grupo suplementado mostró un máximo de capacidad antioxidante a las ocho horas de la suplementación. Esto contrasta con el hecho conocido de que los EPP presentan un máximo de absorción entre treinta y sesenta minutos después de la ingesta, mostrando además en muchos casos un segundo pico inferior en torno a ocho horas después de la ingesta, derivado de la liberación de metabolitos colónicos. Sin embargo, como se ha indicado, en este ensayo clínico sobre NEPP fue precisamente en este tiempo más prolongado cuando se detectó el pico en la capacidad antioxidante plasmática; por tanto, la ingesta de estos compuestos contribuiría a asegurar durante períodos prolongados una circulación de metabolitos potencialmente beneficiosos (31).
La segunda diferencia entre el metabolismo de los NEPP y el de los EPP se refiere a la asociación de los primeros con la fibra y las sinergias que pueden establecerse entre ambos constituyentes de los alimentos. En un estudio de fermentación in vitro se comparó la formación de metabolitos microbianos de NEPP a partir de dos productos ricos en estos compuestos, uno de ellos con un 15% de fibra y el segundo con un 70% de fibra. Mientras que el primero generó menos de 15 ng metabolitos/g NEPP, el segundo dio lugar a más de 80 ng metabolitos/g NEPP. Se debe señalar que estos metabolitos no se generan por la fermentación de la fibra, por lo que esa mayor formación a mayor cantidad de fibra indica que las bacterias cuyo crecimiento es favorecido por la presencia de la fibra son a la vez bacterias capaces de transformar los NEPP (32). Al mismo tiempo, los NEPP estimulan la fermentación de la fibra (33), tratándose por tanto de una potenciación bidireccional. Un aspecto relevante es que, aunque la fibra dietética lleva siendo estudiada desde hace varias décadas y en ocasiones puede pensarse que ya se sabe todo sobre este componente alimentario, tan solo en los últimos meses se han publicado varios trabajos en revistas biomédicas muy relevantes enfatizando la importancia en salud de este constituyente (4, 34-35).
En resumen, la combinación de estudios preclínicos y clínicos ha mostrado que los NEPP dan lugar a metabolitos con la misma estructura química que los EPP. Sin embargo, presentan respecto a estos últimos una absorción retardada y una sinergia con la fibra dietética.
Aunque el mayor interés en el estudio del metabolismo de los polifenoles está evidentemente relacionado con los efectos en salud humana, recientemente un trabajo ha evaluado los metabolitos derivados de EPP y NEPP en nutrición animal, ya que de la formación de más cantidades de estos compuestos puede esperarse un mayor bienestar para el animal y efectos también en la calidad de la carne obtenida. En este estudio se suplementó a pollos con una dieta estándar, una dieta enriquecida con un 8% de orujo de uva (derivado de la vinificación) que equivaldría a una alta concentración de NEPP, y un 0,1% de extracto de semilla de uva, aportando una gran cantidad de EPP. En ambos grupos se observó un incremento significativo de metabolitos fenólicos respecto al grupo control, mostrando que tanto los EPP como los NEPP son metabolizados en animales de este tipo (36).
Otros aspectos importantes en la investigación actual sobre el metabolismo de los polifenoles y sus implicaciones en salud tienen que ver con la posible interacción con el resto de la dieta, así como con la búsqueda de biomarcadores de ingesta. Por lo que se refiere al primer aspecto, hay que tener en cuenta que los polifenoles no suelen consumirse aislados, sino en el conjunto de una dieta global y en combinación con otros alimentos. Por esta razón, se planteó un ensayo preclínico en el que se evaluaron los efectos de una dieta alta en grasa y azúcar como modelo de una dieta occidentalizada en el metabolismo de los polifenoles, estudiando a cuatro grupos de animales: dieta estándar (STD), dieta alta en grasa y azúcar (HFHS), dieta estándar suplementada con extracto de semilla de uva (STD-GSE) y dieta alta en grasa y azúcar suplementada con extracto de semilla de uva (HFHS-GSE). Lo que se observó al evaluar las principales familias de metabolitos derivados de la fermentación colónica de polifenoles fue que en los grupos STD y HFHS los niveles de estos compuestos eran muy bajos y no se observaban diferencias entre las dietas, como era esperable. En el caso de la dieta STD-GSE se observó un aumento significativo de ácidos fenilvaléricos, fenilpropiónicos, fenilacéticos y cinámicos, igualmente tal y como era esperable. Pero el resultado más destacable es que en el grupo HFHS-GSE hubo un descenso drástico de los metabolitos derivados de polifenoles en comparación con el grupo STD-GSE. Es decir, que existía algo en estos animales que bloqueaba la formación de los metabolitos (37). Dado que se ha descrito que las dietas altas en grasa y azúcares alteran la microbiota colónica, por ejemplo aumentando las proporciones de enterobacterias y de Escherichia coli (38), estas modificaciones en la microbiota podrían estar relacionadas con los efectos observados en el metabolismo, ya que impedirían que se generaran los metabolitos fenólicos. Por tanto, no resultaría útil desde un punto de vista de salud seguir una dieta desequilibrada que puntualmente se enriqueciera con polifenoles, ya que estos no serían metabolizados adecuadamente.
Finalmente, resulta muy relevante la búsqueda de marcadores de ingesta de polifenoles, donde la determinación de metabolitos específicos puede resultar muy útil. En este sentido, cabe destacar que los estudios en nutrición siguen basándose en gran medida en encuestas nutricionales, es decir, valores de ingesta auto reportados por el individuo con todas las limitaciones que esto implica. En la búsqueda de biomarcadores de ingesta validados se ha concluido que diversos metabolitos de polifenoles podrían ser empleados como biomarcadores de ingesta. Sin embargo, en otros existen variaciones interindividuales que no permiten su aplicación a una población general; posteriormente se comentarán estas variaciones interindividuales.
EFECTOS CARDIOMETABÓLICOS DE POLIFENOLES
Finalmente, con relación a los efectos en salud de los polifenoles cabe detenerse específicamente en los NEPP por haber sido mucho menos estudiados, ya que sobre los efectos de los EPP existe una amplia evidencia (12, 13). Los NEPP, tras experimentar el proceso de metabolización anteriormente explicado, pueden dar lugar a dos clases de efectos: locales y sistémicos. Los efectos locales pueden tener lugar en las capas superiores del tubo digestivo, donde pueden ejercer dar su capacidad antioxidante o sus propiedades de inhibición de enzimas digestivas. Posteriormente, en el colon pueden modular la actividad de la microbiota intestinal, regular la integridad de la barrera intestinal o presentar distintos mecanismos con actividad anticancerígena (39-41). No obstante, en el contexto de este artículo resulta pertinente centrarse en los efectos sistémicos de los NEPP.
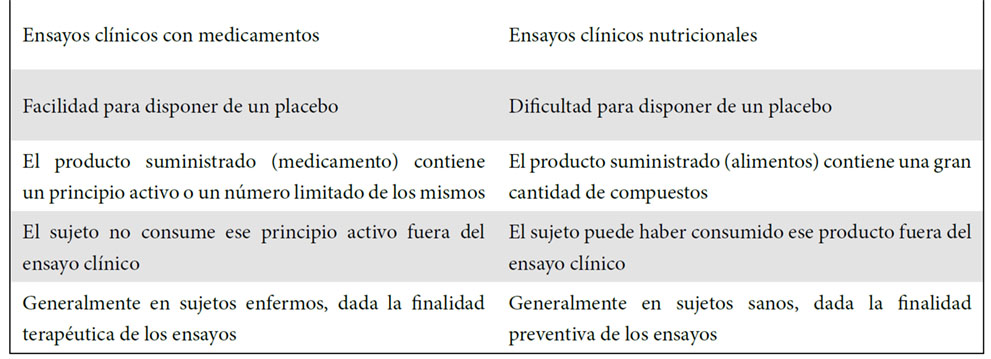
Brevemente, y por situar los estudios que se han realizado sobre los efectos en salud de los NEPP en un contexto más amplio, se debe señar que los ensayos clínicos nutricionales presentan varios aspectos específicos en comparación con los ensayos clínicos con medicamentos. Estas diferencias (ausencia del placebo, diversidad de fuentes del compuesto estudiado, combinación de múltiples compuestos en la matriz, estado de salud de los sujetos, etc.) se muestran en la Tabla 2 y deben ser tenidas en cuenta al ponderar los diseños y resultados de ensayos clínicos nutricionales.
Un producto que ha sido extensamente empleado como caso de estudio en la investigación sobre los efectos en salud de los NEPP es el orujo de uva. Se trata del subproducto obtenido en la elaboración del vino tinto y se caracteriza por un contenido muy elevado en NEPP (superior al 20%) así como por un contenido muy alto en fibra dietética insoluble (superior al 60%); de hecho, gran parte de los NEPP forman parte de esta fibra dietética. En un ensayo clínico llevado a cabo en sujetos normo- e hipercolesterolémicos con objeto de evaluar los efectos cardioprotectores del orujo de uva, los voluntarios fueron repartidos entre un grupo control y un grupo suplementado con 7,5 g/día de este producto durante 6 semanas (42). Tras este periodo, ni en el grupo control ni en los sujetos suplementados normocolesterolémicos se produjeron cambios significativos en parámetros de riego cardiovascular. Mientras que en el grupo suplementado los sujetos hipercolesterolémicos mostraron descensos significativos de colesterol total, colesterol LDL y triglicéridos plasmáticos. Resulta destacable que estas modificaciones se alcanzaron con una cantidad de producto que correspondiente a un enfoque nutricional, es decir, fácilmente incorporable a una dieta habitual como ingrediente en diversos alimentos. En este ensayo se observó también un descenso significativo de la tensión arterial, sistólica y diastólica. Tanto en la modificación lipídica como en la de la tensión arterial, los efectos observados fueron superiores a los descritos previamente para polifenoles y fibra por separado, lo que podría estar asociado a la sinergia que se puede dar entre ambos constituyentes.
Por otro lado, en la evaluación de los efectos potencialmente beneficiosos de los NEPP resulta relevante comparar la contribución específica de estos compuestos frente a la de los EPP. Un ensayo preclínico reciente (43) empleó como modelo la flor de Jamaica (Hibiscus sabdariffa L.), un producto que se usa tradicionalmente en México para preparar infusiones. Los cálices con los que se prepara la infusión tienen un mayor contenido en EPP (1,4%) en comparación con el residuo que queda tras preparar la infusión (0,7%). Por el contrario, este residuo presenta un contenido en NEPP (1,3%) superior al de los cálices (0,7%). Por esta razón, se planteó un estudio con cuatro grupos de animales: dieta estándar (STD), dieta alta en grasa y alta en fructosa (HFHFr), dieta alta en grasa y alta en fructosa enriquecida con cálices de Jamaica (HFHr-CAL) y dieta alta en grasa y alta en fructosa enriquecida con el residuo de la decocción (HFHr-RES). Mientras que la dieta HFHFr-CAL pretendía evaluar los efectos de una suplementación con EPP, la dieta HFHFr-RES pretendía explorar aquellos asociados a una suplementación con NEPP. Ambos componentes dieron lugar a diversos efectos beneficiosos por ejemplo en la glucosa sanguínea, con un descenso significativo de los valores de glucosa alterados por la dieta HFHFr; en concreto, tanto los animales con la dieta HFHFr-CAL como los de la dieta HFHFr-RES volvieron a valores de glucosa similares a los de la dieta STD. Estos resultados muestran el potencial en salud de los NEPP a pesar de ser mucho menos estudiados que los EPP. De hecho, ambas clases de compuestos mostraron también efectos significativamente beneficiosos en relación con otros parámetros como son el peso corporal total, el peso del tejido adiposo mesentérico, la insulina plasmática, los niveles de triglicéridos en plasma y adipocitos (concomitantes con un aumento de estos compuestos en heces) y el tamaño de los adipocitos.
Recientemente, se ha abordado el potencial de los NEPP en la regulación del metabolismo glucídico. Así, se llevó a cabo un ensayo clínico en sujetos que presentaban al menos dos factores del síndrome metabólico (44). En un ensayo aleatorizado y cruzado, un total de 50 sujetos fue dividido en dos grupos que comenzaron el estudio o bien recibiendo el orujo de uva (8 g/día) o bien participando en una fase control (se han comentado ya las dificultades para encontrar placebos adecuados en los ensayos clínicos nutricionales, lo que hace que en ocasiones solo sea posible una fase de control en la que los sujetos no reciben ninguna suplementación, pero al estar expuestos al mismo seguimiento que los sujetos suplementados, pueden llevar a cabo los cambios inconscientes en hábitos de vida que se producen por participar en un ensayo clínico). Tras finalizar esta primera fase de seis semanas de duración, se efectuó un periodo de lavado de cuatro semanas y los sujetos participaron después durante otras seis semanas en la fase de suplementación/control. Al inicio y final de cada una de las etapas se recogieron muestras de sangre, orina y heces. El resultado más relevante de este ensayo fue que la suplementación con orujo de uva a dosis nutricionales produjo un efecto beneficioso en la regulación del metabolismo de la insulina, dando lugar a un descenso significativo en el índice HOMA-IR (homeostatic model assessment for insulin resistance) a la vez que un aumento significativo en el índice QUICKI (quantitative insulin-sensitivity check index). Estos resultados son relevantes teniendo en cuenta que los sujetos participantes en el estudio presentaban varios factores de síndrome metabólico, así como que la resistencia a la acción de la insulina es uno de los parámetros subyacentes en este síndrome. Se han descrito diversos mecanismos por los que los polifenoles regulan el metabolismo de la insulina, tales como un aumento de la captura de glucosa, la modulación de la vía de señalización de la insulina, un aumento de la secreción de GLP-1 (péptido similar al glucagón tipo 1) y de su vida media o el bloqueo de DPP-4 (dipeptidil peptidasa 4) (45). Sin embargo, cabe señalar que en este ensayo cínico (al igual que se ha observado en otros con polifenoles) aproximadamente la mitad de los sujetos respondieron al tratamiento, dando lugar a la mejora en la sensibilidad a la insulina, mientras que la otra mitad eran sujetos no respondedores. Actualmente, uno de los campos en los que se desarrolla la investigación sobre los polifenoles es precisamente intentar averiguar qué factores influyen para que ciertos sujetos respondan o no a la acción de estos compuestos; así, se han podido identificar distintos metabotipos (perfiles de metabolitos circulantes generados tras la ingesta de alimentos ricos en polifenoles) que se asociarían con la capacidad de los polifenoles para generar o no ciertos cambios metabólicos (46).
Finalmente, cabe destacar que otro campo en el que actualmente se vienen desarrollando investigaciones con relación a los efectos de los polifenoles en salud es su posible capacidad para regular las alteraciones generadas en el estado postprandial. Así, se ha descrito que los drásticos aumentos de glicemia y trigliceridemia en sujetos diabéticos constituyen un factor independiente de riesgo cardiovascular (47-48). En la actualidad, diversos ensayos clínicos han evaluado la capacidad de los polifenoles, principalmente los EPP, para regular la glicemia postprandial (49-50) y se están desarrollando diversos ensayos para determinar el posible efecto específico de los NEPP, a través de sus metabolitos de circulación prolongada.
CONCLUSIONES
Como se ha mostrado a lo largo del artículo, existe ya una evidencia científica acumulada en relación con los efectos beneficiosos asociados a la ingesta de polifenoles de la dieta. Sin embargo, existen distintos aspectos todavía abiertos y en los que será necesario profundizar en los próximos años:
– Realizar una aproximación completa a estos compuestos que considere tanto la contribución de los EPP como la de los NEPP, mucho menos estudiados hasta el momento. Especialmente, teniendo en cuenta que se ha demostrado que los NEPP presentan un contenido relevante en alimentos comunes, son metabolizados al menos parcialmente y su ingesta se asocia a la mejora en diversos parámetros de riego cardiometabólico.
– Identificar la microbiota responsable de las transformaciones de los polifenoles. A pesar de que en este campo ha habido avances importantes en los últimos años, pudiendo identificar algunas bacterias responsables de la transformación de polifenoles específicos, en general los conocimientos en este punto siguen siendo muy limitados.
– Desarrollar marcadores de ingesta validados y relativamente sencillos de determinar, preferentemente para las distintas clases de polifenoles o incluso para polifenoles específicos. Aunque ya ha habido avances en este sentido, completar este proceso sería un paso muy importante, permitiendo desarrollar ensayos clínicos mucho más robustos en lo que se refiere a la verificación del cumplimiento de las instrucciones dadas.
– Plantear, siempre que sea posible, un enfoque de dieta global, considerando las interacciones que los polifenoles pueden establecer con otros componentes del mismo alimento y con el conjunto de los alimentos de la dieta.
– Avanzar en el estudio de las diferencias interindividuales que se encuentran en los ensayos clínicos con polifenoles, es decir, entre sujetos respondedores y no respondedores. Para ello, se deben explorar posibles factores subyacentes en los sujetos, tales como la microbiota basal o modificaciones epigenéticas.
– Establecer, tras la superación de todas las limitaciones anteriores, recomendaciones de salud pública sobre la ingesta recomendada de polifenoles, que puedan trasladarse al conjunto de la población o a grupos poblacionales específicos. En definitiva, el objetivo final de las investigaciones sobre polifenoles de la dieta debe ser que estas lleguen a tener una traslación clara a la sociedad.
BIBLIOGRAFÍA
- Hu FB, Manson JE, Stampfer MJ et al. Diet, lifestyle, and the risk of type 2 diabetes mellitus in women. New Engl J Med 2001; 345: 790-797.
- Key TJ, Allen NE, Spencer EA et al. The effect of diet on risk of cancer. Lancet 2002; 360: 861-868.
- Feigin VL, Roth JA, Naghavi M. Global burden of stroke and risk factors in 188 countries, during 1990–2013: a systematic analysis for the Global Burden of Disease Study 2013. Lancet Neurol 2016; 15: 913-924.
- GBD 2017 Diet Collaborators. Health effects of dietary risks in 195 countries, 1990–2017: a systematic analysis for the Global Burden of Disease Study 2017. Lancet 2019; 393: 1958-1972.
- Willett W, Rockström J, Loken B et al. Food in the Anthropocene: the EAT–Lancet Commission on healthy diets from sustainable food systems. Lancet 2019; 393: 447-492.
- McKenzie GG, Delfino JM, Keen CL et al. Dimeric procyanidins are inhibitors of NF-Κb-DNA binding. Biochem Pharmcol 2009; 78(9): 1252-1262.
- Schaffer S, Halliwell B. Do polyphenols enter the brain and does it matter? : some theoretical and practical considerations. Genes Nutr 2012; 7: 99-109.
- Rodríguez-Ramiro I, Ramos S, Bravo L et al. Procyanidin B2 induces Nrf2 translocation and glutathione S-transferase P1 expression via ERKs and p38-MAPK pathways and protect human colonic cells against oxidative stress. Eur J Nutr 2012; 51: 881-892.
- Gobert M, Rémond D, Loonis M et al. Fruits, vegetables and their polyphenols protect dietary lipids from oxidation during gastric digestion. Food Function 2014; 5: 2166-2174.
- Boto-Ordóñez M, Urpi-Sarda M, Queipo-Ortuño MI et al. High levels of Bifidobacteria are associated with increased levels of anthocyanin microbial metabolites: a randomized clinical trial. Food Function 2014; 5: 1932-1938.
- Shi Y, Williamson G. Quercetin lowers plasma uric acid in pre-hyperuricaemic males: a randomised, double-blinded, placebo-controlled, cross-over trial. Br J Nutr 2016; 115: 800-806.
- Serino A, Salazar G. Protective role of polyphenols against vascular inflammation, aging and cardiovascular disease. Nutrients 2019; 11(1): 53.
- Van Dam RM, Naidoo N, Landberg R. Dietary flavonoids and the development of type 2 diabetes and cardiovascular diseases: review of recent findings. Curr Op Lipidol 2013; 24: 25-33.
- Bondonno NP, Dalgaard F, Kyro C et al. Flavonoid intake is associated with lower mortality in the Danish Diet Cancer and Health Cohort. Nat Commun 2019; 10: 3651.
- Squilaro C, Schettino C, Sampaolo S. Adult-onset brain tumors and neurodegeneration: are polyphenols protective?. J Cell Physiol 2018; 233: 3955-3967.
- Pérez-Jiménez J, Díaz-Rubio ME, Saura-Calixto F. Non-extractable polyphenols, a major dietary antioxidant: occurrence, metabolic fate and health effects. Nutr Res Rev 2013; 26: 118-129.
- Pérez-Jiménez J, Arranz S, Saura-Calixto F. Proanthocyanidin content in foods is largely underestimated in the literature data: an approach to quantification of missing proanthocyanidins. Food Res Int 2009; 42: 1381-1388.
- Neveu V, Pérez-Jiménez J, Vos F et al. Phenol-Explorer: an online comprehensive database on polyphenol contents in foods. Database 2010: 1-9.
- Pérez-Jiménez J, Fezeu L, Touvier M et al. Dietary intake of 337 polyphenols in French adults. Am J Clin Nutr 2011; 93: 1220-1228.
- Tresserra-Rimbau A, Medina-Remón, Pérez-Jiménez J et al. Dietary intake and major food sources of polyphenols in a Spanish population at high cardiovascular risk: the PREDIMED study. Nutr Metab Cardiovasc Dis 2013; 23: 953-959.
- Nascimento-Souza A, Gontijo de Paiva P, Pérez-Jiménez J . Estimated dietary intake and major food sources of polyphenols in elderly of Viçosa, Brazil: a population-based study. Eur J Nutr 2018; 57: 617-627.
- Pérez-Jiménez J, Saura-Calixto F. Macromolecular antioxidants or non-extractable polyphenols in fruit and vegetables: intake in four European countries. Food Res Intl 2015; 74: 315-323.
- Goñi I, Hernández-Galiot A. Intake of nutrient and non-nutrient dietary antioxidants: contribution of macromolecular antioxidant polyphenols in an elderly mediterranean population. Nutrients 2019; 11(9): 2165.
- Cardona F, Andrés-Lacueva C, Tulipani S. Benefits of polyphenols on gut microbiota and implications in human health. J Nutr Biochem 2013; 24: 1415-1422.
- Touriño S, Pérez-Jiménez J, Mateos-Martín M.L et al. Metabolites in contact with the rat digestive tract after ingestion of a phenolic-rich dietary fiber matrix. J Agric Food Chem 2011; 59: 5955-5963.
- Mateos-Martín ML, Pérez-Jiménez J, Fuguet E et al. Non-extractable proanthocyanidins from grape are a source of bioavailable (epi)catechin and derived metabolites in rats. Br J Nutr 2012; 108: 290-297.
- Larrosa M, Luceri C, Vivoli E et al. Polyphenol metabolites from colonic microbiota exert anti-inflammatory activity on different inflammation models. Molec Nutr Food Res 2009; 53: 1044-1054.
- Scazzocchio B, Varí R, Filesi C et al. Protocatechuic acid activates key components of insulin signaling pathway mimicking insulin activity. Molec Nutr Food Res 2015; 59: 1472-1481.
- Sánchez-Patán, Chioua M, Garrido I et al. Synthesis, analytical features, and biological relevance of 5-(3′,4′-Dihydroxyphenyl)-γ-valerolactone, a microbial metabolite derived from the catabolism of dietary flavan-3-ols. J Agric Food Chem 2011; 59: 7083-7091.
- Rodríguez-Mateos A, Feliciano RP, Boeres A et al. Cranberry (poly)phenol metabolites correlate with improvements in vascular function: a double-blind, randomized, controlled, dose-response, crossover study. Molec Nutr Food Res 2016; 60: 2130-2140.
- Pérez-Jiménez J, Serrano J, Tabernero M et al. Bioavailability of phenolic antioxidants associated with dietary fiber: plasma antioxidant capacity after acute and long-term intake in humans. Plant Foods Human Nutr 2009; 64: 102-107.
- Saura-Calixto F, Pérez-Jiménez J, Touriño S et al. Proanthocyanidin metabolites associated with dietary fibre from in vitro colonic fermentation and proanthocyanidin metabolites in human plasma. Molec Nutr Food Res 2010; 54: 939-946.
- Grabber JH, Ress D, Ralph J. Identifying new lignin bioengineering targets: impact of epicatechin, quercetin glycoside, and gallate derivatives on the lignification and fermentation of maize cell walls. J Agric Food Chem 2012; 60: 5152-5160.
- Rubin R. High-fiber diet might protect against range of conditions. JAMA 2019; 321: 1653-1655.
- Reynolds A, Mann J, Cummings J et al. Carbohydrate quality and human health: a series of systematic reviews and meta-analyses. Lancet 2019; 393: 434-445.
- Muñoz-González I, Chamorro S, Pérez-Jiménez J et al. Phenolic metabolites in plasma and thigh meat of chickens supplemented with grape byproducts. J Agric Food Chem 2019; 67: 4463-4471.
- Molinar-Toribio E, Fuguet E, Ramos-Romero S et al. A high-fat high-sucrose diet affects the long-term metabolic fate of grape proanthocyanidins in rats. Eur J Nutr 2018; 57: 339-349.
- Ramos-Romero S, Molinar-Toribio E, Gómez L et al. Effect of d-fagomine on excreted enterobacteria and weight gain in rats fed a high-fat high-sucrose diet. Obesity 2014; 22: 976-979.
- Lizárraga D, Vinardell MP, Noé V. A Lyophilized red grape pomace containing proanthocyanidin-rich dietary fiber induces genetic and metabolic alterations in colon mucosa of female C57Bl/6J mice. J Nutr 2011; 141: 1597-1604.
- López-Oliva ME, Pozuelo MJ, Rotger R et al. Grape antioxidant dietary fibre prevents mitochondrial apoptotic pathways by enhancing Bcl-2 and Bcl-xL expression and minimising oxidative stress in rat distal colonic mucosa. Br J Nutr 2013; 109: 4-16.
- Sánchez-Tena S, Lizárraga D, Miranda A et al. Grape antioxidant dietary fiber inhibits intestinal polyposis in ApcMin/+ mice: relation to cell cycle and immune response. Carcinogenesis 2013; 34: 1881-1888.
- Pérez-Jiménez J, Serrano J, Tabernero M et al. Effects of grape antioxidant dietary fiber on cardiovascular disease risk factors. Nutr 2008; 24: 646-653.
- Amaya-Cruz D, Pérez-Ramírez I, Pérez-Jiménez J et al. Comparison of the bioactive potential of Roselle (Hibiscus sabdariffa L.) calyx and its by-product: phenolic characterization by UPLC-QTOF MSE and their anti-obesity effect in vivo. Food Res Int 2019; 126: 108589.
- Martínez-Maqueda D, Zapatera B, Gallego-Narbón A et al. A 6-weeks supplementation with grape pomace to subjects at cardiometabolic risk ameliorates insulin sensitivity, without affecting other metabolic syndrome markers. Food Funct 2018; 9(11): 6010-6019.
- Ávila JAD, García JR, Aguilar GAG et al. The antidiabetic mechanisms of polyphenols related to increased glucagon-like peptide-1 (GLP1) and insulin signaling. Molecules 2017; 22: 903.
- Selma MV, González-Sarrías A, Salas-Salvadó J et al. The gut microbiota metabolism of pomegranate or walnut ellagitannins yields two urolithin-metabotypes that correlate with cardiometabolic risk biomarkers: comparison between normoweight, overweight-obesity and metabolic syndrome. Clin Nutr 2018; 37: 897-905.
- Bansal S, Buring JE, Rifai N et al. Fasting compared with nonfasting triglycerides and risk of cardiovascular events in women. JAMA 2007; 298(3): 309-316.
- Jiang J, Zhao L, Lin L et al. Postprandial blood glucose outweighs fasting blood glucose and HbA1c in screening coronary heart disease. Sci Rep 2017; 7(1): 14212.
- Törrönen R, Sarkkinen E, Niskanen T et al. Postprandial glucose, insulin and glucagon-like peptide 1 responses to sucrose ingested with berries in healthy subjects. Br J Nutr 2012; 107(10): 1445-1451.
- Castro-Acosta MI, Smith L, Miller LJ et al. Drinks containing anthocyanin-rich blackcurrant extract decrease postprandial blood glucose, insulin and incretin concentration. J Nutr Biochem 2016; 38: 154-161.
DECLARACIÓN DE TRANSPARENCIA
La autora de este artículo es co-inventora de la patente WO 2017013299 A1, destinada a la obtención de ingredientes ricos en polifenoles no extraíbles
ranm tv
Jara Pérez JiménezLuís María Gil-Carcedo García
Institute of Food Science, Technology and Nutrition, Spanish Research
Council (ICTAN-CSIC) Jose Antonio Nováis, 10, 28040 Madrid
Tlf.: +34 91 549 23 00 ext. 231223 | jara.perez@ictan.csic.es
Año 2019 · número 136 (03) · páginas 298 a 307
Enviado*: 14.11.19
Revisado: 20.11.19
Aceptado: 26.12.19
* Fecha de lectura en la RANM


