Resumen
La sobrecarga de hierro se observa en pacientes con anemia crónica en los que para mantener su hemoglobina dentro de límites aceptables requieren el aporte periódico de concentrado de hematíes. La sobrecarga de hierro es una inevitable consecuencia del régimen transfusional. El organismo no tiene un mecanismo fisiológico para excretar el hierro y el único mecanismo posible es mediante el tratamiento quelante que capta el hierro y lo elimina por hígado o riñón.
Cuando la transferrina se satura por encima del 70% se genera NTBI (Non Transferrin Bound Iron) y LPI (Labile Plasma Iron). LPI es una fracción muy tóxica que atraviesa las membranas celulares y causa especies reactivas de oxígeno (ROS) con oxidación de proteínas, peroxidación de membranas lipídicas y oxidación del DNA mitocondrial y nuclear. Los órganos mas afectados son hígado (fibrosis y cirrosis hepática), corazón (miocardiopatía) y órganos endocrinos(diabetes, otras lesiones).
Existen 3 quelantes de hierro: deferoxamina (sc/iv), deferiprona y deferasirox (orales). Se comenta su utilización en anemias congénitas (modelo talasemia) y adquiridas (modelo síndromes mielodisplásicos) y su posible utilización pretrasplante en los transplantes de progenitores hematopoyéticos.
Abstract
Iron overload is observed in patients with chronic anemia in which to maintain their hemoglobin within acceptable limits require the periodic supply of packed red blood cells. Iron overload is an inevitable consequence of the transfusion regimen. The organism does not have a physiological mechanism to excrete iron and the only possible mechanism is through the chelating treatment that captures iron and eliminates it by liver or kidney.
When transferrin is saturated above 70%, NTBI (Non Transferrin Bound Iron) and LPI (Labile Plasma Iron) are generated. LPI is a very toxic fraction that crosses the cell membranes and causes reactive oxygen species (ROS) with protein oxidation, peroxidation of lipid membranes and oxidation of mitochondrial and nuclear DNA. The organs most affected are liver (fibrosis and liver cirrhosis), heart (cardiomyopathy) and endocrine organs (diabetes, other injuries).
There are 3 iron chelators: deferoxamine (sc / iv), deferiprone and deferasirox (oral). Its use in congenital anemias (thalassemia model) and acquired anemia (model myelodysplastic syndromes) and its possible pretransplant use in haematopoietic progenitor cell transplants is discussed.
Palabras clave: Sobrecarga de hierro; Resonancia magnética; Hígado y corazón; Quelantes de hierro.
Keywords: Iron Overload; Liver and Cardiac; Magnetic Resonance; Quelation Therapy.
Introducción
El hierro es un mineral esencial para los organismos vivos, que lo requieren para su crecimiento y desarrollo.
Interviene activamente en el funcionamiento de varias proteínas involucradas en la producción de energía oxidativa, la respiración mitocondrial, la biosíntesis de ADN o el transporte de oxígeno.
Al ser un metal indispensable en el metabolismo celular, su absorción, transporte, almacenamiento y liberación, tienen que estar críticamente regulados. (1)
La hepcidina es el elemento clave de la homeostasis del hierro (2). Controla la absorción de este a nivel intestinal y su liberación por parte de los macrófagos. Su disminución condiciona un aumento de la absorción de hierro, con una mayor liberación por parte de los macrófagos y su aumento supone el fenómeno contrario. El gen que codifica la hepcidina es el HAMP (hepcidin antimicrobial peptide) (3), situado en el cromosoma 19. Consta de 3 exones y 2 intrones, y codifica un prepéptido de 24 aminoácidos, que posteriormente se fragmenta en 25 Aa. Puede detectarse tanto en suero como en orina (1, 2, 3).
El hierro plasmático circula unido a la transferrina. Normalmente la capacidad de saturación de transferrina es del 30%. Una saturación de transferrina inferior a 16% indica, en general, anemia ferropénica, mientras que una saturación superior a 50-70% establece el diagnóstico de sobrecarga férrica (4).
El hierro se acumula en los compartimentos de depósito en forma de ferritina y hemosiderina. El hígado es el órgano de depósito fundamental de hierro. La concentración de ferritina sérica, en condiciones normales, es un indicador de los depósitos de hierro. Niveles bajos de ferritina indican depósitos de hierro depleccionados y unos niveles altos, sobrecarga de hierro.
Breve concepto del metabolismo del hierro:
El contenido total de hierro del organismo en individuos sanos es aproximadamente de 2.5-3 g. en mujeres y 3-4 g. en varones, y está distribuido en 2 compartimentos: hierro funcional constituido por la hemoglobina 2g (60-70%), mioglobina-enzimas 0.165 (5.0%) y hierro en depósitos 0.5-1 g (20-30%). Existe además una pequeña cantidad de hierro circulante o de transporte ligado a la transferrina, lo que supone alrededor de 3-4 mg (0.1%). (5)
Absorción de hierro:
El metabolismo de hierro es un circuito cerrado en el que, en condiciones normales, la cantidad de hierro absorbida (1 mg/diario) es igual al que se pierde como consecuencia de la descamación epitelial y la eliminación por el sudor, la orina, las heces o la saliva. La figura primordial de la absorción del hierro y su reciclaje es la hormona hepcidina (3). Juega un papel fundamental en la homeostasis del hierro y en la inflamación (2, 3). Desarrolla su actividad mediante su unión a la ferroportina, que es la proteína exportadora encargada de liberar el hierro (6). La ferroportina está presente en enterocitos, hepatocitos y macrófagos, y es regulada negativamente por la hepcidina. De tal modo que cuando los niveles de hepcidina están aumentados, degrada a la ferroportina y no se produce la liberación de hierro por las células intestinales y los macrófagos (1). Lo contrario sucede cuando los niveles de hepcidina disminuyen, la liberación de hierro por las células intestinales y las células del sistema macrofágico aumenta. (Figura 1)
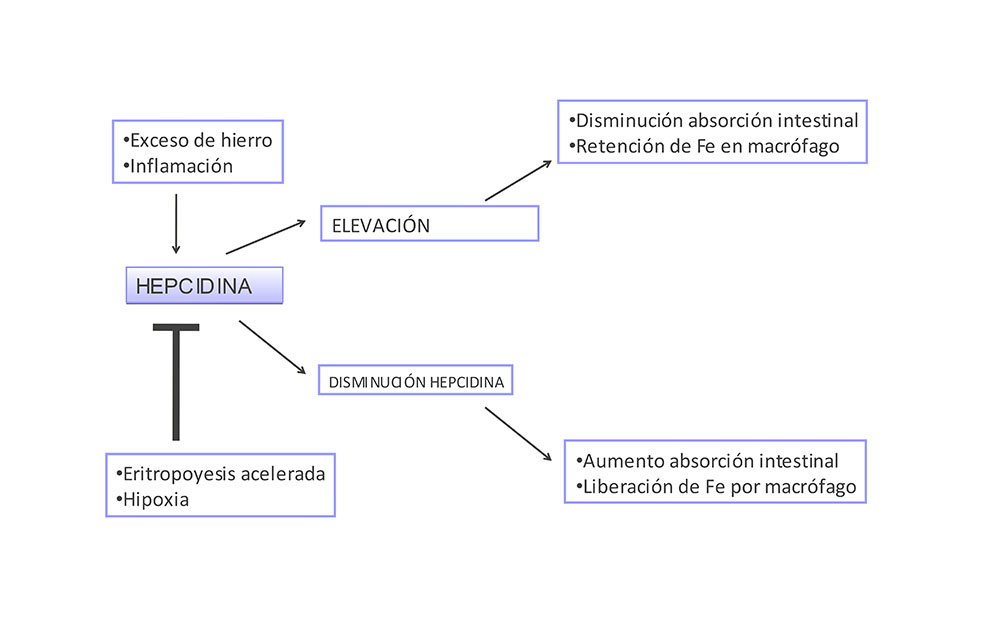
Transporte de hierro en el plasma:
El hierro desde la célula intestinal no puede circular libremente en el plasma, por ser sumamente tóxico, y es captado por la transferrina, proteína también de síntesis hepática, que es capaz de transportar 2 átomos de hierro. Solamente un 30% de las moléculas de transferrina circulantes se encuentran saturadas de hierro (2). A través de la transferrina el hierro se distribuye hacia las células que presentan receptores para la transferrina.
Depósito de hierro:
El hierro circulante en forma de hemoglobina constituye el 70% del total del hierro corporal. El resto se encuentra en los depósitos, siempre unido a proteínas, por su toxicidad. Los depósitos se localizan en las células del parenquima hepático y en el sistema mononuclear fagocítico de hígado, bazo y médula ósea, en forma de dos compuestos ferritina – una apoferritina, proteína de 24 subunidades, sintetizada en el hígado y la hemosiderina, similar a la anterior pero insoluble en agua. Esta última puede ponerse de manifiesto mediante la tinción con azul de Prusia.
La ferritina circula en el plasma, y sus niveles reflejan el estado de reserva de hierro en el organismo. Se encuentra disminuido en la anemia ferropénica, y aumentado en la sobrecarga férrica (7).
Condiciones que demandan la producción de eritrocitos: como hemorragia aguda, hipoxia y altitud, tratamientos con eritropoyetina (EPO) o enfermedades que cursan con eritropoyesis ineficaz, controlan negativamente la transcripción de hepcidina . De ahí nace la idea de la posible existencia de un “factor regulador eritroide” (8), que controlaría directamente la hepcidina. En el año 2014 el grupo de Ganz y colaboradores (9), descubren en modelo murino la eritroferrona (ERFE).
La eritroferrona directamente inhibe la expresión de hepcidina en los hepatocitos, es decir, actúa como un regulador negativo de la hepcidina. También está involucrada en la respuesta de la anemia de la inflamación (10). (Figura 2)
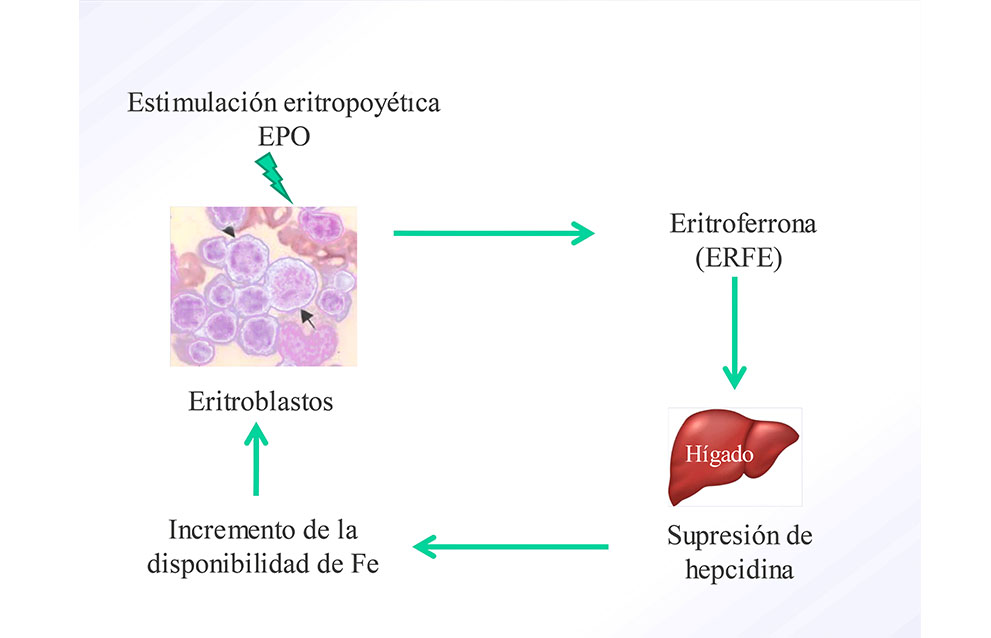
El descubrimiento de la eritroferrona puede ser un camino futuro que permita el desarrollo de nuevas terapias, tanto en la β talasemia como en otras patologías con sobrecarga de hierro.
Sobrecarga de hierro. Daño celular y orgánico:
Como hemos podido observar en el apartado anterior, el organismo humano dispone de métodos eficaces y complejos para la absorción de hierro por el intestino, su transporte, almacenamiento y liberación. Sin embargo, no cuenta con un método fisiológico capaz de eliminar el exceso de hierro acumulado.
Por ello, en determinadas circunstancias, bien por defectos congénitos del metabolismo del hierro, como en el caso de: a) Hemocromatosis hereditarias, en las que debido a un descenso de la síntesis de hepcidina, hay un aumento de absorción de hierro, que no comentaremos en este trabajo, ó b) En pacientes con anemias crónicas, que precisan un régimen transfusional periódico para mantener su hemoglobina, se va a producir sobrecarga de hierro. Además muchos de estos pacientes anémicos con eritropoyesis ineficaz, tienen descenso de hepcidina, aumento de absorción de hierro y sobrecarga de hierro, incluso antes de comenzar las transfusiones (10).
Cada unidad de concentrado de hematíes contiene unos 200-250 mg. de hierro, con lo cual, al cabo de 4 años, un paciente con talasemia mayor puede llegar a recibir un total de 20-25 g. de hierro (100 CH en los 4 años) (11, 12, 13).
A medida que avanza el número de transfusiones, la transferrina se satura de hierro. Con una saturación superior al 60-70% se detecta en el plasma hierro libre no ligado a transferrina (NTBI, non transferrin bound iron), cuya composición química es muy heterogénea, con una fracción tóxica, “lábile plasma iron”, hierro plasmático lábil (LPI), que tiene la particularidad de poder atravesar las membranas celulares, y llegar a células del organismo como miocardiocitos, hepatocitos y células del sistema endocrino. Esta fracción tóxica a través de las reacciones de Fenton o Haber-Weiss, genera radicales hidróxilo con la producción de especies reactivas de oxígeno (ROS), y el consiguiente daño celular y orgánico (14).
Los mecanismos antioxidantes celulares son incapaces de resolver el exceso oxidativo y se produce daño directo sobre el ADN mitocondrial y nuclear, y sobre las membranas lipídicas y las proteínas (14).
En el ADN los radicales hidroxílicos reaccionan específicamente con la desoxirribosa de las bases nitrogenadas purínicas y pirimidínicas generando locus altamente mutagénicos, sugiriendo la asociación de este estrés oxidativo con la inestabilidad genómica y la adquisición de anomalías cromosómicas, roturas y otras lesiones.
Especialmente vulnerable a estas alteraciones es el ADN mitocondrial, debido a que carece de histonas y a que sus sistemas de reparación del ADN son menos eficaces que los sistemas de reparación del ADN nuclear (15,16).
Se ha demostrado la alta correlación entre NTBI-LPI y el aumento de apoptosis. La apoptosis es un evento patogénico relevante, que se observa comúnmente en los precursores hematopoyéticos de los SMD (17), sobretodo en los SMD de bajo riesgo. La sobrecarga férrica también se ha relacionado con la ateroesclerosis, por la oxidación de lipoproteínas de baja densidad (18).
En definitiva, en la sobrecarga de hierro se produce daño celular y tisular que está en relación directa con el incremento de NTBT, y sobretodo con la fracción LPI, que producen especies reactivas de oxígeno con lesión del ADN nuclear y mitocondrial, y peroxidación de membranas lipídicas que afectan a órganos diana (como corazón, hígado, bazo, páncreas, gonadas y otras glándulas endocrinas) (19, 20,21,22).
El hierro se acumula primero en el sistema reticuloendotelial del bazo, de la médula ósea y de las células de Kupffer hepáticas, y ya finalmente cuando la sobrecarga férrica es importante afecta, además del hígado (fibrosis hepática, cirrosis e incluso carcinoma hepatocelular), al resto de los órganos señalados.
Métodos de medida de la sobrecarga férrica:
El tratamiento y manejo de la sobrecarga de hierro requiere una evaluación segura, exacta y reproductible, dado que el objetivo del tratamiento quelante no es hacer desaparecer totalmente los depósitos de hierro, sino conseguir unos niveles de hierro que no sean dañinos para el organismo.
Estos métodos son el índice de saturación de la transferrina, la ferritina, la medida de la concentración hepática de hierro, (LIC, Liver Iron Concentration), mediante biopsia hepática o resonancia magnética, la medida de hierro por RM en otros órganos, y la determinación de NTBI o LPI.
El índice de saturación de la transferrina y la ferritina, se emplean como métodos de escrutinio para detectar sobrecarga férrica.
La ferritina es un método sencillo, muy sensible al diagnóstico y que ha supuesto un pilar fundamental en el tratamiento de los pacientes con talasemia mayor.
Existe correlación entre la ferritina sérica y los depósitos de hierro hepáticos, de tal modo que mediciones seriadas de ferritina son de gran utilidad en la monitorización de la sobrecarga de hierro, y tiene valor pronóstico relevante. Los valores de ferritina <2500 ng/ml se correlacionan en los pacientes talasémicos con una mayor supervivencia libre de enfermedad cardíaca, mientras que valores de ferritina >2500 ng/ml indican incremento de mortalidad por cardiopatía (22).
Sin embargo, puede presentar cierta variabilidad, dado que es un reactante de fase aguda y puede incrementarse como respuesta a infecciones, inflamación, citolisis hepáticas, hemólisis o enfermedades malignas (23). Por ello, se recomienda tambien la medida directa del hierro hepático, dado que el hígado es el órgano de almacenamiento del hierro.
No obstante, en la práctica clínica, las mediciones señaladas de ferritina siguen siendo una herramienta clave en la monitorización sistemática de la sobrecarga férrica (23).
La determinación de la concentración hepática de hierro por biopsia hepática (LIC, Liver iron concentrations), está considerado como el mejor método y patrón estandar de valoración de los depósitos de hierro (19).
Los valores normales de LIC son de 1.2 mg. de hierro por gramo de tejido seco. Valores de 3-7 mg. son indicativos de sobrecarga de hierro leve, >7 mg. de sobrecarga moderada, lo que implica tratamiento quelante de hierro y >15 mg. indican sobrecarga grave con posible afectación cardíaca y muerte por cardiopatía, que requiere tratamiento quelante intensivo.
Sin embargo este método no está exento de ciertos riesgos e inconvenientes, dado que es un método invasivo y puede, en determinadas circunstancias, estar contraindicado. Por otra parte, requiere una muestra de biopsia superior a 1 mg. de tejido hepático, y además en pacientes con fibrosis o cirrosis hepática, puede existir una gran heterogeneidad de los depósitos de unas zonas a otras, con un gran coeficiente de variabilidad.
En el momento actual, la determinación de la concentración hepática de hierro mediante resonancia magnética (RM) ha sustituido a la medida de hierro por biopsia hepática, y es el método estandar de medida de la sobrecarga de hierro (24).
Se ha observado una buena correlación ente la determinación del hierro por biopsia hepática y la concentración hepática de hierro por RM (25).
Al ser una técnica incruenta, puede realizarse el estudio seriado programado de la medición de LIC.
Es importante tambien la medida del hierro cardiaco dado que a pesar de la terapéutica quelante, un porcentaje elevado de pacientes con sobrecarga de hierro transfusional fallecen de miocardiopatía,(26), así como aconsejable medir el hierro en otros órganos, como páncreas o glándula pituitaria (27,28).
La medida de hierro cardíaco mediante T2* (relaxometría con secuencias multi eco de gradiente), es una herramienta rápida eficaz y reproductible para monitorizar los depósitos del corazón (29).
Valores cardíacos de RM superiores 20 ms, se consideran dentro de la normalidad y la quelación dependerá de la sobrecarga hepática de hierro. Valores de 20 a 10 ms, indican depósito moderado de hierro en miocardio ventricular, pero el riesgo de complicaciones es bajo, aunque es en este punto cuando debe comenzarse una quelación rápida, eficaz para eliminar el hierro acumulado. Cuando T2* disminuye por debajo de 20 ms, se produce una progresiva disminución de la fracción de eyección. Los valores de RM por debajo de 10 ms, presentan sobrecarga cardíaca con riesgo inminente de complicaciones, arritmias y riesgo de muerte por miocardiopatía (30). Sin una terapéutica quelante eficaz, un 50% de los pacientes con T2*<6 ms, tienen riesgo de desarrollar fallo cardíaco en un año (27).
La sobrecarga cardíaca es rara en pacientes que reciben menos de 70 concentrados de hematíes. Sin embargo, en pacientes con 10-20 concentrados ya es necesario evaluar la sobrecarga de hierro hepática.
En resúmen, dentro de los métodos de medida de la sobrecarga, se recomienda realizar ferritina, LIC por resonancia magnética y RM del corazón.
La capacidad de medir los niveles de NTBI y LPI puede ser útil para detectar posible daño tóxico precozmente (31), incluso años antes de que se produzca el daño hepático o cardíaco. Sin embargo, estas pruebas todavía no se encuentran estandarizadas para su uso rutinario en la práctica clínica (32).
Tratamiento de la sobrecarga de hierro. Quelación
El organismo humano no cuenta con un método fisiológico para la excrección de hierro. La única manera de eliminar el hierro, en los pacientes anémicos, es mediante el tratamiento quelante, captando el hierro y eliminándolo por heces u orina.
La sobrecarga de hierro afecta negativamente a la supervivencia de los pacientes, tanto con talasemia mayor (22, 31), como en síndromes mielodisplásicos de bajo riesgo, en los que se ha demostrado que el número de transfusiones y el valor de la ferritina tienen un impacto pronóstico negativo sobre la supervivencia global y la supervivencia libre de progresión a leucemia (33,34), y los pacientes que reciben un tratamiento quelante, mejoran la supervivencia en relación con los que no lo reciben (33,34,35).
También en pacientes que son candidatos a un trasplante alogénico de progenitores hemotopoyéticos, la mortalidad relacionada con el trasplante es mayor cuando existe sobrecarga férrica (36).
Dado que el daño tisular está directamente relacionado con el aumento de hierro no unido a transferrina y a la fracción LPI, el objetivo de un buen tratamiento quelante es eliminar LPI (31) y revertir el efecto tóxico del hierro sobre los órganos diana. Existen varios trabajos que demuestran el beneficio del efecto quelante en los pacientes con sobrecarga de hierro eliminando LPI (31,32).
Los pacientes candidatos al tratamiento quelante son los que presentan anemia congénita o adquirida, transfusión dependiente:
Congénitas: talasemia mayor y hemoglobinopatías, anemias diseritropoyéticas, anemia de Fanconi, determinadas anemias hemolíticas, etc.
Adquiridas: síndrome mielodisplásico de bajo riesgo, aplasia medular adquirida, mielofibrosis, etc.
Trasplante alogénico de progenitores hematopoyéticos.
El tratamiento quelante en estos pacientes, se basa en la utilización de agentes quelantes. Tres son los quelantes comercializados cuyas características se exponen en la tabla (tabla I):

Talasemia mayor:
La Deferoxamina fue descubierta en 1960, y comenzó a utilizarse en estos pacientes en la década de los 70. En 1978 se demuestra que una infusión subcutánea durante 8-10 horas diarias, durante varios días a la semana, consigue un balance negativo de hierro, detectándose a finales de los 80 el claro impacto de la Deferoxamina sobre la supervivencia de los pacientes talasémicos. Los pacientes bien quelados tienen a los 25 años una supervivencia cercana al 100%, en comparación a los pacientes pobremente quelados cuya supervivencia a los 5 años no supera el 32% (22). Su principal inconveniente es que no se absorbe por vía oral, con lo cual su administración tiene que ser intravenosa o subcutánea.
La administración subcutánea 8-12 horas al día durante 5-7 días a la semana, ha demostrado sobradamente la eficacia de la quelación. El problema fundamental es la dificultad de administración y la falta de adherencia del tratamiento, sobre todo en pacientes adolescentes.
Por ello, un gran avance en el tratamiento fue el descubrimiento de los quelantes orales de hierro: Deferiprona y Deferasirox.
La Deferiprona ha demostrado eficacia en la sobrecarga de hierro cardíaco en enfermos pobremente quelados, en donde asociada a Deferoxamina puede conseguir un balance negativo de hierro, y revertir la cardopatia.
Por otra parte, el tratamiento combinado Deferiprona/Deferoxamina, puede ser mejor tolerado al disminuir la dosis de Deferoxamina.
Debido a la menor quelación de hierro hepático y a los efectos adversos, como neutropenia y agranulocitosis, su uso es inferior al de Deferasirox.
Varios estudios han demostrado la eficacia de Deferasirox versus Deferoxamina en la quelación de hierro, tanto hepático como cardíaco (30), así como su capacidad de disminuir la fracción LPI desde las primeras semanas de tratamiento. Con la presentación en comprimidos recubiertos, se consigue una disminución de los efectos adversos, con mejor tolerabilidad, adherencia y satisfacción por el tratamiento. Al conseguir una mayor concentración del fármaco, la dosis se reduce un 30% (37).
La asociación de dos quelantes orales (Deferiprona y Deferasirox) no ha sido suficientemente estudiada, aunque se está comenzando a utilizar en pacientes que no consiguen una quelación óptima.
La quelación debe de instaurarse de forma precoz, dado que una vez el exceso de hierro se deposita en los tejidos, es más difícil eliminarlo.
En el momento actual, aunque todos los quelantes son útiles en el tratamiento de la talasemia (38) y otras anemias transfusión dependientes, el tratamiento generalmente utilizado es el Deferasirox.
En la talasemia existen guías internacionales consensuadas con objetivos muy concretos sobre cuándo comenzar la quelación, qué métodos de medida, con qué frecuencia, cómo analizar los efectos adversos.
Síndrome mielodisplásico (SMD):
Más del 80% de los pacientes con SMD, desarrollan anemia a lo largo de su vida (34).
La anemia es el síntoma más característico de los SMD. A pesar de las opciones terapéuticas disponibles, en muchos pacientes el tratamiento se basa en las trasfusiones de hematíes. La dependencia transfusional ha sido identificada como un factor pronóstico adverso en varios trabajos, con una supervivencia menor en relación con los no trasfundidos (34,39).
El tratamiento transfusional crónico en pacientes con SMD de bajo riesgo, causa una sobrecarga de hierro que está en relación con el número de concentrados de hematíes transfundidos, y con la eritropoyesis ineficaz típica de los SMD de bajo riesgo (12,40). Además de presentar una supervivencia menor, tienen un mayor riesgo de evolucionar a leucemia aguda, dado que el hierro es un elemento clave en la proliferación de las células malignas (39).
Basado en los estudios realizados en la talasemia mayor, se han extrapolado estos resultados y pensado que el tratamiento quelante podría mejorar la sobrecarga férrica en los pacientes con SMD, así como la supervivencia y el riesgo de evolucionar hacia leucemia aguda mieloblástica (34,39). Son numerosos los trabajos, la mayoría de ellos retrospectivos, alguno prospectivo, que confirman que los pacientes en tratamiento quelante, con SMD de bajo riesgo o intermedio 1, tuvieron una supervivencia global claramente más satisfactoria, incluso con menor morbimortalidad cardíaca asociada y menor evolución a leucemia aguda ( 33, 35,40,41).
En el estudio IRON 2, estudio prospectivo, promovido por nuestro grupo de trabajo de eritropatología, se analizó la evolución de 263 pacientes con SMD de bajo riesgo o intermedio-1, y se observó una mejor supervivencia, con menores complicaciones cardíacas (34) en los enfermos quelados versus los no quelados.
Estos hallazgos han sido confirmados más recientemente en un estudio prospectivo realizado durante 5 años, en 600 pacientes con SMD. Con una mediana de seguimiento de 24 meses, se observa que los pacientes quelados tienen una mediana de supervivencia de 104 meses en relación con los no quelados, con una mediana de 52.2 meses (p< 0.0001) con un menor número de eventos cardíacos (42).
La sobrecarga de hierro definida como una ferritina sérica superior a 1000 ng/ml, se ha considerado en numerosas guías clínicas “de consenso” como un dato analítico para comenzar el tratamiento quelante en SMD transfusión dependiente (43).
El Deferasirox ha sido el quelante más utilizado, dado que por los efectos adversos la Deferiprona se ha utilizado escasamente en los SMD, y la Deferoxamina por su forma de administración tiene una baja adherencia al tratamiento, con pérdida de seguimiento de un gran número de pacientes (44).
Un aspecto relativamente controvertido sobre el tratamiento quelante, está en relación con la mejoría hematopoyética observada en algunos pacientes, sin que se haya podido aclarar cuál es el mecanismo fisiológico causante de este beneficio. Así se han reseñado subida de la cifra de hemoglobina, de los neutrófilos y de las plaquetas (45,46).
A pesar de las recomendaciones actuales basadas en la evidencia (35,47), la aceptación generalizada sobre el efecto beneficioso de la quelación en SMD no es universalmente reconocida (48), en parte debido a que son pacientes mayores, con varias comorbilidades y a la falta de ensayos aleatorizados que justifiquen plenamente el tratamiento.
En la actualidad, para subsanar dicho problema, está en marcha el ensayo TELESTO estudio prospectivo, aletorizado, con Deferasirox versus placebo en SMD con IPSS baja o intermedio-1, y con una ferritina superior a 1000 ng/ml, o que hayan recibido más de 20 concentrados de hematíes (NTC 00940602). El objetivo principal es analizar la supervivencia.
Finalmente otro aspecto inherente de la sobrecarga férrica está en relación con el transplante alogénico de médula ósea. La cifra de ferritina se relaciona inversamente con la supervivencia (36). A mayor concentración de ferritina, menor supervivencia y mayor probabilidad de mortalidad relacionada con el transplante (36,49).
La sobrecarga férrica pretrasplante induce incremento de infecciones, mayor incidencia de enfermedad venooclusiva hepática post-trasplante, así como mayor asociación con enfermedad injerto contra huésped crónico (36,50).
También en los pacientes que van a ser sometidos a trasplante, está indicado el tratamiento quelante.
Conclusiones
La hepcidina es la hormona clave en la homeostasis del hierro. Controla la absorción de hierro intestinal y su liberación por parte de los macrófagos.
- Cuando la transferrina se satura por encima de 60-70%, se produce NTBI (notransferrin bound iron), y su fracción lábil LPI (labile plasma iron) LIP es capaz de atravesar las membranas de hepatocitos, miocardiocitos y células endocrinas. Mediante la generación de especies reactivas de oxígeno (ROS) produce efecto citotóxico y genotóxico directo con lesión celular y daño tisular.
- Para un buen manejo de la sobrecarga férrica, hay que monitorizar los depósitos de hierro. El organismo no dispone de un mecanismo fisiológico capaz de eliminar el hierro. En pacientes anémicos transfusión dependientes, los agentes quelantes que captan el hierro y lo eliminan por hígado o riñón, son la terapia de elección.
- El efecto beneficioso del tratamiento quelante sobre la supervivencia de los pacientes con talasemia mayor, ha sido confirmado desde la década de los 80. Todos los preparados son eficaces para disminuir los depósitos de hierro. La Deferoxamina en la actualidad se utiliza, fundamentalmente, asociada de Deferiprona, para el tratamiento intensivo de la sobrecarga férrica con afectación cardíaca. El Deferasirox es el tratamiento más utilizado.
- El efecto beneficioso del tratamiento quelante sobre la supervivencia de los pacientes con síndrome mielodisplásico de bajo riesgo, también ha sido confirmado en varios estudios. Existen guías clínicas generalizadas que recomiendan su uso.
Bibliografía
- Fleming RE, Ponka P. Iron overload in Human Disease. N Engl J Med 2012; 366(4): 348-359.
- Hentze MW, Muckenthaler MU, Galy B, Camachella C. Two to tango: Regulation of mammalian iron metabolism. Cell 2010, 142: 24-36.
- Ganz TI, Memeth E. Hepcidin and iron homeostasis. Biochim Biophys Acta 2012, 1823(9): 1434-1443.
- Villegas A. Metabolismo del hierro. En: ”Utilidad de la resonancia magnética en el diagnóstico de la sobrecarga férrica”. Coordinadora A. Villegas. Madrid CECE.ES.ISBN 978-84-938864-31. 2012 Pp 15-25
- Finch C. Regulators of iron balance in humans. Blood 1994,84:1697-1700
- Nemeth E, Tutle MS, Powelson J et al. Hepcidine regulates cellular iron efflux by binding to ferroportin and inducing its internalization. Science 2004;306:2090-2093.
- Jensen PD. Evaluation of iron overload. Br J Haematol 2004; 124: 697-711.
- Casanovas G, Vujic Spasig M, Casu C et al. The murine growth differentation factor 15 is not essential for systemic iron homeostasis in phebotomized mice. Haematologica 2013; 98(3): 444-447.
- Kautz L, Yang G, Vabre EV, Rivella S, Nemeth E, Ganz T. Identification of erythroferrone as an erythroid regulator of iron metabolism. Nat Genet 2014; 46(7): 678-684.
- Kautz L, Jung GI, Nemeth E, Ganz T. Erythroferrone contributes to recovery from anemia of inflammation. Blood 2014; 124(16): 2569-2574.
- Remacha AF, Arrizabalaga B, del Cañizo C, Sanz G, Villegas A. Iron overload and chelation therapy in patients with low-risk myelodysplastic síndromes with transfusion requirements. Ann Hematol 2010; 89(4): 147-154.
- Ambaglio I, Malcovali L, Papaemmanuil E et al. Inappropiately low hepcidin levels in patients with myelodysplastic syndrome carrying a somatic mutation of SF3B1. Haematologica 2013; 98(2): 420-423.
- Vifrano A, Calvaruso G, Lai E et al. The era of comparable life expentancy between thalassaemia major and intermedia: It is time to revisit the major-intermedia dichotomy. Br J Haematol 2017; 176: 124-130.
- Ivars D, Collado R, Diaz L. Antioxidant system aberrations as response to generation of reactive oxygen species (ROS) in low/intermediate-1 risk myelodysplastic syndrome. Leuk Res 2013; 37(S1): S 127.
- Gao X, Campian JL, Qian M et al. Mitochondrial DNA damage in iron overload. J Biol Chem 2009; 284(8): 4767-4775.
- Shvartsman M, Kikkeri R, Shanzer A et al. Non-transferrin Bound Iron reaches mitochondria by a chelator-inacessible mechanism: biological and clinical implications. Am J Physiol Cell Physiol 2007; 293(4): 1383-1394.
- Cortelezzi A, Cattaneo C, Cristianis S et al. Iron transferrin Bound Iron in myelodysplastic syndromes: a marker of ineffective erytropoieisis. Hematol J 2000; 1(3): 153-158.
- Vinchi F, Muckenthaler MU, Da Silva et al. Atherogenesis and iron: from epidemiology to cellular level. Front Pharmacol 2014; 5(94): 1-19.
- Angelucci E, Brittenham GM, Mclaren CE et al. Hepatic iron concentration and total body iron stores in thalassemia major. N Engl J Med 2000; 343: 327-331
- Wood JC. Cardiac iron across different transfusion-dependent diseases. Blood Rev 2008; 22: 14-21.
- Noetzli LJ, Coates TD, Wood JC. Pancreatic iron loading in chronically transfused sickle cell disease is lower than in thalassaemia major. Br J Haematol 2011; 152: 229-233.
- Olivieri NF, Brittienham GM. Iron-chelating therapy and the treatment of thalassemia. Blood 1997; 89: 739-761.
- Villegas A. Métodos de cuantificación de la sobrecarga férrica. En “Utilidad de la resonancia magnética en el diagnóstico de la sobrecarga férrica”. Coordinadora A. Villegas. Madrid CEGE.ES.ISBW 978-84-938864-3. 1. 2012 Pp 30-39.
- Anderson LJ, Westwood MA, Holden S et al. Myocardial iron clearance during reversal of siderotic cardiomyopathy with intravenous deferroxiamine: a prospective study usin T2* cardiovascular magnetic resonance. Br. J. Haematol 2004; 127: 348-355.
- St Pierre TG, Clark PA, Chua-Anusen W et al. Non invasive measurement and imaging of liver iron concentrations using proton magnetic resonance. Blood 2005; 105: 855-861.
- Porter JB, Abeysinghe RD, Marshall L, Hider RC, Sing S. Kinetics of removal and reapareance of non-transferrin bound plasma iron with deferoxamine therapy. Blood 1996; 88: 705-713.
- Wood JC. Guidelines for quantifying iron overload. Hematology Am. Soc Hematol Educ Program 2014(1): 210-215.
- Pennell DJ, Porter JB, Piga A et al. Sustained improvements in myocardial T2* over 2 years in severely iron ever loaded patients with beta thalassemia major treated with deferasirox or deferoxamine. Am J Hematol 2015; 90(2): 91-96.
- Westwood MA, Firmin DN, Gildo M et al. Intercentre reproductibility of magnetic resonance T2* measurements of myocardial iron thalassemia. Int J Cardiovasc Imaging 2005; 21: 531-538.
- Pennell DJ, Porter JB, Piga A et al. A 1 year randomized controlled trial of deferasirox vs desferroxamina for myocardial iron removal in beta thalassemia major (CORDELIA). Blood 2014; 123(10): 1447-1454.
- Porter JB, El-Alfy M, Viprasit V et al. Utility of labile plasma iron and transferrin saturation in addition to serum ferritin as iron overload markers in different underlying anemias before and after deferasirox treatment. Eur J Haematol 2016; 96(1): 19-26.
- De Swart L, Hendriks JCM, Van der Vorm LN et al. Second international round robin for the quantification on of serum non-transferrin-bound iron and labile plasma iron in patients with iron-overload disorders. Hematologica 2016; 101(1): 38-45.
- Malcovati L, Germing U, Kuendgen A et al. Time dependent pronostic scoring system for predicting survival and leukemia evolution in myelodysplastic syndromes. J. Clin Oncol 2007; 25: 3503-3510.
- Remacha AF, Arrizabalaga B, Villegas A et al. Evolution of iron overload in patients with low-risk myelodysplastic syndrome iron chelation therapy and organ complications. Ann Hematol 2015; 94(5) 779-787.
- Mainnous AG, Tanner RJ, Hulihan MM, Amaya M, Coates TD. The impact of chelation therapy on survival in transfusional iron overload: a meta-analysis of myelodysplastic syndrome. Br J Haematol 2014; 167(3): 720-723.
- Angelucci E, Pilo F. Iron overload before, during and after hematopoietic stem cells transplantation. Prog Educ. EHA 22nd Congress. Madrid. June 2017 P.5.
- Taher AT, Origa R, Perrsotta S et al. New film-coated tablet formulation of deferasirox is well tolerated in patients with thalassemia or lower-risk MDS: results of the randomized phase I ECLIPSE study. Am J Hematol 2017. doi 10.1002/ajh 24 668.
- Xia S, Zhang W, Huang L, Jiang H. Comparative efficary and safety of Deferoxamine, Deferiprone and Deferasirox on severe thalassemia. A meta-analysis of 16 Randomized Controlled Trials. Plos One 2013; 8(12) e 82662.
- Malcovati L, Porta MG, Pascutto C et al. Prognostic factors and life expectancy in myelodysplastic syndromes classified according to WHO criteria: a basis for clinical decision making. J Clin Oncol 2005; 23(30): 7594-7603.
- Cazzola M, Malcovati L. Myelodysplastic syndromes coping with ineffective hematopoiesis. N Engl J Med 2005; 352: 536-538.
- Rose C, Brechignac S, Vassillief D. Does iron chelation therapy improve survival in regularly transfused lower risk MDS patients?. A multicenter study by GMF. Leuk Res 2010; 34(7): 864-870.
- Lyons RM, Marek BJ, Paley C et al. Comparison of 24-month outcomes in chelated and no-chelated lower-risk patients with myelodysplastic syndromes in a prospective registry. Leuk Res 2014; 38(2): 149-154.
- Arrizabalaga A, del Cañizo C, Remacha A, Sanz G, Villegas A. Guía de quelación del paciente con síndrome mielodisplásico. Haematologica 2008; 91(1): 3-10.
- González FA, Arrizabalaga B, Villegas A et al. Estudio del tratamiento con deferoxamina en perfusión contínua subcutánea para la sobrecarga de hierro en pacientes con síndrome mielodisplásico. Med Clin 2005; 124: 641-644.
- Angelucci E, Santini V, Di Tucci AA et al. Deferasirox for transfusion-dependent patients with myelodysplastic syndromes : safety, efficacy and beyond (GIMENA MDS 0306 Trial). Eur J Haematol 2014; 92(6): 527-536.
- Breccia M, Voso MT, Aloe Spiriti MA et al. An increase in hemoglobin platelets and white bood cells levels by iron chelation as single treatment in multitransfused patients with myelodysplastic syndromes: clinical evidences and possible biological mechanisms. Ann Hematol 2015; 94(5): 771-777.
- Lyons RM, Marek BJ, Paley C et al. Relation between chelation and clinical outcomes in lower-risk patients with myelodysplastic syndromes: Registry analysis at 5 years. Leuk Res 2017; 56: 88-95.
- Butter A, Patton WN. Iron chelation therapy in myelodysplastic syndromes: we need more evidency, not more guidelines. Intern Med J 2012; 42: 481-484.
- Armand P, Kim HT, Cutler CS et al. Prognostic impact of elevated pretransplatation serum ferritin in patients undergoing myeloablative stem cell transplantation. Blood 2007; 109: 4586-4588.
- Tefferi A. Iron overload and stem cell transplant and the beat goes on. Am J Hematol 2011; 86: 825-826.
Ana Villegas Martínez
Real Academia Nacional de Medicina de España
C/ Arrieta, 12 · 28013 Madrid
Tlf.: +34 91 159 47 34 | Email de correspondencia
Año 2018 · número 135 (01) · páginas 20 a 27
Enviado*: 06.02.18
Revisado: 13.02.18
Aceptado: 13.03.18
* Fecha de lectura en la RANM


